硫及其化合物在生产生活中具有广泛的应用,根据所学知识,回答下列问题:
(1) 溶液显
溶液显_______________ 性,判断的理由是_______________ (用离子方程式表示),若将该溶液蒸干,最终所得固体为_______________ (填化学式)。
(2) 的
的 溶液中,各离子浓度由大到小的关系为
溶液中,各离子浓度由大到小的关系为_______________ 。
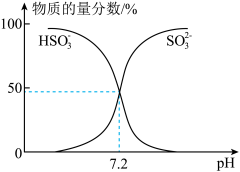
(3)常温下,在某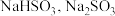 混合溶液中,部分含硫微粒的物质的量分数随
混合溶液中,部分含硫微粒的物质的量分数随 的变化曲线如图所示,根据图示,
的变化曲线如图所示,根据图示, 的水解平衡常数
的水解平衡常数
_______________ 。
(4)常温下,某浓度的 溶液中:
溶液中:
① 为
为_______________ (填“强”或“弱”)电解质。
②往 溶液中滴加少量的
溶液中滴加少量的 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为_______________ ,此时所得溶液的
_______________ (填“变大”、“变小”或“不变”)。
(5)在 的
的 溶液中加入等体积
溶液中加入等体积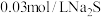 溶液,有黑色
溶液,有黑色 沉淀生成,反应后溶液中
沉淀生成,反应后溶液中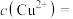
_______________ [已知: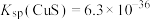 ](忽略溶液混合时体积的变化)。
](忽略溶液混合时体积的变化)。
(1)
 溶液显
溶液显(2)
 的
的 溶液中,各离子浓度由大到小的关系为
溶液中,各离子浓度由大到小的关系为(3)常温下,在某
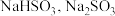 混合溶液中,部分含硫微粒的物质的量分数随
混合溶液中,部分含硫微粒的物质的量分数随 的变化曲线如图所示,根据图示,
的变化曲线如图所示,根据图示, 的水解平衡常数
的水解平衡常数

(4)常温下,某浓度的
 溶液中:
溶液中:①
 为
为②往
 溶液中滴加少量的
溶液中滴加少量的 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为
(5)在
 的
的 溶液中加入等体积
溶液中加入等体积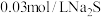 溶液,有黑色
溶液,有黑色 沉淀生成,反应后溶液中
沉淀生成,反应后溶液中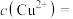
 ](忽略溶液混合时体积的变化)。
](忽略溶液混合时体积的变化)。
更新时间:2024-02-07 13:04:01
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】硫酸铁铵[NH4Fe(SO4)2·xH2O]是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如图:
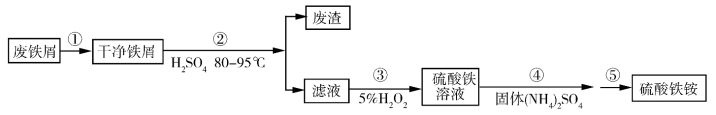
回答下列问题:
(1)步骤①的操作中用热的饱和Na2CO3溶液浸泡废铁屑,目的是_______ 。
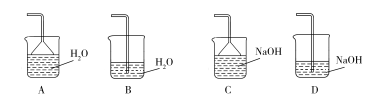
(2)步骤②加快化学反应速率的方法有_______ ;温度保持80~95 ℃,采用的合适加热方式是_______ ;铁屑中含有少量硫化物杂质,反应产生的气体需要净化处理,合适的装置为_______ (填标号)。
(3)步骤③中发生的离子反应方程式_______ ,步骤⑤蒸发浓缩时温度不宜过高,否则产率会降低,产品不纯。原因是_______ 。
(4)用冷水洗涤硫酸铁铵晶体的操作是_______ 。
(5)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150 ℃时,失掉2个结晶水,失重8.41%。硫酸铁铵晶体的化学式为_______ 。

回答下列问题:
(1)步骤①的操作中用热的饱和Na2CO3溶液浸泡废铁屑,目的是
(2)步骤②加快化学反应速率的方法有

(3)步骤③中发生的离子反应方程式
(4)用冷水洗涤硫酸铁铵晶体的操作是
(5)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150 ℃时,失掉2个结晶水,失重8.41%。硫酸铁铵晶体的化学式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】某工厂以重晶石(主要含BaSO4)为原料,生产“电子陶瓷工业支柱”——钛酸(BaTiO3)的工艺流程如下:
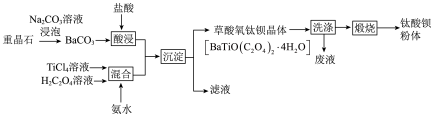
回答下列问题:
(l)为提高BaCO3的酸浸速率,可采取的措施为__ (写出一条即可);常温下,TiCl4为液体且易水解,配制一定浓度的TiCl4溶液的方法是 ____ 。
(2)用Na2CO3溶液浸泡重晶石(假设杂质不与Na2CO3反应),能将BaSO4转化为BaCO3,此反应的平衡常数K=___ (填写计算结果);若不考虑CO32-的水解,要使2. 33g BaSO4恰好完全转化为BaCO3,则至少需要浓度为1.0mol·L-1Na2CO3溶液 ___ mL。(已知:Ksp(BaSO4)=1.0×10-10、Ksp(BaCO3)=5.0×10-9)
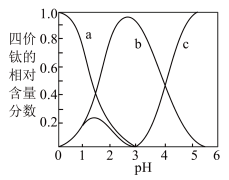
(3)流程中“混合”溶液的钛元素在不同pH时主要以TiO(OH)+、TiOC2O4、TiO(C2O4)22-三种形式存在(变化曲线如右图所示)。实际制备工艺中,先用氨水调节混合溶液的pH于2.8左右,再进行“沉淀”,其反应的离子方程式为____ ;图中曲线c对应钛的形式为____ (填粒子符号)。
(4)流程中“滤液”的主要成分为____ ;隔绝空气煅烧草酸氧钛钡晶体得到钛酸钡粉体和气态产物,试写出反应的化学方程式:____ 。

回答下列问题:
(l)为提高BaCO3的酸浸速率,可采取的措施为
(2)用Na2CO3溶液浸泡重晶石(假设杂质不与Na2CO3反应),能将BaSO4转化为BaCO3,此反应的平衡常数K=
(3)流程中“混合”溶液的钛元素在不同pH时主要以TiO(OH)+、TiOC2O4、TiO(C2O4)22-三种形式存在(变化曲线如右图所示)。实际制备工艺中,先用氨水调节混合溶液的pH于2.8左右,再进行“沉淀”,其反应的离子方程式为

(4)流程中“滤液”的主要成分为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某化学小组欲探究铁及其化合物的氧化性和还原性,请回答下列问题:
(1)除胶头滴管外,你认为本实验必不可缺少的一种玻璃仪器是_______ 。
(2)请帮他们完成以下实验报告:
实验目的:探究铁及其化合物的氧化性和还原性。
试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、锌片、铜片。
实验记录(划斜线部分不必填写):
实验结论:_______ 。
(3)根据以上结论判断,下列物质中既有氧化性,又有还原性的有:_______ 。(填序号)
A.Cl2 B.Na C.Na+ D.Cl- E.SO2 F。NO2
(4)亚铁盐在溶液中易被氧化,而实验室中需要纯净的亚铁盐溶液。那么保存亚铁盐溶液时应该如何防止亚铁盐被氧化_______ 。
(1)除胶头滴管外,你认为本实验必不可缺少的一种玻璃仪器是
(2)请帮他们完成以下实验报告:
实验目的:探究铁及其化合物的氧化性和还原性。
试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、锌片、铜片。
实验记录(划斜线部分不必填写):
| 序号 | 实验内容 | 实验现象 | 离子方程式 | 实验结论 |
| ① | 在FeCl2溶液中滴入适量氯水 | 溶液由浅绿色变为棕黄色 | Fe2+具有还原性 | |
| ② | 在FeCl2溶液中加入锌片 |  | Zn+Fe2+=Zn2++Fe | |
| ③ | 在FeCl3溶液中加入足量铁粉 | Fe+2Fe3+=3 Fe2+ | Fe3+具有氧化性 | |
| ④ |  | Fe3+具有氧化性 |
(3)根据以上结论判断,下列物质中既有氧化性,又有还原性的有:
A.Cl2 B.Na C.Na+ D.Cl- E.SO2 F。NO2
(4)亚铁盐在溶液中易被氧化,而实验室中需要纯净的亚铁盐溶液。那么保存亚铁盐溶液时应该如何防止亚铁盐被氧化
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】降低大气中C02的含量及有效地开发利用CO2,已引起了全世界的普遍重视。
(1)CO2加氢合成DME(二甲醚)是解决能源危机的研究方向之一。
①2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g)△H= -122.4kJ·mol-1
CH3OCH3(g)+3H2O(g)△H= -122.4kJ·mol-1
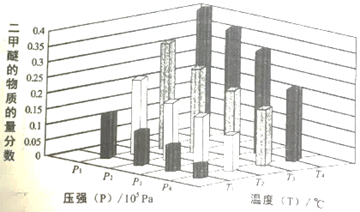
某温度下,将2.0molCO2(g)和6.0molH2(g)充入容积为2L的密闭容器中,反应到达平衡时、改变压强和温度,平衡体系中CH3OCH3(g)的物质分数变化情况如图所示,则p1______ p2(填“>”“<”或“=”,下同)。若T1、P1,T3、P3时平衡常数分别为K1、K3,则K1______ K3,T1、P1时H2的平衡转化率为____________ 。
②在恒容密闭容器里按体积比为1:3充入二氧化碳和氢气,一定条件下反应达到平衡状态。当改变反应的某一个条件后,下列能说明平衡一定向逆反应方向移动的是______ (填序号)。
A. 反应物的浓度增大 B. 混合气体的密度减小
C. 正反应速率小于逆反应速率 D. 氢气的转化率减小
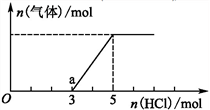
(2)将一定量的CO2气体通入氢氧化钠的溶液中,向所得溶液中边滴加稀盐酸边振荡至过量,产生的气体与盐酸物质的量的关系如图(忽略气体的溶解和HCl的挥发)。请回答:通入1mol HCl时,溶液中所含溶质的化学式_____________ ,a点溶液中各离子浓度由大到小的关系式为___________________ 。
(3)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其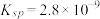 。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为
。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为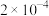 mol·L-1,则生成沉淀所需CaCl2溶液的最小浓度为
mol·L-1,则生成沉淀所需CaCl2溶液的最小浓度为__________ mol·L-1.
(1)CO2加氢合成DME(二甲醚)是解决能源危机的研究方向之一。
①2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g)△H= -122.4kJ·mol-1
CH3OCH3(g)+3H2O(g)△H= -122.4kJ·mol-1
某温度下,将2.0molCO2(g)和6.0molH2(g)充入容积为2L的密闭容器中,反应到达平衡时、改变压强和温度,平衡体系中CH3OCH3(g)的物质分数变化情况如图所示,则p1
②在恒容密闭容器里按体积比为1:3充入二氧化碳和氢气,一定条件下反应达到平衡状态。当改变反应的某一个条件后,下列能说明平衡一定向逆反应方向移动的是
A. 反应物的浓度增大 B. 混合气体的密度减小
C. 正反应速率小于逆反应速率 D. 氢气的转化率减小
(2)将一定量的CO2气体通入氢氧化钠的溶液中,向所得溶液中边滴加稀盐酸边振荡至过量,产生的气体与盐酸物质的量的关系如图(忽略气体的溶解和HCl的挥发)。请回答:通入1mol HCl时,溶液中所含溶质的化学式

(3)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其
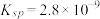 。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为
。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为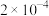 mol·L-1,则生成沉淀所需CaCl2溶液的最小浓度为
mol·L-1,则生成沉淀所需CaCl2溶液的最小浓度为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】研究电解质在水溶液中的平衡能了解它的存在形式。
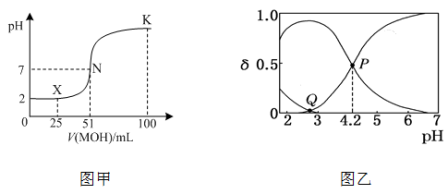
(1)常温下,向100mL0.01mol•L-1HA溶液中逐滴加入0.02mol•L-1MOH溶液,所得溶液的pH随MOH溶液的体积变化如图甲所示 溶液体积变化忽略不计
溶液体积变化忽略不计 。
。
①常温下,0.01mol•L-1HA溶液中由水电离出的c(H+)=___ mol•L-1。
②常温下一定浓度的MA稀溶液的pH=a,则a___ 7(填“>”、“<”或“=”),用离子方程式表示其原因为___ 。
③X点时,溶液中c(H+)、c(M+)、c(A-)由大到小的顺序是___ 。
④K点时,溶液中c(H+)+c(M+)-c(OH-)=___ 。
(2)20℃时,在c(H2C2O4)+c(HC2O )+c(C2O
)+c(C2O )=0.100mol•L-1的H2C2O4、NaOH混合溶液中,H2C2O4、HC2O
)=0.100mol•L-1的H2C2O4、NaOH混合溶液中,H2C2O4、HC2O 、C2O
、C2O 的物质的量分数δ随溶液pH变化的关系如图乙所示。
的物质的量分数δ随溶液pH变化的关系如图乙所示。
①Q点:c(H2C2O4)___ c(HC2O )(填“>”、“<”或“=”)。
)(填“>”、“<”或“=”)。
②该温度下HC2O 的电离常数K=
的电离常数K=___ 。
(3)25℃时,某溶液中Fe3+的浓度为0.010mol/L,使Fe3+沉淀完全的pH为___ 。(Ksp[Fe(OH)3]=4×10-38,lg2=0.3)

(1)常温下,向100mL0.01mol•L-1HA溶液中逐滴加入0.02mol•L-1MOH溶液,所得溶液的pH随MOH溶液的体积变化如图甲所示
 溶液体积变化忽略不计
溶液体积变化忽略不计 。
。①常温下,0.01mol•L-1HA溶液中由水电离出的c(H+)=
②常温下一定浓度的MA稀溶液的pH=a,则a
③X点时,溶液中c(H+)、c(M+)、c(A-)由大到小的顺序是
④K点时,溶液中c(H+)+c(M+)-c(OH-)=
(2)20℃时,在c(H2C2O4)+c(HC2O
 )+c(C2O
)+c(C2O )=0.100mol•L-1的H2C2O4、NaOH混合溶液中,H2C2O4、HC2O
)=0.100mol•L-1的H2C2O4、NaOH混合溶液中,H2C2O4、HC2O 、C2O
、C2O 的物质的量分数δ随溶液pH变化的关系如图乙所示。
的物质的量分数δ随溶液pH变化的关系如图乙所示。①Q点:c(H2C2O4)
 )(填“>”、“<”或“=”)。
)(填“>”、“<”或“=”)。②该温度下HC2O
 的电离常数K=
的电离常数K=(3)25℃时,某溶液中Fe3+的浓度为0.010mol/L,使Fe3+沉淀完全的pH为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】铵盐是比较重要的盐类物质,请回答下列问题。
(1)草酸是二元弱酸,能形成两种铵盐。
①(NH4)2C2O4溶液呈酸性,溶液中各离子浓度由大到小的顺序为_______ 。
②NH4HC2O4溶液中,c(H2C2O4)-c(C2O )=
)=_______ 。
(2)氯化铵是最常见的铵盐,在工业生产中用途广泛。
①热的浓氯化铵溶液可以清洗铁器表面锈迹,写出相关反应的离子方程式:_______ 。
②常温下,向100 mL 0.2 mol·L-1的氨水中逐滴加入0.2 mol·L-1的盐酸,所得溶液的pH、溶液中NH 和NH3·H2O的物质的量分数与加入盐酸的体积的关系如图所示。
和NH3·H2O的物质的量分数与加入盐酸的体积的关系如图所示。
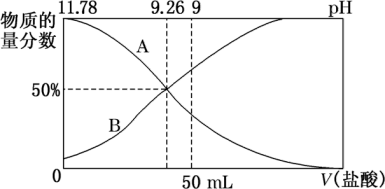
a.表示NH3·H2O物质的量分数变化的曲线是_______ (填“A”或“B”)。
b.NH3·H2O的电离常数为_______ 。
c.当加入盐酸的体积为50 mL时,溶液中c(NH )-c(NH3·H2O)=
)-c(NH3·H2O)=_______ mol·L-1(用式子表示)。
③常温下,在20 mL a mol·L-1氨水中滴加20 mL b mol·L-1盐酸恰好使溶液呈中性。常温下,NH 的水解常数Kh=
的水解常数Kh=_______ (用含a、b的代数式表示)。
(1)草酸是二元弱酸,能形成两种铵盐。
①(NH4)2C2O4溶液呈酸性,溶液中各离子浓度由大到小的顺序为
②NH4HC2O4溶液中,c(H2C2O4)-c(C2O
 )=
)=(2)氯化铵是最常见的铵盐,在工业生产中用途广泛。
①热的浓氯化铵溶液可以清洗铁器表面锈迹,写出相关反应的离子方程式:
②常温下,向100 mL 0.2 mol·L-1的氨水中逐滴加入0.2 mol·L-1的盐酸,所得溶液的pH、溶液中NH
 和NH3·H2O的物质的量分数与加入盐酸的体积的关系如图所示。
和NH3·H2O的物质的量分数与加入盐酸的体积的关系如图所示。
a.表示NH3·H2O物质的量分数变化的曲线是
b.NH3·H2O的电离常数为
c.当加入盐酸的体积为50 mL时,溶液中c(NH
 )-c(NH3·H2O)=
)-c(NH3·H2O)=③常温下,在20 mL a mol·L-1氨水中滴加20 mL b mol·L-1盐酸恰好使溶液呈中性。常温下,NH
 的水解常数Kh=
的水解常数Kh=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】自然界中的金以单质形态夹杂在矿石中。金矿粉经过氰化、吸附和解吸附、电解等步骤得到金单质,生产中产生的含氰废水需处理后才能排放。
(1)氰化工艺中,金溶解于NaCN溶液生成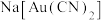 。
。
①25℃时, 。在25℃某NaCN溶液中,
。在25℃某NaCN溶液中,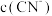 是
是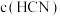 的620倍,该溶液pH为
的620倍,该溶液pH为_______ 。
②金矿溶于NaCN溶液的化学反应方程式为_______ 。
(2)吸附步骤中使用活性炭,电解步骤将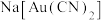 转变为Au。
转变为Au。
①“吸附”和“解吸附”的目的是_______ 。
②电解时阴极发生的电极反应式为_______ 。
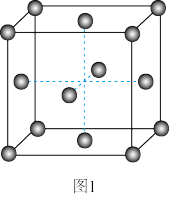
③金的晶胞结构如题图1所示。该晶胞中包含的金原子数目为_______ 。
(3)用 溶液处理含氰废水,在
溶液处理含氰废水,在 的催化下,使有毒的
的催化下,使有毒的 转化为
转化为 、
、 等。
等。
① 核外电子排布式为
核外电子排布式为_______ 。
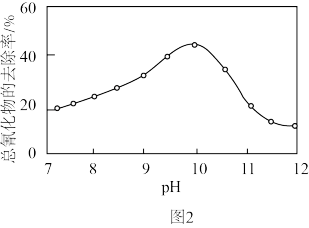
②在 催化下,总氰化物(
催化下,总氰化物( 、HCN等)去除率随溶液初始pH变化如题图2所示。pH从8变化到11,总氯化物去除率变化的原因可能是
、HCN等)去除率随溶液初始pH变化如题图2所示。pH从8变化到11,总氯化物去除率变化的原因可能是_______ 。
(1)氰化工艺中,金溶解于NaCN溶液生成
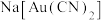 。
。①25℃时,
 。在25℃某NaCN溶液中,
。在25℃某NaCN溶液中,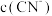 是
是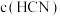 的620倍,该溶液pH为
的620倍,该溶液pH为②金矿溶于NaCN溶液的化学反应方程式为
(2)吸附步骤中使用活性炭,电解步骤将
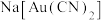 转变为Au。
转变为Au。①“吸附”和“解吸附”的目的是
②电解时阴极发生的电极反应式为
③金的晶胞结构如题图1所示。该晶胞中包含的金原子数目为

(3)用
 溶液处理含氰废水,在
溶液处理含氰废水,在 的催化下,使有毒的
的催化下,使有毒的 转化为
转化为 、
、 等。
等。①
 核外电子排布式为
核外电子排布式为②在
 催化下,总氰化物(
催化下,总氰化物( 、HCN等)去除率随溶液初始pH变化如题图2所示。pH从8变化到11,总氯化物去除率变化的原因可能是
、HCN等)去除率随溶液初始pH变化如题图2所示。pH从8变化到11,总氯化物去除率变化的原因可能是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】我们的生活离不开化学,化学物质在不同的领域发挥着重要的作用。根据要求回答下列问题:
(1)工业上可用TiCl4制备纳米材料TiO2,用TiCl4制备TiO2∙xH2O的化学方程式是_______ 。
(2)乙二酸(H2C2O4)俗称草酸,在实验研究和化学工业中应用广泛。25℃时,向10mL 0.1 mol∙L-1 H2C2O4溶液中逐滴加入0.1 mol∙L-1NaOH溶液,溶液中含碳微粒的物质的量分数随溶液pH变化如图所示:
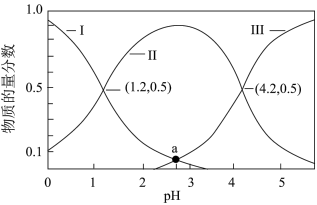
①等浓度的Na2C2O4和NaHC2O4混合溶液显_______ 性(填“酸”“碱”或“中”)并请通过计算说明_______ 。25℃时,草酸的电离平衡常数分别是Ka1、Ka2,则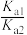 =
=_______ 。
②a点溶液中,c(Na+)_______ 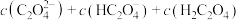 (填“>”“=”或“<”),此时溶液的pH=
(填“>”“=”或“<”),此时溶液的pH=_______ 。
(3)①酸性高锰酸钾应该用_______ 滴定管盛装(填“酸式”或“碱式”)。
②若要测定草酸亚铁晶体(FeC2O4∙xH2O)的x值,步骤如下:称取0.5400g草酸亚铁晶体溶于一定浓度的硫酸中,用KMnO4酸性溶液滴定,达到滴定终点时,消耗0.1000 mol∙L-1的酸性KMnO4溶液18.00mL。则x=_______ 。(FeC2O4的摩尔质量是144g/mol)
(1)工业上可用TiCl4制备纳米材料TiO2,用TiCl4制备TiO2∙xH2O的化学方程式是
(2)乙二酸(H2C2O4)俗称草酸,在实验研究和化学工业中应用广泛。25℃时,向10mL 0.1 mol∙L-1 H2C2O4溶液中逐滴加入0.1 mol∙L-1NaOH溶液,溶液中含碳微粒的物质的量分数随溶液pH变化如图所示:

①等浓度的Na2C2O4和NaHC2O4混合溶液显
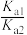 =
=②a点溶液中,c(Na+)
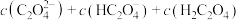 (填“>”“=”或“<”),此时溶液的pH=
(填“>”“=”或“<”),此时溶液的pH=(3)①酸性高锰酸钾应该用
②若要测定草酸亚铁晶体(FeC2O4∙xH2O)的x值,步骤如下:称取0.5400g草酸亚铁晶体溶于一定浓度的硫酸中,用KMnO4酸性溶液滴定,达到滴定终点时,消耗0.1000 mol∙L-1的酸性KMnO4溶液18.00mL。则x=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】用硫酸分解磷尾矿[主要成分为Ca5(PO4)3F]可制得中强酸磷酸。已知:25℃时,H3PO4的电离平衡常数:K1=7.1×10-3;K2=6.3×10-8;K3=4.2×10-13。请回答:
(1)NaH2PO4溶液中c(HPO )
)____ c(H3PO4)(填“<”,“>”或“=”)。
(2)25℃时,H2PO (aq)+OH-(aq)
(aq)+OH-(aq) HPO
HPO (aq)+H2O(l)的平衡常数K=
(aq)+H2O(l)的平衡常数K=____ 。
(3)Ca5(PO4)3F(s)+OH-(aq) Ca5(PO4)3OH(s)+F-(aq),溶液中c(F-)随溶液的pH和温度(T)的变化曲线如图所示。
Ca5(PO4)3OH(s)+F-(aq),溶液中c(F-)随溶液的pH和温度(T)的变化曲线如图所示。
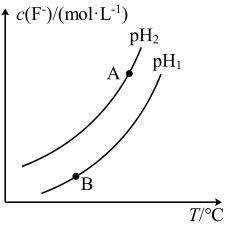
则:pH1____ pH2(“<”,“>”或“=”,下同);A、B两点的溶液中用F-表示的反应速率v(A)____ v(B)。
(4)下列说法正确的是____ 。
(1)NaH2PO4溶液中c(HPO
 )
)(2)25℃时,H2PO
 (aq)+OH-(aq)
(aq)+OH-(aq) HPO
HPO (aq)+H2O(l)的平衡常数K=
(aq)+H2O(l)的平衡常数K=(3)Ca5(PO4)3F(s)+OH-(aq)
 Ca5(PO4)3OH(s)+F-(aq),溶液中c(F-)随溶液的pH和温度(T)的变化曲线如图所示。
Ca5(PO4)3OH(s)+F-(aq),溶液中c(F-)随溶液的pH和温度(T)的变化曲线如图所示。
则:pH1
(4)下列说法正确的是
| A.磷酸溶液中存在3个平衡 |
| B.向pH=2的磷酸溶液中加入NaH2PO4固体,溶液酸性降低 |
C.向NaH2PO4溶液中滴加稀盐酸的过程中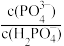 的值增大 的值增大 |
| D.向NaH2PO4溶液中滴加NaOH至过量,水的电离程度先增大后减小 |
您最近一年使用:0次
【推荐1】(1)在粗制MgCl2晶体中常含有杂质Fe2+,在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质最好采用的是_________ (填下面的选项),加入该氧化剂时,温度不能太高,原因是_________ 。
A.KMnO4 B.H2O2 C.HNO3 D.氯水
然后再加入适当物质调节溶液pH,可以达到除去Fe3+而不损失MgCl2的目的,调节溶液pH可选用下列中的有_________ 。
A.Mg2(OH)2CO3 B.MgO C.NH3·H2O D.Mg(OH)2
某溶液中含Mg2+和Fe3+,c(Mg2+)=0.02mol/L,加入双氧水和磷酸(设溶液体积增加1倍),使Fe3+恰好沉淀完全,即溶液中c(Fe3+)=1.0×10-5mol/L,此时是否有Mg3(PO4)2沉淀生成?_________ (FePO4、Mg3(PO4)2的Ksp分别为1.3×10-22、1.0×10-24)
(2)常温下Ksp[Fe(OH)3]=8.0×10−38,Ksp[Cu(OH)2]=3.0×10−20,通常认为残留在溶液中的离子浓度小于1×10−5mol⋅L−1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0mol⋅L−1,为除去溶液中的Fe3+而不影响Cu2+,溶液的pH的范围为_________ 。(已知lg5=0.7)。
(3)矿物中各种原生铜的硫化物经氧化、淋滤后可变成CuSO4溶液,并向内部渗透,遇到深层的闪锌矿(ZnS)和方铅矿(PbS),可慢慢转化为铜蓝(CuS)。写出硫酸铜与ZnS反应的离子方程式为:_________ 。
A.KMnO4 B.H2O2 C.HNO3 D.氯水
然后再加入适当物质调节溶液pH,可以达到除去Fe3+而不损失MgCl2的目的,调节溶液pH可选用下列中的有
A.Mg2(OH)2CO3 B.MgO C.NH3·H2O D.Mg(OH)2
某溶液中含Mg2+和Fe3+,c(Mg2+)=0.02mol/L,加入双氧水和磷酸(设溶液体积增加1倍),使Fe3+恰好沉淀完全,即溶液中c(Fe3+)=1.0×10-5mol/L,此时是否有Mg3(PO4)2沉淀生成?
(2)常温下Ksp[Fe(OH)3]=8.0×10−38,Ksp[Cu(OH)2]=3.0×10−20,通常认为残留在溶液中的离子浓度小于1×10−5mol⋅L−1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0mol⋅L−1,为除去溶液中的Fe3+而不影响Cu2+,溶液的pH的范围为
(3)矿物中各种原生铜的硫化物经氧化、淋滤后可变成CuSO4溶液,并向内部渗透,遇到深层的闪锌矿(ZnS)和方铅矿(PbS),可慢慢转化为铜蓝(CuS)。写出硫酸铜与ZnS反应的离子方程式为:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】锶(Sr)为第五周期第ⅡA族元素,其化合物六水氯化锶(SrCl2·6H2O)是实验室重要的分析试剂,工业上常以天青石(主要成分为SrSO4)为原料制备,生产流程如下:
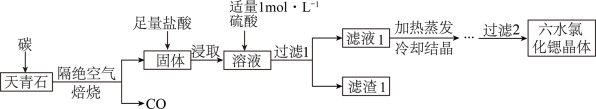
已知:①经盐酸浸取后,溶液中除含有Sr2+和Cl-外,还含有少量Ba2+杂质
②SrSO4、BaSO4的溶度积常数分别为3.3×10-7、1.1×10-10
③SrCl2·6H2O的摩尔质量为267 g·mol-1
(1)工业上天青石焙烧前先研磨粉碎,其目的是___
(2)工业上天青石隔绝空气高温焙烧,若0.5 mol SrSO4中只有硫元素被还原,转移了3 mol电子。写出该反应的化学方程式____
(3)加入硫酸的目的是_____ ;为了提高原料的利用率,滤液1中Sr2+的浓度应不高于__________ mol·L-1(注:此时滤液1中Ba2+浓度为1×10-5 mol·L-1 )。
(4)滤渣1的主要成分是____________ ,滤液1经蒸发浓缩、冷却结晶、过滤后,需对所得的六水氯化锶晶体进行洗涤、干燥。证明六水氯化锶晶体已洗涤干净的实验操作及现象为___________
(5)工业上常通过电解熔融SrCl2制锶单质。由SrCl2·6H2O制取氯化锶的方法是_________

已知:①经盐酸浸取后,溶液中除含有Sr2+和Cl-外,还含有少量Ba2+杂质
②SrSO4、BaSO4的溶度积常数分别为3.3×10-7、1.1×10-10
③SrCl2·6H2O的摩尔质量为267 g·mol-1
(1)工业上天青石焙烧前先研磨粉碎,其目的是
(2)工业上天青石隔绝空气高温焙烧,若0.5 mol SrSO4中只有硫元素被还原,转移了3 mol电子。写出该反应的化学方程式
(3)加入硫酸的目的是
(4)滤渣1的主要成分是
(5)工业上常通过电解熔融SrCl2制锶单质。由SrCl2·6H2O制取氯化锶的方法是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】元素铬(Cr)在自然界主要以+3价和+6价存在。请回答下列问题:
(1)利用铬铁矿(FeO•Cr2O3)冶炼制取金属铬的工艺流程如图所示:
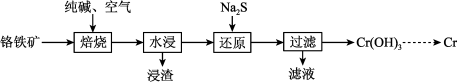
①为加快焙烧速率和提高原料的利用率,可采取的措施之一是___ 。
②浸出液的主要成分为Na2CrO4,向“滤液”中加入酸化的氯化钡溶液有白色沉淀生成,则“还原”操作中发生反应的离子方程式为___ 。
(2)已知25℃时Cr3+恰好完全沉淀时溶液pH为5,(Cr3+浓度降至10-5mol∙L-1可认为完全沉淀)则Cr(OH)3的溶度积常数Ksp=___ 。
(3)用石墨电极电解铬酸钠(Na2CrO4)溶液,可制重铬酸钠(Na2Cr2O7),实验装置如图所示(已知:2CrO42-+2H+ Cr2O72-+H2O)。
Cr2O72-+H2O)。
①电极b连接电源的__ 极(填“正”或“负”),b极发生的电极反应:___ 。
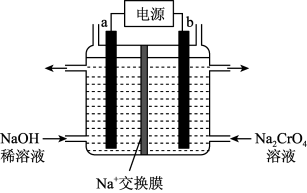
②电解一段时间后,测得阳极区溶液中Na+物质的量由amol变为bmol,则理论上生成重铬酸钠的物质的量是___ mol。
(1)利用铬铁矿(FeO•Cr2O3)冶炼制取金属铬的工艺流程如图所示:

①为加快焙烧速率和提高原料的利用率,可采取的措施之一是
②浸出液的主要成分为Na2CrO4,向“滤液”中加入酸化的氯化钡溶液有白色沉淀生成,则“还原”操作中发生反应的离子方程式为
(2)已知25℃时Cr3+恰好完全沉淀时溶液pH为5,(Cr3+浓度降至10-5mol∙L-1可认为完全沉淀)则Cr(OH)3的溶度积常数Ksp=
(3)用石墨电极电解铬酸钠(Na2CrO4)溶液,可制重铬酸钠(Na2Cr2O7),实验装置如图所示(已知:2CrO42-+2H+
 Cr2O72-+H2O)。
Cr2O72-+H2O)。①电极b连接电源的

②电解一段时间后,测得阳极区溶液中Na+物质的量由amol变为bmol,则理论上生成重铬酸钠的物质的量是
您最近一年使用:0次



