医学上常用酸性 溶液和草酸溶液的反应来测定血钙的含量。测定方法如下:
溶液和草酸溶液的反应来测定血钙的含量。测定方法如下:
①将2.00mL血液用蒸馏水稀释至20.00mL后,向其中加入足量 溶液,反应生成
溶液,反应生成 沉淀,过滤后,将沉淀用足量稀硫酸处理得
沉淀,过滤后,将沉淀用足量稀硫酸处理得 溶液;
溶液;
②将①得到的 溶液装入锥形瓶内,再用
溶液装入锥形瓶内,再用 酸性
酸性 溶液滴定,达到终点时用去
溶液滴定,达到终点时用去 溶液的体积为10.00mL。
溶液的体积为10.00mL。
(1)酸性 溶液与
溶液与 反应的离子方程式为
反应的离子方程式为___________ 。
(2)滴定时,酸性 溶液可盛放在___________中。
溶液可盛放在___________中。
(3)判断滴定终点的颜色变化是___________ 。
(4)实验测得该血液中钙的含量为___________  。
。
(5)若滴定过程中,锥形瓶内液体外溅,将导致测定结果___________ 。
(6)已知:25℃时, 的
的 ,
, 的
的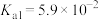 ,
,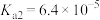 。
。 溶液中,
溶液中,
___________  (填“>”“=”或“<”)。
(填“>”“=”或“<”)。
 溶液和草酸溶液的反应来测定血钙的含量。测定方法如下:
溶液和草酸溶液的反应来测定血钙的含量。测定方法如下:①将2.00mL血液用蒸馏水稀释至20.00mL后,向其中加入足量
 溶液,反应生成
溶液,反应生成 沉淀,过滤后,将沉淀用足量稀硫酸处理得
沉淀,过滤后,将沉淀用足量稀硫酸处理得 溶液;
溶液;②将①得到的
 溶液装入锥形瓶内,再用
溶液装入锥形瓶内,再用 酸性
酸性 溶液滴定,达到终点时用去
溶液滴定,达到终点时用去 溶液的体积为10.00mL。
溶液的体积为10.00mL。(1)酸性
 溶液与
溶液与 反应的离子方程式为
反应的离子方程式为(2)滴定时,酸性
 溶液可盛放在___________中。
溶液可盛放在___________中。| A.酸式滴定管 | B.碱式滴定管 | C.聚四氟乙烯滴定管 | D.锥形瓶 |
(4)实验测得该血液中钙的含量为
 。
。(5)若滴定过程中,锥形瓶内液体外溅,将导致测定结果
(6)已知:25℃时,
 的
的 ,
, 的
的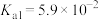 ,
,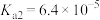 。
。 溶液中,
溶液中,
 (填“>”“=”或“<”)。
(填“>”“=”或“<”)。
更新时间:2024-02-04 11:28:46
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】 是生活中常用的膨松剂,也可作为抑酸剂,更是一种重要的化工原料。
是生活中常用的膨松剂,也可作为抑酸剂,更是一种重要的化工原料。
(1)为探究 溶液的酸碱性,某同学用
溶液的酸碱性,某同学用_______ (填“广泛pH试纸”或“酸度计”)测得25℃ 溶液的pH为8.3,说明
溶液的pH为8.3,说明 的电离程度
的电离程度_______ 水解程度(填“>”或“<”)。
(2)向2支盛有 溶液的试管中,分别加入
溶液的试管中,分别加入 的
的 、
、 溶液,现象如下表:
溶液,现象如下表:
说明 溶液
溶液_______ (填“促进”或“抑制”) 的电离;请写出
的电离;请写出 溶液和
溶液和 溶液反应的离子方程式
溶液反应的离子方程式_______ 。
(3)已知 在水溶液中存在自耦电离平衡:
在水溶液中存在自耦电离平衡: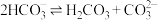
 。以下关于
。以下关于 溶液的说法正确的是_______(填序号)。
溶液的说法正确的是_______(填序号)。
 是生活中常用的膨松剂,也可作为抑酸剂,更是一种重要的化工原料。
是生活中常用的膨松剂,也可作为抑酸剂,更是一种重要的化工原料。(1)为探究
 溶液的酸碱性,某同学用
溶液的酸碱性,某同学用 溶液的pH为8.3,说明
溶液的pH为8.3,说明 的电离程度
的电离程度(2)向2支盛有
 溶液的试管中,分别加入
溶液的试管中,分别加入 的
的 、
、 溶液,现象如下表:
溶液,现象如下表:加入 溶液 溶液 | 加入 溶液 溶液 | |
| 现象 | 有白色沉淀产生 | 有红褐色沉淀、气泡产生 |
 溶液
溶液 的电离;请写出
的电离;请写出 溶液和
溶液和 溶液反应的离子方程式
溶液反应的离子方程式(3)已知
 在水溶液中存在自耦电离平衡:
在水溶液中存在自耦电离平衡: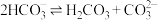
 。以下关于
。以下关于 溶液的说法正确的是_______(填序号)。
溶液的说法正确的是_______(填序号)。A. 的电离方程式为: 的电离方程式为: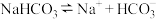 |
B.溶液中 |
C.溶液中 |
D.溶液中 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】运用化学反应原理研究常见元素的单质及其化合物有重要意义。
(1)合成氨反应N2(g)+3H2(g) 2NH3(g),△H<0。若在恒温、恒压条件下向平衡体系中通入氩气,则平衡
2NH3(g),△H<0。若在恒温、恒压条件下向平衡体系中通入氩气,则平衡__________ 移动(填“向左”“向右”或“不”);使用催化剂,上述反应的△H________ (填“增大” “减小” 或“不变”)。
(2)向Na2C2O4溶液加入少量石蕊,溶液显_____ 色,请用离子方程式表示出现该现象的原因:__________________________________ ;
(3)pH相同的氨水和氢氧化钠,分别用蒸馏水稀释至原来溶液的100倍,则稀释后两种溶液的pH分别为m和n,则m______ n(选填“>”“<”“=”);
(4)有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl―NH4Cl为电解质溶液制造新型燃料电池。请写出该电池的正极反应式____________________________ 。
(5)氢气燃烧热值高。实验测得,在常温常压下,4gH2完全燃烧生成液态水,放出571.6kJ热量,则表示H2燃烧热的热化学方程式为____________________ 。
(6)某温度(t℃)时,测得0.01mol・L-1的NaOH溶液的pH=11。在此温度下,将pH=a的H2SO4溶液VaL与pH=b的NaOH溶液VbL混合,若所得混合液为中性,且a+b=12,则Va∶Vb=__________ 。
(1)合成氨反应N2(g)+3H2(g)
 2NH3(g),△H<0。若在恒温、恒压条件下向平衡体系中通入氩气,则平衡
2NH3(g),△H<0。若在恒温、恒压条件下向平衡体系中通入氩气,则平衡(2)向Na2C2O4溶液加入少量石蕊,溶液显
(3)pH相同的氨水和氢氧化钠,分别用蒸馏水稀释至原来溶液的100倍,则稀释后两种溶液的pH分别为m和n,则m
(4)有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl―NH4Cl为电解质溶液制造新型燃料电池。请写出该电池的正极反应式
(5)氢气燃烧热值高。实验测得,在常温常压下,4gH2完全燃烧生成液态水,放出571.6kJ热量,则表示H2燃烧热的热化学方程式为
(6)某温度(t℃)时,测得0.01mol・L-1的NaOH溶液的pH=11。在此温度下,将pH=a的H2SO4溶液VaL与pH=b的NaOH溶液VbL混合,若所得混合液为中性,且a+b=12,则Va∶Vb=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】氮和硫的化合物在工农业生产、生活中具有重要应用。请回答下列问题:
(1)航天领域中常用肼 作为火箭发射的助燃剂。
作为火箭发射的助燃剂。
①已知各共价键键能如下表:
 ;
;
_______  。
。
② 与氨气相似,是一种碱性气体,易溶于水,生成弱碱
与氨气相似,是一种碱性气体,易溶于水,生成弱碱 。用电离方程式表示
。用电离方程式表示 显碱性的原因
显碱性的原因_______ 。
(2)查阅资料可知,常温下,部分弱电解质的电离平衡常数如表:
① 的电离平衡常数的表达式
的电离平衡常数的表达式
_______ ;
②常温下,等浓度的下列溶液a. 溶液;b.
溶液;b. 溶液;c.
溶液;c. 溶液,其
溶液,其 由大到小的顺序是
由大到小的顺序是_______ (用字母表示)。
(3)某同学设计一个肼 燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中
燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中 为阳离子交换膜。
为阳离子交换膜。_______ (填“正极”或“负极”),负极的电极反应式为_______ 。
②若甲中有 氧气(标准状况下)参加反应,乙中通过离子交换膜的阳离子个数为
氧气(标准状况下)参加反应,乙中通过离子交换膜的阳离子个数为____ ,丙中硫酸铜溶液的浓度_______ (填“变大”、“变小”或“不变”)。
(1)航天领域中常用肼
 作为火箭发射的助燃剂。
作为火箭发射的助燃剂。①已知各共价键键能如下表:
 |  |  |  |  | |
键能 | 946 | 497 | 193 | 391 | 463 |
 的结构如图
的结构如图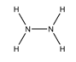
 ;
;
 。
。②
 与氨气相似,是一种碱性气体,易溶于水,生成弱碱
与氨气相似,是一种碱性气体,易溶于水,生成弱碱 。用电离方程式表示
。用电离方程式表示 显碱性的原因
显碱性的原因(2)查阅资料可知,常温下,部分弱电解质的电离平衡常数如表:
| 弱电解质 |  |  |  |
电离平衡常数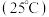 |  | 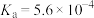 | 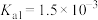 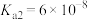 |
 的电离平衡常数的表达式
的电离平衡常数的表达式
②常温下,等浓度的下列溶液a.
 溶液;b.
溶液;b. 溶液;c.
溶液;c. 溶液,其
溶液,其 由大到小的顺序是
由大到小的顺序是(3)某同学设计一个肼
 燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中
燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中 为阳离子交换膜。
为阳离子交换膜。
②若甲中有
 氧气(标准状况下)参加反应,乙中通过离子交换膜的阳离子个数为
氧气(标准状况下)参加反应,乙中通过离子交换膜的阳离子个数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】硫脲(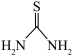 )可用作橡胶的硫化促进剂、金属矿物的浮选剂。已知硫脲易溶于水,易被氧化,受热时部分发生异构化反应而生成硫氰化铵。实验室制备硫脲的装置如图所示(夹持和加热装置略)。
)可用作橡胶的硫化促进剂、金属矿物的浮选剂。已知硫脲易溶于水,易被氧化,受热时部分发生异构化反应而生成硫氰化铵。实验室制备硫脲的装置如图所示(夹持和加热装置略)。

(1)仪器a的名称是
(2)反应开始时,先打开
 ,当观察到
,当观察到 ,这样操作的目的是
,这样操作的目的是(3)装置B中除生成硫脲外,还生成一种碱,写出装置B中发生反应的化学方程式:
(4)装置B反应后的液体经分离、提纯、烘干可得产品。测定产品的纯度:
称取m g产品,加水溶解配成250 mL溶液,取25 mL于锥形瓶中,加入稀硫酸酸化,用
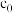 mol⋅L
mol⋅L 酸性
酸性 标准溶液滴定,滴定至终点时消耗标准溶液V mL(已知滴定时,硫脲转化为
标准溶液滴定,滴定至终点时消耗标准溶液V mL(已知滴定时,硫脲转化为 、
、 和
和 ,假设杂质不参与反应)。
,假设杂质不参与反应)。①该实验中滴加酸性
 标准溶液的正确操作是
标准溶液的正确操作是
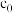 、V的代数式表示)。
、V的代数式表示)。③若滴定前平视酸性
 标准溶液液面读数,滴定后俯视液面读数,计算得到的待测产品纯度比实际纯度
标准溶液液面读数,滴定后俯视液面读数,计算得到的待测产品纯度比实际纯度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】滴定实验是化学学科中重要的定量实验。请回答下列问题:
(1)酸碱中和滴定——用浓度为0.1000 mol·L-1的标准盐酸滴定未知浓度的 溶液,表格中记录了实验数据:
溶液,表格中记录了实验数据:
①下列操作造成测定结果偏高的是_______ (填字母)。
A.滴定终点读数时,俯视滴定管刻度,其他操作正确
B.盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗
C.酸式滴定管用蒸馏水洗净后,未用标准盐酸润洗
D.滴定前,盛装标准液的滴定管尖嘴有气泡,滴定后气泡消失
②该 溶液的物质的量浓度为
溶液的物质的量浓度为_______  (计算结果保留四位有效数字)。
(计算结果保留四位有效数字)。
(2)氧化还原滴定——取一定量的草酸 溶液置于锥形瓶中,加入适量稀硫酸,用标准酸性高锰酸钾溶液滴定。滴定时
溶液置于锥形瓶中,加入适量稀硫酸,用标准酸性高锰酸钾溶液滴定。滴定时 溶液应装在
溶液应装在_______ (填“酸”或“碱”)式滴定管中,滴定终点时滴定现象是_______ 。
(3)沉淀滴定——滴定剂和被滴定物的生成物比滴定剂与指示剂的生成物更难溶。参考表中的数据,若用 滴定
滴定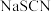 溶液,可选用的指示剂是_______(填字母)。
溶液,可选用的指示剂是_______(填字母)。
(1)酸碱中和滴定——用浓度为0.1000 mol·L-1的标准盐酸滴定未知浓度的
 溶液,表格中记录了实验数据:
溶液,表格中记录了实验数据:| 滴定次数 | 待测液体积/ | 标准盐酸体积/ | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 1.02 | 20.3 |
| 第二次 | 20.00 | 1.00 | 19.99 |
| 第三次 | 20.00 | 0.10 | 22.10 |
A.滴定终点读数时,俯视滴定管刻度,其他操作正确
B.盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗
C.酸式滴定管用蒸馏水洗净后,未用标准盐酸润洗
D.滴定前,盛装标准液的滴定管尖嘴有气泡,滴定后气泡消失
②该
 溶液的物质的量浓度为
溶液的物质的量浓度为 (计算结果保留四位有效数字)。
(计算结果保留四位有效数字)。(2)氧化还原滴定——取一定量的草酸
 溶液置于锥形瓶中,加入适量稀硫酸,用标准酸性高锰酸钾溶液滴定。滴定时
溶液置于锥形瓶中,加入适量稀硫酸,用标准酸性高锰酸钾溶液滴定。滴定时 溶液应装在
溶液应装在(3)沉淀滴定——滴定剂和被滴定物的生成物比滴定剂与指示剂的生成物更难溶。参考表中的数据,若用
 滴定
滴定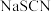 溶液,可选用的指示剂是_______(填字母)。
溶液,可选用的指示剂是_______(填字母)。| 难溶物 |  |  |  |  |  |
| 颜色 | 白 | 浅黄 | 白 | 砖红 | 白 |
 | 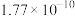 | 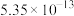 | 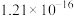 | 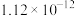 |  |
A. | B. | C. | D. |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】(1)配平氧化还原反应方程式:
C2O42-+____ MnO4-+____ H+=____ CO2↑+____ Mn2++____ H2O
(2)称取6.0 g含H2C2O4·2H2O、KHC2O4和K2SO4的试样,加水溶解,配成250 mL溶液。量取两份此溶液各25 mL,分别置于两个锥形瓶中。
①第一份溶液中加入酚酞试液,滴加0.25 mol·L-1NaOH溶液至20 mL时,溶液由无色变为浅红色。该溶液被中和的H+的总物质的量为________ mol。
②第二份溶液中滴加0.10 mol·L-1的酸性高锰酸钾溶液。
A.KMnO4溶液在滴定过程中作________ (填“氧化剂”或“还原剂”),该滴定过程________ (填“需要”或“不需要”)另加指示剂。滴至16 mL时反应完全,此时溶液颜色由________ 变为__________ 。
B.若在接近终点时,用少量蒸馏水将锥形瓶冲洗一下,再继续滴定至终点,则所测结果__________ (填“偏大”、“偏小”或“无影响”)。
C.若在达到滴定终点时俯视读数,则所得结果________ (填“偏大”、“偏小”或“无影响”)。
③原试样中H2C2O4·2H2O的质量分数为________ ,KHC2O4的质量分数为__________ 。
C2O42-+
(2)称取6.0 g含H2C2O4·2H2O、KHC2O4和K2SO4的试样,加水溶解,配成250 mL溶液。量取两份此溶液各25 mL,分别置于两个锥形瓶中。
①第一份溶液中加入酚酞试液,滴加0.25 mol·L-1NaOH溶液至20 mL时,溶液由无色变为浅红色。该溶液被中和的H+的总物质的量为
②第二份溶液中滴加0.10 mol·L-1的酸性高锰酸钾溶液。
A.KMnO4溶液在滴定过程中作
B.若在接近终点时,用少量蒸馏水将锥形瓶冲洗一下,再继续滴定至终点,则所测结果
C.若在达到滴定终点时俯视读数,则所得结果
③原试样中H2C2O4·2H2O的质量分数为
您最近一年使用:0次



