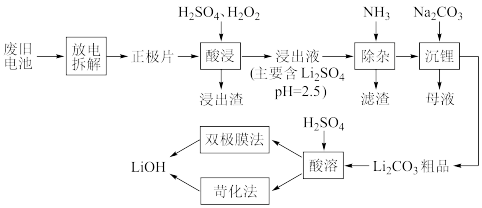
利用以下流程回收废旧电池正极材料(主要含 、
、 等)中
等)中 金属资源.
金属资源.
已知:i. 难溶于水可溶于酸,
难溶于水可溶于酸, 、
、 微溶于水.
微溶于水.
ii.25℃时,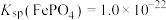 ,
, 的
的 ,
, ,
, .
.
(1)“放电拆解”过程中 从
从__________ (填“正”或“负”,下同)极经电解质溶液移向__________ 极.
(2)“酸浸”过程生成 的化学方程式为
的化学方程式为_________ .
(3)“浸出液”检测出微量 ,此时
,此时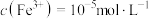 ,则溶液中
,则溶液中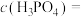
________ .
(4) 溶解度随温度升高而降低.“沉锂”后为提高
溶解度随温度升高而降低.“沉锂”后为提高 的析出量和纯度应进行的操作为
的析出量和纯度应进行的操作为_________ .
(5)“双极膜法”获得 的原理如图.
的原理如图.

① 从
从__________ (选填“一室”“二室”或“三室”)获得.
②该法总反应化学方程式为__________ .
③该法产生可在流程中循环使用的物质为__________ (填化学式).
(6)“苛化法”获得 的流程如图.
的流程如图.
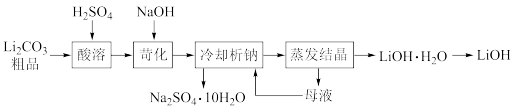
下列有关苛化法和双极膜法说法正确的是____________(填标号).
 、
、 等)中
等)中 金属资源.
金属资源.
已知:i.
 难溶于水可溶于酸,
难溶于水可溶于酸, 、
、 微溶于水.
微溶于水.ii.25℃时,
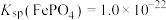 ,
, 的
的 ,
, ,
, .
.(1)“放电拆解”过程中
 从
从(2)“酸浸”过程生成
 的化学方程式为
的化学方程式为(3)“浸出液”检测出微量
 ,此时
,此时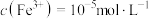 ,则溶液中
,则溶液中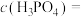
(4)
 溶解度随温度升高而降低.“沉锂”后为提高
溶解度随温度升高而降低.“沉锂”后为提高 的析出量和纯度应进行的操作为
的析出量和纯度应进行的操作为(5)“双极膜法”获得
 的原理如图.
的原理如图.
①
 从
从②该法总反应化学方程式为
③该法产生可在流程中循环使用的物质为
(6)“苛化法”获得
 的流程如图.
的流程如图.
下列有关苛化法和双极膜法说法正确的是____________(填标号).
| A.相较于苛化法,双极膜法工艺更简单 | B.相较于苛化法,双极膜法副产物之一为清洁能源 |
| C.相较于双极膜法,苛化法的产物纯度更高 | D.相较于双极膜法,苛化法耗酸量更少 |
更新时间:2024-02-17 17:08:47
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】草酸钴可用于指示剂和催化剂。一种利用水钴矿(主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO)制取CoC2O4·2H2O的工艺流程如图所示。
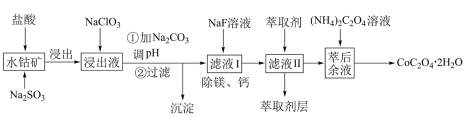
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+;
②常温下,Ksp(MgF2)=6.25×10-9,Ksp(CaF2)=2.25×10-11;
③部分阳离子的氢氧化物形式沉淀时溶液的pH见下表。
回答下列问题:
(1)CoC2O4·2H2O中C的价态为___________ ,Co2O3中Co的价层电子排布式为___________ 。
(2)浸出液中Fe2+与加入NaClO3发生反应的离子方程式为___________ 。
(3)加Na2CO3调节pH时,需要控制pH的范围是___________ ,沉淀1的主要成分有___________ (填化学式)。
(4)常温下,向滤液Ⅰ中加入NaF溶液除去Ca2+、Mg2+,当Ca2+沉淀完全时(离子浓度小于1.0×10-5mol/L即为该离子沉淀完全),Mg2+的浓度为___________ mol/L(保留到小数点后一位)。
(5)测定产品中草酸钴晶体的质量分数:称取草酸钴样品3.050g,用稀硫酸酸化,加入100.0mL0.1000mol/LKMnO4溶液,加热(该条件下Co2+不被氧化),充分反应后将溶液冷却至室温,将溶液完全转移到250mL容量瓶中定容。然后取25mL用0.2000mol/LFeSO4溶液进行滴定,到达滴定终点后,消耗18.00mLFeSO4溶液。
①若用盐酸酸化,则测得的草酸钴晶体的质量分数会___________ (填“偏大”“偏小”或“不变”)。
②计算样品中草酸钴晶体CoC2O4·2H2O的质量分数为___________ 。

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+;
②常温下,Ksp(MgF2)=6.25×10-9,Ksp(CaF2)=2.25×10-11;
③部分阳离子的氢氧化物形式沉淀时溶液的pH见下表。
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | A1(OH)3 | Co(OH)2 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 4.0 | 7.6 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 5.2 | 9.2 | 9.8 |
(1)CoC2O4·2H2O中C的价态为
(2)浸出液中Fe2+与加入NaClO3发生反应的离子方程式为
(3)加Na2CO3调节pH时,需要控制pH的范围是
(4)常温下,向滤液Ⅰ中加入NaF溶液除去Ca2+、Mg2+,当Ca2+沉淀完全时(离子浓度小于1.0×10-5mol/L即为该离子沉淀完全),Mg2+的浓度为
(5)测定产品中草酸钴晶体的质量分数:称取草酸钴样品3.050g,用稀硫酸酸化,加入100.0mL0.1000mol/LKMnO4溶液,加热(该条件下Co2+不被氧化),充分反应后将溶液冷却至室温,将溶液完全转移到250mL容量瓶中定容。然后取25mL用0.2000mol/LFeSO4溶液进行滴定,到达滴定终点后,消耗18.00mLFeSO4溶液。
①若用盐酸酸化,则测得的草酸钴晶体的质量分数会
②计算样品中草酸钴晶体CoC2O4·2H2O的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】软锰矿主要成分为MnO2,还含有CaCO3、Fe2O3、Al2O3等杂质。工业上利用软锰矿制取碳酸锰(MnCO3)流程如下:
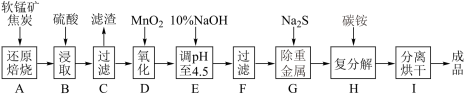
其中,还原焙烧主反应为:2MnO2+C=2MnO+CO2↑。根据要求回答问题:
(1)步骤D中Fe2+被氧化,该反应的离子方程式为______________ 。
(2)步骤H的离子方程式为______________ 。
(3)加入Na2S可以除去Pb2+、Al3+等离子。已知Ksp(PbS)=1×10-28,Ksp(MnS)= 1×10-9.6,当溶液中c(Pb2+)=1×10-5mol·L-1时,溶液中c(Mn2+)允许的最大值为______________ 。
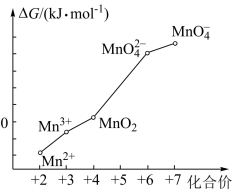
(4)pH=0的溶液中,不同价态锰的微粒的能量(△G)如右图。若某种含锰微粒(如Mn3+)的能量处于相邻价态两种微粒(Mn2+和MnO2)能量连线左上方,则该微粒不稳定并发生歧化反应,转化为相邻价态的微粒。
①MnO 能否稳定存在于pH=0的溶液中?答:
能否稳定存在于pH=0的溶液中?答:______________ (“能”或“不能”);
②将Mn3+歧化反应设计为原电池,可测定反应平衡常数。电池负极反应为________ ,平衡常数表达式为______________ ;
③实验室可利用以下反应检验Mn2+存在:2Mn2++ 5S2O + 8H2O → 16H++ 10SO
+ 8H2O → 16H++ 10SO + 2MnO
+ 2MnO ,确认Mn2+存在的现象是
,确认Mn2+存在的现象是_____________ ;检验时必须控制Mn2+浓度和用量不能过大,否则实验失败。理由是______________ 。

其中,还原焙烧主反应为:2MnO2+C=2MnO+CO2↑。根据要求回答问题:
(1)步骤D中Fe2+被氧化,该反应的离子方程式为
(2)步骤H的离子方程式为
(3)加入Na2S可以除去Pb2+、Al3+等离子。已知Ksp(PbS)=1×10-28,Ksp(MnS)= 1×10-9.6,当溶液中c(Pb2+)=1×10-5mol·L-1时,溶液中c(Mn2+)允许的最大值为

(4)pH=0的溶液中,不同价态锰的微粒的能量(△G)如右图。若某种含锰微粒(如Mn3+)的能量处于相邻价态两种微粒(Mn2+和MnO2)能量连线左上方,则该微粒不稳定并发生歧化反应,转化为相邻价态的微粒。
①MnO
 能否稳定存在于pH=0的溶液中?答:
能否稳定存在于pH=0的溶液中?答:②将Mn3+歧化反应设计为原电池,可测定反应平衡常数。电池负极反应为
③实验室可利用以下反应检验Mn2+存在:2Mn2++ 5S2O
 + 8H2O → 16H++ 10SO
+ 8H2O → 16H++ 10SO + 2MnO
+ 2MnO ,确认Mn2+存在的现象是
,确认Mn2+存在的现象是
您最近一年使用:0次
【推荐3】[Ni(NH3)6]Cl2在有机合成中有广泛应用。以镍废渣(主要含Ni、CuO、FeO、ZnO、Al2O3、MgO、CaCO3和SiO2)为原料制备[Ni(NH3)6]Cl2的工艺流程如下。回答下列问题: 都不能氧化
都不能氧化 。
。
②25℃时,几种氢氧化物和氟化物的 如表所示:
如表所示:
③25℃时,几种金属硫化物的 如表所示:
如表所示:
(1)“酸浸”之前“球磨”,目的是___________ ,“酸浸”时适当加热可以提高反应速率,但是温度过高,速率反而减小,其原因是___________ 。
(2)“除铜锌”时,测得溶液中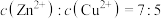 ,最先沉淀的离子是
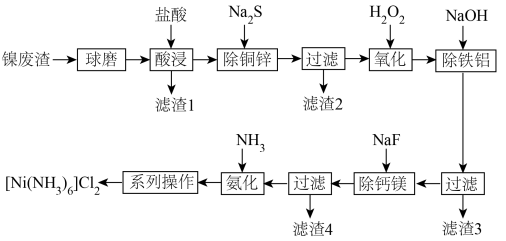
,最先沉淀的离子是___________ (填离子符号,下同),若溶液中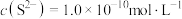 ,此时溶液中被除干净的离子是
,此时溶液中被除干净的离子是___________ (当溶液中某离子的浓度小于或等于 时,认为该离子已被除干净)。
时,认为该离子已被除干净)。
(3)Na2S溶液呈碱性的原因是___________ (用离子方程式表示)。
(4)“除铁铝”中, 时,
时,
___________  。
。
(5)已知常温下, ,则NaF的水解常数
,则NaF的水解常数
___________ ;“除钙镁”时,不能选用玻璃仪器,其原因是___________ 。
 都不能氧化
都不能氧化 。
。②25℃时,几种氢氧化物和氟化物的
 如表所示:
如表所示:| 物质 | Fe(OH)3 | Al(OH)3 | Ni(OH)2 | CaF2 | MgF2 |
 |  | 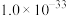 | 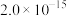 |  |  |
 如表所示:
如表所示:| 金属硫化物 | FeS | NiS | CuS | ZnS |
 | 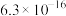 |  |  | 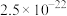 |
(1)“酸浸”之前“球磨”,目的是
(2)“除铜锌”时,测得溶液中
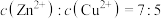 ,最先沉淀的离子是
,最先沉淀的离子是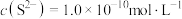 ,此时溶液中被除干净的离子是
,此时溶液中被除干净的离子是 时,认为该离子已被除干净)。
时,认为该离子已被除干净)。(3)Na2S溶液呈碱性的原因是
(4)“除铁铝”中,
 时,
时,
 。
。(5)已知常温下,
 ,则NaF的水解常数
,则NaF的水解常数
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】工业合成氨是人类科学技术的一项重大突破,我国目前氨的生产能力位居世界首位。合成氨反应为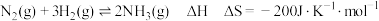 。回答下列问题:
。回答下列问题:
(1)已知 和
和 的燃烧热(
的燃烧热( )分别为
)分别为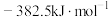 和
和 ,则合成氨反应的
,则合成氨反应的
_______ ;合成氨反应的逆过程能自发进行的最低温度为_______  。
。
(2)在合成氨过程中,需要不断分离出氨的原因为_______ (填字母)。
A.有利于平衡正向移动 B.防止催化剂中毒 C.提高正反应速率
(3)某温度下,在容积为 的恒容密闭容器中模拟工业合成氨,充入
的恒容密闭容器中模拟工业合成氨,充入 和
和 的总物质的量为
的总物质的量为 ,容器内起始压强为标准压强
,容器内起始压强为标准压强 ,容器内各组分的物质的量分数与反应时间
,容器内各组分的物质的量分数与反应时间 的关系如图所示:
的关系如图所示:_______ (填物质名称)的物质的量分数的变化情况。
② 内,平均反应速率
内,平均反应速率
_______  。
。
③达平衡时容器内压强为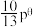 ,则标准平衡常数
,则标准平衡常数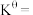
_______ [对于反应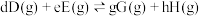 ,标准平衡常数
,标准平衡常数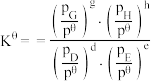 ,其中
,其中 为标准压强,
为标准压强,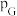 、
、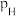 、
、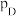 、
、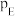 为各组分的平衡分压,分压
为各组分的平衡分压,分压 总压
总压 物质的量分数]。
物质的量分数]。
(4)利用热再生氨电池可实现 电镀废液的浓缩再生。该电池的工作原理如图所示,甲、乙两室均预加相同的
电镀废液的浓缩再生。该电池的工作原理如图所示,甲、乙两室均预加相同的 电镀废液,向甲室中加入足量氨气后电池开始工作。
电镀废液,向甲室中加入足量氨气后电池开始工作。_______ 。
②理论上每转移 电子,乙室中溶液的质量变化为
电子,乙室中溶液的质量变化为_______ g。
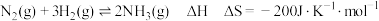 。回答下列问题:
。回答下列问题:(1)已知
 和
和 的燃烧热(
的燃烧热( )分别为
)分别为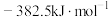 和
和 ,则合成氨反应的
,则合成氨反应的
 。
。(2)在合成氨过程中,需要不断分离出氨的原因为
A.有利于平衡正向移动 B.防止催化剂中毒 C.提高正反应速率
(3)某温度下,在容积为
 的恒容密闭容器中模拟工业合成氨,充入
的恒容密闭容器中模拟工业合成氨,充入 和
和 的总物质的量为
的总物质的量为 ,容器内起始压强为标准压强
,容器内起始压强为标准压强 ,容器内各组分的物质的量分数与反应时间
,容器内各组分的物质的量分数与反应时间 的关系如图所示:
的关系如图所示: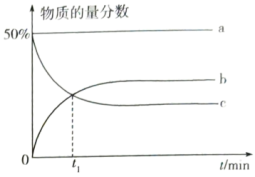
②
 内,平均反应速率
内,平均反应速率
 。
。③达平衡时容器内压强为
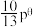 ,则标准平衡常数
,则标准平衡常数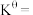
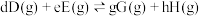 ,标准平衡常数
,标准平衡常数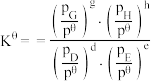 ,其中
,其中 为标准压强,
为标准压强,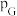 、
、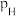 、
、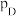 、
、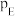 为各组分的平衡分压,分压
为各组分的平衡分压,分压 总压
总压 物质的量分数]。
物质的量分数]。(4)利用热再生氨电池可实现
 电镀废液的浓缩再生。该电池的工作原理如图所示,甲、乙两室均预加相同的
电镀废液的浓缩再生。该电池的工作原理如图所示,甲、乙两室均预加相同的 电镀废液,向甲室中加入足量氨气后电池开始工作。
电镀废液,向甲室中加入足量氨气后电池开始工作。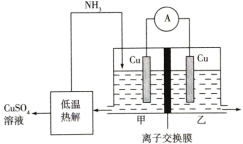
②理论上每转移
 电子,乙室中溶液的质量变化为
电子,乙室中溶液的质量变化为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】X、Y、Z三种短周期元素,其中X元素的原子序数大于Y,且X、Y的氧化物都是形成酸雨的主要物质。Z是地壳中含量最高的金属元素;而地壳中含量最高的非金属元素与X同主族、与Y同周期。
(1)实验室用H2XO4制取XO2气体的化学反应方程式为__________________ 。(请用具体元素符号表示化学式,下同)
(2)t℃时,0.1 mol·L-1的NaHXO3溶液pH=6,该溶液中各离子浓度由大到小顺序排列为__________ 。
(3)请写出Z的氧化物与烧碱溶液反应的离子方程式__________________________ 。
(4)一定条件下,YO与YO2存在下列反应:YO(g)+ YO2(g) Y2O3(g),其平衡常数表达式为K=
Y2O3(g),其平衡常数表达式为K=_______ 。
(5)工业上用氧化YH3法制取YO,该反应的热化学方程式为:
4YH3(g)+5O2(g)=4YO(g)+6H2O(g) △H="-905.8" kJ·mol-1;
已知Y2(g)+O2(g)=2YO(g) △H="+180" kJ·mol-1,则YH3与氧气反应产生两种无污染物质的热化学式为____________________ 。
(6)一定条件下,如图所示装置可实现有机物的电化学储氢(忽略其他有机物)。
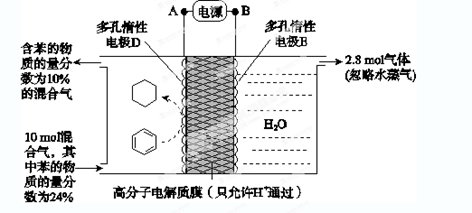
①导线中电子移动方向为________ 。(用A、D表示)
②生成目标产物的电极反应式为__________________ 。
③该储氢装置的电流效率η=____________________ 。
(η=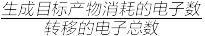 ×100%,计算结果保留小数点后1位)
×100%,计算结果保留小数点后1位)
(1)实验室用H2XO4制取XO2气体的化学反应方程式为
(2)t℃时,0.1 mol·L-1的NaHXO3溶液pH=6,该溶液中各离子浓度由大到小顺序排列为
(3)请写出Z的氧化物与烧碱溶液反应的离子方程式
(4)一定条件下,YO与YO2存在下列反应:YO(g)+ YO2(g)
 Y2O3(g),其平衡常数表达式为K=
Y2O3(g),其平衡常数表达式为K=(5)工业上用氧化YH3法制取YO,该反应的热化学方程式为:
4YH3(g)+5O2(g)=4YO(g)+6H2O(g) △H="-905.8" kJ·mol-1;
已知Y2(g)+O2(g)=2YO(g) △H="+180" kJ·mol-1,则YH3与氧气反应产生两种无污染物质的热化学式为
(6)一定条件下,如图所示装置可实现有机物的电化学储氢(忽略其他有机物)。

①导线中电子移动方向为
②生成目标产物的电极反应式为
③该储氢装置的电流效率η=
(η=
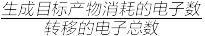 ×100%,计算结果保留小数点后1位)
×100%,计算结果保留小数点后1位)
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】电化学原理在生产生活中运用广泛,下面是常见的一些运用。
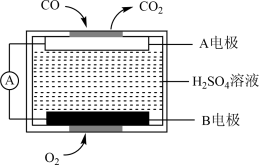
I.汽车尾气中氮氧化合物、碳氧化合物的处理会污染环境,运用电化学方法可以进行NO的消除和CO含量检测。
(1)间接电解法除NO。其原理如图所示,从A口中出来的气体是_______ ,电解池阴极的电极反应式_______ 。用离子方程式表示吸收柱中除去NO的原理_______ 。

(2)用电化学气敏传感器测定汽车尾气中CO含量,原理如图所示,B电极是该电池的_______ (填“正极”或“负极”),A电极上的电极反应式为_______ 。
II.运用电解Na2CO3溶液制备小苏打和烧碱,原理如下图所示。
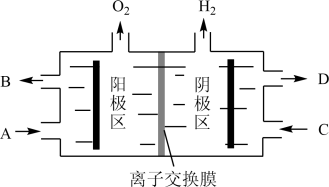
(3)B处排出的溶液主要溶质为_______ 。电解槽中的离子交换膜为_______ (填“阴”或“阳”)离子交换膜,当阳极区收集到1.12L气体(标准状况下),阴极区质量变化_______ g。
III.电解法可用于提纯金属。已知粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(杂质与酸不反应),某小组在实验室条件下以CuSO4溶液为电解液,用电解的方法实现粗铜精炼,并对阳极泥进行回收。
步骤一:电解精炼铜
步骤二:电解完成后,该小组同学按以下流程对电解液进行处理:
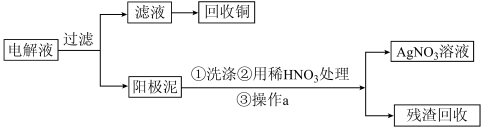
(4)步骤一结束后,电解过程中,CuSO4的浓度会_______ (填“增大”或“不变”或“减小”)
(5)残渣含有少量的黄金,为了回收金,查阅了相关资料(见下表)
从资料中可知,金很难与硝酸反应,但却可溶于王水(浓硝酸与浓盐酸按体积比1:3的混合物)。请从化学平衡的角度解释金能溶于王水的原因_______ 。
I.汽车尾气中氮氧化合物、碳氧化合物的处理会污染环境,运用电化学方法可以进行NO的消除和CO含量检测。
(1)间接电解法除NO。其原理如图所示,从A口中出来的气体是

(2)用电化学气敏传感器测定汽车尾气中CO含量,原理如图所示,B电极是该电池的

II.运用电解Na2CO3溶液制备小苏打和烧碱,原理如下图所示。

(3)B处排出的溶液主要溶质为
III.电解法可用于提纯金属。已知粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(杂质与酸不反应),某小组在实验室条件下以CuSO4溶液为电解液,用电解的方法实现粗铜精炼,并对阳极泥进行回收。
步骤一:电解精炼铜
步骤二:电解完成后,该小组同学按以下流程对电解液进行处理:

(4)步骤一结束后,电解过程中,CuSO4的浓度会
(5)残渣含有少量的黄金,为了回收金,查阅了相关资料(见下表)
| 反应原理 | 化学平衡常数 | |
| 反应1 | Au+6HNO3(浓)⇌Au(NO3)3+3NO2↑+3H2O | <<1 |
| 反应2 | Au3++4Cl-=AuCl | >>1 |
从资料中可知,金很难与硝酸反应,但却可溶于王水(浓硝酸与浓盐酸按体积比1:3的混合物)。请从化学平衡的角度解释金能溶于王水的原因
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】某课外小组探索利用废合金(含有铝、铁、铜)粉末制取纯净的氯化铝溶液、绿矾晶体和胆矾晶体,其实验方案如图:

试回答下列问题:
(1)操作①的名称为_____________ ,所用的玻璃仪器有烧杯、玻璃棒还有____________ 。
(2)写出A→D反应离子方程式____________________ .
(3)滤液E经蒸发浓缩、_______________ 得绿矾晶体。
(4)由滤渣F制CuSO4溶液有途径I和途径Ⅱ两种,你认为最佳途径是_______ ,理由是__________ .
(5)一定温度下,某同学将绿矾配成约0.1mol/L FeSO4溶液,测得溶液的pH=3。请用离子方程式解释原因:____________ ;该溶液中c( )-c(Fe2+)=
)-c(Fe2+)=___________ mol/L(填数值).
(6)若要测定所配溶液中Fe2+的准确浓度,取20.00mL溶液于锥形瓶中,可再直接用下列_________ (填编号)标准溶液进行滴定:
a.0.10mol•L-1 NaOH溶液
b.0.02mol•L-1 KMnO4酸性溶液
c.0.20mol•L-1 KMnO4酸性溶液
d.0.10mol•L-1 KSCN溶液
滴定终点的现象是___________

试回答下列问题:
(1)操作①的名称为
(2)写出A→D反应离子方程式
(3)滤液E经蒸发浓缩、
(4)由滤渣F制CuSO4溶液有途径I和途径Ⅱ两种,你认为最佳途径是
(5)一定温度下,某同学将绿矾配成约0.1mol/L FeSO4溶液,测得溶液的pH=3。请用离子方程式解释原因:
 )-c(Fe2+)=
)-c(Fe2+)=(6)若要测定所配溶液中Fe2+的准确浓度,取20.00mL溶液于锥形瓶中,可再直接用下列
a.0.10mol•L-1 NaOH溶液
b.0.02mol•L-1 KMnO4酸性溶液
c.0.20mol•L-1 KMnO4酸性溶液
d.0.10mol•L-1 KSCN溶液
滴定终点的现象是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐2】工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备高纯硫酸锰,工艺如下图所示。回答下列问题: ]形成氢氧化物沉淀的pH范围如下:
]形成氢氧化物沉淀的pH范围如下:
(1) 的价电子排布式为
的价电子排布式为___________ ,在元素周期表中Zn处于___________ 区。
(2)提高“溶浸”速率,可采取的措施是___________ 。(答一条即可)
(3)“氧化”中添加适量的 的作用是
的作用是___________ 。
(4)“调pH”除铁和铝,溶液的pH范围应调节为___________ ~6之间。
(5)“除杂2”的目的是生成 沉淀除去
沉淀除去 。若溶液酸度过高,
。若溶液酸度过高, 沉淀不完全,原因是
沉淀不完全,原因是___________ 。
(6)电解酸化的硫酸锰溶液可制取二氧化锰,写出电解时阳极的电极反应式___________ 。

 ]形成氢氧化物沉淀的pH范围如下:
]形成氢氧化物沉淀的pH范围如下:| 金属离子 |  |  |  |  |  |  |  |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)
 的价电子排布式为
的价电子排布式为(2)提高“溶浸”速率,可采取的措施是
(3)“氧化”中添加适量的
 的作用是
的作用是(4)“调pH”除铁和铝,溶液的pH范围应调节为
(5)“除杂2”的目的是生成
 沉淀除去
沉淀除去 。若溶液酸度过高,
。若溶液酸度过高, 沉淀不完全,原因是
沉淀不完全,原因是(6)电解酸化的硫酸锰溶液可制取二氧化锰,写出电解时阳极的电极反应式
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】以Al(OH)3、H2SO4、工业硝酸铵(含FeSO4)为原料制备透明氧化铝陶瓷的工艺流程如下:
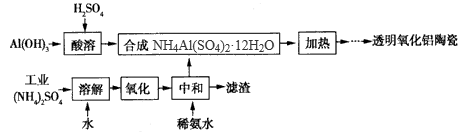
回答下列问题:
(1)氧化步骤中需加入稍过量的氧化剂,下列物质中最合适的是_____ 。
a. NaClOb.H2O2c. KMnO4d.K2Cr2O7
(2)选用上述氧化剂之后,需取少量溶液检验Fe2+是否已全部被氧化,所加试剂为_____ (写名称)。
(3)如何检验中和液中的杂质离子已完全除尽?______________________________ 。
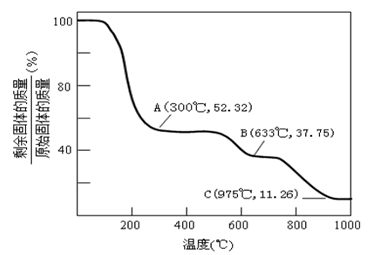
(4)固体NH4Al(SO4)2·12H2O(相对分子质量453)在加热时,固体残留率随温度的变化如图所示。由300℃加热至633℃时发生反应的化学方程式为_________________________________ ;(已知该反应为非氧化还原反应)975℃剩余固体成分的化学式为________________________ 。

回答下列问题:
(1)氧化步骤中需加入稍过量的氧化剂,下列物质中最合适的是
a. NaClOb.H2O2c. KMnO4d.K2Cr2O7
(2)选用上述氧化剂之后,需取少量溶液检验Fe2+是否已全部被氧化,所加试剂为
(3)如何检验中和液中的杂质离子已完全除尽?
(4)固体NH4Al(SO4)2·12H2O(相对分子质量453)在加热时,固体残留率随温度的变化如图所示。由300℃加热至633℃时发生反应的化学方程式为

您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐1】过碳酸钠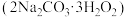 俗称固体双氧水,是由碳酸钠、过氧化氢和水三组分体系利用氢键所形成的不稳定的复合物,高温下容易分解,易溶于水。可以替代过氧化钙作为水产养殖业的供氧剂,给在贮运过程中的鱼、虾等生物供氧保鲜,放氧速率高于过氧化钙。某实验小组模拟工业生产过碳酸钠,装置如图所示。
俗称固体双氧水,是由碳酸钠、过氧化氢和水三组分体系利用氢键所形成的不稳定的复合物,高温下容易分解,易溶于水。可以替代过氧化钙作为水产养殖业的供氧剂,给在贮运过程中的鱼、虾等生物供氧保鲜,放氧速率高于过氧化钙。某实验小组模拟工业生产过碳酸钠,装置如图所示。

(1)装置中仪器A的名称为_______ 。
(2)按图连接好装置后,先将饱和 溶液和稳定剂在三颈烧瓶中混合均匀,再从仪器B中缓慢滴入
溶液和稳定剂在三颈烧瓶中混合均匀,再从仪器B中缓慢滴入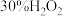 溶液,在磁力搅拌下充分反应。下列物质中,可作为稳定剂使用的是_______。
溶液,在磁力搅拌下充分反应。下列物质中,可作为稳定剂使用的是_______。
(3)反应过程中要控制温度不能太高,原因是________
(4)反应后向混合物中加入 固体,搅拌、静置、过滤、洗涤、低温干燥,得到过碳酸钠固体。加入
固体,搅拌、静置、过滤、洗涤、低温干燥,得到过碳酸钠固体。加入 固体的作用是
固体的作用是________
(5)过碳酸钠样品纯度的测定。
取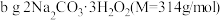 配成
配成 溶液,取
溶液,取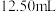 溶液于锥形瓶,加入足量稀硫酸,用
溶液于锥形瓶,加入足量稀硫酸,用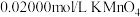 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 (已知:
(已知: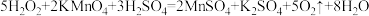 )
)
①实验达到滴定终点的现象是_______ ;
②该过氧碳酸钠的产品纯度为_______ (用字母表示);
③滴定时间过长,测得过碳酸钠产品纯度将_______ (填“偏高”、“偏低”或“无影响”)。
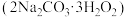 俗称固体双氧水,是由碳酸钠、过氧化氢和水三组分体系利用氢键所形成的不稳定的复合物,高温下容易分解,易溶于水。可以替代过氧化钙作为水产养殖业的供氧剂,给在贮运过程中的鱼、虾等生物供氧保鲜,放氧速率高于过氧化钙。某实验小组模拟工业生产过碳酸钠,装置如图所示。
俗称固体双氧水,是由碳酸钠、过氧化氢和水三组分体系利用氢键所形成的不稳定的复合物,高温下容易分解,易溶于水。可以替代过氧化钙作为水产养殖业的供氧剂,给在贮运过程中的鱼、虾等生物供氧保鲜,放氧速率高于过氧化钙。某实验小组模拟工业生产过碳酸钠,装置如图所示。
(1)装置中仪器A的名称为
(2)按图连接好装置后,先将饱和
 溶液和稳定剂在三颈烧瓶中混合均匀,再从仪器B中缓慢滴入
溶液和稳定剂在三颈烧瓶中混合均匀,再从仪器B中缓慢滴入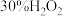 溶液,在磁力搅拌下充分反应。下列物质中,可作为稳定剂使用的是_______。
溶液,在磁力搅拌下充分反应。下列物质中,可作为稳定剂使用的是_______。A. | B. | C. | D. |
(4)反应后向混合物中加入
 固体,搅拌、静置、过滤、洗涤、低温干燥,得到过碳酸钠固体。加入
固体,搅拌、静置、过滤、洗涤、低温干燥,得到过碳酸钠固体。加入 固体的作用是
固体的作用是(5)过碳酸钠样品纯度的测定。
取
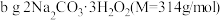 配成
配成 溶液,取
溶液,取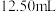 溶液于锥形瓶,加入足量稀硫酸,用
溶液于锥形瓶,加入足量稀硫酸,用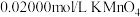 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 (已知:
(已知: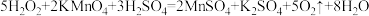 )
)①实验达到滴定终点的现象是
②该过氧碳酸钠的产品纯度为
③滴定时间过长,测得过碳酸钠产品纯度将
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】工业上利用氧化铝基废催化剂(主要成分为Al2O3,还含有少量Pd)回收Al2(SO4)3及Pd的工艺流程如下:

回答下列问题:
(1)氧化铝基废催化剂在焙烧前需粉碎,原因是_________ 。
(2)焙烧时发生反应的化学方程式为_________ 。若焙烧温度过高,则会导致硫酸铵固体分解。其分解产物除NH3、H2O、N2外,还有能使品红溶液褪色的气体。(NH4)2SO4固体高温分解时氧化产物与还原产物的物质的量之比为__________ 。
(3)浸液Y的主要成分的化学式为___________ 。
(4)“热还原”过程中发生反应的化学方程式为___________ 。
(5)Pd是优良的储氢金属,其储氢原理为2Pd(s)+xH2(g)=2PdHx(s),其中 x的最大值为0.80。已知Pd的密度为 12.00g· cm-3,则5.00cm3 Pd能够储存标准状况下H2的最大体积为_____ (精确到 0.01)L。

回答下列问题:
(1)氧化铝基废催化剂在焙烧前需粉碎,原因是
(2)焙烧时发生反应的化学方程式为
(3)浸液Y的主要成分的化学式为
(4)“热还原”过程中发生反应的化学方程式为
(5)Pd是优良的储氢金属,其储氢原理为2Pd(s)+xH2(g)=2PdHx(s),其中 x的最大值为0.80。已知Pd的密度为 12.00g· cm-3,则5.00cm3 Pd能够储存标准状况下H2的最大体积为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,K2FeO4为紫色固体,易溶于水,微溶于浓KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在0℃~5℃、强碱性溶液中较稳定。实验小组制备高铁酸钾(K2FeO4)并探究其性质。
Ⅰ.湿法制备K2FeO4
(1)制备NaClO,实验装置如图。玻璃管a的作用是___________ 。

(2)制备K2FeO4晶体
第一步:将制得的NaClO(含NaOH)饱和溶液与FeCl3饱和溶液的混合溶液,具体做法是:边搅拌,边将___________ 缓慢滴加到___________ 中得Na2FeO4;相关化学方程式___________ 。
第二步:加入适量KOH固体至饱和,得湿产品;
第三步:洗涤、干燥,得K2FeO4晶体。
II.提纯K2FeO4
(3)粗产品[含有Fe(OH)3、NaCl、KCl等杂质]的实验方案为:将一定量的K2FeO4粗产品溶于冷的3mol·L-1KOH溶液中,___________ 。(实验中须使用的试剂有:饱和KOH溶液,乙醇,真空干燥器)。
Ⅲ.测定K2FeO4纯度
(4)通过以下方法测定高铁酸钾样品的纯度:称取0.6000g高铁酸钾样品,完全溶解于浓KOH溶液中,再加入足量亚铬酸钾{K[Cr(OH)4]}反应后配成100.00mL溶液;取上述溶液20.00mL于锥形瓶中,加入稀硫酸调至pH=2,用0.1000mol·L-1硫酸亚铁铵溶液滴定,消耗标准硫酸亚铁铵溶液15.00mL。测定过程中发生反应:
a.Cr(OH) +FeO
+FeO =Fe(OH)3+CrO
=Fe(OH)3+CrO +OH-
+OH-
b.2CrO +2H+=Cr2O
+2H+=Cr2O +H2O
+H2O
c.Cr2O +6Fe2+=14H+=2Cr3+6Fe3++7H2O
+6Fe2+=14H+=2Cr3+6Fe3++7H2O
计算K2FeO4样品的纯度(写出计算过程)。___________
Ⅰ.湿法制备K2FeO4
(1)制备NaClO,实验装置如图。玻璃管a的作用是

(2)制备K2FeO4晶体
第一步:将制得的NaClO(含NaOH)饱和溶液与FeCl3饱和溶液的混合溶液,具体做法是:边搅拌,边将
第二步:加入适量KOH固体至饱和,得湿产品;
第三步:洗涤、干燥,得K2FeO4晶体。
II.提纯K2FeO4
(3)粗产品[含有Fe(OH)3、NaCl、KCl等杂质]的实验方案为:将一定量的K2FeO4粗产品溶于冷的3mol·L-1KOH溶液中,
Ⅲ.测定K2FeO4纯度
(4)通过以下方法测定高铁酸钾样品的纯度:称取0.6000g高铁酸钾样品,完全溶解于浓KOH溶液中,再加入足量亚铬酸钾{K[Cr(OH)4]}反应后配成100.00mL溶液;取上述溶液20.00mL于锥形瓶中,加入稀硫酸调至pH=2,用0.1000mol·L-1硫酸亚铁铵溶液滴定,消耗标准硫酸亚铁铵溶液15.00mL。测定过程中发生反应:
a.Cr(OH)
 +FeO
+FeO =Fe(OH)3+CrO
=Fe(OH)3+CrO +OH-
+OH-b.2CrO
 +2H+=Cr2O
+2H+=Cr2O +H2O
+H2Oc.Cr2O
 +6Fe2+=14H+=2Cr3+6Fe3++7H2O
+6Fe2+=14H+=2Cr3+6Fe3++7H2O计算K2FeO4样品的纯度(写出计算过程)。
您最近一年使用:0次



