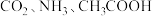 是中学化学中常见的物质,常温下,有关物质的电离常数如下表:
是中学化学中常见的物质,常温下,有关物质的电离常数如下表:| 物质 |  |  |  |
| 电离常数 |  、 、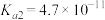 |  |  |
(1)
 是一种温室气体,在“双碳”目标的形势下,工业生产中产生的
是一种温室气体,在“双碳”目标的形势下,工业生产中产生的 可用氨水吸收富集,氨水吸收
可用氨水吸收富集,氨水吸收 后的溶液中存在的离子有
后的溶液中存在的离子有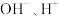 、
、(2)
 在水溶液中的电离方程式是
在水溶液中的电离方程式是已知
 ,则常温下
,则常温下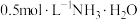 溶液的
溶液的
(3)
 (标准状况)
(标准状况) 与
与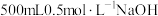 溶液充分反应,该反应的离子方程式是
溶液充分反应,该反应的离子方程式是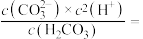
(4)常温下,
 水溶液的
水溶液的
更新时间:2024-02-22 14:59:31
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室常用加热铵盐和碱的混合物的方法制取氨气。
(1)写出图中大试管中发生反应的化学方程式______________________________ 。

(2)收集氨气时,判断氨气是否收集满可采用的方法是_________________________ 。
(3)也可利用加热浓氨水的方法制取少量的氨气,此法利用了氨水的________ 性质。将收集满氨气的烧瓶组装成如图所示的装置。

当挤压胶头滴管,使少量的水进入烧瓶,打开弹簧夹可以观察到的现象是:_______________ 。
(1)写出图中大试管中发生反应的化学方程式

(2)收集氨气时,判断氨气是否收集满可采用的方法是
(3)也可利用加热浓氨水的方法制取少量的氨气,此法利用了氨水的

当挤压胶头滴管,使少量的水进入烧瓶,打开弹簧夹可以观察到的现象是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氮元素的单质和化合物在生活生产中有广泛用途。
(1)氮分子中化学键名称是_______ ;氮分子的电子式为:_______ ;已知 分子与
分子与 分子结构相似,
分子结构相似, 熔点高于
熔点高于 ,其原因是(从化学键和晶体的角度用文字表述原因)
,其原因是(从化学键和晶体的角度用文字表述原因)_______ 。
(2)如图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。
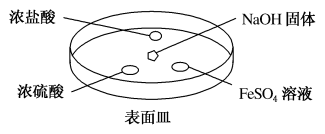
浓盐酸液滴附近会出现白烟,发生反应的化学方程式为_______ ;浓硫酸液滴上方没有明显现象,一段时间后浓硫酸的液滴中有白色固体,其中所含的正盐作为一种化肥俗称:_______ ,长期施用容易造成土壤酸化板结; 液滴中先出现灰绿色沉淀,一段时间后变成红褐色,发生的化学方程式分别是
液滴中先出现灰绿色沉淀,一段时间后变成红褐色,发生的化学方程式分别是_______ 和_______ 。
(3)将氨通入水中溶液呈碱性的原因(用方程式表示)_______ 。
(4)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),写出反应的化学方程式并用单线桥标出电子转移方向和数目_______ ,该反应中被氧化的元素是_______ ,还原产物是_______ 。若反应中有3mol电子发生转移,参与反应的氨的质量为_______ g。
(1)氮分子中化学键名称是
 分子与
分子与 分子结构相似,
分子结构相似, 熔点高于
熔点高于 ,其原因是(从化学键和晶体的角度用文字表述原因)
,其原因是(从化学键和晶体的角度用文字表述原因)(2)如图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。

浓盐酸液滴附近会出现白烟,发生反应的化学方程式为
 液滴中先出现灰绿色沉淀,一段时间后变成红褐色,发生的化学方程式分别是
液滴中先出现灰绿色沉淀,一段时间后变成红褐色,发生的化学方程式分别是(3)将氨通入水中溶液呈碱性的原因(用方程式表示)
(4)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),写出反应的化学方程式并用单线桥标出电子转移方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)写出工业冶炼金属钠的化学方程式:___________ 。
(2)写出氨在催化剂作用下被O2氧化的化学方程式:___________ ;写出向AlCl3溶液中滴加过量氨水的离子方程式:___________ 。
(3)蓝铜矿的主要成分为2CuCO3·Cu(OH)2,将它与焦炭一起加热时,可以产生Cu、CO2和H2O。请写出该反应的化学方程式:___________ 。
(4)溴主要以Br-形式存在于海水中,工业上一种制备Br2的操作步骤为:
①一定条件下,将Cl2通入浓缩的海水中,生成Br2
②利用热空气将Br2吹出,并用浓Na2CO3溶液吸收,生成NaBr、NaBrO3等
③用硫酸酸化步骤②得到的混合物。
步骤②用浓Na2CO3溶液吸收的目的是___________ ;
步骤③所发生的化学反应方程式为:___________ 。
(2)写出氨在催化剂作用下被O2氧化的化学方程式:
(3)蓝铜矿的主要成分为2CuCO3·Cu(OH)2,将它与焦炭一起加热时,可以产生Cu、CO2和H2O。请写出该反应的化学方程式:
(4)溴主要以Br-形式存在于海水中,工业上一种制备Br2的操作步骤为:
①一定条件下,将Cl2通入浓缩的海水中,生成Br2
②利用热空气将Br2吹出,并用浓Na2CO3溶液吸收,生成NaBr、NaBrO3等
③用硫酸酸化步骤②得到的混合物。
步骤②用浓Na2CO3溶液吸收的目的是
步骤③所发生的化学反应方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】25 ℃时,部分物质的电离平衡常数如下表所示:
(1)NH3·H2O的电离方程式是_____________ ,25 ℃时,物质的量浓度为0.10 mol/L的氨水中,c(OH-)=___________ (列出算式即可)。
(2)25 ℃时,物质的量浓度相等的CH3COONa溶液和NaClO溶液pH大小关系是:CH3COONa________ (填“>”“<”或“=”)NaClO,请结合题目有关信息说明原因__________ 。
(3)向NaClO溶液中通入少量二氧化碳气体,发生反应的离子方程式是_____ ,结合所给数据说明生成该产物的理由__________ 。
化学式 | CH3COOH | H2CO3 | HClO | NH3·H2O |
电离平 衡常数 | Ka=1.75×10-5 | Ka1=4.5×10-7 Ka2=4.7×10-11 | Ka=3.0×10-8 | Kb=1.8×10-5 |
(2)25 ℃时,物质的量浓度相等的CH3COONa溶液和NaClO溶液pH大小关系是:CH3COONa
(3)向NaClO溶液中通入少量二氧化碳气体,发生反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表是几种弱电解质的电离平衡常数、难溶电解质的溶度积Ksp(25℃)。
回答下列问题:
(1)由上表分析,若①CH3COOH,②HCO3-,③C6H5OH,④H2PO4-均可看做酸,则它们酸性由强到弱的顺序为_____________ (填编号)。
(2)写出C6H5OH与Na3PO4反应的离子方程式_______________________________ 。
(3)25℃时,将等体积等浓度的醋酸和氨水混合,混合液中:c(CH3COO-)____ c(NH4+)(填“>”、“=”或“<”)。
(4)25℃时,向10mL0.01mol/L苯酚溶液中滴加VmL0.01mol/L氨水,混合液中粒子浓度关系正确的是__________ (填字母序号)。
A.若混合液pH>7,则V≥10
B.若混合液 pH<7,则c(NH4+)>c(C6H5O-)>c(H+)>c(OH-)
C.V=10时,混合液中水的电离程度小于10mL0.01mol/L苯酚溶液中水的电离程度
D.V= 5时,2c(NH3·H2O)+2c(NH4+)=c(C6H5O-)+c(C6H5OH)
(5)水解反应是典型的可逆反应,水解反应的化学平衡常数称为水解常数(用Kb表示),类比化学平衡常数的定义,请写出Na2CO3第一步水解反应的水解常数的表达式:____________ 。
(6)I,如图所示,有T1、T2两种温度下两条BaSO4在水中的沉淀溶解平衡曲线,回答下列问题:
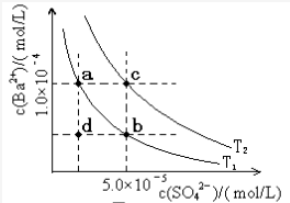
①T1______ T2(填“>”、“=”或‘‘<”),T2温度时 Ksp(BaSO4)=_______________ ;
②讨论T1温度时BaSO4的沉淀溶解平衡曲线,下列说法正确的是______ (填字母序号)。
A.加入Na2SO4可使溶液由a点变为b点
B.在T1曲线上方区域(不含曲线)任意一点时,均有BaSO4沉淀生成
C.蒸发溶剂可能使溶液由d点变为曲线上a,b之间的某一点(不含a,b)
D.升温可使溶液由b点变为d点
II.现有0.2mol的BaSO4沉淀,每次用1L饱和Na2CO3溶液(浓度为1.7mol/L)处理。若使BaSO4中的SO42-全部转化到溶液中,需要反复处理_____ 次。[提示:BaSO4(s)+CO32-(aq) BaCO3(s)+SO42-(aq)]
BaCO3(s)+SO42-(aq)]
| 电解质 | 电离方程式 | 电离常数K或Ksp |
| CH3COOH | CH3COO CH3COO-+H+ CH3COO-+H+ | 1.76×10-5 |
| H2CO3 | H2CO3 H++HCO3- H++HCO3-HCO3-  H++CO32- H++CO32- | K1=4.31×10-7 K2=5.61×10-11 |
| C6H5OH | C6H5OH C6H5O-+H+ C6H5O-+H+ | 1.1×10-10 |
| H3PO4 | H3PO4  H++H2PO4- H++H2PO4-H2PO4-  H++HPO42- H++HPO42-HPO42-  H++PO43- H++PO43- | K1=7.52×10-3 K2=6.23×10-8 K3=2.20×10-13 |
| NH3·H2O | NH3·H2O NH4++OH- NH4++OH- | 1.76×10-5 |
| BaSO4 | BaSO4(s) Ba2+(aq)+SO42-(aq) Ba2+(aq)+SO42-(aq) | 1.07×10-10 |
| BaCO3 | BaCO3(s) Ba2+(aq)+CO2-(aq) Ba2+(aq)+CO2-(aq) | 2.58×10-9 |
回答下列问题:
(1)由上表分析,若①CH3COOH,②HCO3-,③C6H5OH,④H2PO4-均可看做酸,则它们酸性由强到弱的顺序为
(2)写出C6H5OH与Na3PO4反应的离子方程式
(3)25℃时,将等体积等浓度的醋酸和氨水混合,混合液中:c(CH3COO-)
(4)25℃时,向10mL0.01mol/L苯酚溶液中滴加VmL0.01mol/L氨水,混合液中粒子浓度关系正确的是
A.若混合液pH>7,则V≥10
B.若混合液 pH<7,则c(NH4+)>c(C6H5O-)>c(H+)>c(OH-)
C.V=10时,混合液中水的电离程度小于10mL0.01mol/L苯酚溶液中水的电离程度
D.V= 5时,2c(NH3·H2O)+2c(NH4+)=c(C6H5O-)+c(C6H5OH)
(5)水解反应是典型的可逆反应,水解反应的化学平衡常数称为水解常数(用Kb表示),类比化学平衡常数的定义,请写出Na2CO3第一步水解反应的水解常数的表达式:
(6)I,如图所示,有T1、T2两种温度下两条BaSO4在水中的沉淀溶解平衡曲线,回答下列问题:

①T1
②讨论T1温度时BaSO4的沉淀溶解平衡曲线,下列说法正确的是
A.加入Na2SO4可使溶液由a点变为b点
B.在T1曲线上方区域(不含曲线)任意一点时,均有BaSO4沉淀生成
C.蒸发溶剂可能使溶液由d点变为曲线上a,b之间的某一点(不含a,b)
D.升温可使溶液由b点变为d点
II.现有0.2mol的BaSO4沉淀,每次用1L饱和Na2CO3溶液(浓度为1.7mol/L)处理。若使BaSO4中的SO42-全部转化到溶液中,需要反复处理
 BaCO3(s)+SO42-(aq)]
BaCO3(s)+SO42-(aq)]
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】硫化氢气体是一种剧毒气体,易溶于水形成酸性溶液。查阅得,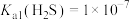 ,
, ;
;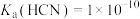 。按所给信息回答下列问题。
。按所给信息回答下列问题。
(1)书写 第二步电离方程式:
第二步电离方程式:_______ 。
(2)向 的
的 溶液中加入等浓度的
溶液中加入等浓度的 时,电离平衡向
时,电离平衡向_______ 移动(填“左”或“右”),混合溶液中
_______ 。(填“增大”、“减小”或“不变”)
(3)能证明 酸性强于
酸性强于 的是:_______。
的是:_______。
(4)下列反应不能发生的是_______ (填字母)。
a. b.
b.
c. d.
d.
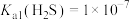 ,
, ;
;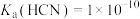 。按所给信息回答下列问题。
。按所给信息回答下列问题。(1)书写
 第二步电离方程式:
第二步电离方程式:(2)向
 的
的 溶液中加入等浓度的
溶液中加入等浓度的 时,电离平衡向
时,电离平衡向
(3)能证明
 酸性强于
酸性强于 的是:_______。
的是:_______。A.相同温度下,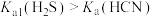 |
| B.溶液能使紫色石蕊试液变红 |
C.等浓度、等体积的 溶液和 溶液和 溶液分别与等浓度的 溶液分别与等浓度的 溶液反应, 溶液反应, 消耗的 消耗的 溶液体积更多 溶液体积更多 |
D.常温下,将 气体通入 气体通入 溶液有 溶液有 生成 生成 |
a.
 b.
b.
c.
 d.
d.
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】根据电离平衡常数(用Ka表示)的大小可以判断弱电解质的相对强弱。25℃时,有关物质的电离平衡常数如下表所示:
(1)25℃时,H2S、HClO、H2CO3、H2SO3的酸性由强到弱的顺序为:_______ 。
(2)25℃时,0.01mol·L-1的HClO溶液中的c(H+)为_______ ,将此HClO溶液加水稀释(设温度不变),下列各量增大的是_______ (填写字母)。
A.c(H+) B.c(H+)·c(OH-) C. D.
D.
(3)相同条件下,0.1mol·L-1下列溶液中,pH最大的是_______。
(4)根据H2SO3的电离平衡常数计算25℃时0.06mol·L-1Na2SO3溶液的pH=_______ 。(忽略 的第二步水解)
的第二步水解)
(5)25℃时,向NaClO溶液中通入少量CO2,发生反应的离子方程式为_______ 。
| 酸 | H2S | HClO | H2CO3 | H2SO3 |
| 电离平衡常数(25℃) | Ka1=1.1×10-7Ka2=1.3×10-13 | Ka1=4.0×10-8 | Ka1=4.5×10-7 Ka2=4.7×10-11 | Ka1=1.4×10-2 Ka2=6.0×10-8 |
(2)25℃时,0.01mol·L-1的HClO溶液中的c(H+)为
A.c(H+) B.c(H+)·c(OH-) C.
 D.
D.
(3)相同条件下,0.1mol·L-1下列溶液中,pH最大的是_______。
| A.NaHSO4 | B.NaCl | C.Na2CO3 | D.Na2SO3 |
 的第二步水解)
的第二步水解)(5)25℃时,向NaClO溶液中通入少量CO2,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有以下物质:①氯化铁溶液 ②干冰 ③冰醋酸 ④亚硫酸钠晶体 ⑤液态氯化氢 ⑥纯蔗糖 ⑦硫酸铝晶体 ⑧熔融的氢氧化钡 ⑨硫酸氢钠溶液
(1)其中,能导电的是:___ ;属于电解质的是:___ ;属于非电解质的是:___ 。
(2)写出下列几种物质在水溶液中的电离方程式:
硫酸氢钠_____ ;亚硫酸______ ;硫氢化钠_____ ;氢氧化钡_____ ;
(3)将上述的①⑦的水溶液加热并蒸干,其中能得到相应的盐的是____ (填序号);不能得到相应盐的溶液,加热蒸干并灼烧后的产物为_____ 。
(4)⑦在日常生活中经常可见,其中,泡沫灭火器中的一种液体为硫酸铝溶液,另一种为碳酸氢钠溶液,倒置使这两种液体混合后,即可产生大量的泡沫,请用离子方程式描述这一过程___ 。
(1)其中,能导电的是:
(2)写出下列几种物质在水溶液中的电离方程式:
硫酸氢钠
(3)将上述的①⑦的水溶液加热并蒸干,其中能得到相应的盐的是
(4)⑦在日常生活中经常可见,其中,泡沫灭火器中的一种液体为硫酸铝溶液,另一种为碳酸氢钠溶液,倒置使这两种液体混合后,即可产生大量的泡沫,请用离子方程式描述这一过程
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题
(1)用离子方程式解释NH4Cl呈酸性的原因:_______
(2)25℃时,pH均为2的三种酸的电离平衡常数如下表:
试回答下列问题:
①下列四种离子结合质子能力最强的是___________ (填序号)。
a. b.ClO- c.CH3COO- d.
b.ClO- c.CH3COO- d.
②常温下将CH3COOH溶液加水稀释过程中,下列表达式的数据一定变大的是___________ 。
A. B.
B. C.
C. D .
D . E.
E.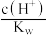
③体积均为10 mL,pH均为2的醋酸溶液与HX溶液分别加水稀释至1000 mL,稀释过程中pH变化如图所示。
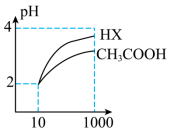
稀释后,HX溶液中水电离出来的c(H+)___________ (填“>”、“<”或“=”)醋酸溶液中水电离出来的c(H+);CH3COOH的电离平衡常数___________ (填“>”、“<”或“=”)HX的电离平衡常数,理由是___________ 。
(1)用离子方程式解释NH4Cl呈酸性的原因:
(2)25℃时,pH均为2的三种酸的电离平衡常数如下表:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 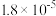 |  、 、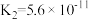 |  |
①下列四种离子结合质子能力最强的是
a.
 b.ClO- c.CH3COO- d.
b.ClO- c.CH3COO- d.
②常温下将CH3COOH溶液加水稀释过程中,下列表达式的数据一定变大的是
A.
 B.
B. C.
C. D .
D . E.
E.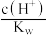
③体积均为10 mL,pH均为2的醋酸溶液与HX溶液分别加水稀释至1000 mL,稀释过程中pH变化如图所示。

稀释后,HX溶液中水电离出来的c(H+)
您最近一年使用:0次



