回答下列问题
(1)用离子方程式解释NH4Cl呈酸性的原因:_______
(2)25℃时,pH均为2的三种酸的电离平衡常数如下表:
试回答下列问题:
①下列四种离子结合质子能力最强的是___________ (填序号)。
a. b.ClO- c.CH3COO- d.
b.ClO- c.CH3COO- d.
②常温下将CH3COOH溶液加水稀释过程中,下列表达式的数据一定变大的是___________ 。
A. B.
B. C.
C. D .
D . E.
E.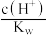
③体积均为10 mL,pH均为2的醋酸溶液与HX溶液分别加水稀释至1000 mL,稀释过程中pH变化如图所示。
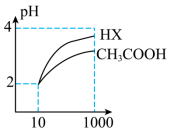
稀释后,HX溶液中水电离出来的c(H+)___________ (填“>”、“<”或“=”)醋酸溶液中水电离出来的c(H+);CH3COOH的电离平衡常数___________ (填“>”、“<”或“=”)HX的电离平衡常数,理由是___________ 。
(1)用离子方程式解释NH4Cl呈酸性的原因:
(2)25℃时,pH均为2的三种酸的电离平衡常数如下表:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 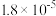 |  、 、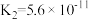 |  |
①下列四种离子结合质子能力最强的是
a.
 b.ClO- c.CH3COO- d.
b.ClO- c.CH3COO- d.
②常温下将CH3COOH溶液加水稀释过程中,下列表达式的数据一定变大的是
A.
 B.
B. C.
C. D .
D . E.
E.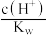
③体积均为10 mL,pH均为2的醋酸溶液与HX溶液分别加水稀释至1000 mL,稀释过程中pH变化如图所示。

稀释后,HX溶液中水电离出来的c(H+)
更新时间:2024-03-21 12:36:56
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】为了证明一水合氨(NH3·H2O)是弱电解质,常温下,甲、乙、丙三人分别选用下列试剂进行实验:0.010 mol·L-1氨水、NH4Cl溶液、NH4Cl晶体、酚酞试剂、pH试纸、蒸馏水。
(1)甲用pH试纸测出0.010 mol·L-1氨水的pH为10,则认定NH3·H2O是弱电解质,你认为这一方法____ (填“正确”或“不正确”),理由是___________________________ 。
(2)乙取出10 mL 0.010 mol·L-1氨水,用pH试纸测出其pH=a,然后用蒸馏水稀释至1 000 mL,再用pH试纸测出其pH=b,若要确认NH3·H2O是弱电解质,则a、b应满足的关系为________ (用等式或不等式表示)。
(3)丙取出10 mL 0.010 mol·L-1氨水,滴入2滴酚酞溶液,显粉红色,再加入NH4Cl晶体少量,颜色变____ (填“深”或“浅”)。你认为这一方法____ (填“能”或“不能”)证明NH3·H2O是弱电解质,原因是________ 。
(1)甲用pH试纸测出0.010 mol·L-1氨水的pH为10,则认定NH3·H2O是弱电解质,你认为这一方法
(2)乙取出10 mL 0.010 mol·L-1氨水,用pH试纸测出其pH=a,然后用蒸馏水稀释至1 000 mL,再用pH试纸测出其pH=b,若要确认NH3·H2O是弱电解质,则a、b应满足的关系为
(3)丙取出10 mL 0.010 mol·L-1氨水,滴入2滴酚酞溶液,显粉红色,再加入NH4Cl晶体少量,颜色变
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.已知:在相同条件下醋酸与氨水电离程度相同,现有浓度均为0.1mol/L的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸铵、⑦硫酸氢铵、⑧氨水。
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是 填序号
填序号
____ 。
(2)若④、⑤、⑥、⑦、⑧五种溶液中NH 浓度相等,则五种溶液的物质的量浓度由大到小的顺序是
浓度相等,则五种溶液的物质的量浓度由大到小的顺序是 填序号
填序号
___ 。
Ⅱ 已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
(3)pH相等的下列溶液,它们的物质的量浓度由大到小排列的顺序是____ (用编号填写)
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(4)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:____ 。
(5)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO-)-c(Na+)=____ (填准确数值 。
。
(6)25℃时,将amol•L-1的醋酸与bmol•L-1氢氧化钠等体积混合,反应后溶液恰好显中性,用a、b表示醋酸的电离平衡常数为____ 。
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是
 填序号
填序号
(2)若④、⑤、⑥、⑦、⑧五种溶液中NH
 浓度相等,则五种溶液的物质的量浓度由大到小的顺序是
浓度相等,则五种溶液的物质的量浓度由大到小的顺序是 填序号
填序号
Ⅱ
 已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | Ka=1.8×10-5 | Ka1=4,.3×10-7 Ka2=5.6×10-11 | Ka=3.0×10-8 |
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(4)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:
(5)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO-)-c(Na+)=
 。
。(6)25℃时,将amol•L-1的醋酸与bmol•L-1氢氧化钠等体积混合,反应后溶液恰好显中性,用a、b表示醋酸的电离平衡常数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】砷(As)位于元素周期表的第四行与氮、磷同列。砷有多种化合物,用途广泛。完成下列填空:
(1)写出砷原子核外最外层电子的电子排布式。_______ 。
(2)1个砷的氢化物分子中含_______ 个化学键。
(3)砷化镓(GaAs)和氮化镓(GaN)都是原子间以共价键结合而成的晶体。GaAs熔点为1238°C、GaN熔点为1500°C,GaAs熔点低于GaN的原因是_______ 。
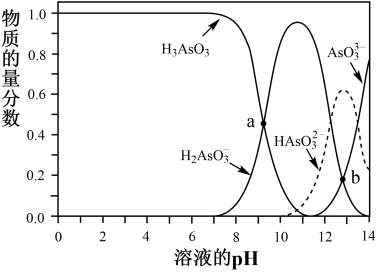
亚砷酸(H3AsO3) 可以用于治疗白血病。25°C,向0.1mol·L-1 H3AsO3溶液中滴加0.1mol·L-1KOH溶液,各种微粒的物质的量分数与溶液pH的关系如图所示。
(4)人体血液的pH在7.35~7.45,患者用药后人体中含砷元素的主要微粒是_______ 。
(5)25°C,H2AsO 电离程度小于水解程度,依据是:
电离程度小于水解程度,依据是: _______ 。
(6)以酚酞为指示剂,将KOH溶液滴入H3AsO3溶液中,滴定终点的离子方程式是_______ 。
(7)b点溶液中:c(K+)_______ 2c(HAsO )+4c(AsO
)+4c(AsO ) (选填 “<”“>”或“=”)
) (选填 “<”“>”或“=”)
(1)写出砷原子核外最外层电子的电子排布式。
(2)1个砷的氢化物分子中含
(3)砷化镓(GaAs)和氮化镓(GaN)都是原子间以共价键结合而成的晶体。GaAs熔点为1238°C、GaN熔点为1500°C,GaAs熔点低于GaN的原因是
亚砷酸(H3AsO3) 可以用于治疗白血病。25°C,向0.1mol·L-1 H3AsO3溶液中滴加0.1mol·L-1KOH溶液,各种微粒的物质的量分数与溶液pH的关系如图所示。

(4)人体血液的pH在7.35~7.45,患者用药后人体中含砷元素的主要微粒是
(5)25°C,H2AsO
 电离程度小于水解程度,依据是:
电离程度小于水解程度,依据是: (6)以酚酞为指示剂,将KOH溶液滴入H3AsO3溶液中,滴定终点的离子方程式是
(7)b点溶液中:c(K+)
 )+4c(AsO
)+4c(AsO ) (选填 “<”“>”或“=”)
) (选填 “<”“>”或“=”)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】写出下列物质在水溶液中的电离方程式。
Na2CO3:_______________________
CH3COOH:________________________ ;
NH4Cl:_________________________
H2SO4:__________________________ ;
H2CO3:__________________________ ;
Na2CO3:
CH3COOH:
NH4Cl:
H2SO4:
H2CO3:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】按要求书写方程式
(1)NH4Cl溶液呈酸性的原因(离子方程式)___________
(2)Na2CO3溶液呈碱性的原因(离子方程式)___________
(3)H3PO2的电离方程式(已知:H3PO2是一元弱酸)___________
(4)在碱性条件下,甲烷燃料电池正极的电极方程式___________
(5)泡沫灭火器的原理(化学方程式)___________
(1)NH4Cl溶液呈酸性的原因(离子方程式)
(2)Na2CO3溶液呈碱性的原因(离子方程式)
(3)H3PO2的电离方程式(已知:H3PO2是一元弱酸)
(4)在碱性条件下,甲烷燃料电池正极的电极方程式
(5)泡沫灭火器的原理(化学方程式)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】常温下,部分酸的电离常数如表所示
(1) 相同的三种酸,其酸的浓度从大到小顺序为
相同的三种酸,其酸的浓度从大到小顺序为_______ 。
(2)若HCN的起始浓度为 ,平衡时
,平衡时 约为
约为_______  。若使此溶液中HCN的电离程度增大且
。若使此溶液中HCN的电离程度增大且 也增大的方法是
也增大的方法是_______ 。
(3)中和等量的NaOH,消耗等pH的氢氟酸和硫酸的体积分别为a L、b L,则a_______ (填“大于”“小于”或“等于”,下同)b。
(4)向NaCN溶液中通入少量的 ,发生反应的离子方程式为
,发生反应的离子方程式为_______
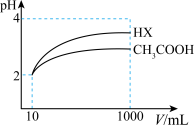
(5)25℃时,体积为10mL、pH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化如图,则HX的电离平衡常数_______ (填“大于”“小于”或“等于”,下同)醋酸的电离平衡常数,稀释后,HX溶液中水电离出来的
_______ 醋酸溶液中水电离出来的 。
。
| 化学式 | HF | HCN |  |
| 电离常数 | 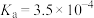 | 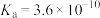 |  , , |
 相同的三种酸,其酸的浓度从大到小顺序为
相同的三种酸,其酸的浓度从大到小顺序为(2)若HCN的起始浓度为
 ,平衡时
,平衡时 约为
约为 。若使此溶液中HCN的电离程度增大且
。若使此溶液中HCN的电离程度增大且 也增大的方法是
也增大的方法是(3)中和等量的NaOH,消耗等pH的氢氟酸和硫酸的体积分别为a L、b L,则a
(4)向NaCN溶液中通入少量的
 ,发生反应的离子方程式为
,发生反应的离子方程式为(5)25℃时,体积为10mL、pH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化如图,则HX的电离平衡常数

 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
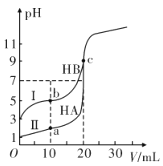
【推荐1】现有HA、HB和H2C三种酸。室温下用0.1mol·L-1NaOH溶液分别滴定20.00 mL浓度均为0.1mol·L-1的HA、HB两种酸的溶液,滴定过程中溶液的pH随滴入的NaOH 溶液体积的变化如图所示。
(1)a点时的溶液中由水电离出的c(H+)=________ mol·L-1,Ka(HB)=________ 。
(2)与曲线I 上的c点对应的溶液中各离子浓度由大到小的顺序为________ ;b点对应的溶液中c(HB)____ c(B-)(填“>”“<”或“=”)。
(3)已知常温下向0.1mol·L-1的NaHC 溶液中滴入几滴石蕊试液后溶液变成红色。
①若测得此溶液的pH=1,则NaHC的电离方程式为_______________ 。
②若在此溶液中能检测到H2C 分子,则此溶液中c(C2-)________ c(H2C)(填“>”“<”或“=”)。
③若H2C的一级电离为H2C=H++ HC-,常温下0.1mol·L-1H2C溶液中的c(H+ )=0.11mol·L-1,则0.1mol·L-1NaHC溶液中的c(H+)________ 0.01mol·L-1(填“>”“<”或“=”)。
(1)a点时的溶液中由水电离出的c(H+)=
(2)与曲线I 上的c点对应的溶液中各离子浓度由大到小的顺序为
(3)已知常温下向0.1mol·L-1的NaHC 溶液中滴入几滴石蕊试液后溶液变成红色。
①若测得此溶液的pH=1,则NaHC的电离方程式为
②若在此溶液中能检测到H2C 分子,则此溶液中c(C2-)
③若H2C的一级电离为H2C=H++ HC-,常温下0.1mol·L-1H2C溶液中的c(H+ )=0.11mol·L-1,则0.1mol·L-1NaHC溶液中的c(H+)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】查阅资料获得25℃时部分弱电解质的电离平衡常数数据:
回答下列问题:
(1) 的电离方程式为
的电离方程式为___________ 。
(2)物质的量浓度相同的HF、HClO、 、
、 中,
中, 由大到小的顺序是
由大到小的顺序是___________ 。
(3)常温下, 的氨水的pH约为
的氨水的pH约为___________ ( )。
)。
(4)常温下, 的水溶液的pH
的水溶液的pH___________ 7(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
(5)常温下,在 的
的 溶液中,水电离出来的
溶液中,水电离出来的 为
为___________  。
。
| 化学式 | HF | HClO |  |  |  |
| 电离常数 | 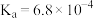 | 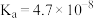 | 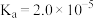 | 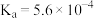 | 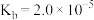 |
(1)
 的电离方程式为
的电离方程式为(2)物质的量浓度相同的HF、HClO、
 、
、 中,
中, 由大到小的顺序是
由大到小的顺序是(3)常温下,
 的氨水的pH约为
的氨水的pH约为 )。
)。(4)常温下,
 的水溶液的pH
的水溶液的pH ”、“
”、“ ”或“
”或“ ”)。
”)。(5)常温下,在
 的
的 溶液中,水电离出来的
溶液中,水电离出来的 为
为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题
(1)在常温下,将浓度均为 的硫酸与氢氧化钠等体积混合后(假设混合后溶液的体积为混合前溶液的体积之和),溶液的pH=
的硫酸与氢氧化钠等体积混合后(假设混合后溶液的体积为混合前溶液的体积之和),溶液的pH=___________ (已知lg5=0.7)
(2)25℃时,pH均为2的三种酸的电离平衡常数如下表:
试回答下列问题:
①下列四种离子结合质子能力最强的是___________ (填序号)。
a. b.
b. c.
c. d.
d.
②常温下将 溶液加水稀释过程中,下列表达式的数据一定变大的是
溶液加水稀释过程中,下列表达式的数据一定变大的是___________ 。
A. B.
B. C.
C. D.
D. E.
E.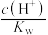
③体积均为10mL,pH均为2的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如图所示。
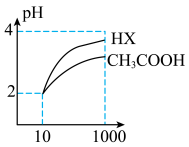
稀释后,HX溶液中水电离出来的
___________ (填“>”、“<”或“=”)醋酸溶液中水电离出来的 ;
; 的电离平衡常数
的电离平衡常数___________ (填“>”、“<”或“=”)HX的电离平衡常数,理由是___________ 。
(1)在常温下,将浓度均为
 的硫酸与氢氧化钠等体积混合后(假设混合后溶液的体积为混合前溶液的体积之和),溶液的pH=
的硫酸与氢氧化钠等体积混合后(假设混合后溶液的体积为混合前溶液的体积之和),溶液的pH=(2)25℃时,pH均为2的三种酸的电离平衡常数如下表:
| 化学式 |  |  |  |
| 电离平衡常数 |  |  、 、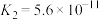 |  |
①下列四种离子结合质子能力最强的是
a.
 b.
b. c.
c. d.
d.
②常温下将
 溶液加水稀释过程中,下列表达式的数据一定变大的是
溶液加水稀释过程中,下列表达式的数据一定变大的是A.
 B.
B. C.
C. D.
D. E.
E.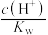
③体积均为10mL,pH均为2的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如图所示。

稀释后,HX溶液中水电离出来的

 ;
; 的电离平衡常数
的电离平衡常数
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】相同温度下,等物质的量浓度的NaX、NaY、NaZ三种正盐溶液,测得溶液的pH分别是7、9、10。则相对应的酸HX、HY、HZ的酸性强弱顺序为_______
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)常温下,有A、B、C、D四种无色溶液,它们分别是CH3COONa溶液、NH4Cl溶液、盐酸和NaNO3溶液中的一种。已知A、B溶液中水的电离程度相同,A、C溶液的pH相同。则B是_____________ ,C是_____________ 。
(2)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测其离子浓度大小顺序有以下几种:
a. c(Cl-)>c(NH4+)>c(H+)>c(OH-) b. c(Cl-)>c(NH4+)>c(OH-)>c(H+)
c. c(NH4+)>c(Cl-)>c(OH-)>c(H+) d. c(Cl-)>c(H+)>c(NH4+)>c(OH-)
则:
①上述关系一定不正确的是____________ 填序号)。
②溶液中只有一种溶质,则该溶液中离子浓度的大小关系为____________ 填序号)。
③若四种离子浓度关系有c(NH4+)=c(Cl-),则该溶液显______________________ (填“酸性”“碱性”或“中性”)。
(2)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测其离子浓度大小顺序有以下几种:
a. c(Cl-)>c(NH4+)>c(H+)>c(OH-) b. c(Cl-)>c(NH4+)>c(OH-)>c(H+)
c. c(NH4+)>c(Cl-)>c(OH-)>c(H+) d. c(Cl-)>c(H+)>c(NH4+)>c(OH-)
则:
①上述关系一定不正确的是
②溶液中只有一种溶质,则该溶液中离子浓度的大小关系为
③若四种离子浓度关系有c(NH4+)=c(Cl-),则该溶液显
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】二氧化碳(碳酸)、碳酸氢盐及碳酸盐在生产和生活中有广泛的用途。H2CO3、HClO的电离平衡常数如表:
(1)将少量CO2气体通入NaClO溶液中,反应的离子方程式:______ 。
(2)小苏打(NaHCO3)可用作糕点的发酵剂。NaHCO3溶液是显____ (填“酸”、“碱”或“中”)性,溶液中含碳微粒浓度大小关系为______ 。
(3)泡沫灭火器中存放的物质主要是NaHCO3和A12(SO4)3溶液,使用时,将两物质混合即可产生大量的CO2气体,用平衡移动原理解释灭火原理:_______ 。
(4)25℃时,潮湿的石膏雕像表面会发生反应:CaSO4(s)+CO (aq)
(aq) CaCO3(s)+SO
CaCO3(s)+SO (aq),其平衡常数K=
(aq),其平衡常数K=_______ (填数值)[已知:Ksp(CaSO4)=9.1×10-6,Ksp(CaCO3)=2.8×10-9]。
| 弱酸 | H2CO3 | HClO |
| 电离平衡常数(25℃) | K1=4.2×10-7 K2=4.8×10-11 | K1=3.0×10-8 |
(1)将少量CO2气体通入NaClO溶液中,反应的离子方程式:
(2)小苏打(NaHCO3)可用作糕点的发酵剂。NaHCO3溶液是显
(3)泡沫灭火器中存放的物质主要是NaHCO3和A12(SO4)3溶液,使用时,将两物质混合即可产生大量的CO2气体,用平衡移动原理解释灭火原理:
(4)25℃时,潮湿的石膏雕像表面会发生反应:CaSO4(s)+CO
 (aq)
(aq) CaCO3(s)+SO
CaCO3(s)+SO (aq),其平衡常数K=
(aq),其平衡常数K=
您最近一年使用:0次



