为了证明一水合氨(NH3·H2O)是弱电解质,常温下,甲、乙、丙三人分别选用下列试剂进行实验:0.010 mol·L-1氨水、NH4Cl溶液、NH4Cl晶体、酚酞试剂、pH试纸、蒸馏水。
(1)甲用pH试纸测出0.010 mol·L-1氨水的pH为10,则认定NH3·H2O是弱电解质,你认为这一方法____ (填“正确”或“不正确”),理由是___________________________ 。
(2)乙取出10 mL 0.010 mol·L-1氨水,用pH试纸测出其pH=a,然后用蒸馏水稀释至1 000 mL,再用pH试纸测出其pH=b,若要确认NH3·H2O是弱电解质,则a、b应满足的关系为________ (用等式或不等式表示)。
(3)丙取出10 mL 0.010 mol·L-1氨水,滴入2滴酚酞溶液,显粉红色,再加入NH4Cl晶体少量,颜色变____ (填“深”或“浅”)。你认为这一方法____ (填“能”或“不能”)证明NH3·H2O是弱电解质,原因是________ 。
(1)甲用pH试纸测出0.010 mol·L-1氨水的pH为10,则认定NH3·H2O是弱电解质,你认为这一方法
(2)乙取出10 mL 0.010 mol·L-1氨水,用pH试纸测出其pH=a,然后用蒸馏水稀释至1 000 mL,再用pH试纸测出其pH=b,若要确认NH3·H2O是弱电解质,则a、b应满足的关系为
(3)丙取出10 mL 0.010 mol·L-1氨水,滴入2滴酚酞溶液,显粉红色,再加入NH4Cl晶体少量,颜色变
2018高二上·全国·专题练习 查看更多[4]
(已下线)2018年10月7日 《每日一题》人教选修4--每周一测(已下线)2019年10月6日 《每日一题》选修4—— 每周一测(已下线)3.3.2 影响盐类水解的因素(基础练)-2020-2021学年高二化学十分钟同步课堂专练(苏教版选修4)新疆乌鲁木齐市第八中学2020-2021学年高二上学期期末考试化学试题
更新时间:2018-10-12 06:32:32
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】现有以下物质:①NaCl晶体②液态SO3③液态氯化氢④汞⑤BaSO4固体⑥纯蔗糖(C12H22O11) ⑦酒精(C2H5OH) ⑧熔化的KNO3,请回答下列问题(用序号):
(1)以上物质中能导电的是_________________ 。
(2)以上物质中属于电解质的是___________________ 。
(3)以上物质中属于非电解质的是____________________ 。
(1)以上物质中能导电的是
(2)以上物质中属于电解质的是
(3)以上物质中属于非电解质的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】请回答下列问题:
(1)某浓度的稀氨水中存在电离平衡: ,若想增大该溶液中
,若想增大该溶液中 的浓度而不增大OH-的浓度,应采取的措施是(忽略溶液体积的变化)
的浓度而不增大OH-的浓度,应采取的措施是(忽略溶液体积的变化)( )
A.适当升高温度 B.加入NH4Cl固体 C.通入NH3 D.加入少量浓盐酸
(2)常温下,有pH相同、体积相同的a.CH3COOH溶液和b.HCl溶液,现采取以下措施:
①分别加适量醋酸钠晶体后,CH3COOH溶液中c(H+)________ (填“增大”“减小”或“不变”,下同),HCl溶液中c(H+)___________ 。
②分别加水稀释10倍后,CH3COOH溶液中的c(H+)_______ (填“>”“=”或“<”)HCl溶液中的c(H+)。
③分别加等浓度的NaOH溶液至恰好反应,所需NaOH溶液的体积:CH3COOH溶液______ (填“>”“=”或“<”)HCl溶液。
④温度都升高20℃,CH3COOH溶液中c(H+)_______ (填“>”“=”或“<”)HCl溶液中c(H+)。
(3)将0.1 mol/L的CH3COOH溶液加水稀释,下列有关稀释后CH3COOH溶液的说法正确的是( )
A.电离程度增大 B.溶液中离子总数增多
C.溶液导电性增强 D.溶液中醋酸分子增多
(1)某浓度的稀氨水中存在电离平衡:
 ,若想增大该溶液中
,若想增大该溶液中 的浓度而不增大OH-的浓度,应采取的措施是(忽略溶液体积的变化)
的浓度而不增大OH-的浓度,应采取的措施是(忽略溶液体积的变化)A.适当升高温度 B.加入NH4Cl固体 C.通入NH3 D.加入少量浓盐酸
(2)常温下,有pH相同、体积相同的a.CH3COOH溶液和b.HCl溶液,现采取以下措施:
①分别加适量醋酸钠晶体后,CH3COOH溶液中c(H+)
②分别加水稀释10倍后,CH3COOH溶液中的c(H+)
③分别加等浓度的NaOH溶液至恰好反应,所需NaOH溶液的体积:CH3COOH溶液
④温度都升高20℃,CH3COOH溶液中c(H+)
(3)将0.1 mol/L的CH3COOH溶液加水稀释,下列有关稀释后CH3COOH溶液的说法正确的是
A.电离程度增大 B.溶液中离子总数增多
C.溶液导电性增强 D.溶液中醋酸分子增多
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】在某温度下,冰醋酸(纯醋酸)加水稀释过程中,溶液的导电能力如图所示,则:
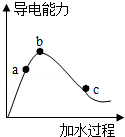
(1)用湿润的pH试纸测量a处溶液的pH,测量结果______ (偏大、偏小或不变)
(2)比较a、b、c三点的下列数据大小或等量关系:(如a>b>c、c=a>b、a=b=c等)
①醋酸的电离程度:_________ 。
②a、b、c三点溶液用1mol/L氢氧化钠溶液中和,消耗氢氧化钠溶液体积:______ 。
(3)在稀释过程中,随着c(CH3COOH)的降低,下列始终保持增大趋势的量是______ 。
A.c(H+) B.H+个数 C.CH3COOH个数 D.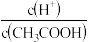

(1)用湿润的pH试纸测量a处溶液的pH,测量结果
(2)比较a、b、c三点的下列数据大小或等量关系:(如a>b>c、c=a>b、a=b=c等)
①醋酸的电离程度:
②a、b、c三点溶液用1mol/L氢氧化钠溶液中和,消耗氢氧化钠溶液体积:
(3)在稀释过程中,随着c(CH3COOH)的降低,下列始终保持增大趋势的量是
A.c(H+) B.H+个数 C.CH3COOH个数 D.
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知常温下部分弱电解质的电离平衡常数如表:
(1)常温下,物质的量浓度相同的三种溶液 ①NaF溶液;②NaClO溶液;③Na2CO3溶液,其pH由大到小的顺序是___________ 。(填序号)
(2)25℃时,用离子方程式说明NH4Cl溶液呈酸性的原因:___________ ,pH=4的NH4Cl溶 液中各离子浓度的大小关系为___________ ,该溶液中水电离出的氢离子的浓度为___________ 。
(3)向足量的次氯酸钠中通入少量的二氧化碳的离子方程式___________ 。
(4)室温下,经测定0.1mol·L-1NaHSO3溶液pH=4.0,则c( )
) ___________ c(H2SO3)(填“>”、“=”、“<”)。
(5)25℃时,若氨水的浓度为2.0 mol·L-1,溶液中的c(OH-)=___________ mol·L-1,将SO2通入该氨水中,当c(OH-)降至1.0×10-6mol·L-1时,溶液中 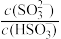 =
=___________ 。
| 化学式 | HF | HClO | H2CO3 | H2SO3 | NH3·H2O |
| 电离常数 | 6.8×10-4 | 4.7×10-8 | K1=4.3×10-7 K2=5.6×10-11 | Ka1=1.4×10-2 Ka2=6.0×10-8 | Kb=1.8×10-5 |
(2)25℃时,用离子方程式说明NH4Cl溶液呈酸性的原因:
(3)向足量的次氯酸钠中通入少量的二氧化碳的离子方程式
(4)室温下,经测定0.1mol·L-1NaHSO3溶液pH=4.0,则c(
 )
) (5)25℃时,若氨水的浓度为2.0 mol·L-1,溶液中的c(OH-)=
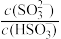 =
=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】乙二酸( 或HOOCCOOH)俗称草酸,是一种二元弱酸,在工业上可作漂白剂、鞣革剂,在实验研究和化学工业中应用广泛。
或HOOCCOOH)俗称草酸,是一种二元弱酸,在工业上可作漂白剂、鞣革剂,在实验研究和化学工业中应用广泛。
(1)草酸第一步电离的电离方程式为___________________________ 。
(2)草酸可用来测定未知浓度的 溶液(用草酸滴定
溶液(用草酸滴定 溶液)。
溶液)。
①实验过程中,草酸应用___________ (填“酸式”或“碱式”)滴定管盛装。
②判断达到滴定终点时的现象为_______________________________________________________ 。
③若滴定完成后仰视读数,则测得的 溶液浓度
溶液浓度___________ (“偏高”、“偏低”或“无影响”)。
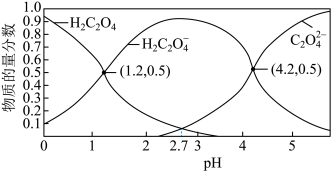
(3)常温下,草酸溶液中微粒的物质的量分数随溶液pH的变化如图所示:
已知:常温下, 的电离平衡常数
的电离平衡常数 ,
, 。
。
①常温下,草酸的电离平衡常数
___________ 。
②相同条件下,物质的量浓度均为0.1 的
的 溶液的pH比
溶液的pH比 溶液的pH
溶液的pH__________ (填“大”或“小”)。
③常温下,向10mL 0.1
 溶液中逐滴加入0.1
溶液中逐滴加入0.1 KOH溶液,随着KOH溶液体积的增加,当溶液中
KOH溶液,随着KOH溶液体积的增加,当溶液中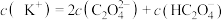 时,加入的V(KOH溶液)
时,加入的V(KOH溶液)___________ (填“>”、“=”或“<”)10mL,若加入KOH溶液体积为10mL溶液中 、
、 、
、 的浓度由大到小的顺序为
的浓度由大到小的顺序为________________________ 。
 或HOOCCOOH)俗称草酸,是一种二元弱酸,在工业上可作漂白剂、鞣革剂,在实验研究和化学工业中应用广泛。
或HOOCCOOH)俗称草酸,是一种二元弱酸,在工业上可作漂白剂、鞣革剂,在实验研究和化学工业中应用广泛。(1)草酸第一步电离的电离方程式为
(2)草酸可用来测定未知浓度的
 溶液(用草酸滴定
溶液(用草酸滴定 溶液)。
溶液)。①实验过程中,草酸应用
②判断达到滴定终点时的现象为
③若滴定完成后仰视读数,则测得的
 溶液浓度
溶液浓度(3)常温下,草酸溶液中微粒的物质的量分数随溶液pH的变化如图所示:

已知:常温下,
 的电离平衡常数
的电离平衡常数 ,
, 。
。①常温下,草酸的电离平衡常数

②相同条件下,物质的量浓度均为0.1
 的
的 溶液的pH比
溶液的pH比 溶液的pH
溶液的pH③常温下,向10mL 0.1

 溶液中逐滴加入0.1
溶液中逐滴加入0.1 KOH溶液,随着KOH溶液体积的增加,当溶液中
KOH溶液,随着KOH溶液体积的增加,当溶液中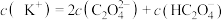 时,加入的V(KOH溶液)
时,加入的V(KOH溶液) 、
、 、
、 的浓度由大到小的顺序为
的浓度由大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】水中存在电离平衡:H2O H++OH-。若在水中分别加入下列各物质:①NaOH(s) ②NH4Cl(s) ③Na2CO3(s) ④CH3COOH(l) ⑤Na(s) ⑥K2SO4,试回答下列问题:
H++OH-。若在水中分别加入下列各物质:①NaOH(s) ②NH4Cl(s) ③Na2CO3(s) ④CH3COOH(l) ⑤Na(s) ⑥K2SO4,试回答下列问题:
(1)能使水的电离平衡向左移动的是___________ 。
(2)溶液呈酸性的是___________ 。
(3)能促进水的电离,且溶液pH>7的是______;能抑制水的电离,且溶液呈酸性的是___________ 。
(4)写出③、⑤中加入水中反应的离子方程式:
③___________ ;
⑤___________ 。
 H++OH-。若在水中分别加入下列各物质:①NaOH(s) ②NH4Cl(s) ③Na2CO3(s) ④CH3COOH(l) ⑤Na(s) ⑥K2SO4,试回答下列问题:
H++OH-。若在水中分别加入下列各物质:①NaOH(s) ②NH4Cl(s) ③Na2CO3(s) ④CH3COOH(l) ⑤Na(s) ⑥K2SO4,试回答下列问题:(1)能使水的电离平衡向左移动的是
(2)溶液呈酸性的是
(3)能促进水的电离,且溶液pH>7的是______;能抑制水的电离,且溶液呈酸性的是
(4)写出③、⑤中加入水中反应的离子方程式:
③
⑤
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】完成下列问题。
(1)用离子方程式表示下列盐溶液的水解反应,不能发生水解的写“不发生水解”字样,并说明溶液的酸碱性:
①K2CO3_______ ,溶液呈_______ 性;
②Na2SO4_______ ,溶液呈_______ 性;
③CuCl2_______ ,溶液呈_______ 性。
(2)将AlCl3溶于水后,经加热蒸发、蒸干,灼烧,最后所得白色固体的主要成分是_______ ;用化学方程式表述产生白色固体的过程:_______ 、_______ 。
(1)用离子方程式表示下列盐溶液的水解反应,不能发生水解的写“不发生水解”字样,并说明溶液的酸碱性:
①K2CO3
②Na2SO4
③CuCl2
(2)将AlCl3溶于水后,经加热蒸发、蒸干,灼烧,最后所得白色固体的主要成分是
您最近一年使用:0次

 的水溶液呈
的水溶液呈 溶液蒸干、灼烧,最后得到的主要固体产物是
溶液蒸干、灼烧,最后得到的主要固体产物是 纯碱溶液的
纯碱溶液的 ,则此溶液中水电离出的
,则此溶液中水电离出的 等于
等于

