25 ℃时,部分物质的电离平衡常数如下表所示:
(1)NH3·H2O的电离方程式是_____________ ,25 ℃时,物质的量浓度为0.10 mol/L的氨水中,c(OH-)=___________ (列出算式即可)。
(2)25 ℃时,物质的量浓度相等的CH3COONa溶液和NaClO溶液pH大小关系是:CH3COONa________ (填“>”“<”或“=”)NaClO,请结合题目有关信息说明原因__________ 。
(3)向NaClO溶液中通入少量二氧化碳气体,发生反应的离子方程式是_____ ,结合所给数据说明生成该产物的理由__________ 。
化学式 | CH3COOH | H2CO3 | HClO | NH3·H2O |
电离平 衡常数 | Ka=1.75×10-5 | Ka1=4.5×10-7 Ka2=4.7×10-11 | Ka=3.0×10-8 | Kb=1.8×10-5 |
(2)25 ℃时,物质的量浓度相等的CH3COONa溶液和NaClO溶液pH大小关系是:CH3COONa
(3)向NaClO溶液中通入少量二氧化碳气体,发生反应的离子方程式是
更新时间:2023-08-15 11:54:15
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】常压下,取不同浓度、不同温度的氨水测定,得到下表实验数据。
(1)温度升高,NH3·H2O的电离平衡向________ (填“左”、“右”)移动,能支持该结论的表中数据是__________ ;
a.电离常数 b.电离度 c.c(OH-) d.c(氨水)
(2)表中c(OH-)基本不变的原因是________________________ 。
| 温度(℃) | c(氨水)(mol/L) | 电离常数 | 电离度(%) | c(OH-)(mol/L) |
| 0 | 16.56 | 1.37×10-5 | 9.098 | 1.507×10-2 |
| 10 | 15.16 | 1.57×10-5 | 10.18 | 1.543×10-2 |
| 20 | 13.63 | 1.71×10-5 | 11.2 | 1.527×10-2 |
(1)温度升高,NH3·H2O的电离平衡向
a.电离常数 b.电离度 c.c(OH-) d.c(氨水)
(2)表中c(OH-)基本不变的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】请按要求回答:
(1)①写出FeO的名称___________________ .②写出纯碱的化学式___________________ .
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由______________________________________ .
(3)用化学方程式解释不能用带玻璃塞的试剂瓶盛放氢氧化钠溶液的原因______________________ .
(4)写出次氯酸在水中的电离方程式______________________________________ .
(5)写出铜和稀硫酸在双氧水的作用下反应的离子方程式_______________________________ .
(1)①写出FeO的名称
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由
(3)用化学方程式解释不能用带玻璃塞的试剂瓶盛放氢氧化钠溶液的原因
(4)写出次氯酸在水中的电离方程式
(5)写出铜和稀硫酸在双氧水的作用下反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】25℃时,有关物质的电离常数如下表:
(1)碳酸的二级电离平衡常数表达式为K=___________ 。
(2)25℃时,下列五种离子结合质子的能力由大到小的顺序是___________ (用字母表示)。
A. B.
B.  C.
C.  D.
D.  E.
E. 
(3)下列反应不能发生的是___________(填正确答案标号)。
(4)25℃时,向100mL0.1 的HNO2溶液中加入蒸馏水,将其稀释到1L后,下列说法错误的是___________(填正确答案标号)。
的HNO2溶液中加入蒸馏水,将其稀释到1L后,下列说法错误的是___________(填正确答案标号)。
(5)常温下,pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序是___________ 。
| 物质 | CH3COOH | H2CO3 | HClO | HNO2 |
| 电离常数 |  | 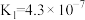 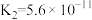 |  |  |
(1)碳酸的二级电离平衡常数表达式为K=
(2)25℃时,下列五种离子结合质子的能力由大到小的顺序是
A.
 B.
B.  C.
C.  D.
D.  E.
E. 
(3)下列反应不能发生的是___________(填正确答案标号)。
A. |
B. |
C.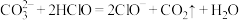 |
D. |
 的HNO2溶液中加入蒸馏水,将其稀释到1L后,下列说法错误的是___________(填正确答案标号)。
的HNO2溶液中加入蒸馏水,将其稀释到1L后,下列说法错误的是___________(填正确答案标号)。| A.HNO2的电离程度增大 | B.Ka(HNO2)增大 |
C.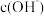 增大 增大 | D.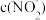 减小 减小 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按要求回答下列问题:
(1) 时,物质的量浓度均为
时,物质的量浓度均为 的几种盐溶液的
的几种盐溶液的 如下表所示。
如下表所示。
①溶液Ⅳ显碱性的原因是_______ (用离子方程式表示)。
②写出溶液Ⅲ中阴离子浓度由大到小的关系:_______ 。
③溶液Ⅱ中,
_______ (填“>”“<”或“=”)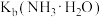 。
。
④溶液Ⅰ中,由水电离产生的
_______  。
。
(2)几种离子开始沉淀时的 如下表所示。
如下表所示。
①向含相同浓度 、
、 、
、 的溶液中滴加氢氧化钠溶液,
的溶液中滴加氢氧化钠溶液,_______ (填离子符号)最先沉淀,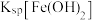
_______ (填“>”“<”或“=”)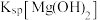 。
。
② 时,若要使
时,若要使 硫酸铜溶液中的铜离子沉淀较为完全(使铜离子浓度降至原来的千分之一),则应向溶液中加入氢氧化钠溶液。使溶液的
硫酸铜溶液中的铜离子沉淀较为完全(使铜离子浓度降至原来的千分之一),则应向溶液中加入氢氧化钠溶液。使溶液的 为
为_______ (已知: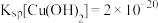 )
)
(1)
 时,物质的量浓度均为
时,物质的量浓度均为 的几种盐溶液的
的几种盐溶液的 如下表所示。
如下表所示。| 序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 溶液 |  溶液 溶液 |  溶液 溶液 |  溶液 溶液 |  溶液 溶液 |
 | 5 | 7 | 8.4 | 10.3 |
①溶液Ⅳ显碱性的原因是
②写出溶液Ⅲ中阴离子浓度由大到小的关系:
③溶液Ⅱ中,

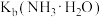 。
。④溶液Ⅰ中,由水电离产生的

 。
。(2)几种离子开始沉淀时的
 如下表所示。
如下表所示。| 离子 |  |  |  |
 | 7.6 | 4.4 | 40.4 |
①向含相同浓度
 、
、 、
、 的溶液中滴加氢氧化钠溶液,
的溶液中滴加氢氧化钠溶液,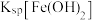
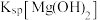 。
。②
 时,若要使
时,若要使 硫酸铜溶液中的铜离子沉淀较为完全(使铜离子浓度降至原来的千分之一),则应向溶液中加入氢氧化钠溶液。使溶液的
硫酸铜溶液中的铜离子沉淀较为完全(使铜离子浓度降至原来的千分之一),则应向溶液中加入氢氧化钠溶液。使溶液的 为
为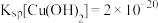 )
)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】醋酸是我们很熟悉的一种有机物。
(1)生活中可使用醋酸除暖瓶中的水垢,由此说明醋酸具有的性质是____ 。
A.挥发性 B.酸性比碳酸强 C.难电离 D.易溶于水
(2)某同学为了解醋酸溶液的导电性进行了相应实验,右图为冰醋酸(无水醋酸晶体)在稀释过程中溶液的导电性变化关系图。
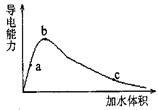
请回答:
①在稀释过程中,a 、b、c三处溶液的pH值由大到小的顺序是____________ 。
②从b点到c点,溶液中 的比值
的比值______ (填“增大”、“减小”或“不变”)。
③ b点时溶液除水以外各种分子、离子的浓度由大到小的顺序是________________ 。
(1)生活中可使用醋酸除暖瓶中的水垢,由此说明醋酸具有的性质是
A.挥发性 B.酸性比碳酸强 C.难电离 D.易溶于水
(2)某同学为了解醋酸溶液的导电性进行了相应实验,右图为冰醋酸(无水醋酸晶体)在稀释过程中溶液的导电性变化关系图。

请回答:
①在稀释过程中,a 、b、c三处溶液的pH值由大到小的顺序是
②从b点到c点,溶液中
 的比值
的比值③ b点时溶液除水以外各种分子、离子的浓度由大到小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)已知25℃时NH3·H2O的Kb=2.0 10-5
10-5
①求0.10mol/L的NH3·H2O的c(OH-)=______________ mol/L
②若向其中加入固体NH4Cl,使c(NH )的浓度达到0.20mol/L,则c(OH-)=
)的浓度达到0.20mol/L,则c(OH-)=________ mol/L
③25℃时,将a mol•L-1的氨水与0.01mol•L-1的盐酸等体积混合,若混合后溶液的pH=7,用含a的代数式表示NH3•H2O的电离常数Kb=___________________ 。
(2)25℃时,0.10mol•L﹣1的HA溶液中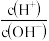 =1010。
=1010。
①该HA溶液的pH=________ 。
②25℃时,将等浓度等体积的氨水与HA溶液相混合, 该混合溶液的pH________ 7。(填“<”、“>”或“=”)
(1)已知25℃时NH3·H2O的Kb=2.0
 10-5
10-5①求0.10mol/L的NH3·H2O的c(OH-)=
②若向其中加入固体NH4Cl,使c(NH
 )的浓度达到0.20mol/L,则c(OH-)=
)的浓度达到0.20mol/L,则c(OH-)=③25℃时,将a mol•L-1的氨水与0.01mol•L-1的盐酸等体积混合,若混合后溶液的pH=7,用含a的代数式表示NH3•H2O的电离常数Kb=
(2)25℃时,0.10mol•L﹣1的HA溶液中
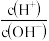 =1010。
=1010。①该HA溶液的pH=
②25℃时,将等浓度等体积的氨水与HA溶液相混合, 该混合溶液的pH
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,用0.1000mol/LNaOH溶液分别滴定20.00mL0.1000mol/LHCl溶液和20.00mL0.1000mol/LCH3COOH溶液,得到2条滴定曲线,如图所示:

(1)判断滴定HCl溶液的曲线是________ (填“图1”或“图2”);
(2)a=________ mL;
(3)c(Na+)=c(CH3COO-)的点是________ ;
(4)E点对应离子浓度由大到小的顺序为__________________________________ 。
(5)图1中,从A点到B点,溶液中水的电离程度逐渐________ (填“增大”或“减小”或“不变”);
(6)氢氧化钠溶液滴定盐酸溶液过程中,用酚酞作指示剂,请描述滴定终点的判断____________________________ 。

(1)判断滴定HCl溶液的曲线是
(2)a=
(3)c(Na+)=c(CH3COO-)的点是
(4)E点对应离子浓度由大到小的顺序为
(5)图1中,从A点到B点,溶液中水的电离程度逐渐
(6)氢氧化钠溶液滴定盐酸溶液过程中,用酚酞作指示剂,请描述滴定终点的判断
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知H2A在水中存在以下平衡:H2A=H++HA-,HA- H++A2-。
H++A2-。
(1)NaHA溶液的pH___ (填大于、小于或等于)Na2A溶液的pH。
(2)某温度下,若向0.1mol/L的NaHA溶液中逐滴滴加0.1mol/LKOH溶液至溶液呈中性。此时该混合溶液中下列关系中,一定正确的是___ 。
A.c(H+)·c(OH-)=1×10-14 B.c(Na+)+c(K+)=c(HA-)+2c(A2-)
C.c(Na+)>c(K+) D.c(Na+)+c(K+)=0.05mol/L
(3)已知常温下H2A的钙盐(CaA)的饱和溶液中存在以下平衡:CaA(s) Ca2+(aq)+A2-(aq) ΔH>0。若要使该溶液中Ca2+浓度变小,可采取的措施有
Ca2+(aq)+A2-(aq) ΔH>0。若要使该溶液中Ca2+浓度变小,可采取的措施有___ 。
A.升高温度 B.降低温度 C.加入NH4Cl晶体 D.加入Na2A固体
 H++A2-。
H++A2-。(1)NaHA溶液的pH
(2)某温度下,若向0.1mol/L的NaHA溶液中逐滴滴加0.1mol/LKOH溶液至溶液呈中性。此时该混合溶液中下列关系中,一定正确的是
A.c(H+)·c(OH-)=1×10-14 B.c(Na+)+c(K+)=c(HA-)+2c(A2-)
C.c(Na+)>c(K+) D.c(Na+)+c(K+)=0.05mol/L
(3)已知常温下H2A的钙盐(CaA)的饱和溶液中存在以下平衡:CaA(s)
 Ca2+(aq)+A2-(aq) ΔH>0。若要使该溶液中Ca2+浓度变小,可采取的措施有
Ca2+(aq)+A2-(aq) ΔH>0。若要使该溶液中Ca2+浓度变小,可采取的措施有A.升高温度 B.降低温度 C.加入NH4Cl晶体 D.加入Na2A固体
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】在室温下,下列五种溶液,请根据要求填写下列空白:
①0.1mol•L-1NH4Cl溶液;②0.1mol•L-1CH3COONH4溶液;③0.1mol•L-1NH4HSO4溶液;④0.1mol•L-1NH3·H2O和0.1mol•L-1NH4Cl混合液;⑤0.1mol•L-1氨水
(1)溶液①呈___ (填“酸”、“碱”或“中”)性,其原因是___ (用离子方程式表示)。
(2)溶液①至⑤中,c(NH )从大到小的顺序是
)从大到小的顺序是___ 。
(3)在溶液④中___ (填离子符号)的浓度为0.1mol/L;NH3·H2O和___ (填离子符号)的浓度之和为0.2mol/L。
(4)室温下,测得溶液②的pH=7,则说明CH3COO-的水解程度___ (填“>”、“<”或“=”,下同)NH 的水解程度,CH3COO-与NH
的水解程度,CH3COO-与NH 浓度的大小关系是c(CH3COO-)
浓度的大小关系是c(CH3COO-)___ c(NH )。
)。
(5)常温下,某水溶液M中存在的离子有Na+、A2-、HA-、H+、OH-,存在的分子有H2O、H2A。
①写出酸H2A的电离方程式:___ 。
②若溶液M由10mL2mol•L-1NaHA溶液与10mL2mol•L-1NaOH溶液混合而得,则溶液M的pH___ (填“>”、“<”或“=”)7。
①0.1mol•L-1NH4Cl溶液;②0.1mol•L-1CH3COONH4溶液;③0.1mol•L-1NH4HSO4溶液;④0.1mol•L-1NH3·H2O和0.1mol•L-1NH4Cl混合液;⑤0.1mol•L-1氨水
(1)溶液①呈
(2)溶液①至⑤中,c(NH
 )从大到小的顺序是
)从大到小的顺序是(3)在溶液④中
(4)室温下,测得溶液②的pH=7,则说明CH3COO-的水解程度
 的水解程度,CH3COO-与NH
的水解程度,CH3COO-与NH 浓度的大小关系是c(CH3COO-)
浓度的大小关系是c(CH3COO-) )。
)。(5)常温下,某水溶液M中存在的离子有Na+、A2-、HA-、H+、OH-,存在的分子有H2O、H2A。
①写出酸H2A的电离方程式:
②若溶液M由10mL2mol•L-1NaHA溶液与10mL2mol•L-1NaOH溶液混合而得,则溶液M的pH
您最近一年使用:0次



