Ⅰ.镓及其化合物在合金工业、制药工业、电池工业有广泛的应用。回答下列问题:
(1)基态Ga原子的价层电子排布式为_____ 。
(2)一种含镓的药物合成方法如图所示:____ ,
_____ 。
Ⅱ.硒是人体需要的重要微量元素之一,参与体内多种代谢。
(3)①在同一周期中比Se元素的第一电离能大的元素有____ 种。
②Se的某种同素异形体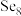 为环状结构,是
为环状结构,是 的等电子体,
的等电子体,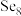 环中Se原子的杂化方式为
环中Se原子的杂化方式为_____ 。Se−Se−Se平均键角最接近:____ (填选项序号)。
a. b.
b. c.
c.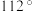
(4)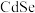 的一种晶体为闪锌矿型结构,晶胞结构如图所示。其中原子坐标参数A为
的一种晶体为闪锌矿型结构,晶胞结构如图所示。其中原子坐标参数A为 ,则C的原子坐标参数分别为
,则C的原子坐标参数分别为_____ ,已知Cd和Se的原子半径分别为b nm和c nm,则该晶胞中原子的体积占晶胞体积的百分率为_____ (列出计算式)。
(1)基态Ga原子的价层电子排布式为
(2)一种含镓的药物合成方法如图所示:
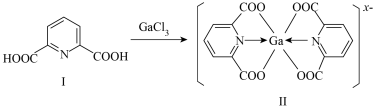

Ⅱ.硒是人体需要的重要微量元素之一,参与体内多种代谢。
(3)①在同一周期中比Se元素的第一电离能大的元素有
②Se的某种同素异形体
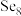 为环状结构,是
为环状结构,是 的等电子体,
的等电子体,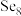 环中Se原子的杂化方式为
环中Se原子的杂化方式为a.
 b.
b. c.
c.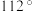
(4)
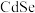 的一种晶体为闪锌矿型结构,晶胞结构如图所示。其中原子坐标参数A为
的一种晶体为闪锌矿型结构,晶胞结构如图所示。其中原子坐标参数A为 ,则C的原子坐标参数分别为
,则C的原子坐标参数分别为
更新时间:2024-02-17 21:47:57
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】高温炼铜的反应之一为2CuFeS2+O2 Cu2S+2FeS+SO2。
Cu2S+2FeS+SO2。
(1)Cu+基态核外电子排布式为___________ 。
(2)Cu、Zn的第二电离能:I2(Cu)________ (填“>”“<”或“=”)I2(Zn)。
(3)SO2分子中S原子的轨道杂化类型为________ ,分子的立体构型为________ 。
(4)[Cu(CH3CN)4]+是非常稳定的络合离子,配体中σ键和π键个数之比为________ 。
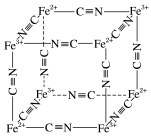
(5)Fe2+、Fe3+能与CN-络合,其结构如图所示。该离子可形成铁蓝钾盐,该钾盐的化学式为_________ 。
 Cu2S+2FeS+SO2。
Cu2S+2FeS+SO2。(1)Cu+基态核外电子排布式为
(2)Cu、Zn的第二电离能:I2(Cu)
(3)SO2分子中S原子的轨道杂化类型为
(4)[Cu(CH3CN)4]+是非常稳定的络合离子,配体中σ键和π键个数之比为
(5)Fe2+、Fe3+能与CN-络合,其结构如图所示。该离子可形成铁蓝钾盐,该钾盐的化学式为

您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】短周期元素X、Y、Z组成的化合物Y2X和ZX2.Y2X溶于水形成的溶液能与ZX2反应生成一种化合物Y2ZX3.已知三种元素原子的质子总数为25,且Z和Y的原子序数之和比X的原子序数2倍还多1,Z原子有2个电子层,最外层电子数是核外电子数的 倍,试回答:
倍,试回答:
(1)X元素的名称:_______ ,Y元素在元素周期表中的位置____________ ,Z元素的原子结构示意图_______________
(2)Y2X对应水化物的电子式________ ,其中存在的化学键有_____________ .
(3)X的氢化物比同主族的氢化物的熔沸点明显偏高的原因___________________ .
 倍,试回答:
倍,试回答:(1)X元素的名称:
(2)Y2X对应水化物的电子式
(3)X的氢化物比同主族的氢化物的熔沸点明显偏高的原因
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】氮、磷、氯、溴、铁、铜等元素及其化合物在现代农业、科技和国防建设中有着许多独特的用途。LiFePO4是新型锂离子电池的电极材料,可利用FeCl3、NH4H2PO4、LiC1和苯胺(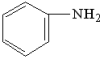 )等原料来制备。回答下列问题。
)等原料来制备。回答下列问题。
(1)铁元素在元素周期表中的位置为_______ ,基态Fe2+的价层电子排布图(轨道表达式)为_______ 。
(2)NH4H2PO4中,除氢元素外,其余三种元素第一电离能最大的是_______ (填元素符号)。
(3)苯胺和甲苯相对分子质量接近,但苯胺熔点明显比甲苯的高,原因是_______ 。
(4)红磷在氯气中燃烧可以得到PCl3和PCl5,其中气态PCl3分子的立体构型为_______ 。研究发现固态PCl5和PBr5的结构分别为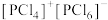 和
和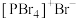 ,则它们的晶体类型为
,则它们的晶体类型为_______ 。
(5)已知NH3分子中H-N-H的键角为107.3°,则配合物[Cu(NH3)4]SO4中H-N-H的键角_______ 107.3°(填“大于”“小于”“等于”)。
(6)铁酸钇是一种典型的单相多铁性材料,其正交相晶胞结构以及各原子的投影位置如图所示。

已知1号O原子空间坐标为(0,0, ),2号O原子空间坐标为(
),2号O原子空间坐标为( ,
, −m,
−m, −n),则3号Fe原子的空间坐标为
−n),则3号Fe原子的空间坐标为_______ ,若晶胞参数分别为apm、bpm和cpm,阿伏加德罗常数的值用NA表示,则该晶体的密度为_______ g·cm−3(列出表达式)。
 )等原料来制备。回答下列问题。
)等原料来制备。回答下列问题。(1)铁元素在元素周期表中的位置为
(2)NH4H2PO4中,除氢元素外,其余三种元素第一电离能最大的是
(3)苯胺和甲苯相对分子质量接近,但苯胺熔点明显比甲苯的高,原因是
(4)红磷在氯气中燃烧可以得到PCl3和PCl5,其中气态PCl3分子的立体构型为
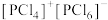 和
和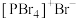 ,则它们的晶体类型为
,则它们的晶体类型为(5)已知NH3分子中H-N-H的键角为107.3°,则配合物[Cu(NH3)4]SO4中H-N-H的键角
(6)铁酸钇是一种典型的单相多铁性材料,其正交相晶胞结构以及各原子的投影位置如图所示。

已知1号O原子空间坐标为(0,0,
 ),2号O原子空间坐标为(
),2号O原子空间坐标为( ,
, −m,
−m, −n),则3号Fe原子的空间坐标为
−n),则3号Fe原子的空间坐标为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】过渡元素因其独特的化学性质和物理特性,在现代工农业生产和科技发展方面发挥着重要作用。不仅在金属材料、合金材料、磁性材料、催化剂、医疗器材等多个传统领城有着广泛的用途,还在新材料的开发、能源的生产利用等方而展现出新的潜力。
(1)Fe元素在元素周期表中的位置为__________ ,Fe元素的原子结构示意图为__________ 。基态 的核外电子排布式为
的核外电子排布式为__________ 。
(2)基态Cr原子价层电子的轨道表示式为__________ 。
(3)基态Zn原子中有__________ 种不同能量的电子。
(4)配位化学创始人维尔纳发现,取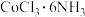 (黄色)、
(黄色)、 (紫红色)、
(紫红色)、 (绿色)和
(绿色)和 (紫色)四种化合物各1mol分别溶于水,加入足量硝酸银溶液,生成AgCl的物质的量分别为3mol、2mol、1mol和1mol。请根据实验事实用配合物的形式写出
(紫色)四种化合物各1mol分别溶于水,加入足量硝酸银溶液,生成AgCl的物质的量分别为3mol、2mol、1mol和1mol。请根据实验事实用配合物的形式写出 的化学式:
的化学式:__________ 。
(1)Fe元素在元素周期表中的位置为
 的核外电子排布式为
的核外电子排布式为(2)基态Cr原子价层电子的轨道表示式为
(3)基态Zn原子中有
(4)配位化学创始人维尔纳发现,取
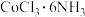 (黄色)、
(黄色)、 (紫红色)、
(紫红色)、 (绿色)和
(绿色)和 (紫色)四种化合物各1mol分别溶于水,加入足量硝酸银溶液,生成AgCl的物质的量分别为3mol、2mol、1mol和1mol。请根据实验事实用配合物的形式写出
(紫色)四种化合物各1mol分别溶于水,加入足量硝酸银溶液,生成AgCl的物质的量分别为3mol、2mol、1mol和1mol。请根据实验事实用配合物的形式写出 的化学式:
的化学式:
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐2】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:
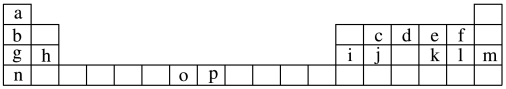
(1)元素p为26号元素,请写出其基态原子的电子排布式________________ 。
(2)d与a反应的产物的分子,空间构型为_________________ 。
(3)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:________________________________________ 。
(4)o、p两元素的部分电离能数据列于下表:
比较两元素的I2、I3可知,气态o2+再失去一个电子比气态p2+再失去一个电子难。对此,你的解释是___________________________________ 。
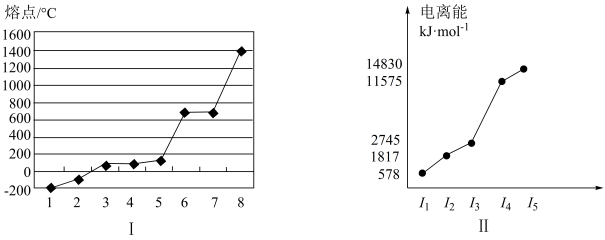
(5)第三周期8种元素按单质熔点高低的顺序如图Ⅰ所示,其中电负性最大的是________ (填图中的序号)。
(6)表中所列的某主族元素的电离能情况如图Ⅱ所示,则该元素是________ (填元素符号)。

(1)元素p为26号元素,请写出其基态原子的电子排布式
(2)d与a反应的产物的分子,空间构型为
(3)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:
(4)o、p两元素的部分电离能数据列于下表:
| 元素 | o | p | |
| 电离能/ (kJ·mol-1) | I1 | 717 | 759 |
| I2 | 1 509 | 1 561 | |
| I3 | 3 248 | 2 957 | |
比较两元素的I2、I3可知,气态o2+再失去一个电子比气态p2+再失去一个电子难。对此,你的解释是
(5)第三周期8种元素按单质熔点高低的顺序如图Ⅰ所示,其中电负性最大的是
(6)表中所列的某主族元素的电离能情况如图Ⅱ所示,则该元素是

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】 主要用于电镀工业、生产镍镉电池,用作油脂加氢催化剂、媒染剂等。某兴趣小组用含镍废催化剂(主要含有
主要用于电镀工业、生产镍镉电池,用作油脂加氢催化剂、媒染剂等。某兴趣小组用含镍废催化剂(主要含有 ,还含有
,还含有 、
、 、
、 及其他不溶于酸、碱的杂质)制备
及其他不溶于酸、碱的杂质)制备 ,其流程如下:
,其流程如下:
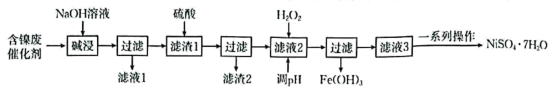
已知:①常温下,部分金属化合物的 近似值如表所示:
近似值如表所示:
②金属活泼性: 。
。
③ 。
。
回答下列问题:
(1) 元素在元素周期表中的位置为
元素在元素周期表中的位置为_______ ,其基态原子的价层电子排布式为_______ 。
(2)“滤液1”中的主要溶质为 、
、_______ 。
(3)加入硫酸时, 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(4)加入 的目的是将
的目的是将 氧化为
氧化为 ,该步骤
,该步骤_______ (填“能”或“不能”)用适量稀硝酸代替,理由是_______ 。然后调节溶液的 ,则此时应调节溶液的
,则此时应调节溶液的 至少为
至少为_______ (保留3位有效数字,离子浓度小于或等于 时认为沉淀完全),检验“滤液3”中杂质金属离子已除尽的操作和现象是
时认为沉淀完全),检验“滤液3”中杂质金属离子已除尽的操作和现象是_______ 。
(5)用配位滴定法测定粗品中 的纯度。取
的纯度。取 粗品溶于水(滴加几滴稀硫酸)配成
粗品溶于水(滴加几滴稀硫酸)配成 溶液,取
溶液,取 溶液于锥形瓶中,滴入几滴紫脲酸胺指示剂(紫色试剂,遇
溶液于锥形瓶中,滴入几滴紫脲酸胺指示剂(紫色试剂,遇 显橙黄色),用浓度为
显橙黄色),用浓度为 的
的 标准液滴定,平均消耗标准液
标准液滴定,平均消耗标准液 。已知:
。已知: 。粗品中
。粗品中 的纯度是
的纯度是_______ %;下列操作会使测定结果偏低的是_______ (填标号)。
A.锥形瓶中溶液颜色由橙黄色局部变为紫色后立即停止滴定
B.滴定前滴定管尖嘴内有气泡,滴定后尖嘴内无气泡
C.滴定前平视读数,滴定后仰视读数
 主要用于电镀工业、生产镍镉电池,用作油脂加氢催化剂、媒染剂等。某兴趣小组用含镍废催化剂(主要含有
主要用于电镀工业、生产镍镉电池,用作油脂加氢催化剂、媒染剂等。某兴趣小组用含镍废催化剂(主要含有 ,还含有
,还含有 、
、 、
、 及其他不溶于酸、碱的杂质)制备
及其他不溶于酸、碱的杂质)制备 ,其流程如下:
,其流程如下:
已知:①常温下,部分金属化合物的
 近似值如表所示:
近似值如表所示:| 化学式 |  |  | 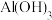 |  |  |
 近似值 近似值 | 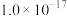 | 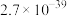 | 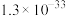 | 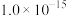 |  |
 。
。③
 。
。回答下列问题:
(1)
 元素在元素周期表中的位置为
元素在元素周期表中的位置为(2)“滤液1”中的主要溶质为
 、
、(3)加入硫酸时,
 发生反应的离子方程式为
发生反应的离子方程式为(4)加入
 的目的是将
的目的是将 氧化为
氧化为 ,该步骤
,该步骤 ,则此时应调节溶液的
,则此时应调节溶液的 至少为
至少为 时认为沉淀完全),检验“滤液3”中杂质金属离子已除尽的操作和现象是
时认为沉淀完全),检验“滤液3”中杂质金属离子已除尽的操作和现象是(5)用配位滴定法测定粗品中
 的纯度。取
的纯度。取 粗品溶于水(滴加几滴稀硫酸)配成
粗品溶于水(滴加几滴稀硫酸)配成 溶液,取
溶液,取 溶液于锥形瓶中,滴入几滴紫脲酸胺指示剂(紫色试剂,遇
溶液于锥形瓶中,滴入几滴紫脲酸胺指示剂(紫色试剂,遇 显橙黄色),用浓度为
显橙黄色),用浓度为 的
的 标准液滴定,平均消耗标准液
标准液滴定,平均消耗标准液 。已知:
。已知: 。粗品中
。粗品中 的纯度是
的纯度是A.锥形瓶中溶液颜色由橙黄色局部变为紫色后立即停止滴定
B.滴定前滴定管尖嘴内有气泡,滴定后尖嘴内无气泡
C.滴定前平视读数,滴定后仰视读数
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】硼及其化合物在新材料、工农业生产等方面用途很广。请回答下列问题:
(1)B的基态原子核外电子排布式为____________________ 。
(2)BF3的立体构型是_____________________ ;HF能与BF3化合得到HBF4,从化学键形成角度分析HF与BF3能化合的原因___________ 。
(3)H3BO3为一元酸,与足量NaOH溶液反应得到[B(OH)4]-,H3BO3和[B(OH)4]-中B的杂化轨道类型分别为为____________ 、____________ 。
(4)NaBH4被认为是有机化学上的“万能还原剂”,NaBH4的电子式为_____________ ,其中三种元素的电负性由大到小的顺序是__________________________ 。
(5)自然界中含硼元素的钠盐是一种天然矿藏,其化学式写作Na2B4O7·10H2O,实际上它的结构单元是由两个H3BO3和两个[B(OH)4]-缩合而成的双六元环,应该写成Na2[B4O5(OH)4]·8H2O,其结构如图所示,
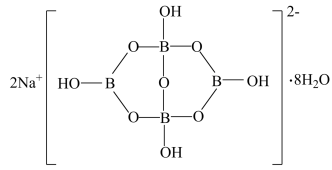
它的阴离子可形成链状结构,则该晶体中不存在的作用力是_________ (填选项字母)。
A.离子键 B.共价键 C.氢键 D.金属键 E.范德华力
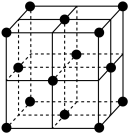
(6)某种金属锂的硼氢化物是优质固体电解质,并具有高储氢密度。阳离子为Li+,每个阴离子是由12个硼原子和12个氢原子所构成的原子团。阴离子在晶胞中的位置如图所示,其堆积方式为____________ ,Li+占据阴离子组成的所有最小正四面体中心,该化合物的化学式为____________ (用最简整数比表示)。假设晶胞边长为a pm,用NA代表阿伏加 德罗常数的值,则该晶胞的密度为___________ g/cm3(用含a,NA的代数式表示) 。
(1)B的基态原子核外电子排布式为
(2)BF3的立体构型是
(3)H3BO3为一元酸,与足量NaOH溶液反应得到[B(OH)4]-,H3BO3和[B(OH)4]-中B的杂化轨道类型分别为为
(4)NaBH4被认为是有机化学上的“万能还原剂”,NaBH4的电子式为
(5)自然界中含硼元素的钠盐是一种天然矿藏,其化学式写作Na2B4O7·10H2O,实际上它的结构单元是由两个H3BO3和两个[B(OH)4]-缩合而成的双六元环,应该写成Na2[B4O5(OH)4]·8H2O,其结构如图所示,

它的阴离子可形成链状结构,则该晶体中不存在的作用力是
A.离子键 B.共价键 C.氢键 D.金属键 E.范德华力
(6)某种金属锂的硼氢化物是优质固体电解质,并具有高储氢密度。阳离子为Li+,每个阴离子是由12个硼原子和12个氢原子所构成的原子团。阴离子在晶胞中的位置如图所示,其堆积方式为

您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
解题方法
【推荐2】吉非替尼是一种合成的苯胺喹唑啉类化合物,是肺癌治疗的一线用药,良好的药效和广阔的市场前景引起很多学者兴趣,其中一种合成路线如图所示:

(1)化合物I中官能团的名称为____ ,反应①的反应类型为____ 。
(2)化合物II的结构简式为____ ,加热条件下,I与NaOH溶液反应的离子方程式为____ 。
(3)化合物III中C原子的杂化类型为____ 。
(4)化合物IV是比化合物I相对分子质量大14的同系物。化合物IV的芳香族同分异构体中,写出符合题意的其中任意一种结构简式____ 。
①苯环上有三个取代基;②能发生银镜反应;③能发生水解反应,1mol该有机物能够与3molNaOH溶液反应。④核磁共振氢谱图有5组峰,且面积比为1:1:2:2:6。
(5)已知:①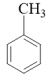
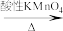
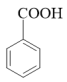

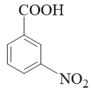
②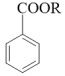

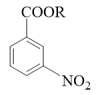
写出以 、
、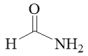 和CH3OH为原料(无机试剂任选)制备
和CH3OH为原料(无机试剂任选)制备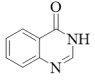 的合成路线流程图
的合成路线流程图____ 。

(1)化合物I中官能团的名称为
(2)化合物II的结构简式为
(3)化合物III中C原子的杂化类型为
(4)化合物IV是比化合物I相对分子质量大14的同系物。化合物IV的芳香族同分异构体中,写出符合题意的其中任意一种结构简式
①苯环上有三个取代基;②能发生银镜反应;③能发生水解反应,1mol该有机物能够与3molNaOH溶液反应。④核磁共振氢谱图有5组峰,且面积比为1:1:2:2:6。
(5)已知:①

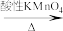



②



写出以
 、
、 和CH3OH为原料(无机试剂任选)制备
和CH3OH为原料(无机试剂任选)制备 的合成路线流程图
的合成路线流程图
您最近一年使用:0次
【推荐3】A、B、C、D、E、F、G是元素周期表前四周期中常见的七种元素,其原子序数依次增大,其相关信息如下表:
(1)AB32-的立体构型为________ ,其中A的杂化轨道类型是_________________________ ;
(2)A22-与B22+互为等电子体,则B22+的电子式可表示为______________ ,1molB22+中含有共用电子对的数目 为_____________ ;
(3)AD2是一种常用的溶剂,AD2的分子中存在___ 个π键。表中C、D、E三种元素分别与氢形成的共价键中,键长最大的是________ (用具体元素符号组成的化学键表示)。
(4)下列有关A2H2的说法正确的是_____ 。
A.分子中所有原子都满足8电子稳定结构 B.每个分子中σ键和π键数目之比为2:3
C.它是由极性键和非极性键构成的分子 D.分子的空间构型为直线形
(5)写出G元素的原子核外电子排布式___________ ;工业上常通过在空气中煅烧G的低价 含硫矿获得G单质,请写出该反应的方程式_____________________________ ;若往含有G2+的溶液中加过量氢氧化钠溶液,可生成Na2[G(OH)4]溶液,Na2[G(OH)4]具有的化学键类型有________ 。
A.离子键 B.极性共价键 C.非极性共价键 D.配位键
(6)表中F元素与Mn、Fe在工业上统称“黑色金属”,Mn、Fe 均为第 4 周期过渡金属元素,两元素的部分电离能数据列于下表:
F元素为_____ (填写元素名称);请写出基态 Mn2+的价电子轨道排布图____________________ ,比较两元素的 I2、 I3可知,气态 Mn2+再失去 1个电子比气态 Fe2+再失去 1个电子难,请解释原因__________________________________________________________ 。
| 元素 | 相关信息 |
| A | A的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| B | B原子基态时s电子与p电子数目相同 |
| C | C在组成化合物时没有正价 |
| D | 常温常压下,D单质是淡黄色固体,常在火山口附近沉积 |
| E | E和D同周期,E的电负性大于D |
| F | F原子基态时未成对电子数是同周期中最多的 |
| G | G的一种核素的质量数为63,中子数为34 |
(2)A22-与B22+互为等电子体,则B22+的电子式可表示为
(3)AD2是一种常用的溶剂,AD2的分子中存在
(4)下列有关A2H2的说法正确的是
A.分子中所有原子都满足8电子稳定结构 B.每个分子中σ键和π键数目之比为2:3
C.它是由极性键和非极性键构成的分子 D.分子的空间构型为直线形
(5)写出G元素的原子核外电子排布式
A.离子键 B.极性共价键 C.非极性共价键 D.配位键
(6)表中F元素与Mn、Fe在工业上统称“黑色金属”,Mn、Fe 均为第 4 周期过渡金属元素,两元素的部分电离能数据列于下表:
| 元素 | Mn | Fe | |
| 电离能/kJmol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 4048 | 2957 | |
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】2020年12月17日凌晨1时59分,“嫦娥五号”首次实现了我国地外天体采样返回目标,标志着我国航天事业迈出了一大步。带回的月壤中包含了H、O、N、Al、S、Cd、Zn、Ti、Cu、Au、Cr等多种元素。回答下列问题:
(1)一些氧化物的熔点如表所示:
解释表中氧化物之间熔点差异的原因:____ 。
(2)Cr2O 的结构如图所示。则该离子中σ键与π键的个数比为
的结构如图所示。则该离子中σ键与π键的个数比为____ 。
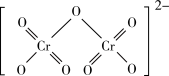
(3)[Cr(NH3)3(H2O)2Cl]2+中配体分子NH3、H2O的空间结构和相应的键角如图所示。H2O的键角小于NH3的键角,原因是____ 。
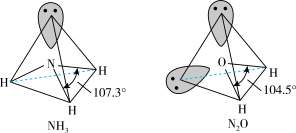
(4)已知TiO2与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示,该阳离子的化学式为____ ,阴离子的空间构型为____ 。
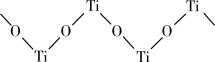
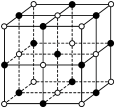
(5)已知TiN晶体的晶胞结构如图所示,若该晶胞中Ti原子与N原子的最近距离为apm,阿伏加德罗常数的值为NA,则晶胞的密度为____ g•cm-3。[M(TiN)=62g•mol-1,用含a、NA的代数式表示]
(1)一些氧化物的熔点如表所示:
| 氧化物 | Li2O | MgO | P4O6 | SO2 |
| 熔点/℃ | 1570 | 2800 | 23.8 | -75.5 |
(2)Cr2O
 的结构如图所示。则该离子中σ键与π键的个数比为
的结构如图所示。则该离子中σ键与π键的个数比为
(3)[Cr(NH3)3(H2O)2Cl]2+中配体分子NH3、H2O的空间结构和相应的键角如图所示。H2O的键角小于NH3的键角,原因是

(4)已知TiO2与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示,该阳离子的化学式为

(5)已知TiN晶体的晶胞结构如图所示,若该晶胞中Ti原子与N原子的最近距离为apm,阿伏加德罗常数的值为NA,则晶胞的密度为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐2】铁、钴均为第四周期第Ⅷ族元素,它们的单质及化合物具有广泛用途。回答下列问题:
(1)基态Co2+中的未成对电子数为___ ;Fe和Co的第四电离能I4(Fe)___ I4(Co)(填“>”、“<”或“=”)。
(2)将1molCoCl3·4NH3溶于水中,加入足量AgNO3溶液生成1molAgCl沉淀。则CoCl3·4NH3中配离子的化学式为___ ;已知孤电子对与成键电子的排斥作用大于成键电子对与成键电子的排斥作用,试判断NH3分子与钴离子形成配合物后H—N—H键角___ (填“变大”、“变小”或“不变”)。
(3)铁氮化合物(FexNy)在磁记录材料领域有着广泛的应用前景。某FexNy的制备需铁、氮气、丙酮和乙醇参与。
①丙酮(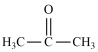 )分子中碳原子轨道的杂化类型是
)分子中碳原子轨道的杂化类型是___ ,1mol丙酮分子中含有σ键的数目为___ 。
②C、H、O三种元素的电负性由小到大的顺序为___ 。
③乙醇的沸点高于丙酮,这是因为___ 。
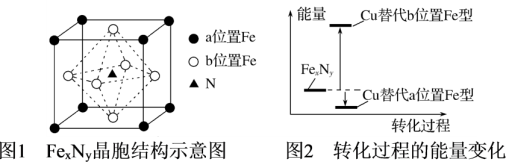
(4)某FexNy的晶胞如图1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x-n)CunNy。FexNy转化为两种Cu替代型产物的能量变化如图2所示。
①该结构中单纯分析铁的堆积,其堆积方式为___ 。
②其中更稳定的Cu替代型产物的化学式为____ 。
③若更稳定的Cu替代型产物的密度为ρg/cm3,则该晶胞中相邻的两个Fe原子的距离为___ nm。
(1)基态Co2+中的未成对电子数为
(2)将1molCoCl3·4NH3溶于水中,加入足量AgNO3溶液生成1molAgCl沉淀。则CoCl3·4NH3中配离子的化学式为
(3)铁氮化合物(FexNy)在磁记录材料领域有着广泛的应用前景。某FexNy的制备需铁、氮气、丙酮和乙醇参与。
①丙酮(
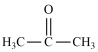 )分子中碳原子轨道的杂化类型是
)分子中碳原子轨道的杂化类型是②C、H、O三种元素的电负性由小到大的顺序为
③乙醇的沸点高于丙酮,这是因为
(4)某FexNy的晶胞如图1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x-n)CunNy。FexNy转化为两种Cu替代型产物的能量变化如图2所示。

①该结构中单纯分析铁的堆积,其堆积方式为
②其中更稳定的Cu替代型产物的化学式为
③若更稳定的Cu替代型产物的密度为ρg/cm3,则该晶胞中相邻的两个Fe原子的距离为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】B、N、F、Ti、Fe等都是重要的材料元素,其单质及化合物在诸多领域中都有广泛的应用。
(1)基态Ti原子s轨道上总共有_______ 个电子,其价电子轨道表达式为____________ 。
(2)在基态N原子中,核外存在______ 对自旋相反的电子,核外电子占据的最高能层符号为______ ,占据该能层电子的电子云轮廓图形状为__________________ 。
(3)南京理工大学团队成功合成了能在室温稳定存在的五氮阴离子盐(N5)6(H3O)3(NH4)4Cl,五氮阴离子N5-是制备全氮类物质N5+N5-的重要中间体,下列说法正确的是_____ 。
A. (N5)6(H3O)3(NH4)4Cl 中含四种离子 B. N5+N5-属于化合物
C. 每个N5-中含有36个电子 D. N5+N5-中既含极性键又含非极性键
(4)BF3分子空间结构为___________ ;在NH3中N原子的杂化方式为_______ 。
(5)六氟合钛酸钾(K2TiF6)中存在[TiF6]2- 配离子,则钛元素的化合价是_______ ,配体是_________ 。
(6)碳酸盐的热分解是由于晶体中阳离子结合碳酸根离子中的氧离子,使碳酸根离子分解为二氧化碳分子的结果。已知
请解释碱土金属元素碳酸盐热分解温度的变化规律:_______________________ 。
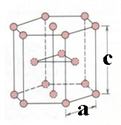
(7)金属钛有两种同素异形体,常温下是六方堆积,高温下是体心立方堆积。如图所示是钛晶体的一种晶胞,晶胞参数a=0.295nm,c =0.469 nm,则该钛晶体的密度为_____ g·cm-3(用NA 表示阿伏伽德罗常数的值,列出计算式即可)。
(1)基态Ti原子s轨道上总共有
(2)在基态N原子中,核外存在
(3)南京理工大学团队成功合成了能在室温稳定存在的五氮阴离子盐(N5)6(H3O)3(NH4)4Cl,五氮阴离子N5-是制备全氮类物质N5+N5-的重要中间体,下列说法正确的是
A. (N5)6(H3O)3(NH4)4Cl 中含四种离子 B. N5+N5-属于化合物
C. 每个N5-中含有36个电子 D. N5+N5-中既含极性键又含非极性键
(4)BF3分子空间结构为
(5)六氟合钛酸钾(K2TiF6)中存在[TiF6]2- 配离子,则钛元素的化合价是
(6)碳酸盐的热分解是由于晶体中阳离子结合碳酸根离子中的氧离子,使碳酸根离子分解为二氧化碳分子的结果。已知
| 碳酸盐 | MgCO3 | CaCO3 | SrCO3 | BaCO3 |
| 热分解温度/℃ | 402 | 900 | 1172 | 1360 |
| 阳离子半径/pm | 66 | 99 | 112 | 135 |
请解释碱土金属元素碳酸盐热分解温度的变化规律:
(7)金属钛有两种同素异形体,常温下是六方堆积,高温下是体心立方堆积。如图所示是钛晶体的一种晶胞,晶胞参数a=0.295nm,c =0.469 nm,则该钛晶体的密度为

您最近一年使用:0次



