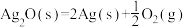下列说法正确的是
| A.增大压强,活化分子百分数增多,化学反应速率增大 |
B.C(石墨,s)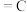 (金刚石,s) (金刚石,s) 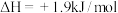 ,则金刚石比石墨稳定 ,则金刚石比石墨稳定 |
C.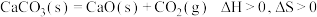 ,不论在何种条件下都不可能自发进行 ,不论在何种条件下都不可能自发进行 |
D.在恒温恒容下,发生反应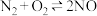 ,若在容器中充入 ,若在容器中充入 ,正、逆反应的速率均不变 ,正、逆反应的速率均不变 |
更新时间:2024-03-02 07:20:12
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】汽车发动机工作时会引发 和
和 反应,其能量变化如图所示:下列说法正确的是
反应,其能量变化如图所示:下列说法正确的是
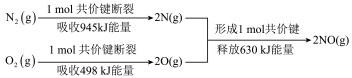
 和
和 反应,其能量变化如图所示:下列说法正确的是
反应,其能量变化如图所示:下列说法正确的是
A.上述反应中 是氧化剂 是氧化剂 |
B. (g)和 (g)和 (g)反应生成2molNO(g)时吸收183kJ能量 (g)反应生成2molNO(g)时吸收183kJ能量 |
C.1mol气态氮原子转化成 (g)时,能放出945kJ能量 (g)时,能放出945kJ能量 |
D.从图中数据可知 比 比 更稳定 更稳定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列叙述正确的是
A.密闭容器中存在: ,当时 ,当时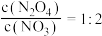 ,该反应到达限度 ,该反应到达限度 |
B.反应 在室温下能自发进行,该反应的 在室温下能自发进行,该反应的 |
C.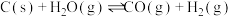 达平衡后,再补充足够碳, 达平衡后,再补充足够碳, 平衡转化率增大 平衡转化率增大 |
D.已知 (石墨,s) (石墨,s)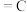 (金刚石,s) (金刚石,s)  ,则石墨比金刚石稳定 ,则石墨比金刚石稳定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】一定条件下,物质的量均为 0.3mol 的 X(g)与Y(g)在容积固定的密闭容器中发生反应:X(g)+3Y(g)⇌2Z(g) ΔH=-akJ•mol -1,下列说法正确的是
| A.达到平衡后,向平衡体系中充入稀有气体,正反应速率不发生变化 |
| B.反应一段时间后,X 与Y 的物质的量之比仍为 1:1 |
| C.达到平衡时,反应放出 0.1akJ 的热量 |
| D.X 与Y的物质的量相等,说明反应已达到平衡 |
您最近一年使用:0次
单选题
|
适中
(0.64)
名校
【推荐2】下列说法正确的是
| A.不管什么反应使用催化剂,都可以加快反应速率 |
B.可逆反应A(g) B(g)+C(g),增大压强正反应速率减小,逆反应速率增大 B(g)+C(g),增大压强正反应速率减小,逆反应速率增大 |
| C.对达到平衡的一个放热的可逆反应,若降低温度正反应速率减小,逆反应速率增大 |
| D.参加反应物质的性质是决定化学反应速率的主要因素 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】研究硫酸铜的量对锌与稀硫酸反应生成氢气速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。下列说法不正确的是
| 实验混合溶液 | A | B | C | D | E | F |
| 4 mol/LH2SO4溶液(mL) | 30 |  |  |  |  | 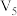 |
| 饱和CuSO4溶液(mL) | 0 | 0.5 | 2.5 | 5 | 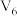 | 20 |
| H2O(mL) | 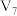 | 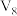 | 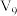 | 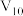 | 10 | 0 |
| 时间(s) | 60 | 50 | 40 | 30 | 20 | 45 |
| A.B组相较于A组反应速率加快,是因为形成了Zn-Cu-稀硫酸原电池 |
| B.加入MgSO4与Ag2SO4可以起与硫酸铜相同的加速作用 |
C. , ,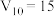 |
| D.F组时间比E组长,可能是置换出的铜太多,覆盖在锌粒表面,阻碍了反应的进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】用一定质量的锌粒与某浓度的稀硫酸反应制取H2,若要增大反应速率,则下列选项中采取的措施全部正确的是
①滴入几滴CuSO4溶液 ②将锌粒改为锌粉 ③改加浓硫酸 ④适当降低温度
①滴入几滴CuSO4溶液 ②将锌粒改为锌粉 ③改加浓硫酸 ④适当降低温度
| A.①③ | B.①② | C.②③ | D.①④ |
您最近一年使用:0次
【推荐2】我国学者结合实验和计算机模拟结果,研究了乙烯与苯的反应过程,如图所示(其中-Ph表示苯基)。下列说法正确的是
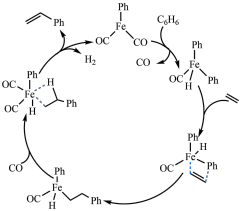
A.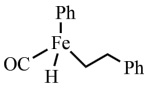 是该反应的催化剂 是该反应的催化剂 |
| B.反应过程涉及配位键的断裂和形成 |
| C.反应过程涉及到的化合物中氢元素均显+1价 |
| D.总反应分五步进行,为加成反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】在一定温度下,10mL 1.0mol/L H2SO4与Zn粒发生反应。不同时刻测定生成H2的体积(已折算为标准状况)如下表。
下列叙述不正确的是(溶液体积变化忽略不计)
| t/min | 0 | 1 | 3 | 5 | 7 | 9 |
| V(H2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)
| A.0~5 min的平均反应速率:v(H2SO4)≈0.02mol/(L•min) |
| B.5~9 min的平均反应速率:v(H2SO4)< 0.02mol/(L•min) |
| C.反应到5 min时,c(H2SO4)=0.010mol/L |
| D.反应到5 min时,Zn溶解了65mg |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】对于反应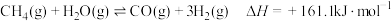 ,下列说法正确的是
,下列说法正确的是
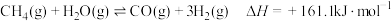 ,下列说法正确的是
,下列说法正确的是| A.该反应在任何温度下都能自发进行 |
B. 和 和 充分反应时,吸收的热量为322.2kJ 充分反应时,吸收的热量为322.2kJ |
C.反应的平衡常数可表示为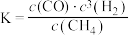 |
D.其他条件相同,增大 ,CH4的转化率下降 ,CH4的转化率下降 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】对于某可逆反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列叙述正确的是
4NO(g)+6H2O(g),下列叙述正确的是
 4NO(g)+6H2O(g),下列叙述正确的是
4NO(g)+6H2O(g),下列叙述正确的是| A.该反应为放热反应,则该反应只有在低温下才能自发进行 |
| B.保持容器内气体压强不变,向其中加入He,化学反应速率不变 |
| C.保持容器容积不变,向其中加入He,化学反应速率增大 |
| D.达到化学平衡时,4v正(O2)=5v逆(NO) |
您最近一年使用:0次

 )的能量
)的能量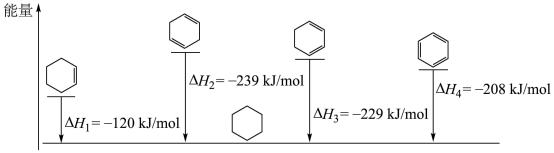
 ,说明碳碳双键加氢放出的热量与分子内碳碳双键数目成正比
,说明碳碳双键加氢放出的热量与分子内碳碳双键数目成正比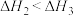 ,说明单双键交替的两个碳碳双键间存在相互作用,有利于物质稳定
,说明单双键交替的两个碳碳双键间存在相互作用,有利于物质稳定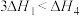 ,说明苯分子中不存在三个完全独立的碳碳双键
,说明苯分子中不存在三个完全独立的碳碳双键 ,说明苯分子比
,说明苯分子比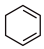 稳定
稳定