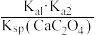在水溶液中主要以
在水溶液中主要以 、
、 的形式存在。方解石(主要成分
的形式存在。方解石(主要成分 )在天然水体中会逐渐溶解并释放
)在天然水体中会逐渐溶解并释放 ,与水体中的
,与水体中的 形成
形成 难溶物。体系中
难溶物。体系中 与
与 关系如下图所示,
关系如下图所示, 为
为 、
、 、
、 、
、 的浓度,单位为
的浓度,单位为 。已知天然水体表面
。已知天然水体表面 的分压保持恒定,
的分压保持恒定, 的电离方程式可写成
的电离方程式可写成 。下列说法错误的是
。下列说法错误的是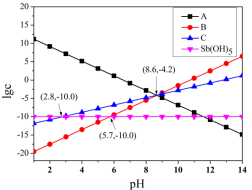
A.直线 代表的粒子为 代表的粒子为 |
B. 难溶物的 难溶物的 的数量级为 的数量级为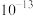 |
C. 的电离平衡常数的数值为 的电离平衡常数的数值为 |
D.溶液中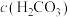 随着 随着 的增大而减小 的增大而减小 |
更新时间:2024-02-23 18:14:57
|
相似题推荐
单选题
|
较难
(0.4)
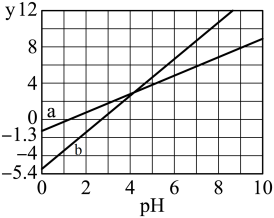
【推荐1】常温下,某二元弱酸H2A溶液中离子浓度与pH的关系如图所示{y为lg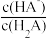 或lg
或lg }。下列说法错误的是
}。下列说法错误的是
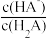 或lg
或lg }。下列说法错误的是
}。下列说法错误的是
A.曲线a为lg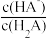 与pH的变化关系 与pH的变化关系 |
| B.该温度下,H2A的Ka1为10-1.3 |
| C.升高温度,则图中曲线a、b下移 |
| D.曲线a、b的交点处,溶液中c(A2—)=c(HA—) |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】类比pH的定义,对于稀溶液可以定义pC=-lgC,pKa=-lgKa。常温下,某浓度H2A溶液在不同pH值下,测得pC(H2A)、pC(HA-)、pC(A2-)变化如图所示。下列说法正确的是


| A.pH=6.00时,c(H2A)>c(HA-)>c(A2-) |
| B.常温下,pKa1(H2A)=5.30 |
| C.NaHA溶液中,c(H2A)<c(A2-) |
| D.pH=0.80~5.30时,c(H2A)+c(HA-)+c(A2-)先增大后减小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】Na2S2O5(焦亚硫酸钠)具有较强的还原性,25℃时,将0.5molNa2S2O5溶于水配成IL溶液,溶液中部分微粒浓度随溶液酸碱性变化如图所示。已知:Ksp(BaSO4)=1.0×10-10,Ksp(BaSO3)=5.0×10-7。下列说法正确的是
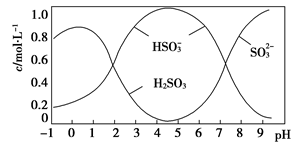

A.Na2S2O5水溶液pH=4.5是因为S2O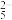 水解所致 水解所致 |
B.由图象可知,25℃时,HSO 的水解平衡常数约为10-7 的水解平衡常数约为10-7 |
C.向溶液中加入碱性物质使溶液pH升高的过程中,一定存在如下关系:c(Na+)+c(H+)=c(HSO )+2c(SO )+2c(SO )+c(OH-) )+c(OH-) |
D.将部分被空气氧化的该溶液的pH调为10,向溶液中滴加BaCl2溶液使SO 沉淀完全[c(SO 沉淀完全[c(SO )≤1.0×10-5mol·L-1],此时溶液中c(SO )≤1.0×10-5mol·L-1],此时溶液中c(SO )≤0.05mol·L-1 )≤0.05mol·L-1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】某温度下,向10 mL 0.1 mol·L-1 NaCl溶液和10 mL 0.1 mol·L-1 K2CrO4溶液中分别滴加0.1 mol·L-1 AgNO3溶液,滴加过程中pM[-lg c(Cl-)或-lg c(CrO )]与所加AgNO3溶液体积之间的关系如图所示,已知Ag2CrO4为红棕色沉淀。下列说法错误的是
)]与所加AgNO3溶液体积之间的关系如图所示,已知Ag2CrO4为红棕色沉淀。下列说法错误的是
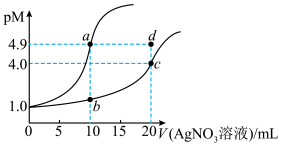
 )]与所加AgNO3溶液体积之间的关系如图所示,已知Ag2CrO4为红棕色沉淀。下列说法错误的是
)]与所加AgNO3溶液体积之间的关系如图所示,已知Ag2CrO4为红棕色沉淀。下列说法错误的是
| A.根据曲线数据计算可知,该温度下Ksp(Ag2CrO4)=4×10-12 |
| B.若将上述两份溶液混合后再逐滴加入AgNO3溶液,先产生白色沉淀 |
| C.若将上述NaCl溶液浓度改为0.2 mol·L-1,则a点会平移至d点 |
| D.a、b、c三点所示溶液中,Ag+的浓度大小关系为b>c>a |
您最近一年使用:0次

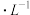 CH3COOH溶液中加入少量水,溶液中
CH3COOH溶液中加入少量水,溶液中 减小
减小 增大
增大 >1
>1 溶液的性质。
溶液的性质。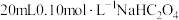 溶液中滴加
溶液中滴加 溶液。
溶液。 溶液。
溶液。 的电离常数
的电离常数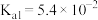 ,
,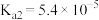 ,
,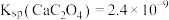 ,溶液混合后体积变化忽略不计。下列说法正确的是
,溶液混合后体积变化忽略不计。下列说法正确的是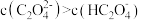 时,
时,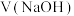 至少大于10mL
至少大于10mL