证据推理是化学学科重要核心素养。下列证据能得出相应推论的是
| 选项 | 证据 | 推论 |
| A | 反应2CO2(g)+6H2(g) C2H4(g)+4H2O(g)能自发进行 C2H4(g)+4H2O(g)能自发进行 | 该反应的△H<0 |
| B | 增大压强,化学反应速率加快 | 增大压强,活化分子百分数增多,有效碰撞概率增大 |
| C | 用pH计测定浓度相等的NaClO溶液和Na2CO3溶液的pH,NaClO溶液碱性更强 | 酸性:H2CO3>HClO |
| D | 向双氧水中滴加浓硫酸,产生气体的速率加快 | 浓硫酸对H2O2的分解具有催化作用 |
| A.A | B.B | C.C | D.D |
更新时间:2024-03-28 19:39:31
|
相似题推荐
【推荐1】化学反应: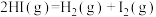 △H实际上是经过两步基元反应完成的:第一步:
△H实际上是经过两步基元反应完成的:第一步: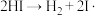 ;第二步:……。该反应过程的能量变化如图所示,下列说法不正确的是
;第二步:……。该反应过程的能量变化如图所示,下列说法不正确的是

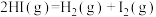 △H实际上是经过两步基元反应完成的:第一步:
△H实际上是经过两步基元反应完成的:第一步: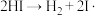 ;第二步:……。该反应过程的能量变化如图所示,下列说法不正确的是
;第二步:……。该反应过程的能量变化如图所示,下列说法不正确的是
A.第一步反应的逆反应的活化能是( ) ) |
B.第二步基元反应是: |
| C.分子有效碰撞几率最大的步骤对应的基元反应是第一步 |
D.若使用催化剂,( )不会发生变化 )不会发生变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法正确的是
| A.碰撞理论认为,反应物分子间必须相互碰撞才有可能发生反应,反应速率的大小与单位时间内反应物分子间有效碰撞的次数成正比 |
| B.电解原理在生产中有着广泛的应用,工业上用电解熔融的氯化钠、氯化镁,氯化铝来冶炼Na、Mg、Al等活泼金属单质 |
| C.盖斯定律表明,一个化学反应的焓变(∆H)不仅与反应的起始和最终状态有关,还与反应的途径及过程有关 |
| D.在工业生产中,研制出性能优良的催化剂可以使反应的温度降低,有效提高反应物的转化率,从而起到很好的节能效果 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,下列各组实验中,反应速率最快的是
| 组号 | 反应温度/℃ | Na2S2O3 | H2SO4 | H2O | ||
| 体积/mL | 浓度/mol·L-1 | 体积/mL | 浓度/mol·L-1 | 体积/mL | ||
| A | 10 | 5 | 0.2 | 10 | 0.1 | 5 |
| B | 10 | 5 | 0.1 | 5 | 0.2 | 10 |
| C | 30 | 5 | 0.2 | 10 | 0.1 | 5 |
| D | 30 | 5 | 0.1 | 5 | 0.2 | 10 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】N2+3H2 2NH3是工业上制造氮肥的重要反应。下列关于该反应的说法正确的是
2NH3是工业上制造氮肥的重要反应。下列关于该反应的说法正确的是
 2NH3是工业上制造氮肥的重要反应。下列关于该反应的说法正确的是
2NH3是工业上制造氮肥的重要反应。下列关于该反应的说法正确的是| A.增加NH3的浓度不影响反应速率 |
| B.升高体系温度能加快反应速率 |
| C.使用催化剂不影响反应速率 |
| D.若反应在密闭容器中进行,N2和H2的转化率能达到100% |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】从烟道废气中回收硫的原理之一: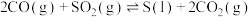
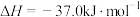 ,在恒压密闭容器中,平衡时SO2的转化率
,在恒压密闭容器中,平衡时SO2的转化率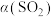 与起始充入的
与起始充入的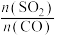 和温度(T)的关系如图所示。下列说法中正确的是
和温度(T)的关系如图所示。下列说法中正确的是
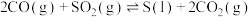
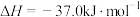 ,在恒压密闭容器中,平衡时SO2的转化率
,在恒压密闭容器中,平衡时SO2的转化率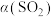 与起始充入的
与起始充入的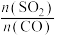 和温度(T)的关系如图所示。下列说法中正确的是
和温度(T)的关系如图所示。下列说法中正确的是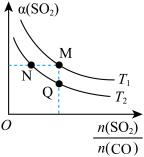
A.正反应的活化能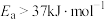 |
B.CO的转化率 :M>N :M>N |
C.正反应速率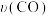 :M>Q :M>Q |
D.该反应的化学平衡常数表达式: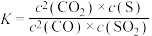 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】铬及其化合物在催化方面具有重要应用。Cr2O3在丙烷脱氢:C3H8(g)=3C(石墨,s)+4H2(g)过程中起到催化作用,其中的部分反应历程如图所示。下列说法错误的是
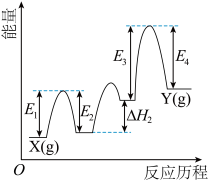

| A.Cr2O3在丙烷脱氢的反应过程中可能作氧化剂和氧化产物 |
| B.该反应的焓变为E1-E2+ΔH2+E3-E4 |
| C.C3H8(g)=3C(石墨,s)+4H2(g),该反应在高温条件下能自发进行 |
| D.该反应可实现将化学能转化为热能 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】对于化学反应方向的判断,下列说法中正确的是
| A.温度、压强一定时,放热的熵减小的反应一定能自发进行 |
| B.温度、压强一定时,焓因素和熵因素共同决定一个化学反应的方向 |
| C.反应焓变是决定反应能否进行的惟一因素 |
| D.固体的溶解过程与熵变无关 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】某兴趣小组将镁条投入水中,镁条表面缓慢产生少量气泡,数分钟后反应停止,镁条表面失去光泽。为了探究 和
和 对镁与水反应的影响,该小组将与水反应后的镁条加入到4种盐溶液中进行对比实验,结果如下。
对镁与水反应的影响,该小组将与水反应后的镁条加入到4种盐溶液中进行对比实验,结果如下。
下列说法错误的是
 和
和 对镁与水反应的影响,该小组将与水反应后的镁条加入到4种盐溶液中进行对比实验,结果如下。
对镁与水反应的影响,该小组将与水反应后的镁条加入到4种盐溶液中进行对比实验,结果如下。| 实验序号 | a | b | c | d |
| 盐溶液(均为0.1 mol/L) | NH4Cl | NaHCO3 | NaCl | NH4HCO3 |
| 溶液起始pH | 5.1 | 8.3 | 7.0 | 7.8 |
| 30 min时产生气体体积(mL) | 1.5 | 0.7 | <0.1 | 1.4 |
| 气体的主要成分 | H2 | |||
| 30 min时镁条表面情况 | 大量固体附着(固体可溶于盐酸) | |||
| A.b、d所得固体中可能有碱式碳酸镁 |
B.根据实验a、d,可以推出 不能促进镁与水反应 不能促进镁与水反应 |
C.综合实验a~d,可以推出 和 和 能够相互促进水解 能够相互促进水解 |
| D.镁与水反应数分钟后停止,是因为其表面被生成的难溶性固体覆盖所致 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法错误的是
| A.相同温度下醋酸的电离度,pH=3的大于pH=4的 |
| B.将pH=5的某酸稀释10倍,测得其pH<6,则该酸为弱酸 |
| C.向HClO稀溶液中不断加水稀释,c(ClO-)与c(H+)之比逐渐减小 |
| D.常温下,等浓度的KA溶液的pH小于K2B溶液的pH,则酸性HA>H2B |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】常温条件下,向V1mL浓度均为c mol·L-1的弱酸HA和HCl混合溶液中逐滴加入0.1mol·L-1弱碱BOH,溶液的导电能力随BOH溶液加入量的变化如图所示(忽略溶液混合时的体积变化)。下列说法错误的是


| A.c = 0.1 mol·L-1 |
| B.b点溶液中c(B+) +c( BOH) =c(A-) +c( HA) |
| C.若c点溶液中c(BOH) >2c(HA),则BA溶液显碱性 |
| D.滴加BOH溶液过程中,水的电离程度先增大后减小 |
您最近一年使用:0次

 与KI溶液反应时,能发生以下反应:①
与KI溶液反应时,能发生以下反应:①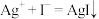
 ,②
,②
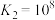 。设计如下装置进行验证,一段时间后,石墨Ⅱ电极上有光亮的物质生成。
。设计如下装置进行验证,一段时间后,石墨Ⅱ电极上有光亮的物质生成。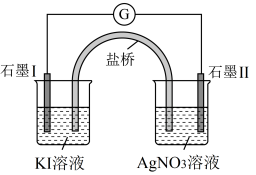
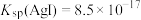 ,氧化性
,氧化性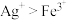 ,下列有关叙述正确的是
,下列有关叙述正确的是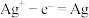
 :
: ;反应活化能:①>②
;反应活化能:①>②

