常温下,CaSO4在水中的沉淀溶解平衡曲线如图所示,已知常温下Ksp(CaSO4)=9×10-6.下列说法正确的是

| A.升高温度曲线会往左下方移动 |
| B.b点加水可以变到b',且此时的Ksp(CaSO4)=9×10-6 |
| C.d点表示CaSO4的过饱和溶液 |
| D.加入Na2SO4(s),可以使溶液由c点变到a点 |
更新时间:2024-04-11 18:14:55
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】工业上为了除去锅炉中的水垢,要向锅炉里注入Na2CO3溶液浸泡一段时间,下列叙述正确的是
A.若c(Na2CO3)=c[(NH4)2CO3],则两溶液中c(CO )也相等 )也相等 |
B.锅炉中加入Na2CO3溶液发生反应的离子方程式为CO (aq)+CaSO4(s) (aq)+CaSO4(s) CaCO3(s)+SO CaCO3(s)+SO (aq) (aq) |
| C.盐酸溶液中,Ksp(CaCO3)增大,Ksp(CaSO4)减小 |
D.向Na2CO3溶液中通入适量的CO2使溶液呈中性时,c(Na+)=c(CO )+c(HCO )+c(HCO ) ) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.将NH4Cl溶液蒸干制备NH4Cl固体 |
| B.施肥时,草木灰不能与NH4Cl混合施用,是因为K2CO3与NH4Cl反应生成氨气,降低肥效 |
| C.相同条件下,氯化银在水中的溶解能力与在氯化钠溶液中的溶解能力相同 |
| D.易溶性强电解质的稀溶液中不存在分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列叙述中正确的是
| A.升高温度,沉淀溶解平衡都是向促进沉淀溶解的方向移动 |
| B.绝对不溶解的物质是不存在的 |
| C.难溶电解质在水溶液中达到沉淀溶解平衡时,沉淀和溶解即停止 |
D.BaSO4(s)⇌SO (aq)+Ba2+(aq)表示溶解平衡;H2O+HSO (aq)+Ba2+(aq)表示溶解平衡;H2O+HSO ⇌SO ⇌SO +H3O+表示水解平衡 +H3O+表示水解平衡 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在平衡体系Ca(OH)2(s) Ca2++2OH- △H<0中,能使c(Ca2+)减小,而使c(OH-)增大的是
Ca2++2OH- △H<0中,能使c(Ca2+)减小,而使c(OH-)增大的是
 Ca2++2OH- △H<0中,能使c(Ca2+)减小,而使c(OH-)增大的是
Ca2++2OH- △H<0中,能使c(Ca2+)减小,而使c(OH-)增大的是| A.加入少量CuCl2固体 | B.加入少量NaCl固体 |
| C.加入少量K2CO3固体 | D.升高体系温度 |
您最近一年使用:0次
【推荐1】下列关于甲、乙、丙、丁四个图象的说法中,正确的是
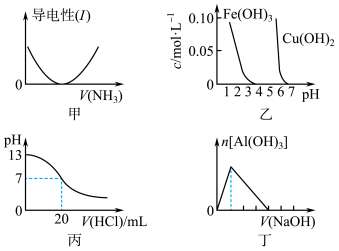

| A.图甲表示向盐酸溶液中通入NH3过程中溶液导电性的变化 |
| B.由图乙可知,若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量CuO至pH在4左右 |
| C.图丙表示25 ℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1氨水,溶液的pH随加入盐酸体积的变化 |
| D.图丁表示向Al2(SO4)3溶液中滴入NaOH溶液,生成Al(OH)3沉淀的量随NaOH溶液体积的变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验设计、现象和结论都正确的是
选项 | 实验 | 现象 | 结论 |
A | 将CO2通入BaCl2溶液中 | 有白色沉淀生成 | 白色沉淀是BaCO3 |
B | 向两支试管中各加入1 mL 1 mol/L的酸性KMnO4溶液,再向两支试管分别加入2 mL 1 mol/L的H2C2O4溶液和2mL0.5mol/L的H2C2O4溶液,记录高锰酸钾溶液褪色所需时间 | 1 mol/L的H2C2O4溶液中高锰酸钾溶液褪色快 | 浓度越大,反应速率越快 |
C | 向含AgCl和AgBr的饱和溶液中加入足量浓AgNO3溶液 | 产生两种颜色沉淀,但以白色为主 |
|
D | 向滴有酚酞的氨水中滴加氯水 | 溶液的红色褪去 | 氯水具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】要除去CuCl2溶液中的Fe3+ ,甲同学不知道调整溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp = 1×10-38,Cu(OH)2的溶度积Ksp=3×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol•L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0mol•L-1,通过调节溶液pH除去Fe3+而不损失Cu2+,调节pH的取值范围
| A.3≤pH<4 | B.3≤pH≤4 |
| C.2<pH≤3 | D.2≤pH<3 |
您最近一年使用:0次

 时,
时, 与
与 在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是
在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是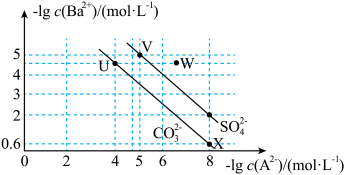
 时,
时,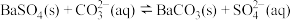 ,其平衡常数
,其平衡常数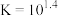
 悬浊液中加水稀释,平衡右移,
悬浊液中加水稀释,平衡右移, 和
和 增大
增大 在水溶液中存在平衡:
在水溶液中存在平衡: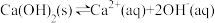 ,升温,溶液碱性增强
,升温,溶液碱性增强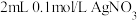 溶液的试管中滴加
溶液的试管中滴加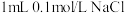 溶液,再向其中滴加4-5滴
溶液,再向其中滴加4-5滴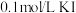 溶液,先观察到白色沉淀,后又产生黄色沉淀,说明
溶液,先观察到白色沉淀,后又产生黄色沉淀,说明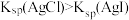
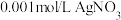 溶液滴入
溶液滴入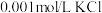 和
和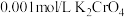 混合溶液中,先产生
混合溶液中,先产生 ,
,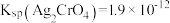 ]
]


