用锌窑渣回收Cu和 。已知锌窑渣主要成分有Fe、
。已知锌窑渣主要成分有Fe、 、
、 、FeS、CuS、
、FeS、CuS、 等。其流程如下图所示:
等。其流程如下图所示:
(1)滤渣的主要成分是_______ ,试剂1的化学式为_______ 。
(2)一般的矿物质用盐酸浸出的速率要比硫酸高,但在实际工业生产中一般用硫酸对矿物质进行酸浸。其原因除了盐酸比硫酸价格高外,你认为还有的原因是______ (填一种原因即可)。
(3)为了得到目标产物,对沉淀1的处理方法为_______ ,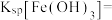
_______ 。
(4)氧化酸浸装置中,氧气的分压对Cu、Fe的溶出率的影响如图所示。_______ 。
②Fe溶出率随氧气分压增大而增大的原因是_______ 。
 。已知锌窑渣主要成分有Fe、
。已知锌窑渣主要成分有Fe、 、
、 、FeS、CuS、
、FeS、CuS、 等。其流程如下图所示:
等。其流程如下图所示: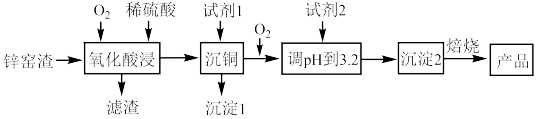
(1)滤渣的主要成分是
(2)一般的矿物质用盐酸浸出的速率要比硫酸高,但在实际工业生产中一般用硫酸对矿物质进行酸浸。其原因除了盐酸比硫酸价格高外,你认为还有的原因是
(3)为了得到目标产物,对沉淀1的处理方法为
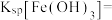
(4)氧化酸浸装置中,氧气的分压对Cu、Fe的溶出率的影响如图所示。
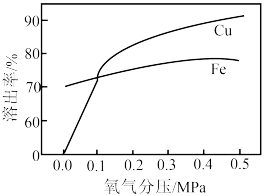
②Fe溶出率随氧气分压增大而增大的原因是
更新时间:2024-04-17 11:41:43
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】研究+6价铬盐不同条件下微粒存在形式及氧化性,某小组同学进行如下实验
已知:资料1: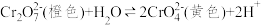
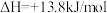 ;
;
资料2:+6价铬盐在一定条件下可被还原为 ,
, 在水溶液中为绿色。
在水溶液中为绿色。
(1)iii和i对比,推测iii的现象是____ 。
(2)ii和i对比,ii中溶液橙色加深。甲认为温度也会影响平衡的移动,橙色加深不一定是 增大影响的结果;乙认为橙色加深一定是
增大影响的结果;乙认为橙色加深一定是 增大对平衡的影响。你认为是否需要再设计实验证明?
增大对平衡的影响。你认为是否需要再设计实验证明?____ (填“是”或“否”),理由是______ 。
(3)对比实验iv与v,可知:在______ 条件下,+6价 被还原为
被还原为______ ,其对应的离子方程式为________ 。
(4)为进一步确定铬(VI)盐溶液的氧化性与酸碱性的关系,某同学进行实验如下:
I.进行实验a和b:
用离子方程式解释a中现象:_______ 。
II.继续进行实验c:
为了说明产生上述现象的原因,补充实验d:向 蒸馏水中滴加
蒸馏水中滴加 的
的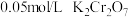 橙色溶液3滴,溶液变成浅橙色。
橙色溶液3滴,溶液变成浅橙色。
①补充实验d的目的是______ 。
②用化学平衡移动原理解释c中现象:_____ 。
③根据实验a~c,可推测: 溶液和铬(VI)盐溶液的反应与溶液酸碱性有关。
溶液和铬(VI)盐溶液的反应与溶液酸碱性有关。
a.碱性条件下, 溶液和铬(VI)盐溶液不发生氧化还原反应;
溶液和铬(VI)盐溶液不发生氧化还原反应;
b.______ 。
④向实验c所得黄色溶液中继续滴加硫酸,产生的现象证实了上述推测。该现象是_____ 。
| 系列 实验I | 装置 | 滴管中的试剂 | 试管中的试剂 | 操作 | 现象 |
| i |
|  水 水 | 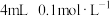  溶液 溶液 | 振荡 | 溶液颜色略微变浅 |
| ii | 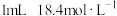 浓硫酸 浓硫酸 | 振荡 | 溶液橙色明显变深 | ||
| iii |  溶液 溶液 | 振荡 | ___________ | ||
| iv | 3滴浓 溶液 溶液 | iii中溶液 | 振荡 | 无明显现象 | |
| v | 过量稀硫酸 | iv中溶液 | 边滴边振荡 | 溶液颜色由黄色逐渐变橙色,最后呈绿色 |
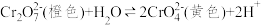
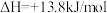 ;
;资料2:+6价铬盐在一定条件下可被还原为
 ,
, 在水溶液中为绿色。
在水溶液中为绿色。(1)iii和i对比,推测iii的现象是
(2)ii和i对比,ii中溶液橙色加深。甲认为温度也会影响平衡的移动,橙色加深不一定是
 增大影响的结果;乙认为橙色加深一定是
增大影响的结果;乙认为橙色加深一定是 增大对平衡的影响。你认为是否需要再设计实验证明?
增大对平衡的影响。你认为是否需要再设计实验证明?(3)对比实验iv与v,可知:在
 被还原为
被还原为(4)为进一步确定铬(VI)盐溶液的氧化性与酸碱性的关系,某同学进行实验如下:
I.进行实验a和b:
| 序号 | 操作 | 现象 |
| a | 向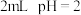 的 的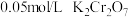 的橙色溶液中滴加饱和 的橙色溶液中滴加饱和 溶液( 溶液( 约为9)3滴 约为9)3滴 | 溶液变绿色 |
| b | 向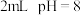 的 的 的 的 黄色溶液中滴加饱和 黄色溶液中滴加饱和 溶液3滴 溶液3滴 | 溶液没有明显变化 |
II.继续进行实验c:
| 序号 | 操作 | 现象 |
| c | 向 饱和 饱和 溶液中滴加 溶液中滴加 的 的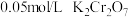 的橙色溶液3滴 的橙色溶液3滴 | 溶液变黄色 |
 蒸馏水中滴加
蒸馏水中滴加 的
的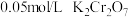 橙色溶液3滴,溶液变成浅橙色。
橙色溶液3滴,溶液变成浅橙色。①补充实验d的目的是
②用化学平衡移动原理解释c中现象:
③根据实验a~c,可推测:
 溶液和铬(VI)盐溶液的反应与溶液酸碱性有关。
溶液和铬(VI)盐溶液的反应与溶液酸碱性有关。a.碱性条件下,
 溶液和铬(VI)盐溶液不发生氧化还原反应;
溶液和铬(VI)盐溶液不发生氧化还原反应;b.
④向实验c所得黄色溶液中继续滴加硫酸,产生的现象证实了上述推测。该现象是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】钨是熔点最高的金属,也是重要的战略物资。自然界中钨矿石主要有黑钨矿和白钨矿两种。其中,黑钨矿主要成分是铁和锰的钨酸盐(FeWO4、MnWO4) 以及少量杂质(含Si、P、As元素的化合物)。由黑钨矿冶炼钨的“黑钨精矿高压碱煮(烧破)一溶剂萃取一蒸发结晶法”工艺流程如下图:
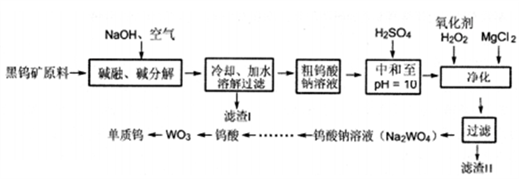
回答下列问题:
(1) 高压碱煮法中,“高压”的目的是_____________ 。
(2) 滤渣1的主要成分中含有的金属元素为_______ 。
(3) 除最后 一步外,流程中钨元素价态均未发生改变,则FeWO4中铁元素的价态为_____ 。第一步黑钨矿原料熔融时,FeWO4发生反应的化学方程式为________ 。
(4) H2SO4中和后溶液中还有SiO32-、AsO33-、AsO43-、PO43-等离子,则加入H2O2时发生反 应的离子方程式为_________ 。
(5) 钨酸钠溶液还含有NaOH、NaCl 和_____ 杂质。为了得到纯净的钨酸,需要经过萃取和反萃取工业流程。该操作中使用到的玻璃仪器有_________ 。 向钨酸钠溶液中加入四辛基氧化铵有机萃取剂萃取分液,此时钨元素处于_____ 层中(填“有机”或“无机”)。然后加入氨水反萃取、结晶得到仲钨酸铵(NH4)6W7O2·7H2O,仲钨酸铵加热分解得到三氧化钨的化学方程式为_________________________ 。

回答下列问题:
(1) 高压碱煮法中,“高压”的目的是
(2) 滤渣1的主要成分中含有的金属元素为
(3) 除最后 一步外,流程中钨元素价态均未发生改变,则FeWO4中铁元素的价态为
(4) H2SO4中和后溶液中还有SiO32-、AsO33-、AsO43-、PO43-等离子,则加入H2O2时发生反 应的离子方程式为
(5) 钨酸钠溶液还含有NaOH、NaCl 和
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】我国是少数几个拥有石煤资源的国家之一,工业上以伴生钒的石煤(主要成分为V2O3,含少量P2O5、SiO2等杂质)为原料制备钒的主要流程如图:
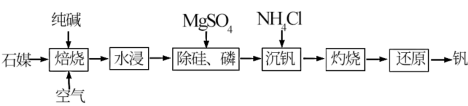
已知:①NH4VO3难溶于水。
②Ksp(MgSiO3)=2.4×10-5,Ksp[Mg3(PO4)2]=2.7×10-27。
请问答下列问题:
(1)焙烧:通入空气的条件下,向石煤中加纯碱焙烧,将V2O3转化为NaVO3的化学方程式为___ 。
(2)除硅、磷。用MgSO4溶液除硅、磷时,Si、P会形成MgSiO3、Mg3(PO4)2沉淀。若沉淀后溶液中c(PO )=1.0×10-8mol/L,则c(SiO
)=1.0×10-8mol/L,则c(SiO )=
)=___ 。随着温度升高,除磷率会显著下降,原因一是温度升高,Mg3(PO4)2溶解度增大;二是___ 。
(3)沉钒。该操作产生的滤液中,两种主要的溶质阴离子是___ (写符号);检验该滤液中两种阴离子方法是___ 。
(4)灼烧。在灼烧NH4VO3的过程中,固体残留率随温度变化的曲线如图所示,则0℃~210℃,发生反应的化学方程式为___ 。
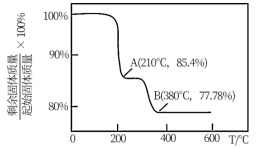
(5)还原。在高温真空条件下,用过量焦炭还原V2O5可以生成钒单质,该反应的化学方程式为___ 。

已知:①NH4VO3难溶于水。
②Ksp(MgSiO3)=2.4×10-5,Ksp[Mg3(PO4)2]=2.7×10-27。
请问答下列问题:
(1)焙烧:通入空气的条件下,向石煤中加纯碱焙烧,将V2O3转化为NaVO3的化学方程式为
(2)除硅、磷。用MgSO4溶液除硅、磷时,Si、P会形成MgSiO3、Mg3(PO4)2沉淀。若沉淀后溶液中c(PO
 )=1.0×10-8mol/L,则c(SiO
)=1.0×10-8mol/L,则c(SiO )=
)=(3)沉钒。该操作产生的滤液中,两种主要的溶质阴离子是
(4)灼烧。在灼烧NH4VO3的过程中,固体残留率随温度变化的曲线如图所示,则0℃~210℃,发生反应的化学方程式为

(5)还原。在高温真空条件下,用过量焦炭还原V2O5可以生成钒单质,该反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】锌的用途广泛,主要用于镀锌板及精密铸造等行业。以粗氧化锌(主要成分为ZnO及少量Fe2O3、CuO、MnO、SiO2)为原料制备锌的工艺流程如图所示:
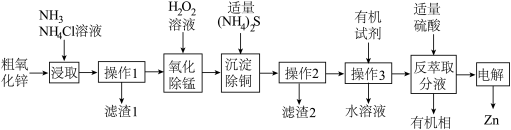
已知:①“浸取”时。ZnO、 CuO转化为[ Zn(NH3)4]2+、[Cu(NH3)4]2+进入溶液:
②25℃时,Ksp(CuS)=6.4×10-36, Ksp(ZnS)=1.6 ×10-24;
③沉淀除铜标准:溶液中 ≤2.0×10-6
≤2.0×10-6
回答下列问题:
(1)“滤渣1”的主要成分为Fe(OH)3、Mn(OH)2和___________ (填化学式),“ 操作3”的名称为___________ 。
(2)“氧化除锰”时,H2O2将Mn2+转化为难溶的MnO2,该反应的离子方程式为___________ 。
(3)“沉淀除铜”时,锌的最终回收率、除铜效果[除铜效果以反应后溶液中铜锌比 表示] 与“(NH4)2 S加入量”[以
表示] 与“(NH4)2 S加入量”[以 表示]的关系曲线如图所示。
表示]的关系曲线如图所示。
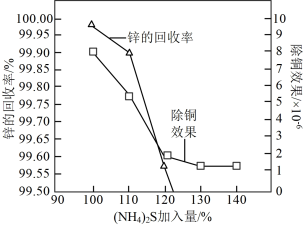
①当(NH4)2S加入量≥100%时,锌的最终回收率下降的原因是___________ (用离子方程式表示),该反应的平衡常数为___________ 。(已知) [ Zn(NH3)4]2+的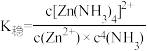 =2. 9 ×109]
=2. 9 ×109]
②“沉淀除铜”时(NH4 )2S加入量最好应选___________ 。
a.100% b.110% c.120% d.130%
(4)电解后溶液中的溶质主要成分是___________ , 可用于循环使用。

已知:①“浸取”时。ZnO、 CuO转化为[ Zn(NH3)4]2+、[Cu(NH3)4]2+进入溶液:
②25℃时,Ksp(CuS)=6.4×10-36, Ksp(ZnS)=1.6 ×10-24;
③沉淀除铜标准:溶液中
 ≤2.0×10-6
≤2.0×10-6回答下列问题:
(1)“滤渣1”的主要成分为Fe(OH)3、Mn(OH)2和
(2)“氧化除锰”时,H2O2将Mn2+转化为难溶的MnO2,该反应的离子方程式为
(3)“沉淀除铜”时,锌的最终回收率、除铜效果[除铜效果以反应后溶液中铜锌比
 表示] 与“(NH4)2 S加入量”[以
表示] 与“(NH4)2 S加入量”[以 表示]的关系曲线如图所示。
表示]的关系曲线如图所示。
①当(NH4)2S加入量≥100%时,锌的最终回收率下降的原因是
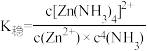 =2. 9 ×109]
=2. 9 ×109]②“沉淀除铜”时(NH4 )2S加入量最好应选
a.100% b.110% c.120% d.130%
(4)电解后溶液中的溶质主要成分是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】草酸锰常用作光敏材料、除污剂(如除墨水)等。以锰渣[主要成分为 、
、 、
、 、
、 、
、 、
、 等]为原料制备草酸锰晶体的工艺如下。
等]为原料制备草酸锰晶体的工艺如下。
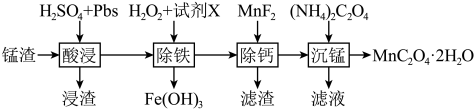
已知部分信息如下:
①几种难溶氢氧化物沉淀的pH.
②几种难溶电解质的溶度积常数如下。
回答下列问题:
(1)“除铁”中双氧水的作用是___________ (用离子方程式表示),应调节pH的范围为___________ 。
(2)分离 的操作需要使用的玻璃仪器有
的操作需要使用的玻璃仪器有___________ ,利用 制备铁红的操作是
制备铁红的操作是___________ 。
(3)化学上,平衡常数大于 时,认为该反应已完全。请通过计算和必要的文字说明“除钙”过程中
时,认为该反应已完全。请通过计算和必要的文字说明“除钙”过程中 是否反应完全:
是否反应完全:___________ 。
(4) 的结构式为
的结构式为 ,带*号的氧原子为配位原子。在“沉锰”中,
,带*号的氧原子为配位原子。在“沉锰”中, 过量时形成配合物。已知:
过量时形成配合物。已知: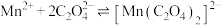 的
的 ;
;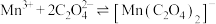 的
的 。
。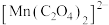 中
中 的配位数为
的配位数为___________ ;在水溶液中,稳定性: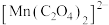
___________ 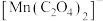 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(5)一定质量的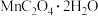 (摩尔质量为
(摩尔质量为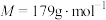 )在空气中灼烧,每一步所得固体纯净物的质量与温度关系如图。
)在空气中灼烧,每一步所得固体纯净物的质量与温度关系如图。

a→b段反应的化学方程式是___________ 。e点对应的氧化物化学式为___________ 。
 、
、 、
、 、
、 、
、 、
、 等]为原料制备草酸锰晶体的工艺如下。
等]为原料制备草酸锰晶体的工艺如下。
已知部分信息如下:
①几种难溶氢氧化物沉淀的pH.
| 难溶氢氧化物 |  |  |  |
| 开始沉淀的pH | 2.7 | 7.6 | 7.7 |
| 完全沉淀的pH | 3.7 | 9.6 | 9.8 |
| 电解质 |  |  | 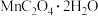 |
 | 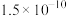 | 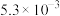 |  |
(1)“除铁”中双氧水的作用是
(2)分离
 的操作需要使用的玻璃仪器有
的操作需要使用的玻璃仪器有 制备铁红的操作是
制备铁红的操作是(3)化学上,平衡常数大于
 时,认为该反应已完全。请通过计算和必要的文字说明“除钙”过程中
时,认为该反应已完全。请通过计算和必要的文字说明“除钙”过程中 是否反应完全:
是否反应完全:(4)
 的结构式为
的结构式为 ,带*号的氧原子为配位原子。在“沉锰”中,
,带*号的氧原子为配位原子。在“沉锰”中, 过量时形成配合物。已知:
过量时形成配合物。已知: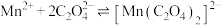 的
的 ;
;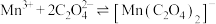 的
的 。
。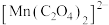 中
中 的配位数为
的配位数为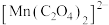
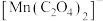 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(5)一定质量的
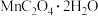 (摩尔质量为
(摩尔质量为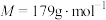 )在空气中灼烧,每一步所得固体纯净物的质量与温度关系如图。
)在空气中灼烧,每一步所得固体纯净物的质量与温度关系如图。
a→b段反应的化学方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】铁黄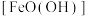 是一种不溶于水的黄色固体,可用作制造黄色颜料,也是制备饮水处理剂一高铁酸钾的原料。一种以工厂废料(含
是一种不溶于水的黄色固体,可用作制造黄色颜料,也是制备饮水处理剂一高铁酸钾的原料。一种以工厂废料(含 、
、 、
、 、CuO)为原料生产铁黄
、CuO)为原料生产铁黄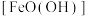 的工艺流程如图所示。
的工艺流程如图所示。
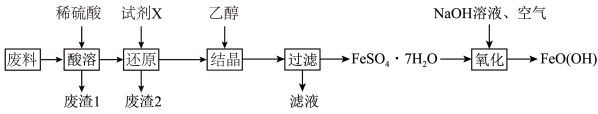
已知: 为酸性氧化物,不与硫酸等强酸反应;
为酸性氧化物,不与硫酸等强酸反应; 易溶于水,难溶于乙醇。
易溶于水,难溶于乙醇。
回答下列问题:
(1)铁黄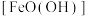 中铁元素化合价为
中铁元素化合价为_______ 。
(2)“酸溶”时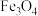 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(3)“废渣1”的主要成分是_______ 。
(4)“还原”时会加入过量的试剂X,“试剂X”宜选择的是_______(填标号)。
(5)“废渣2”的主要成分是_______ 。检验“过滤”的“滤液”中是否含有 所用的试剂为
所用的试剂为_______ (填化学式)溶液。
(6)“氧化”时,理论上氯气氧化性更强,但通常不用氯气代替空气,除考虑成本因素外,另一原因是_______ 。
(7)由 氧化为
氧化为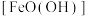 的离子方程式为
的离子方程式为_______ 。
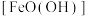 是一种不溶于水的黄色固体,可用作制造黄色颜料,也是制备饮水处理剂一高铁酸钾的原料。一种以工厂废料(含
是一种不溶于水的黄色固体,可用作制造黄色颜料,也是制备饮水处理剂一高铁酸钾的原料。一种以工厂废料(含 、
、 、
、 、CuO)为原料生产铁黄
、CuO)为原料生产铁黄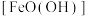 的工艺流程如图所示。
的工艺流程如图所示。
已知:
 为酸性氧化物,不与硫酸等强酸反应;
为酸性氧化物,不与硫酸等强酸反应; 易溶于水,难溶于乙醇。
易溶于水,难溶于乙醇。回答下列问题:
(1)铁黄
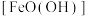 中铁元素化合价为
中铁元素化合价为(2)“酸溶”时
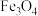 发生反应的离子方程式为
发生反应的离子方程式为(3)“废渣1”的主要成分是
(4)“还原”时会加入过量的试剂X,“试剂X”宜选择的是_______(填标号)。
| A.双氧水 | B.铁粉 | C.氯水 | D.金属铜 |
 所用的试剂为
所用的试剂为(6)“氧化”时,理论上氯气氧化性更强,但通常不用氯气代替空气,除考虑成本因素外,另一原因是
(7)由
 氧化为
氧化为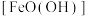 的离子方程式为
的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】某含镍(NiO)废料中有FeO、Al2O3、MgO、SiO2等杂质,用此废料提取NiSO4的工艺流程如图1所示:
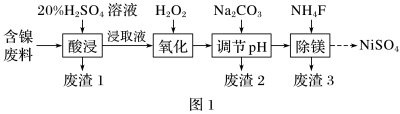
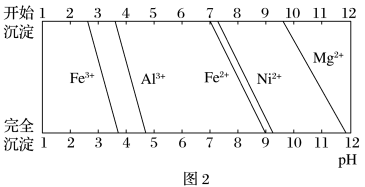
已知:①有关金属离子生成氢氧化物沉淀时溶液的pH如图2所示。
②25 ℃时,NH3·H2O的电离常数Kb=1.8×10-5。HF的电离常数Ka=7.2×10-4,Ksp(MgF2)=7.4×10-11。
(1)加Na2CO3调节溶液的pH至5,得到废渣2的主要成分是_______ (填化学式)。
(2)Mg能与饱和NH4Cl溶液反应产生NH3,请用化学平衡移动原理加以解释:__________________ (用必要的文字和离子方程式回答)。
(3)25 ℃时,1 mol·L-1的NaF溶液中c(OH-)=___________ (列出计算式即可) mol·L-1。NH4F溶液呈____ (填“酸性”“碱性”或“中性”)。
(4)已知沉淀前溶液中c(Mg2+)=1.85×10-3 mol·L-1,当除镁率达到99%时,溶液中c(F-)=____ mol·L-1。

已知:①有关金属离子生成氢氧化物沉淀时溶液的pH如图2所示。

②25 ℃时,NH3·H2O的电离常数Kb=1.8×10-5。HF的电离常数Ka=7.2×10-4,Ksp(MgF2)=7.4×10-11。
(1)加Na2CO3调节溶液的pH至5,得到废渣2的主要成分是
(2)Mg能与饱和NH4Cl溶液反应产生NH3,请用化学平衡移动原理加以解释:
(3)25 ℃时,1 mol·L-1的NaF溶液中c(OH-)=
(4)已知沉淀前溶液中c(Mg2+)=1.85×10-3 mol·L-1,当除镁率达到99%时,溶液中c(F-)=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】某科研人员以废镍催化剂(主要成分为 ,另含
,另含 、
、 、
、 、
、 )为原料回收镍,工艺流程如图:
)为原料回收镍,工艺流程如图:
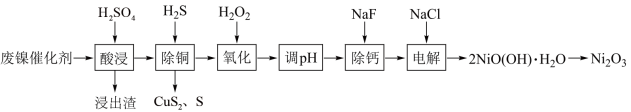
已知:常温下,有关氢氧化物开始沉淀和沉淀完全的 如表:
如表:
回答下列问题:
(1)浸出渣主要成分为___________ (填化学式)。
(2)“氧化”的目的是将溶液中的 氧化为
氧化为 ,温度需控制在
,温度需控制在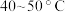 之间,该步骤温度不能太高的原因是
之间,该步骤温度不能太高的原因是___________ 。
(3)“调pH”时,为除去溶液中的铁元素,可向溶液中加入Ni(OH)2试剂来控制pH的范围为___________ 。
(4)“除钙”后,若溶液中 浓度为
浓度为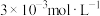 ,则
,则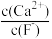 =
=___________ 。[已知常温下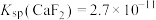 ]
]
(5)高能锂离子电池的总反应为2Li+FeS=Fe+Li2S。用该电池作电源电解含镍酸性废水回收Ni的装置如图(图中X、Y为电极,LiPF6·SO(CH3)2为电解质)。
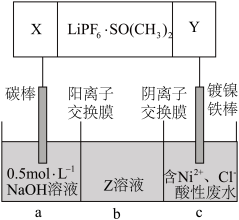
①中间隔室b可以得到的主要物质Z是___________ (填化学式)。
②阳极的电极反应式是___________ 。
 ,另含
,另含 、
、 、
、 、
、 )为原料回收镍,工艺流程如图:
)为原料回收镍,工艺流程如图:
已知:常温下,有关氢氧化物开始沉淀和沉淀完全的
 如表:
如表: |  |  |
| 1.5 | 6.5 | 7.7 |
| 3.7 | 9.7 | 9.2 |
回答下列问题:
(1)浸出渣主要成分为
(2)“氧化”的目的是将溶液中的
 氧化为
氧化为 ,温度需控制在
,温度需控制在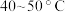 之间,该步骤温度不能太高的原因是
之间,该步骤温度不能太高的原因是(3)“调pH”时,为除去溶液中的铁元素,可向溶液中加入Ni(OH)2试剂来控制pH的范围为
(4)“除钙”后,若溶液中
 浓度为
浓度为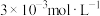 ,则
,则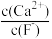 =
=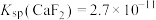 ]
](5)高能锂离子电池的总反应为2Li+FeS=Fe+Li2S。用该电池作电源电解含镍酸性废水回收Ni的装置如图(图中X、Y为电极,LiPF6·SO(CH3)2为电解质)。

①中间隔室b可以得到的主要物质Z是
②阳极的电极反应式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】ZnS常用于制造白色颜料、发光粉和发光油漆等。以火法炼铜的废料(主要成分是ZnO、CuO,含少量PbO、As2O3、SiO2等)为原料制备粗锌和硫化锌的流程如下:
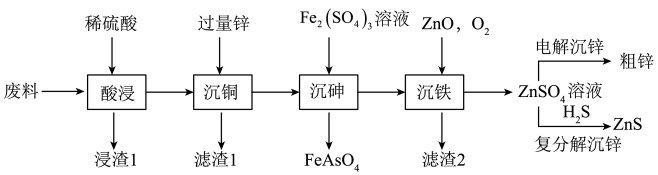
请回答下列问题:
(1)“浸渣1”的主要成分是SiO2和______ (填化学式)。
(2)从“滤渣1”中提取粗铜的操作是将滤渣1______ 过滤、洗涤、干燥,得到粗铜。
(3)“沉铁”中O2的作用是________ (用离子方程式表示)。
(4)“沉铁”过程加入ZnO调节溶液pH,滤液中Fe元素的质量浓度、滤渣2中锌元素质量分数与pH关系如图所示。最适宜的pH为______ 。

(5)以惰性材料为电极,“电解沉锌”的阳极反应式为_________ ,工业上常用电解法精炼锌,阴极材料是______ ,电解质溶液选择________ (填化学式)溶液。
(6)“复分解沉锌”中,Zn2++H2S ZnS↓+2H+的平衡常数K=
ZnS↓+2H+的平衡常数K=______ 。[已知:常温下,Ksp(ZnS)=3.0×10-25,H2S的电离常数Ka1=9.0×10-8,Ka2=1.0×10-12]

请回答下列问题:
(1)“浸渣1”的主要成分是SiO2和
(2)从“滤渣1”中提取粗铜的操作是将滤渣1
(3)“沉铁”中O2的作用是
(4)“沉铁”过程加入ZnO调节溶液pH,滤液中Fe元素的质量浓度、滤渣2中锌元素质量分数与pH关系如图所示。最适宜的pH为

(5)以惰性材料为电极,“电解沉锌”的阳极反应式为
(6)“复分解沉锌”中,Zn2++H2S
 ZnS↓+2H+的平衡常数K=
ZnS↓+2H+的平衡常数K=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】电解法制碱的原料是饱和食盐水,由于粗盐中含有泥沙和Ca2+、Mg2+、Fe3+、SO42-杂质,不符合电解要求,因此必须经过精制。某校实验小组精制粗盐水的实验过程如下:
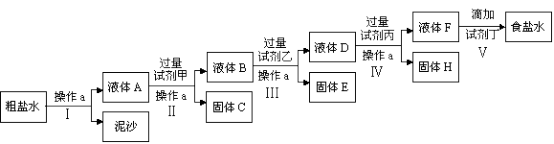
请回答以下问题:
(1)操作a的名称是__________ ,所用玻璃仪器有_____________ ;
(2)在Ⅱ步中,加入过量试剂甲后,生成了两种大量的难溶沉淀,则试剂甲为_________ (填化学式)溶液;
(3)写出固体H所含物质的化学式_____________ ;
(4)在Ⅴ步中,逐滴加入试剂丁直至溶液无明显变化时,写出此过程中发生反应的离子方程式_______________________ ;_______________________ 。

请回答以下问题:
(1)操作a的名称是
(2)在Ⅱ步中,加入过量试剂甲后,生成了两种大量的难溶沉淀,则试剂甲为
(3)写出固体H所含物质的化学式
(4)在Ⅴ步中,逐滴加入试剂丁直至溶液无明显变化时,写出此过程中发生反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】Ti在工业生产和日常生活中有重要用途,以钛铁矿石(FeTiO3,含Fe2O3、Al2O3、SiO2等杂质)为原料制备Ti的流程如下:

已知:
回答下列问题:
(1)碱浸液中含有的金属元素是___________ 。
(2)酸浸时需加热的目的是___________ ,酸浸产生TiO2+的离子方程式为___________ 。
(3)加NaOH溶液调至a=___________ 时,溶液中的杂质离子沉淀完全。
(4)实验时当加入V Lc mol/L H2O2溶液恰好能将酸浸后溶液中的还原性离子全部氧化,则akg钛矿石理论是可制得钛___________ kg(过程中铁、钛无损失),“氧化”中可替代H2O2的物质是___________ 。
(5)制取TiO2·xH2O需加入大量水并加热,其目的是___________ (结合方程式说明)。
(6)为将碱浸液中所含金属化合物转化为金属氧化物,下列试剂必须用到的是___________(按试剂使用先后顺序选填试剂标号)。

已知:
| 金属离子 | Fe3+ | Fe2+ |
| 开始沉淀时(c=0.01 mol·L-1)的pH | 2.2 | 7.5 |
(1)碱浸液中含有的金属元素是
(2)酸浸时需加热的目的是
(3)加NaOH溶液调至a=
(4)实验时当加入V Lc mol/L H2O2溶液恰好能将酸浸后溶液中的还原性离子全部氧化,则akg钛矿石理论是可制得钛
(5)制取TiO2·xH2O需加入大量水并加热,其目的是
(6)为将碱浸液中所含金属化合物转化为金属氧化物,下列试剂必须用到的是___________(按试剂使用先后顺序选填试剂标号)。
| A.氨水 | B.氢氧化钠 | C.硫酸 | D.醋酸 |
您最近一年使用:0次
【推荐3】CoCl2·6H2O是一种饲料营养强化剂。一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2·6H2O的工艺流程如下:

已知:①浸出液含有的阳离子主要有H+、CO2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表(金属离子浓度为0.01 mol/L):
③CoCl2·6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴。
(1)写出浸出过程中Co2O3发生反应的离子方程式:_______________ 。
(2)若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式:_______________ 。
(3)“操作1”中包含3个基本实验操作,它们依次是_____________ 、__________ 和过滤。制得的CoCl2·6H2O在烘干时需减压烘干的原因是_____________ 。
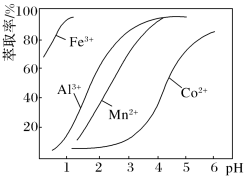
(4)萃取剂对金属离子的萃取率与pH的关系如图向“滤液”中加入萃取剂的目的是____________ ,其使用的最佳pH范围是______ 。
A 2.0~2.5 B 3.0~3.5 C 4.0~4.5 D 5.0~5.5
(注:横坐标依次为1-6;单位:PH)
(5)为测定粗产品中CoCl2·6H2O的含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2·6H2O的质量分数大于100%,其原因可能是__________ 。(答一条即可)

已知:①浸出液含有的阳离子主要有H+、CO2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表(金属离子浓度为0.01 mol/L):
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)写出浸出过程中Co2O3发生反应的离子方程式:
(2)若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式:
(3)“操作1”中包含3个基本实验操作,它们依次是
(4)萃取剂对金属离子的萃取率与pH的关系如图向“滤液”中加入萃取剂的目的是
A 2.0~2.5 B 3.0~3.5 C 4.0~4.5 D 5.0~5.5
(注:横坐标依次为1-6;单位:PH)

(5)为测定粗产品中CoCl2·6H2O的含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2·6H2O的质量分数大于100%,其原因可能是
您最近一年使用:0次




