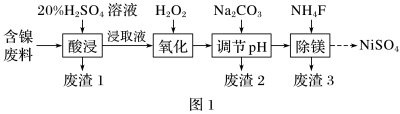
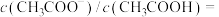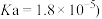某含镍(NiO)废料中有FeO、Al2O3、MgO、SiO2等杂质,用此废料提取NiSO4的工艺流程如图1所示:
已知:①有关金属离子生成氢氧化物沉淀时溶液的pH如图2所示。
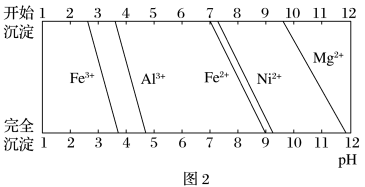
②25 ℃时,NH3·H2O的电离常数Kb=1.8×10-5。HF的电离常数Ka=7.2×10-4,Ksp(MgF2)=7.4×10-11。
(1)加Na2CO3调节溶液的pH至5,得到废渣2的主要成分是_______ (填化学式)。
(2)Mg能与饱和NH4Cl溶液反应产生NH3,请用化学平衡移动原理加以解释:__________________ (用必要的文字和离子方程式回答)。
(3)25 ℃时,1 mol·L-1的NaF溶液中c(OH-)=___________ (列出计算式即可) mol·L-1。NH4F溶液呈____ (填“酸性”“碱性”或“中性”)。
(4)已知沉淀前溶液中c(Mg2+)=1.85×10-3 mol·L-1,当除镁率达到99%时,溶液中c(F-)=____ mol·L-1。

已知:①有关金属离子生成氢氧化物沉淀时溶液的pH如图2所示。

②25 ℃时,NH3·H2O的电离常数Kb=1.8×10-5。HF的电离常数Ka=7.2×10-4,Ksp(MgF2)=7.4×10-11。
(1)加Na2CO3调节溶液的pH至5,得到废渣2的主要成分是
(2)Mg能与饱和NH4Cl溶液反应产生NH3,请用化学平衡移动原理加以解释:
(3)25 ℃时,1 mol·L-1的NaF溶液中c(OH-)=
(4)已知沉淀前溶液中c(Mg2+)=1.85×10-3 mol·L-1,当除镁率达到99%时,溶液中c(F-)=
2020高三·全国·专题练习 查看更多[2]
更新时间:2020-11-22 15:26:58
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】I.已知25℃时,醋酸、碳酸、氢氰酸的电离平衡常数如表:(单位省略)
(1)写出碳酸的第一步电离方程式_________ 。
(2)25℃时,等浓度的三种溶液①NaCN溶液、②Na2CO3溶液、③CH3COONa溶液,pH由大到小的顺序为(填序号)__________ 。
(3)25℃时,向NaCN溶液中通入少量CO2,反应的离子方程式为__________ 。
(4)将浓度为0.02 mol/L的HCN与0.01 mol/LINaOH溶液等体积混合,测得混合溶液中c(Na+)>c(CN-),下列关系正确的是________ 。
a.c(H+)<c(OH-) b.c(H+)+c(HCN)=c(OH-)
c.c(HCN)+c(CN-)=0.01 mol/L
(5)25℃时,浓度均为0.01 mol/L的①NaCN、②CH3COONa、③NaCl溶液中,阴离子总浓度由大到小的顺序为________ (填序号)。
II.酸性高锰酸钾标准溶液是实验室常用的氧化还原滴定标准试剂。
(6)某同学0.1000 mol/L-1的酸性高锰酸钾标准溶液滴定某试样中过氧化氢的含量,反应原理为2 +5H2O2+6H+=2Mn2++8H2O+5O2↑。
+5H2O2+6H+=2Mn2++8H2O+5O2↑。
①滴定时,用________ 装KMnO4溶液
②滴定到达终点的现象是___________ 。
③用移液管吸取25.00 mL试样置于锥形瓶中,重复滴定四次,每次消耗的酸性KMnO4标准溶液体积如下表所示:
则试样中过氧化氢的浓度为________ mol/L-1。
| 醋酸 | 碳酸 | 氢氰酸 |
| Ka=1.7×10-5 | Ka1=4.2×10-7 Ka2=5.6×10-11 | Ka=6.2×10-10 |
(1)写出碳酸的第一步电离方程式
(2)25℃时,等浓度的三种溶液①NaCN溶液、②Na2CO3溶液、③CH3COONa溶液,pH由大到小的顺序为(填序号)
(3)25℃时,向NaCN溶液中通入少量CO2,反应的离子方程式为
(4)将浓度为0.02 mol/L的HCN与0.01 mol/LINaOH溶液等体积混合,测得混合溶液中c(Na+)>c(CN-),下列关系正确的是
a.c(H+)<c(OH-) b.c(H+)+c(HCN)=c(OH-)
c.c(HCN)+c(CN-)=0.01 mol/L
(5)25℃时,浓度均为0.01 mol/L的①NaCN、②CH3COONa、③NaCl溶液中,阴离子总浓度由大到小的顺序为
II.酸性高锰酸钾标准溶液是实验室常用的氧化还原滴定标准试剂。
(6)某同学0.1000 mol/L-1的酸性高锰酸钾标准溶液滴定某试样中过氧化氢的含量,反应原理为2
 +5H2O2+6H+=2Mn2++8H2O+5O2↑。
+5H2O2+6H+=2Mn2++8H2O+5O2↑。①滴定时,用
②滴定到达终点的现象是
③用移液管吸取25.00 mL试样置于锥形瓶中,重复滴定四次,每次消耗的酸性KMnO4标准溶液体积如下表所示:
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 体积(mL) | 17.10 | 18.10 | 17.00 | 16.90 |
则试样中过氧化氢的浓度为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】25℃时,在CH3COOH和CH3COONa的混合溶液中,CH3COOH和CH3COO-二者各自所占的物质的量分数(a)随溶液pH变化的关系如图所示。
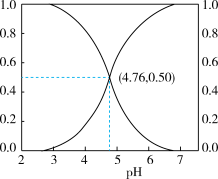
(1)25℃时,CH3COOH的电离平衡常数Ka=________ 。
(2)在pH<4.76的溶液中c(CH3COOH)_______________ c(CH3COO-)(选填“>”、“<”或“=”)。
(3)pH=4.76时,溶液中所有微粒(不考虑H2O)浓度由大到小的顺序为______________ 。
(4)将醋酸和醋酸钠等浓度等体积混合后的溶液中,pH__________ 4.76(选填“>”、“<”或“=”)
(5)四室电渗析法制醋酸的工作原理如下图所示,则阳极电极反应式为____________ ;c膜为__________ 离子交换膜(选填“阳”或“阴”),分析产品室得到醋酸的原因________ 。


(1)25℃时,CH3COOH的电离平衡常数Ka=
(2)在pH<4.76的溶液中c(CH3COOH)
(3)pH=4.76时,溶液中所有微粒(不考虑H2O)浓度由大到小的顺序为
(4)将醋酸和醋酸钠等浓度等体积混合后的溶液中,pH
(5)四室电渗析法制醋酸的工作原理如下图所示,则阳极电极反应式为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】常见元素A、B、M组成的四种物质发生反应:甲+乙=丙+丁,其中甲由A和M组成,乙由B和M组成,丙中只含有M。
(1)若甲为淡黄色固体,乙和丙均为常温下的无色无味气体。则甲的电子式为__ ;常温下丁溶液pH___ 7(填“>”“<”或“=”),用离子方程式解释原因____________ ;
(2)若丁为能使品红褪色的无色气体,丁与水反应生成戊,丙为常见红色金属,化合物甲、乙中原子个数比均为1:2(M均显+1价),原子序数B大于A。回答下列问题:
①A在周期表中位置为___________ ;
②向丁的水溶液中滴入紫色石蕊试液,现象为_____________________ ;
③写出加热条件下上述生成丙的化学方程式__________________ ;
④向MCl2的溶液中通入丁,生成白色MCl沉淀,写出该反应的离子方程式__________ ;
⑤已知常温下弱电解质的电离平衡常数如下:一水合氨Kb=1.8×10-5,戊:Ka1=1.3×10-2, Ka2 = 6.3×10 -8。若一水合氨与丁恰好完全反应生成正盐,则浓度为0.1 mol/L的该正盐溶液呈____ 性(填“酸”或“碱”或“中”);调整二者反应的比值可使溶液呈中性,此时溶液中
____ 2(填“>”“<”或“=”)。
(1)若甲为淡黄色固体,乙和丙均为常温下的无色无味气体。则甲的电子式为
(2)若丁为能使品红褪色的无色气体,丁与水反应生成戊,丙为常见红色金属,化合物甲、乙中原子个数比均为1:2(M均显+1价),原子序数B大于A。回答下列问题:
①A在周期表中位置为
②向丁的水溶液中滴入紫色石蕊试液,现象为
③写出加热条件下上述生成丙的化学方程式
④向MCl2的溶液中通入丁,生成白色MCl沉淀,写出该反应的离子方程式
⑤已知常温下弱电解质的电离平衡常数如下:一水合氨Kb=1.8×10-5,戊:Ka1=1.3×10-2, Ka2 = 6.3×10 -8。若一水合氨与丁恰好完全反应生成正盐,则浓度为0.1 mol/L的该正盐溶液呈

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】亚铁氰化钾钛是一种性能优良的无机离子交换剂,常用溶胶-凝胶法合成球形亚铁氰化钾钛。实验装置如图所示(夹持以及加热装置已省略):
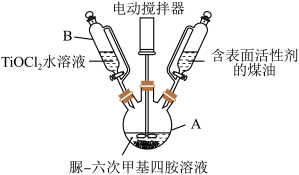
简要步骤如下:
I.取一定量 加到
加到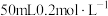 盐酸中,再加水配制成
盐酸中,再加水配制成 溶液。
溶液。
II.在低于10℃下,将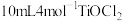 水溶液加到
水溶液加到 脲-六次甲基四胺溶液中。
脲-六次甲基四胺溶液中。
III.边搅拌边将20mL含表面活性剂的煤油慢慢滴加到此混合液中,并加热到70℃,恒温5min后停止搅拌,冷却至室温,分离上层煤油,可得到白色球形的水合二氧化钛凝胶颗粒,再用10%的氨水陈化12h,用水洗涤,待用。
IV.将水合二氧化钛凝胶颗粒在常温下用50mL亚铁氰化钾和HCl的混合溶液浸泡48h后,经一系列操作,可得深褐色亚铁氰化钾钛球形颗粒。
已知:脲-六次甲基四胺溶液不稳定,受热易分解产生氨气。
回答下列问题:
(1)仪器B的名称为___________ ,该仪器的优点是___________ 。
(2)步骤I中配制 溶液时发生反应的化学方程式为
溶液时发生反应的化学方程式为___________ 。
(3)步骤II中在低于10℃下进行的原因是___________ 。
(4)步骤III中恒温5min时,采用___________ 加热。
(5)步骤IV中“一系列操作”包括三个步骤:过滤、___________ 、___________ 。
(6)亚铁氰化钾钛晶体的化学式为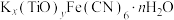 ,实验测得某亚铁氰化钾钛晶体中
,实验测得某亚铁氰化钾钛晶体中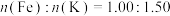 ,则该晶体中
,则该晶体中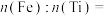
___________ 。

简要步骤如下:
I.取一定量
 加到
加到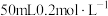 盐酸中,再加水配制成
盐酸中,再加水配制成 溶液。
溶液。II.在低于10℃下,将
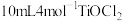 水溶液加到
水溶液加到 脲-六次甲基四胺溶液中。
脲-六次甲基四胺溶液中。III.边搅拌边将20mL含表面活性剂的煤油慢慢滴加到此混合液中,并加热到70℃,恒温5min后停止搅拌,冷却至室温,分离上层煤油,可得到白色球形的水合二氧化钛凝胶颗粒,再用10%的氨水陈化12h,用水洗涤,待用。
IV.将水合二氧化钛凝胶颗粒在常温下用50mL亚铁氰化钾和HCl的混合溶液浸泡48h后,经一系列操作,可得深褐色亚铁氰化钾钛球形颗粒。
已知:脲-六次甲基四胺溶液不稳定,受热易分解产生氨气。
回答下列问题:
(1)仪器B的名称为
(2)步骤I中配制
 溶液时发生反应的化学方程式为
溶液时发生反应的化学方程式为(3)步骤II中在低于10℃下进行的原因是
(4)步骤III中恒温5min时,采用
(5)步骤IV中“一系列操作”包括三个步骤:过滤、
(6)亚铁氰化钾钛晶体的化学式为
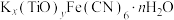 ,实验测得某亚铁氰化钾钛晶体中
,实验测得某亚铁氰化钾钛晶体中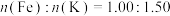 ,则该晶体中
,则该晶体中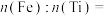
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】合理利用废旧铅蓄电池可缓解铅资源短缺,同时减少污染。一种从废旧铅蓄电池的铅膏中回收铅的生产流程如图所示(部分产物已略去):

已知:①25℃时:Ksp (PbSO4)=1.6×10-8,Ksp(PbCO3)=7.4×10-14,Kal(H2CO3)=4.5×10-7,Ka2(H2CO3)=4.7×10-11;
②PbSiF6和H2SiF6均为能溶于水的强电解质。
(1)过程i中,物质a可以为_______ 和 H2SO4的混合溶液(填标号)。
A.Na2SO3 B.Na2CO3 C.Na2SO4
(2)25℃时,若过程ii发生反应后的母液中c( )=1.6 mol·L-1,c(
)=1.6 mol·L-1,c( )=4.7×10-5mol·L-1,试通过计算判断“PbCO3”中
)=4.7×10-5mol·L-1,试通过计算判断“PbCO3”中_______ (填“有”或“无”)PbSO4固体,此溶液的pH约为_______ 。
(3)过程iii发生反应的离子方程式为_______ 。
(4)过程iv阴极的电极反应式为_______ 。

已知:①25℃时:Ksp (PbSO4)=1.6×10-8,Ksp(PbCO3)=7.4×10-14,Kal(H2CO3)=4.5×10-7,Ka2(H2CO3)=4.7×10-11;
②PbSiF6和H2SiF6均为能溶于水的强电解质。
(1)过程i中,物质a可以为
A.Na2SO3 B.Na2CO3 C.Na2SO4
(2)25℃时,若过程ii发生反应后的母液中c(
 )=1.6 mol·L-1,c(
)=1.6 mol·L-1,c( )=4.7×10-5mol·L-1,试通过计算判断“PbCO3”中
)=4.7×10-5mol·L-1,试通过计算判断“PbCO3”中(3)过程iii发生反应的离子方程式为
(4)过程iv阴极的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
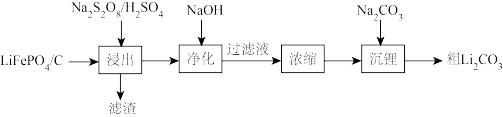
【推荐2】回收磷酸铁锂电池的正极材料,工艺流程如下:
已知:该温度时Co(OH)2、Mn(OH)2的Ksp分别为2.0 ×10-15、1.9×10-13。
回答下列问题:
(1)磷酸铁锂电池在剥离前要充分放电,通过Li+移动把FePO4转化为LiFePO4该电极反应式为_______ 。
(2)磷酸铁锂电池的正极材料“浸出”前需要粉碎,目的是_______ 。
(3)“滤渣”中含有FePO4和C,为了得到纯净的FePO4,简单除碳方法为_______ 。
(4)“净化”时为除尽微量的Mn2+、Co2+,确保浓度控制为等于或小于1 ×10-5mol·L-1,加入NaOH溶液调pH至_______ (填“酸性”或“碱性”)较好。
(5)粗Li2CO3固体表面上黏有Na2CO3溶液和_______ 溶液,工业上用热水而不用冷水清洗固体,原因有_______ 、_______ 、后期易干燥且Li2CO3产率高。
(6)“浸出”过程中发生的化学方程式为_______ 。

已知:该温度时Co(OH)2、Mn(OH)2的Ksp分别为2.0 ×10-15、1.9×10-13。
回答下列问题:
(1)磷酸铁锂电池在剥离前要充分放电,通过Li+移动把FePO4转化为LiFePO4该电极反应式为
(2)磷酸铁锂电池的正极材料“浸出”前需要粉碎,目的是
(3)“滤渣”中含有FePO4和C,为了得到纯净的FePO4,简单除碳方法为
(4)“净化”时为除尽微量的Mn2+、Co2+,确保浓度控制为等于或小于1 ×10-5mol·L-1,加入NaOH溶液调pH至
(5)粗Li2CO3固体表面上黏有Na2CO3溶液和
(6)“浸出”过程中发生的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】碳酸锰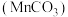 是制造电信器材软磁铁氧体的重要原料。工业上用硫锰矿(主要成分为
是制造电信器材软磁铁氧体的重要原料。工业上用硫锰矿(主要成分为 ,还含少量
,还含少量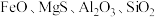 等)制备高纯
等)制备高纯 的流程如下:
的流程如下: 如下表:
如下表:
②室温下, 。回答下列问题:
。回答下列问题:
(1)为了提高硫锰矿在空气中“煅烧”的反应速率,可采取的措施是___________ (任写一种),“尾气”中含有由“煅烧”生成的有害气体的化学式为___________ 。
(2)加入 主要是氧化酸性溶液中的
主要是氧化酸性溶液中的 ,发生反应的离子方程式为
,发生反应的离子方程式为___________ 。
(3)加入氨水调节溶液 为5.0,则溶液中
为5.0,则溶液中
___________ (填“>”“<”或“=”)c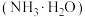 ;溶液中能够完全沉淀的金属离子为
;溶液中能够完全沉淀的金属离子为___________ (填离子符号,金属离子浓度 时,视为沉淀完全)。
时,视为沉淀完全)。
(4)室温下“沉镁”时,离子反应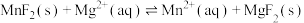 的化学平衡常数
的化学平衡常数
___________ 。
(5)加入 “沉锰”时发生反应的离子方程式为
“沉锰”时发生反应的离子方程式为___________ 。
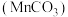 是制造电信器材软磁铁氧体的重要原料。工业上用硫锰矿(主要成分为
是制造电信器材软磁铁氧体的重要原料。工业上用硫锰矿(主要成分为 ,还含少量
,还含少量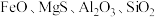 等)制备高纯
等)制备高纯 的流程如下:
的流程如下:
 如下表:
如下表:| 物质 |  |  |  |  |  |
 | 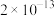 | 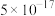 | 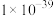 | 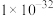 | 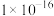 |
 。回答下列问题:
。回答下列问题:(1)为了提高硫锰矿在空气中“煅烧”的反应速率,可采取的措施是
(2)加入
 主要是氧化酸性溶液中的
主要是氧化酸性溶液中的 ,发生反应的离子方程式为
,发生反应的离子方程式为(3)加入氨水调节溶液
 为5.0,则溶液中
为5.0,则溶液中
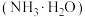 ;溶液中能够完全沉淀的金属离子为
;溶液中能够完全沉淀的金属离子为 时,视为沉淀完全)。
时,视为沉淀完全)。(4)室温下“沉镁”时,离子反应
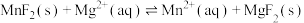 的化学平衡常数
的化学平衡常数
(5)加入
 “沉锰”时发生反应的离子方程式为
“沉锰”时发生反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】钛白粉(TiO2)是重要的白色颜料,LiFePO4是锂离子电池的正极材料。一种利用钛铁矿(主要成分为 FeTiO3和少量 Fe2O3、CaO、SiO2)进行钛白粉和 LiFePO4的联合生产工艺如图所示:

回答下列问题:
(1)LiFePO4中铁的化合价是___________ 。
(2)“酸浸”中主要反应的化学方程式为___________ ,“滤渣 1”的主要成分有___________ 。
(3)操作 I 加入过量 A 的目的是___________ ;硫酸亚铁晶体的溶解度如表所示,其中绿矾(FeSO4 •7H2O)容易被氧化,则“操作 II”包括真空加热浓缩、___________ 、___________ 、洗涤、干燥。
(4)“转化”利用的是 TiO2+的水解过程,则其在 90℃水解的离子方程式为___________ ,“转化后的滤液”可返回到___________ 工序循环利用。
(5)由“沉铁”到制备 LiFePO4的过程中,所需 17% H2O2溶液与草酸(H2C2O4)的质量比是___________ 。

回答下列问题:
(1)LiFePO4中铁的化合价是
(2)“酸浸”中主要反应的化学方程式为
(3)操作 I 加入过量 A 的目的是
| 温度/℃ | 0 | 10 | 30 | 50 | 56.7 | 60 | 64 | 70 | 80 | 90 |
| 溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.2 | 35.3 | 35.6 | 33.0 | 30.5 | 27 |
| 析出晶体 | FeSO4·7H2O | FeSO4·4H2O | FeSO4·H2O | |||||||
(4)“转化”利用的是 TiO2+的水解过程,则其在 90℃水解的离子方程式为
(5)由“沉铁”到制备 LiFePO4的过程中,所需 17% H2O2溶液与草酸(H2C2O4)的质量比是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
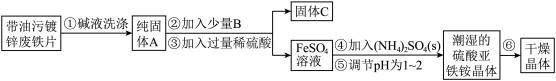
【推荐2】某学习小组以电路板刻蚀液(含有大量Cu2+、Fe2+、Fe3+)为原料制备纳米Cu2O,制备流程如下:
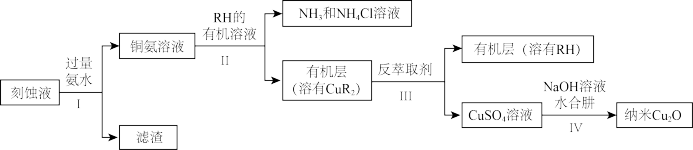
已知:①Cu2O在潮湿的空气中会慢慢氧化生成CuO,也易被还原为Cu;Cu2O不溶于水,极易溶于碱性溶液;Cu2O+2H+ =Cu2++Cu+H2O。
②生成Cu2O的反应:4Cu(OH)2+N2H4∙H2O=2Cu2O+N2↑+7H2O
请回答:
(1)步骤II,写出生成CuR2反应的离子方程式:___________
(2)步骤II,需对水层多次萃取并合并萃取液的目的是__________
(3)步骤III,反萃取剂为________
(4)步骤IV,①制备纳米Cu2O时,控制溶液的pH为5的原因是________
A. B.
B. C.
C. 
②从溶液中分离出纳米Cu2O采用离心法,下列方法也可分离Cu2O的是_________
(5)为测定产品中Cu2O的含量,称取3.960g产品于锥形瓶中,加入30mL硫酸酸化的Fe2(SO4)3溶液(足量),充分反应后用0.2000 mol·L-1标准KMnO4溶液滴定,重复2~3次,平均消耗KMnO4溶液50.00mL。
①产品中Cu2O的质量分数为_____
②若无操作误差,测定结果总是偏高的原因是_____

已知:①Cu2O在潮湿的空气中会慢慢氧化生成CuO,也易被还原为Cu;Cu2O不溶于水,极易溶于碱性溶液;Cu2O+2H+ =Cu2++Cu+H2O。
②生成Cu2O的反应:4Cu(OH)2+N2H4∙H2O=2Cu2O+N2↑+7H2O
请回答:
(1)步骤II,写出生成CuR2反应的离子方程式:
(2)步骤II,需对水层多次萃取并合并萃取液的目的是
(3)步骤III,反萃取剂为
(4)步骤IV,①制备纳米Cu2O时,控制溶液的pH为5的原因是
A.
 B.
B. C.
C. 
②从溶液中分离出纳米Cu2O采用离心法,下列方法也可分离Cu2O的是
(5)为测定产品中Cu2O的含量,称取3.960g产品于锥形瓶中,加入30mL硫酸酸化的Fe2(SO4)3溶液(足量),充分反应后用0.2000 mol·L-1标准KMnO4溶液滴定,重复2~3次,平均消耗KMnO4溶液50.00mL。
①产品中Cu2O的质量分数为
②若无操作误差,测定结果总是偏高的原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】一种利用钢铁厂烟灰 含Fe、Mn、
含Fe、Mn、 ,少量的
,少量的 、CaO及
、CaO及 制备
制备 的工艺流程如下:
的工艺流程如下:
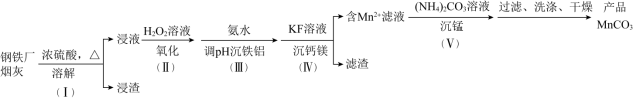
已知 时,下列难溶物的溶度积常数:
时,下列难溶物的溶度积常数:
回答下列问题:
 步骤
步骤 Ⅰ
Ⅰ 浸渣的主要成分是
浸渣的主要成分是________  填化学式
填化学式 。
。
 步骤
步骤 Ⅱ
Ⅱ 加
加 溶液时反应的离子方程式为
溶液时反应的离子方程式为________ ;加氨水调节pH沉铁铝时,步骤 Ⅲ
Ⅲ 应调节的pH适宜范围为
应调节的pH适宜范围为________ 。 部分金属离子开始沉淀与沉淀完全的pH范围如下
部分金属离子开始沉淀与沉淀完全的pH范围如下
 步骤
步骤 Ⅳ
Ⅳ 用KF溶液沉钙镁时,要使
用KF溶液沉钙镁时,要使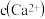 、
、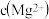 均小于
均小于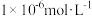 ,则应控制反应液中
,则应控制反应液中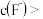
________  ;反应
;反应 的平衡常数
的平衡常数
________ 。
 步骤Ⅴ沉锰时,在
步骤Ⅴ沉锰时,在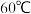 按投料比
按投料比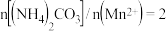 ,溶液的pH对
,溶液的pH对 产率的影响如图
产率的影响如图 所示;
所示; ,按投料比
,按投料比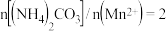 ,反应温度对
,反应温度对 产率的影响如图
产率的影响如图 所示。
所示。
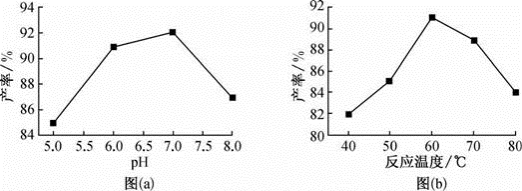
 图
图 中,在
中,在 时,pH越小产率
时,pH越小产率________  填“越高”或“越低”
填“越高”或“越低” ;在
;在 时,pH越大产率越低且纯度也降低,其原因是
时,pH越大产率越低且纯度也降低,其原因是________ 。
 图
图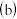 中,温度高于
中,温度高于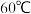 时,温度越高产率越低且纯度也越低,主要原因是
时,温度越高产率越低且纯度也越低,主要原因是________ 。
 含Fe、Mn、
含Fe、Mn、 ,少量的
,少量的 、CaO及
、CaO及 制备
制备 的工艺流程如下:
的工艺流程如下:
已知
 时,下列难溶物的溶度积常数:
时,下列难溶物的溶度积常数:| 难溶物 | 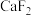 | 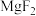 |  |  |
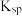 | 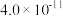 |  | 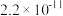 | 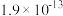 |
回答下列问题:
 步骤
步骤 Ⅰ
Ⅰ 浸渣的主要成分是
浸渣的主要成分是 填化学式
填化学式 。
。 步骤
步骤 Ⅱ
Ⅱ 加
加 溶液时反应的离子方程式为
溶液时反应的离子方程式为 Ⅲ
Ⅲ 应调节的pH适宜范围为
应调节的pH适宜范围为 部分金属离子开始沉淀与沉淀完全的pH范围如下
部分金属离子开始沉淀与沉淀完全的pH范围如下
| 金属离子 |  |  | 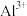 | 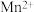 | 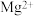 |
| 沉淀pH范围 |  |  | 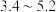 |  |  |
 步骤
步骤 Ⅳ
Ⅳ 用KF溶液沉钙镁时,要使
用KF溶液沉钙镁时,要使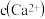 、
、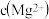 均小于
均小于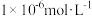 ,则应控制反应液中
,则应控制反应液中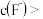
 ;反应
;反应 的平衡常数
的平衡常数
 步骤Ⅴ沉锰时,在
步骤Ⅴ沉锰时,在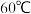 按投料比
按投料比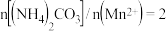 ,溶液的pH对
,溶液的pH对 产率的影响如图
产率的影响如图 所示;
所示; ,按投料比
,按投料比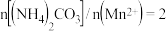 ,反应温度对
,反应温度对 产率的影响如图
产率的影响如图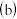 所示。
所示。
 图
图 中,在
中,在 时,pH越小产率
时,pH越小产率 填“越高”或“越低”
填“越高”或“越低” ;在
;在 时,pH越大产率越低且纯度也降低,其原因是
时,pH越大产率越低且纯度也降低,其原因是 图
图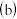 中,温度高于
中,温度高于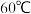 时,温度越高产率越低且纯度也越低,主要原因是
时,温度越高产率越低且纯度也越低,主要原因是
您最近一年使用:0次

 的
的 溶液加水稀释过程中,下列表达式的数据变大的是
溶液加水稀释过程中,下列表达式的数据变大的是 填序号
填序号 。
。

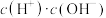
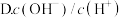
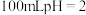 的
的
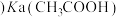 。
。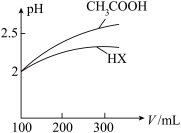
 的混合溶液中,若测得
的混合溶液中,若测得 ,则溶液中离子浓度大小关系是
,则溶液中离子浓度大小关系是