| 系列 实验I | 装置 | 滴管中的试剂 | 试管中的试剂 | 操作 | 现象 |
| i |
|  水 水 | 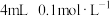  溶液 溶液 | 振荡 | 溶液颜色略微变浅 |
| ii | 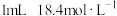 浓硫酸 浓硫酸 | 振荡 | 溶液橙色明显变深 | ||
| iii |  溶液 溶液 | 振荡 | ___________ | ||
| iv | 3滴浓 溶液 溶液 | iii中溶液 | 振荡 | 无明显现象 | |
| v | 过量稀硫酸 | iv中溶液 | 边滴边振荡 | 溶液颜色由黄色逐渐变橙色,最后呈绿色 |
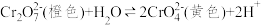
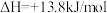 ;
;资料2:+6价铬盐在一定条件下可被还原为
 ,
, 在水溶液中为绿色。
在水溶液中为绿色。(1)iii和i对比,推测iii的现象是
(2)ii和i对比,ii中溶液橙色加深。甲认为温度也会影响平衡的移动,橙色加深不一定是
 增大影响的结果;乙认为橙色加深一定是
增大影响的结果;乙认为橙色加深一定是 增大对平衡的影响。你认为是否需要再设计实验证明?
增大对平衡的影响。你认为是否需要再设计实验证明?(3)对比实验iv与v,可知:在
 被还原为
被还原为(4)为进一步确定铬(VI)盐溶液的氧化性与酸碱性的关系,某同学进行实验如下:
I.进行实验a和b:
| 序号 | 操作 | 现象 |
| a | 向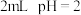 的 的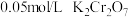 的橙色溶液中滴加饱和 的橙色溶液中滴加饱和 溶液( 溶液( 约为9)3滴 约为9)3滴 | 溶液变绿色 |
| b | 向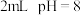 的 的 的 的 黄色溶液中滴加饱和 黄色溶液中滴加饱和 溶液3滴 溶液3滴 | 溶液没有明显变化 |
II.继续进行实验c:
| 序号 | 操作 | 现象 |
| c | 向 饱和 饱和 溶液中滴加 溶液中滴加 的 的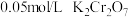 的橙色溶液3滴 的橙色溶液3滴 | 溶液变黄色 |
 蒸馏水中滴加
蒸馏水中滴加 的
的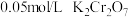 橙色溶液3滴,溶液变成浅橙色。
橙色溶液3滴,溶液变成浅橙色。①补充实验d的目的是
②用化学平衡移动原理解释c中现象:
③根据实验a~c,可推测:
 溶液和铬(VI)盐溶液的反应与溶液酸碱性有关。
溶液和铬(VI)盐溶液的反应与溶液酸碱性有关。a.碱性条件下,
 溶液和铬(VI)盐溶液不发生氧化还原反应;
溶液和铬(VI)盐溶液不发生氧化还原反应;b.
④向实验c所得黄色溶液中继续滴加硫酸,产生的现象证实了上述推测。该现象是
相似题推荐
 )用于制作FTO导电玻璃,FTO玻璃广泛用于液晶显示屏、光催化、薄膜太阳能电池基底等;军事上四氯化锡蒸气与
)用于制作FTO导电玻璃,FTO玻璃广泛用于液晶显示屏、光催化、薄膜太阳能电池基底等;军事上四氯化锡蒸气与 及水汽混合呈浓烟状,可制作烟幕弹。实验室可用熔融的金属锡与干燥氯气利用图装置制备四氯化锡。有关信息如下表:
及水汽混合呈浓烟状,可制作烟幕弹。实验室可用熔融的金属锡与干燥氯气利用图装置制备四氯化锡。有关信息如下表: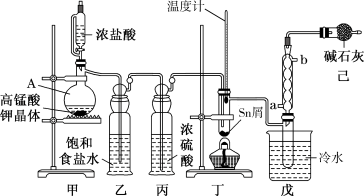
化学式 | Sn |
|
|
熔点/℃ | 232 | 246 | -33 |
沸点/℃ | 2260 | 652 | 114 |
其他性质 | 银白色固体金属 | 无色晶体,Sn(Ⅱ)易被氧化 | 无色液体,遇水反应 |
(2)装置己的作用有
(3)
 和Sn的反应产物可能会有
和Sn的反应产物可能会有 和
和 为防止产品中带入
为防止产品中带入 ,除了通入过量氯气外,应控制温度在
,除了通入过量氯气外,应控制温度在a.114~232℃ b.232~652℃ c.652~2260℃
(4)为了确认丁中
 的生成,可选用以下
的生成,可选用以下a.稀盐酸
b.滴有KSCN(KSCN遇
 变红)溶液的
变红)溶液的 溶液
溶液c.酸性高锰酸钾溶液
(5)氯气在实际生活中的用途很多,可用于饮用水消毒。但对饮用水消毒副作用够,产生影响人体健康的有机氯衍生物。可用氯气制取高铁酸钠净水,补全缺项,并配平离子方程式
______
 ______(______)+______
______(______)+______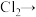 ______
______ ______(______)+
______(______)+
(6)工业上常将氯气转化为漂白粉,工业上利用氯气和石灰乳生产漂白粉的主要化学方程式是
 (主要指NO和
(主要指NO和 )是大气主要污染物之一,有效去除大气中的
)是大气主要污染物之一,有效去除大气中的 是环境保护的重要课题。
是环境保护的重要课题。(1)可以利用
 与
与 反应消除
反应消除 。新型催化剂M能催化
。新型催化剂M能催化 与
与 反应生成
反应生成 。写出该反应的化学方程式
。写出该反应的化学方程式(2)某兴趣小组拟用甲烷与NO的反应设计成原电池对NO进行无污染处理,装置如图所示,
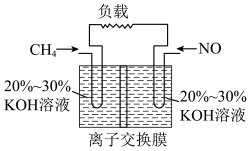
①甲烷的空间结构为
②该装置的能量转化为
③补齐负极的反应式:
 :
:(3)一种新型催化剂能使NO和CO发生反应:
 。在密闭容器中发生该反应时,
。在密闭容器中发生该反应时, 随温度(T)和时间(t)的变化曲线如图所示。
随温度(T)和时间(t)的变化曲线如图所示。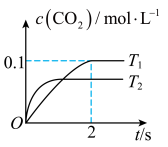
①温度

 (填“大于、小于、等于”)
(填“大于、小于、等于”)②在
 温度下,0~2s内的平均反应速率
温度下,0~2s内的平均反应速率
③在容积固定的恒温容器中,不能说明该反应已达到平衡状态的是
A.混合气体的平均摩尔质量不再变化 B.容器内的气体压强保持不变
C.
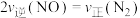 D.容器内混合气体的密度保持不变
D.容器内混合气体的密度保持不变
 气体,设计了如图实验。
气体,设计了如图实验。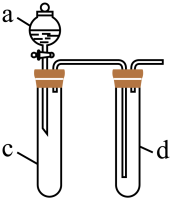
(1)仪器a的名称为
(2)在d中加适量
 溶液,c中放一小块铜片,由a向c中加入
溶液,c中放一小块铜片,由a向c中加入 稀硝酸,c中发生反应的化学方程式是
稀硝酸,c中发生反应的化学方程式是(3)制取硝酸铜的三种方案如表,最佳方案是方案
方案 | 反应物 |
甲 |
|
乙 |
|
丙 |
|
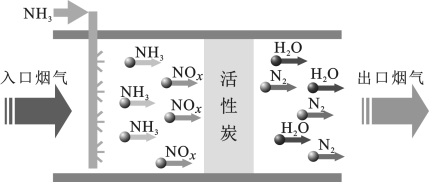
①该流程中活性炭的作用是
 以
以 的形式参加反应,则相应的化学方程式为
的形式参加反应,则相应的化学方程式为②某同学选择如图装置(省略夹持仪器)对该方法进行模拟实验:
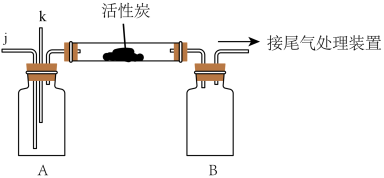
 和
和 从j和k通入A中。其中j通入的气体为
从j和k通入A中。其中j通入的气体为 ,含少量
,含少量 、
、 、
、 等杂质)为原料模拟工业制法的流程如下:
等杂质)为原料模拟工业制法的流程如下:
已知:实验装置见图1,“浸锰”步骤中实验温度对反应影响的变化关系如图2。

请回答:
(1)仪器A名称为
(2)制备流程中,需要向滤液1中加入适量的H2O2溶液,其主要目的是
(3)下列有关表述或操作中,正确的是_______。
| A.滤液1的pH调节可选用KOH、氨水等碱溶液 |
B.“浸锰”过程中,通过增加SO2的通入量、控制通气速度可提升 的浸出率 的浸出率 |
C.为减少“浸锰”反应中生成副产物 ,恒温电磁炉最适宜的控制温度是90℃ ,恒温电磁炉最适宜的控制温度是90℃ |
D.用相应滤液作洗涤剂充分洗涤滤渣1和滤渣2,有助于提高 的产率与纯度 的产率与纯度 |
 的溶解度随温度的变化曲线。流程中对滤液2的“精致结晶”涉及到部分以下步骤:
的溶解度随温度的变化曲线。流程中对滤液2的“精致结晶”涉及到部分以下步骤:
a.在20℃蒸发溶剂;b.在90℃蒸发溶剂;
c.冷却至室温;d.真空干燥;
e.将滤液2转移至蒸发皿中;f.趁热过滤;
g.蒸发至溶液出现晶膜;h.蒸发至大量晶体产生;
i.用冷水洗涤晶体;k.用90℃热水洗涤晶体。
则正确的操作顺序为e→()→()→()→()→d。
(5)某同学采用沉淀
 的方法来分析
的方法来分析 晶体,测定表明产品纯度为103%,导致该误差的可能原因是
晶体,测定表明产品纯度为103%,导致该误差的可能原因是Ⅰ.COS(g)+H2(g)
 H2S(g)+CO(g) △H1=-17kJ/mol;
H2S(g)+CO(g) △H1=-17kJ/mol;Ⅱ.COS(g)+H2O(g)⇌H2S(g)+CO2(g) △H2=-35kJ/mol。
回答下列问题:
(1)两个反应在热力学上趋势均不大,其原因是:
(2)反应CO(g)+H2O(g)⇌H2(g)+CO2(g)的△H=
(3)羰基硫、氢气、水蒸气共混体系初始投料比不变,提高羰基硫与水蒸气反应的选择性的关键因素是
(4)在充有催化剂的恒压密闭容器中只进行反应Ⅰ。设起始充入的n(H2):n(COS)=m,相同时间内测得COS转化率与m和温度(T)的关系如图所示:
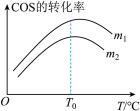
①m1
 ”、“
”、“ ”或“
”或“ ”
” 。
。②温度高于T0,COS转化率减小的可能原因为:i有副应发生;ii
(5)在充有催化剂的恒压密闭容器中进行反应Ⅱ。COS(g)与H2O(g)投料比分别为1:3和1:1,反应物的总物质的量相同时,COS(g)的平衡转化率与温度的关系曲线如图所示:
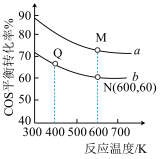
①M点对应的平衡常数
 填“
填“ ”、“
”、“ ”或“
”或“ ”
” ;
;②N点对应的平衡混合气中COS(g)物质的量分数为
③M点和Q点对应的平衡混合气体的总物质的量之比为
【推荐3】以NOx为主要成分的雾霾综合治理是当前重要的研究课题,其中汽车尾气的处理尤为重要。
已知:
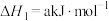
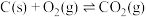

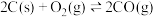
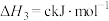
回答下列问题:
(1)汽车尾气中的NO和CO在催化转换器中发生以下反应可减少尾气污染:
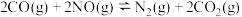 △H。则△H=
△H。则△H=
(2)某温度时,向2L恒容密闭体系中通入2mol CO和1mol NO发生反应:
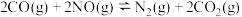
①下列能说明反应达到平衡状态的是
a.
b.体系中混合气体密度不再改变
c.CO与NO转化率的比值不再改变
d.该温度下,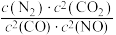 的值不再改变
的值不再改变
②某温度下,该反应达平衡时CO与CO2体积分数之比为3:2,则平衡常数为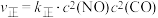 ,
,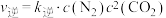 ,则该反应达到平衡时,
,则该反应达到平衡时,
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
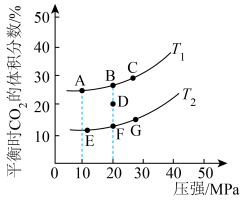
③平衡时CO2的体积分数与温度、压强的关系如图所示。则温度:T1
④若在D点对反应容器升温的同时扩大体积使体系压强减小,重新达到的平衡状态可能是图中A~G点中的
Ⅰ.亚硝酸钠的制备。

(1)装置B的作用是
(2)D中澄清石灰水变浑浊,则C中制备NaNO2的离子方程式为
Ⅱ.探究亚硝酸钠与硫酸反应的气体产物成分。
已知:①NO+NO2+2OH-=2NO
 +H2O
+H2O②气体液化的温度:NO2为21 ℃,NO为-152 ℃
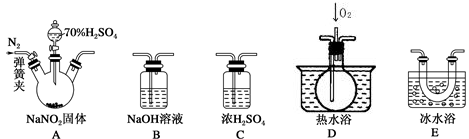
(3)反应前应打开弹簧夹,先通入一段时间氮气,目的是
(4)仪器的连接顺序(按左→右连接):A→C→
(5)在关闭弹簧夹,打开分液漏斗活塞,滴入70%硫酸后,装置A中产生红棕色气体。
①确认装置A中产生的气体含有NO,依据的现象是
②若D中通入过量O2,装置B中的化学方程式是
Ⅲ.设计实验证明酸性条件下NaNO2具有氧化性。
(6)供选用的试剂:NaNO2溶液、KMnO4溶液、Fe2(SO4)3溶液、KI溶液、稀硫酸、淀粉溶液、KSCN溶液

(1)装置A中仪器X的名称为
(2)B装置中盛放的试剂是
(3)F装置中的试剂为
(4)G装置中反应的离子方程式为
①先按要求搭配好装置再检查装置的气密性;
②打开弹簧夹K1和K2,向装置中缓缓通入N2一段时间后,加热装有15.20g FeSO4的硬质玻璃管;
③观察到的实验现象:A装置中有红棕色固体出现,B中有白色沉淀生成,C中品红溶液褪色;
④冷却后A装置中剩余固体的质量为10.88g。
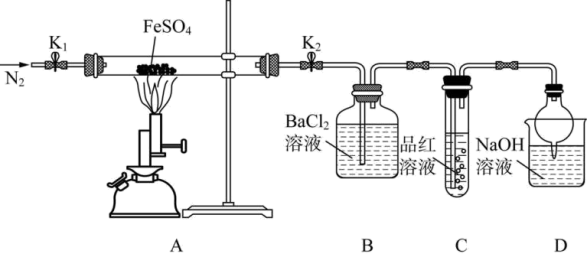
(1)根据B装置中的实验现象可推测分解产物中含有
(2)将装置B、C顺序颠倒能否达到原来的实验目的
(3)D装置中发生的主要反应的化学方程式是
(4)通过计算确定已分解的FeSO4物质的量,写出计算过程


 、浓
、浓
 、稀
、稀

