钪(Sc)及其化合物在超导合金和催化剂等领域有重要应用。一种利用钛白废酸液(含Sc3+、TiO2+、Fe3+的硫酸废液)和赤泥(含Sc2O3,Al2O3,Fe2O3,SiO2)联合制备Sc2O3的工艺流程如图所示。
②常温下,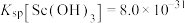 ;
; 。
。
请回答下列问题:
(1)若“浸取”后的浸取液pH<1,则浸渣的主要成分是___________ (填化学式)。
(2)“除钛”时,加入H2O2的作用是___________ 。
(3)25°C时,若使“反萃取”后水溶液中的Sc3+沉淀完全(离子浓度小于10-5mol⋅L ),应控制溶液的pH不低于
),应控制溶液的pH不低于___________ (保留两位有效数字)。
(4)写出“沉钪”时生成Sc2(C2O4)3·6H2O的离子方程式:___________ 。
(5)1 mol草酸钪晶体Sc2(C2O4)3·6H2O充分“灼烧”时,理论上转移电子的物质的量为___________ 。

②常温下,
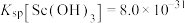 ;
; 。
。请回答下列问题:
(1)若“浸取”后的浸取液pH<1,则浸渣的主要成分是
(2)“除钛”时,加入H2O2的作用是
(3)25°C时,若使“反萃取”后水溶液中的Sc3+沉淀完全(离子浓度小于10-5mol⋅L
 ),应控制溶液的pH不低于
),应控制溶液的pH不低于(4)写出“沉钪”时生成Sc2(C2O4)3·6H2O的离子方程式:
(5)1 mol草酸钪晶体Sc2(C2O4)3·6H2O充分“灼烧”时,理论上转移电子的物质的量为
2024·海南·三模 查看更多[1]
更新时间:2024-04-30 17:34:55
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D、E、X是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。

(1)若A为金属单质,C的焰色试验为黄色,则:
①A与H2O反应的离子方程式为___________ 。
②若X为一种 会造成温室效应的气体,则X的化学式为___________ ,写 出C与E转化为D的反应的离子方程式:___________ 。
(2)若A为Fe,且A与E为同种物质,则:
①反应I的反应条件为___________ ,C的化学式为___________ ,写出一种C的用途:___________ 。
②X为CO,D为由两种元素形成的黑色固体化合物且这两种元素的质量比为7:2,D溶于稀硫酸可用于制取绿矾,写出D与稀硫酸反应的化学方程式:___________ 。

(1)若A为金属单质,C的焰色试验为黄色,则:
①A与H2O反应的离子方程式为
②若X为一种 会造成温室效应的气体,则X的化学式为
(2)若A为Fe,且A与E为同种物质,则:
①反应I的反应条件为
②X为CO,D为由两种元素形成的黑色固体化合物且这两种元素的质量比为7:2,D溶于稀硫酸可用于制取绿矾,写出D与稀硫酸反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某实验小组欲通过测定单位时间内酸性KMnO4溶液和H2C2O4(草酸)溶液反应生成CO2的体积,探究影响该化学反应速率的因素,设计的实验方案如下(KMnO4溶液已酸化),实验装置如图所示。
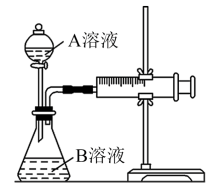
(1)写出酸性KMnO4溶液和H2C2O4(草酸)溶液反应的离子方程式____ 。
(2)该实验探究的是____ 因素对化学反应速率的影响;相同时间内针筒中所得CO2的体积大小关系是①____ ②(填“>”、“<”或“=”)。
(3)若实验①在2min末收集了4.48mLCO2(标准状况下),则在2min末,c( )=
)=___ mol/L。(假设混合溶液体积为50mL)
(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定___ 来比较化学反应速率。
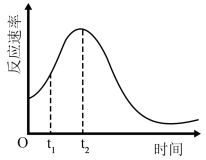
(5)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:①产物Mn2+是反应的催化剂、②____ 。

实验序号 | A溶液 | B溶液 |
① | 20mL0.1mol/LH2C2O4溶液 | 30mL0.01mol/LKMnO4溶液 |
② | 20mL0.2mol/LH2C2O4溶液 | 30mL0.01mol/LKMnO4溶液 |
(2)该实验探究的是
(3)若实验①在2min末收集了4.48mLCO2(标准状况下),则在2min末,c(
 )=
)=(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定
(5)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:①产物Mn2+是反应的催化剂、②

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】 溶液和
溶液和 溶液可发生反应:
溶液可发生反应: 。利用下图所示装置(夹持仪器略去)探究影响反应速率的因素,向A中加入一定体积
。利用下图所示装置(夹持仪器略去)探究影响反应速率的因素,向A中加入一定体积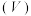 的
的 溶液、
溶液、 溶液和水,充分搅拌;控制体系温度,通过分液漏斗往A中加入醋酸;当导管口气泡均匀稳定冒出时收集气体,用秒表测量收集
溶液和水,充分搅拌;控制体系温度,通过分液漏斗往A中加入醋酸;当导管口气泡均匀稳定冒出时收集气体,用秒表测量收集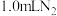 所用时间
所用时间 ,重复多次取平均值。
,重复多次取平均值。
回答下列问题:
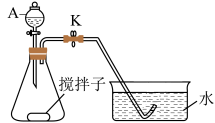
(1)仪器A的名称为_____ 。
(2)若需控制体系温度为 ,采取的合理加热方式为
,采取的合理加热方式为_____ 。
(3)探究反应速率与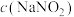 的关系,测得相关实验数据如下表所示。
的关系,测得相关实验数据如下表所示。
①
_____ mL,
_____ mL。
②该实验所得结论为_____ 。
(4)在上述实验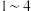 中,甲同学用数字传感器测得溶液中
中,甲同学用数字传感器测得溶液中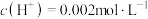 ,甲同学认为
,甲同学认为 作催化剂,增加实验5,用
作催化剂,增加实验5,用 盐酸替代醋酸,若
盐酸替代醋酸,若 ,且反应前后
,且反应前后 不变,则
不变,则
_____ mL。
(5)利用氨水可以将 和
和 吸收,其原理如图所示:
吸收,其原理如图所示:
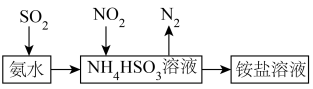
用氨水吸收 能得到含
能得到含 和
和 的吸收液,写出生成
的吸收液,写出生成 反应的离子方程式:
反应的离子方程式:_____ 。若向吸收液中通入过量 ,
, 能与
能与 发生反应生成
发生反应生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为_____ 。
 溶液和
溶液和 溶液可发生反应:
溶液可发生反应: 。利用下图所示装置(夹持仪器略去)探究影响反应速率的因素,向A中加入一定体积
。利用下图所示装置(夹持仪器略去)探究影响反应速率的因素,向A中加入一定体积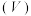 的
的 溶液、
溶液、 溶液和水,充分搅拌;控制体系温度,通过分液漏斗往A中加入醋酸;当导管口气泡均匀稳定冒出时收集气体,用秒表测量收集
溶液和水,充分搅拌;控制体系温度,通过分液漏斗往A中加入醋酸;当导管口气泡均匀稳定冒出时收集气体,用秒表测量收集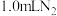 所用时间
所用时间 ,重复多次取平均值。
,重复多次取平均值。回答下列问题:

(1)仪器A的名称为
(2)若需控制体系温度为
 ,采取的合理加热方式为
,采取的合理加热方式为(3)探究反应速率与
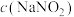 的关系,测得相关实验数据如下表所示。
的关系,测得相关实验数据如下表所示。| 实验编号 |
| 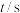 | |||
 溶液 溶液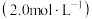 |  溶液 溶液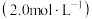 | 盐酸 | 水 | ||
| 1 | 4.0 | 4.0 | 4.0 | 8.0 | 33 |
| 2 | 6.0 |  |  | 6.0 | 15 |
| 3 |  | 4.0 | 4.0 | 4.0 | 83 |
| 4 | 12.0 | 4.0 | 4.0 | 0.0 | 38 |


②该实验所得结论为
(4)在上述实验
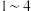 中,甲同学用数字传感器测得溶液中
中,甲同学用数字传感器测得溶液中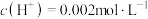 ,甲同学认为
,甲同学认为 作催化剂,增加实验5,用
作催化剂,增加实验5,用 盐酸替代醋酸,若
盐酸替代醋酸,若 ,且反应前后
,且反应前后 不变,则
不变,则
| 实验编号 | 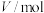 | 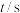 | |||
 溶液 溶液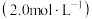 |  溶液 溶液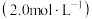 | 盐酸 | 水 | ||
| 5 | 12.0 | 4.0 |  | 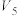 |  |
 和
和 吸收,其原理如图所示:
吸收,其原理如图所示:
用氨水吸收
 能得到含
能得到含 和
和 的吸收液,写出生成
的吸收液,写出生成 反应的离子方程式:
反应的离子方程式: ,
, 能与
能与 发生反应生成
发生反应生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】草酸是一种二元弱酸,可用作还原剂、沉淀剂等。某校课外小组的同学设计利用C2H2气体制取H2C2O4·2H2O。回答下列问题:
(1)甲组的同学以电石(主要成分CaC2,少量CaS及Ca3P2杂质等)为原料,并用下图1装置制取C2H2。___________ (写一种即可)。
②装置B中,NaClO将H2S、PH3 氧化为硫酸及磷酸,本身被还原为NaCl,其中PH3被氧化的离子方程式为___________ 。该过程中,可能产生新的杂质气体Cl2,其原因是:___________ (用离子方程式回答)。
(2)乙组的同学根据文献资料,用Hg(NO3)2作催化剂,浓硝酸氧化C2H2制取H2C2O4·2H2O。制备装置如上图2所示:
①装置D中多孔球泡的作用是___________ 。
②装置D中生成H2C2O4的化学方程式为___________ 。
③从装置D中得到产品,还需经过___________ (填操作名称)、过滤、洗涤及干燥。
(3)丙组设计了测定乙组产品中H2C2O4·2H2O的质量分数实验。他们的实验步骤如下:准确称取m g产品于锥形瓶中,加入适量的蒸馏水溶解,再加入少量稀硫酸,然后用c mol·L-1酸性KMnO4标准溶液进行滴定至终点,共消耗标准溶液V mL。
①滴定终点的现象是___________ 。
②产品中H2C2O4·2H2O的质量分数为___________ (列出含 m、c、V 的表达式)。
(1)甲组的同学以电石(主要成分CaC2,少量CaS及Ca3P2杂质等)为原料,并用下图1装置制取C2H2。
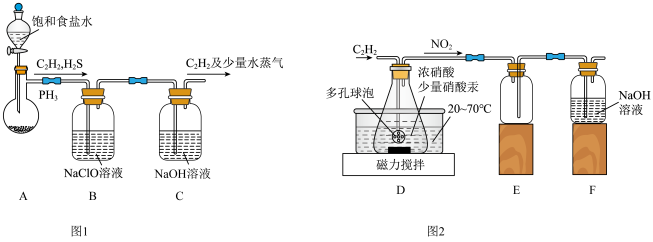
②装置B中,NaClO将H2S、PH3 氧化为硫酸及磷酸,本身被还原为NaCl,其中PH3被氧化的离子方程式为
(2)乙组的同学根据文献资料,用Hg(NO3)2作催化剂,浓硝酸氧化C2H2制取H2C2O4·2H2O。制备装置如上图2所示:
①装置D中多孔球泡的作用是
②装置D中生成H2C2O4的化学方程式为
③从装置D中得到产品,还需经过
(3)丙组设计了测定乙组产品中H2C2O4·2H2O的质量分数实验。他们的实验步骤如下:准确称取m g产品于锥形瓶中,加入适量的蒸馏水溶解,再加入少量稀硫酸,然后用c mol·L-1酸性KMnO4标准溶液进行滴定至终点,共消耗标准溶液V mL。
①滴定终点的现象是
②产品中H2C2O4·2H2O的质量分数为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】为消除燃煤烟气中的SO2、NOx,研究者提出了若干烟气“脱硫”“脱硝”的方法。
(1)在催化剂作用下用CO还原N2O,实现环境治理的无害化处理。
已知:① 2CO(g)+O2(g) 2CO2(g) ∆H1=a kJ∙mol-1
2CO2(g) ∆H1=a kJ∙mol-1
②2N2O(g) 2N2(g)+O2(g) ∆H2=b kJ∙mol-1
2N2(g)+O2(g) ∆H2=b kJ∙mol-1
写出总反应的热化学方程式:_______ 。
(2)利用氨水可以吸收SO2、NO2,原理如下图所示:
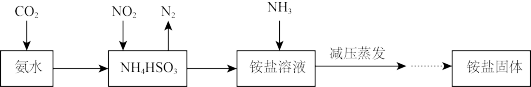
①氨水吸收过量SO2时NH3∙H2O与SO2的物质的量之比为_______ 。
②铵盐溶液要减压蒸发的原因是_______ 。
③吸收NO2时的离子方程式为_______ 。
(3)以NaClO溶液作为吸收剂进行一体化“脱硫”“脱硝”。控制溶液的pH=5.5,将烟气中的SO2、NO转化为 、
、 。
。
①某次实验需要使用480mL0.2mol/L的NaClO溶液,欲用NaClO固体配制该溶液,实验中需用电子天平称量(可精确到0.01)_______ NaClO晶体,配制时需要的玻璃仪器包括:烧杯、玻璃棒、量筒、_______ (写出仪器名称),若定容时俯视刻度线,则所配溶液浓度_______ (填“偏高”“偏低”或“无影响”)。
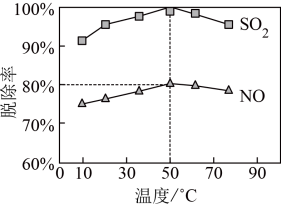
②一定时间内,温度对硫、硝脱除率的影响曲线如图,SO2的脱除率高于NO,可能的原因是_______ (写出1种即可)。若烟气中SO2和NO的体积比为2:1,则50℃时,NaClO溶液吸收烟气后的溶液中 和Cl-的物质的量之比为
和Cl-的物质的量之比为_______ 。
(1)在催化剂作用下用CO还原N2O,实现环境治理的无害化处理。
已知:① 2CO(g)+O2(g)
 2CO2(g) ∆H1=a kJ∙mol-1
2CO2(g) ∆H1=a kJ∙mol-1②2N2O(g)
 2N2(g)+O2(g) ∆H2=b kJ∙mol-1
2N2(g)+O2(g) ∆H2=b kJ∙mol-1写出总反应的热化学方程式:
(2)利用氨水可以吸收SO2、NO2,原理如下图所示:

①氨水吸收过量SO2时NH3∙H2O与SO2的物质的量之比为
②铵盐溶液要减压蒸发的原因是
③吸收NO2时的离子方程式为
(3)以NaClO溶液作为吸收剂进行一体化“脱硫”“脱硝”。控制溶液的pH=5.5,将烟气中的SO2、NO转化为
 、
、 。
。①某次实验需要使用480mL0.2mol/L的NaClO溶液,欲用NaClO固体配制该溶液,实验中需用电子天平称量(可精确到0.01)
②一定时间内,温度对硫、硝脱除率的影响曲线如图,SO2的脱除率高于NO,可能的原因是
 和Cl-的物质的量之比为
和Cl-的物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】X、Y、Z、W为含有相同电子数的分子或离子,均由原子序数小于10的元素组成,X有5个原子核。通常状况下,W为无色液体。
已知:X+Y Z+W
Z+W
(1)Z的空间构型为___________ 。
(2)液态Z和W的电离相似,都可电离出电子数相同的两种离子,液态Z的电离方程式是_____ 。
(3)1mol气态Z与O2反应生成液态W和一种由两种元素组成的气体物质,放出的热量为QkJ,写出该反应的热化学方程式:___________________________ 。
(4)一定温度下,将1mol N2O4置于密闭容器中,保持压强不变,升高温度至T1的过程中,气体由无色逐渐变为红棕色。温度由T1继续升高到T2的过程中,气体逐渐变为无色。若保持T2,增大压强,气体逐渐变为红棕色。气体的物质的量n随温度T变化的关系如图所示。

①温度在T1—T2之间,反应的化学方程式是:_________ 。
②温度在T2—T3之间,气体的平均相对分子质量是(保留1位小数)________ 。
③若将实验所得的平衡混和气体通入足量的水中,欲使气体被完全吸收则至少应同时通入标准状况下的空气________ L。(设空气组成为:N2与O2,体积比4:1)
已知:X+Y
 Z+W
Z+W(1)Z的空间构型为
(2)液态Z和W的电离相似,都可电离出电子数相同的两种离子,液态Z的电离方程式是
(3)1mol气态Z与O2反应生成液态W和一种由两种元素组成的气体物质,放出的热量为QkJ,写出该反应的热化学方程式:
(4)一定温度下,将1mol N2O4置于密闭容器中,保持压强不变,升高温度至T1的过程中,气体由无色逐渐变为红棕色。温度由T1继续升高到T2的过程中,气体逐渐变为无色。若保持T2,增大压强,气体逐渐变为红棕色。气体的物质的量n随温度T变化的关系如图所示。

①温度在T1—T2之间,反应的化学方程式是:
②温度在T2—T3之间,气体的平均相对分子质量是(保留1位小数)
③若将实验所得的平衡混和气体通入足量的水中,欲使气体被完全吸收则至少应同时通入标准状况下的空气
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】2023年,我国新能源汽车产销量占全球比重超过60%、连续9年位居世界第一位;新能源汽车出口120.3万辆,这一可喜成绩的获得离不开化学人的辛苦付出.锰酸锂离子蓄电池是第二代锂离子动力电池,性能优良.工业上用某软锰矿(主要成分为 ,还含有少量铁、铝及硅的氧化物)为原料制备锰酸锂
,还含有少量铁、铝及硅的氧化物)为原料制备锰酸锂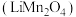 .流程如图:
.流程如图:
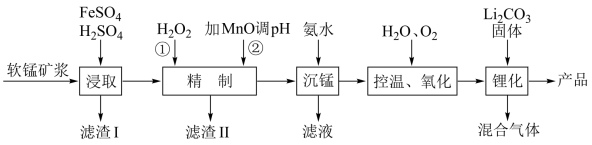
(1)滤渣I的主要成分是___________ 。
(2)已知某离子浓度(用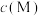 表示)形成沉淀与溶液pH关系,如下图所示
表示)形成沉淀与溶液pH关系,如下图所示
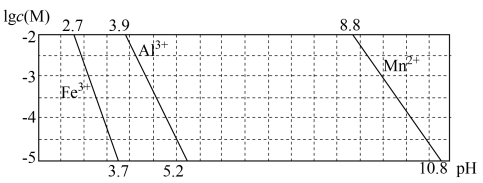
试判断“精制”过程中,加 调节pH的范围是
调节pH的范围是____________ 。
(3)工业上也可以将“精制”后的滤液加入 来合成
来合成 .已知
.已知 的结构式为:
的结构式为: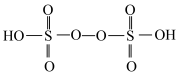 ,其中S的化合价为
,其中S的化合价为____________ .写出该反应的离子方程式_______________
(4)“沉锰”所得溶液回收可用于_____________ 。
(5)“控温、氧化”过程中,溶液温度不宜过高,原因是_______________ 。
(6)“锂化”是将 和
和 按4:1的物质的量比配料,球磨3~5h,然后升温至600~750℃,保温24h,自然冷却至室温得产品.请写出化学反应方程式
按4:1的物质的量比配料,球磨3~5h,然后升温至600~750℃,保温24h,自然冷却至室温得产品.请写出化学反应方程式_____________ 。
 ,还含有少量铁、铝及硅的氧化物)为原料制备锰酸锂
,还含有少量铁、铝及硅的氧化物)为原料制备锰酸锂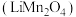 .流程如图:
.流程如图:
(1)滤渣I的主要成分是
(2)已知某离子浓度(用
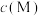 表示)形成沉淀与溶液pH关系,如下图所示
表示)形成沉淀与溶液pH关系,如下图所示
试判断“精制”过程中,加
 调节pH的范围是
调节pH的范围是(3)工业上也可以将“精制”后的滤液加入
 来合成
来合成 .已知
.已知 的结构式为:
的结构式为: ,其中S的化合价为
,其中S的化合价为(4)“沉锰”所得溶液回收可用于
(5)“控温、氧化”过程中,溶液温度不宜过高,原因是
(6)“锂化”是将
 和
和 按4:1的物质的量比配料,球磨3~5h,然后升温至600~750℃,保温24h,自然冷却至室温得产品.请写出化学反应方程式
按4:1的物质的量比配料,球磨3~5h,然后升温至600~750℃,保温24h,自然冷却至室温得产品.请写出化学反应方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】NiSO4·6H2O是一种绿色易溶于水的晶体,广泛应用于镀镍电镀液、催化剂和金属着色剂等方面。某科研小组用富含镍(NiS)的工业废渣(含SiO2、FeO、Al2O3等杂质)制备NiSO4·6H2O,设计流程图如下:

已知:Ksp[Ni(OH)2]=1.0×10−15,Ksp[Fe(OH)2]=1.0×10−16,Ksp[Al(OH)3]= 1.0×10−34,Ksp[Fe(OH)3]=1.0×10−39
根据要求回答下列问题:
(1)将工业废渣粉碎的目的是_______ 。
(2)酸浸过程中,1 mol NiS失去8NA个电子,同时生成一种无色有毒气体,写出该反应的化学方程式:_______ 。
(3)“氧化”过程保持滤液温度在40℃左右,加入6%的H2O2,加入H2O2的目的是_______ ,若上述流程省去“氧化”步骤,则导致的后果是_______ 。
(4)常温下,加入NaOH溶液调节pH,若溶液中c(Ni2+)=0.1 mol·L−1,则溶液的pH范围应调节为4.3~_______ 之间。
(5)小火煮沸的作用是使沉淀颗粒长大,这样做有利于_______ 。
(6)已知加入的Na2CO3溶液足量,确定Ni2+已完全沉淀的简单实验方法是_______ 。

已知:Ksp[Ni(OH)2]=1.0×10−15,Ksp[Fe(OH)2]=1.0×10−16,Ksp[Al(OH)3]= 1.0×10−34,Ksp[Fe(OH)3]=1.0×10−39
根据要求回答下列问题:
(1)将工业废渣粉碎的目的是
(2)酸浸过程中,1 mol NiS失去8NA个电子,同时生成一种无色有毒气体,写出该反应的化学方程式:
(3)“氧化”过程保持滤液温度在40℃左右,加入6%的H2O2,加入H2O2的目的是
(4)常温下,加入NaOH溶液调节pH,若溶液中c(Ni2+)=0.1 mol·L−1,则溶液的pH范围应调节为4.3~
(5)小火煮沸的作用是使沉淀颗粒长大,这样做有利于
(6)已知加入的Na2CO3溶液足量,确定Ni2+已完全沉淀的简单实验方法是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】铍的氧化物广泛应用于原子能、航天、电子、陶瓷等领域,是重要的战略物资。利用绿柱石(主要化学成分为(Be3Al2Si6O18,还含有一定量的FeO和Fe2O3)生产BeO的一种工艺流程如下。
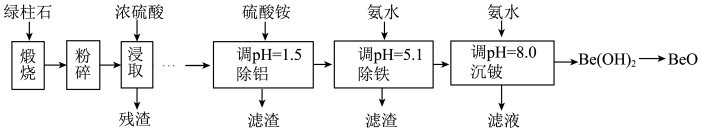
回答问题:
(1)Be3Al2Si6O18中Be的化合价为______ 。Si原子价层电子排布式为_______ 。元素Al与Si中,第一电离能较大的是_______ ,氮原子和氧原子电负性较大的是______ 。
(2)浓硫酸浸取后残渣主要成分是_______ (填化学式)。
(3)该流程中能循环使用的物质是______ (填化学式)。
(4)无水BeCl2可用作聚合反应的催化剂。BeO、Cl2与足量C在600~800℃制备BeCl2的化学方程式为______ 。
(5)沉铍时,将pH从8.0提高到9.0,则铍的损失降低至原来的______ %。

回答问题:
(1)Be3Al2Si6O18中Be的化合价为
(2)浓硫酸浸取后残渣主要成分是
(3)该流程中能循环使用的物质是
(4)无水BeCl2可用作聚合反应的催化剂。BeO、Cl2与足量C在600~800℃制备BeCl2的化学方程式为
(5)沉铍时,将pH从8.0提高到9.0,则铍的损失降低至原来的
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】北京时间2021年10月16日上午,神舟十三号航天员顺利进驻“天和”核心舱,开启为期6个月的航天飞行任务。航天员生活、工作于其中的“天和”核心舱是利用三结砷化镓太阳能电池作为其动力。一种由砷化镓废料(主要成分为GaAs,含Fe2O3、SiO2等杂质)制备镓的工艺流程如图:
②离子完全沉淀的pH值:SiO 为8,GaO
为8,GaO 为5.5。
为5.5。
回答下列问题:
(1)“风化粉碎”的目的是_______ 。
(2)“碱浸”温度控制在70℃左右,温度不能过高或过低的原因是_______ 。
(3)“碱浸”时,GaAs中Ga以NaGaO2的形式进入溶液中,该反应的离子方程式是_______ 。

②离子完全沉淀的pH值:SiO
 为8,GaO
为8,GaO 为5.5。
为5.5。回答下列问题:
(1)“风化粉碎”的目的是
(2)“碱浸”温度控制在70℃左右,温度不能过高或过低的原因是
(3)“碱浸”时,GaAs中Ga以NaGaO2的形式进入溶液中,该反应的离子方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】已知某工业废水中含有大量CuSO4,少量的Ag+、Hg2+以及部分污泥,通过下述过程可从该废水中回收硫酸铜晶体及其它物质。

(1)步骤1的主要操作是___________ 。
(2)步骤2中需加入某种试剂后再将混合物分离,该试剂是(填化学式)__________ ,固体残渣的成分是(填化学式)________________ 。
(3)步骤3中涉及的操作是:蒸发浓缩、_____________ 、过滤、烘干。
(4)步骤2应该在通风橱中进行,原因是____________________________ 。

(1)步骤1的主要操作是
(2)步骤2中需加入某种试剂后再将混合物分离,该试剂是(填化学式)
(3)步骤3中涉及的操作是:蒸发浓缩、
(4)步骤2应该在通风橱中进行,原因是
您最近一年使用:0次

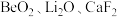 及少量
及少量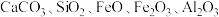 )中提取铍的工艺如图所示:
)中提取铍的工艺如图所示: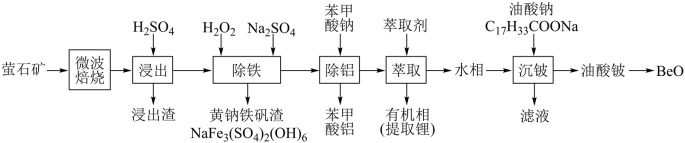
 的方法是
的方法是

