以CO、 为原料合成甲醇的反应为
为原料合成甲醇的反应为
 ,在容积相同的三个恒容密闭容器
,在容积相同的三个恒容密闭容器 、
、 、
、 中均充入1molCO和
中均充入1molCO和 ,三个容器的反应温度分别为
,三个容器的反应温度分别为 、
、 、
、 且恒定不变。三个容器中反应均进行到tmin时CO的体积分数示意图如图,下列说法错误的是
且恒定不变。三个容器中反应均进行到tmin时CO的体积分数示意图如图,下列说法错误的是
 为原料合成甲醇的反应为
为原料合成甲醇的反应为
 ,在容积相同的三个恒容密闭容器
,在容积相同的三个恒容密闭容器 、
、 、
、 中均充入1molCO和
中均充入1molCO和 ,三个容器的反应温度分别为
,三个容器的反应温度分别为 、
、 、
、 且恒定不变。三个容器中反应均进行到tmin时CO的体积分数示意图如图,下列说法错误的是
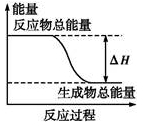
且恒定不变。三个容器中反应均进行到tmin时CO的体积分数示意图如图,下列说法错误的是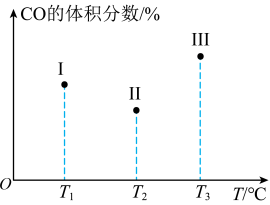
| A.该反应的反应物的总能量大于生成物的总能量 |
B.在容器 或 或 中,无论反应进行到何种程度,一定存在 中,无论反应进行到何种程度,一定存在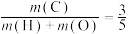 |
| C.高温条件有利于该反应自发进行 |
D.tmin时,容器 中的反应一定没有达到平衡,容器 中的反应一定没有达到平衡,容器 中的反应一定达到了平衡 中的反应一定达到了平衡 |
更新时间:2024-05-11 17:01:05
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列各实验的现象及结论都正确的是
| 选项 | 实验 | 现象 | 结论 |
| A | 常温下将 晶体与 晶体与 晶体在小烧杯中充分混合 晶体在小烧杯中充分混合 | 烧杯壁变热 | 该反应是放热反应 |
| B | 铜粉加入稀硫酸中,加热;再加入少量硝酸钾固体 | 加热时无明显现象,加入硝酸钾后溶液变蓝 | 硝酸钾起催化作用 |
| C | 某溶液加入稀NaOH溶液,在试管口放湿润的红色石蕊试纸 | 湿润的红色石蕊试纸不变蓝 | 原溶液不存在 |
| D | 浓硫酸滴入蔗糖中,产生的气体导入澄清石灰水 | 蔗糖变黑,体积膨胀,生成刺激性气味的气体,澄清石灰水变浑浊 | 浓硫酸具有脱水性和强氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。如图为 (g)和
(g)和 (g)反应生成NO(g)过程中的能量变化:
(g)反应生成NO(g)过程中的能量变化:
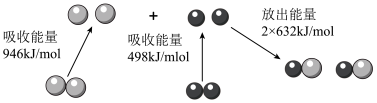
下列说法中正确的是
 (g)和
(g)和 (g)反应生成NO(g)过程中的能量变化:
(g)反应生成NO(g)过程中的能量变化:
下列说法中正确的是
A.通常情况下, (g)比 (g)比 (g)稳定 (g)稳定 |
B. (g)和 (g)和 (g)具有的总能量小于2molNO(g)具有的总能量 (g)具有的总能量小于2molNO(g)具有的总能量 |
| C.破坏相同质量的反应物和生成物中所有的化学键,前者需要的能量多 |
D.28g (g)和32g (g)和32g (g)完全反应生成NO(g),放出的能量为180kJ (g)完全反应生成NO(g),放出的能量为180kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法正确的是
| A.需要加热才能进行的反应一定是吸热反应 |
| B.蒸干氯化铵溶液,得到氯化铵固体 |
C.用惰性电极电解饱和 溶液,一段时间后仍为饱和溶液 溶液,一段时间后仍为饱和溶液 |
| D.H2、I2 (蒸气)和HI的平衡混合气体加压后颜色加深可以用平衡移动原理解释 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】一定条件下,在密闭容器中进行如下反应: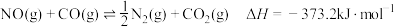 ,达到平衡后,为提高反应速率和CO的转化率,采取的措施正确的是
,达到平衡后,为提高反应速率和CO的转化率,采取的措施正确的是
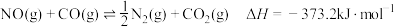 ,达到平衡后,为提高反应速率和CO的转化率,采取的措施正确的是
,达到平衡后,为提高反应速率和CO的转化率,采取的措施正确的是| A.加入催化剂,同时升高温度 | B.加入催化剂,同时增大压强 |
| C.升高温度,同时充入N2 | D.降低温度,同时减小压强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】工业上利用焦炭与水蒸气生产H2的反应原理为C(s)+H2O(g)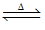 CO(g)+H2(g) ΔH>0;CO(g)+H2O(g)
CO(g)+H2(g) ΔH>0;CO(g)+H2O(g)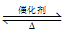 CO2(g)+H2(g) ΔH<0;第二步生产的原料CO来源于第一步的产物。为提高原料的利用率及H2的日产量,下列措施中不可取的是( )
CO2(g)+H2(g) ΔH<0;第二步生产的原料CO来源于第一步的产物。为提高原料的利用率及H2的日产量,下列措施中不可取的是( )
①第一步产生的混合气直接作为第二步的反应物
②第二步生产应采用适当的温度和催化剂
③第一、二步生产中均充入足量水蒸气
④第二步应在低温下进行
⑤第二步生产采用高压
⑥第二步生产中增大CO的浓度
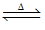 CO(g)+H2(g) ΔH>0;CO(g)+H2O(g)
CO(g)+H2(g) ΔH>0;CO(g)+H2O(g)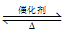 CO2(g)+H2(g) ΔH<0;第二步生产的原料CO来源于第一步的产物。为提高原料的利用率及H2的日产量,下列措施中不可取的是( )
CO2(g)+H2(g) ΔH<0;第二步生产的原料CO来源于第一步的产物。为提高原料的利用率及H2的日产量,下列措施中不可取的是( )①第一步产生的混合气直接作为第二步的反应物
②第二步生产应采用适当的温度和催化剂
③第一、二步生产中均充入足量水蒸气
④第二步应在低温下进行
⑤第二步生产采用高压
⑥第二步生产中增大CO的浓度
| A.①③⑤ | B.②④⑥ |
| C.②③⑤ | D.①④⑤⑥ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是
| A.电解饱和食盐水可以直接制取“84”消毒液 |
| B.溶液导电过程就是电解过程,溶液的pH肯定会发生变化 |
| C.共价化合物中一定没有离子键,离子化合物中一定没有共价键 |
| D.焓减小,熵增加的反应,一定不能自发进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法中,正确的是
A. 转化变为 转化变为 时,熵减小 时,熵减小 |
| B.使用催化剂能使非自发反应转化成自发反应 |
C.室温下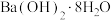 晶体与 晶体与 晶体的反应是非自发反应 晶体的反应是非自发反应 |
D.某反应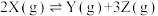 在高温时能自发进行,其逆反应在低温时能自发进行,则该反应的正反应的 在高温时能自发进行,其逆反应在低温时能自发进行,则该反应的正反应的 、 、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列说法正确的是
A.向 的液体平衡体系中加入少量KCl固体,由于生成物浓度增加,平衡逆向移动,所以液体血红色变浅 的液体平衡体系中加入少量KCl固体,由于生成物浓度增加,平衡逆向移动,所以液体血红色变浅 |
B.∆H>0、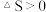 或∆H<0、∆S<0的化学反应都可能自发进行 或∆H<0、∆S<0的化学反应都可能自发进行 |
C.以铜为电极,电解KI溶液 含有少量淀粉 含有少量淀粉 ,阳极附近溶液呈现蓝色 ,阳极附近溶液呈现蓝色 |
D.向稀 中滴加 中滴加 溶液,反应的离子方程式为 溶液,反应的离子方程式为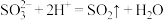 |
您最近一年使用:0次