一定条件下,在密闭容器中进行如下反应: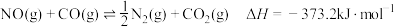 ,达到平衡后,为提高反应速率和CO的转化率,采取的措施正确的是
,达到平衡后,为提高反应速率和CO的转化率,采取的措施正确的是
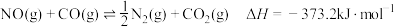 ,达到平衡后,为提高反应速率和CO的转化率,采取的措施正确的是
,达到平衡后,为提高反应速率和CO的转化率,采取的措施正确的是| A.加入催化剂,同时升高温度 | B.加入催化剂,同时增大压强 |
| C.升高温度,同时充入N2 | D.降低温度,同时减小压强 |
更新时间:2023-10-05 22:23:23
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】利用无机离子[LRuIII(H2O)5-和[CeIV(NO3)6]2-(如图可简写为CeIV),可以实现水在催化剂作用下制氧气。其相关机理如图所示:
下列说法正确的是

下列说法正确的是
| A.[CeIV(NO3)6]2-在反应中做催化剂 |
B.催化氧化水的反应为:2H2O O2↑+2H2↑ O2↑+2H2↑ |
| C.若反应①中为H218O,反应②中为H216O,则产生16O18O |
| D.反应③为非氧化还原反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是
| A.增大反应物浓度,可增大单位体积内活化分子的百分数,使有效碰撞次数增大 |
| B.有气体参加的化学反应,若增大压强(即缩小反应容器的容积),可增加活化分子的百分数,从而使反应速率加快 |
| C.升高温度能使化学反应速率加快,主要原因是增加了反应物分子中活化分子的百分数 |
| D.催化剂降低反应活化能,从而增加反应热 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】我国实现了从二氧化碳到淀粉的全合成,该合成分两步进行,首先由 和
和 合成甲醇,然后由甲醇合成淀粉。一定条件下
合成甲醇,然后由甲醇合成淀粉。一定条件下 和
和 催化反应
催化反应
 ,在一恒温恒容密闭容器中充入1mol
,在一恒温恒容密闭容器中充入1mol 和3mol
和3mol 进行上述反应,测得
进行上述反应,测得 (g)和
(g)和 浓度随时间变化如图甲;在不同催化剂作用下发生反应Ⅰ、Ⅱ、Ⅲ,相同时间内
浓度随时间变化如图甲;在不同催化剂作用下发生反应Ⅰ、Ⅱ、Ⅲ,相同时间内 转化率随温度变化关系如图乙。
转化率随温度变化关系如图乙。
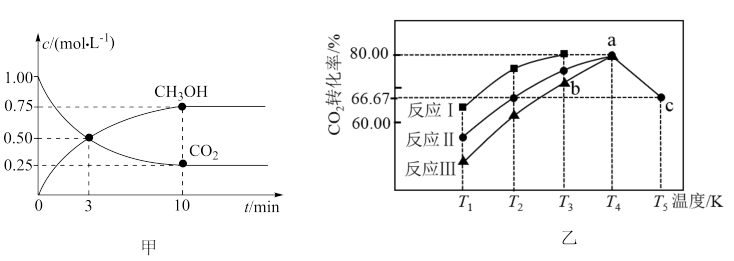
下列有关说法不正确的是
 和
和 合成甲醇,然后由甲醇合成淀粉。一定条件下
合成甲醇,然后由甲醇合成淀粉。一定条件下 和
和 催化反应
催化反应
 ,在一恒温恒容密闭容器中充入1mol
,在一恒温恒容密闭容器中充入1mol 和3mol
和3mol 进行上述反应,测得
进行上述反应,测得 (g)和
(g)和 浓度随时间变化如图甲;在不同催化剂作用下发生反应Ⅰ、Ⅱ、Ⅲ,相同时间内
浓度随时间变化如图甲;在不同催化剂作用下发生反应Ⅰ、Ⅱ、Ⅲ,相同时间内 转化率随温度变化关系如图乙。
转化率随温度变化关系如图乙。
下列有关说法不正确的是
| A.0~10min内,氢气的平均反应速率为0.225mol/(L·min) |
| B.该温度下,第一步反应的平衡常数K=4 |
C.T1到T2段随温度升高 转化率升高可能原因为温度升高、催化剂活性增加 转化率升高可能原因为温度升高、催化剂活性增加 |
D.T4到T5段随温度升高 转化率降低且曲线一致的原因是反应达到平衡,温度升高平衡逆向移动,而催化剂不影响化学平衡移动 转化率降低且曲线一致的原因是反应达到平衡,温度升高平衡逆向移动,而催化剂不影响化学平衡移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验操作正确且能达到相应实验目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 用 试纸测定同温度同浓度 试纸测定同温度同浓度 溶液和 溶液和 溶液的 溶液的 | 酸性: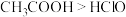 |
| B | 将 固体溶于适量浓盐酸,再用蒸馏水稀释,最后在试剂瓶中加入少量的铁粉 固体溶于适量浓盐酸,再用蒸馏水稀释,最后在试剂瓶中加入少量的铁粉 | 配制 溶液 溶液 |
| C | 将两个相同的 球分别放入热水和冰水里,热水中的 球分别放入热水和冰水里,热水中的 球红棕色加深,冰水中的变浅 球红棕色加深,冰水中的变浅 |  的 的 |
| D | 向 溶液中先滴入5滴 溶液中先滴入5滴 的 的 溶液,再滴入5滴 溶液,再滴入5滴 的 的 溶液 溶液 | 证明: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 CH3OH(g) ΔH,生成1mol CH3OH(g)的能量变化如图曲线Ⅰ所示。曲线Ⅱ表示使用催化剂的情况。下列判断不正确的是
CH3OH(g) ΔH,生成1mol CH3OH(g)的能量变化如图曲线Ⅰ所示。曲线Ⅱ表示使用催化剂的情况。下列判断不正确的是


