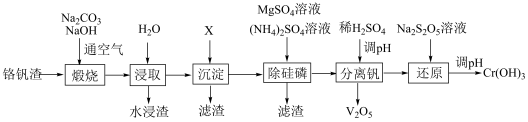
铬和钒具有广泛用途,铬钒中铬和钒以低价态含氧酸盐形式存在,主要杂质为氧化铁及铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如图所示: 形式存在,在碱性介质中以
形式存在,在碱性介质中以 形式存在。
形式存在。
②氧化性: 。
。
请回答下列问题:
(1)基态 原子的价层电子排布式为
原子的价层电子排布式为______ ,基态V原子的未成对电子数为______ 。
(2)“煅烧”后,若铬被氧化为相应的最高价含氧酸盐,则 元素以化合物
元素以化合物______ (填化学式,下同)的形式存在;水浸渣的主要成分为 和
和______ , 中含有的
中含有的 键数目为
键数目为______ 。
(3)“沉淀”步骤得到的滤渣为 ,X可选择______(填标号)。
,X可选择______(填标号)。
(4)“还原”步骤中加入 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为__________________ 。
 形式存在,在碱性介质中以
形式存在,在碱性介质中以 形式存在。
形式存在。②氧化性:
 。
。请回答下列问题:
(1)基态
 原子的价层电子排布式为
原子的价层电子排布式为(2)“煅烧”后,若铬被氧化为相应的最高价含氧酸盐,则
 元素以化合物
元素以化合物 和
和 中含有的
中含有的 键数目为
键数目为(3)“沉淀”步骤得到的滤渣为
 ,X可选择______(填标号)。
,X可选择______(填标号)。A. 溶液 溶液 | B.氨水 | C.硫酸溶液 | D.盐酸 |
(4)“还原”步骤中加入
 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为
更新时间:2024-05-12 15:13:46
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】今有A、B、C、D四种元素,已知A元素是地壳中含量最多的元素;B元素为金属元素,它的原子核外K、L层上电子数之和等于M、N层电子数之和;C元素是第三周期第一电离能最小的元素;D元素在第三周期中电负性最大。
(1)写出A元素原子的核外电子排布式:_______ ;写出B元素原子核外电子排布的价电子构型:_______ ;用电子排布图表示C原子的核外电子排布情况:_______ 。
(2)四种元素电负性由小到大顺序(填元素符号):_______
(1)写出A元素原子的核外电子排布式:
(2)四种元素电负性由小到大顺序(填元素符号):
您最近一年使用:0次
【推荐2】元素周期表前四周期的A、B、C、D、E五种元素,A元素的原子最外层电子排布式为ns1;B元素的原子价电子排布式为ns2np2;C元素位于第二周期且原子中p能级与s能级电子总数相等;D元素原子的M能层的p能级中有3个未成对电子;E元素原子有五个未成对电子。
(1)写出元素名称:C___________ 、D___________ 、E___________ 。
(2)C基态原子的电子排布图为___________ 。
(3)当n=2时,B的最简单气态氢化物的电子式为___________ ,BC2分子的结构式是___________ ;当n=3时,B与C形成的化合物与氢氧化钠溶液反应的离子方程式是:___________ 。
(4)E元素原子的外围电子排布式是___________ 。
(1)写出元素名称:C
(2)C基态原子的电子排布图为
(3)当n=2时,B的最简单气态氢化物的电子式为
(4)E元素原子的外围电子排布式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】X、Y、Z、W、Q、R六种短周期主族元素,原子序数依次增大。X是周期表中半径最小的原子,Z基态原子核外有三个未成对电子,Y、Z、W分别与X形成常见化合物的分子结构依次为正四面体、三角锥形和V形,Q的各级电离能如表,W与R是同族元素。回答下列有关问题:
(1)W原子的电子排布式为_______ 。
(2)化合物Q2W2的电子式_______ ,化合物XYZ的结构式_______ 。
(3)Y、Z、W分别与X形成常见化合物的稳定性顺序是_______ (用分子式表示)。
(4)RW3分子中的键角_______ ,RW2分子的立体构型是_______ 。
(5)根据等电子原理,指出与Z2互为等电子体的微粒有_______ 、_______ 。(要求写一种分子和一种离子)。
| Q | I1 | I2 | I3 | I4 | I5… |
| 电离能(kJ/mol) | 496 | 4562 | 6912 | 9543 | 13353… |
(2)化合物Q2W2的电子式
(3)Y、Z、W分别与X形成常见化合物的稳定性顺序是
(4)RW3分子中的键角
(5)根据等电子原理,指出与Z2互为等电子体的微粒有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】铜基催化剂(包括铜、氧化物、铜合金、单原子和复合材料)因其效率高、成本低和对生态友好而受到重视。
(1)基态铜原子的核外电子有______ 种不同的空间运动状态;第二周期元素中,第一电离能比 大的有
大的有______ 种。
(2)研究发现,以掺有镁的铜纳米合金电还原催化 制
制 有较高的选择性,与氮气相比,
有较高的选择性,与氮气相比, 的键能较低
的键能较低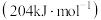 使其成为
使其成为 合成的理想来源。
合成的理想来源。
① 的中心原子的杂化类型为
的中心原子的杂化类型为______ 。
②将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质。
______ (填“属于”或“不属于”)顺磁性物质, 中
中 键角
键角______ (填“>”或“<”) 中
中 键角。
键角。
(3)铜基单原子催化剂能将 转化为
转化为 。
。
① 分子中含有
分子中含有______ 个 键。
键。
②沸点:
______  (填“>”或“<”)。
(填“>”或“<”)。
(4)一种镁铜合金的晶胞结构如图所示,晶胞参数为 ,该晶胞可看成由8个小立方体构成,其中4个小立方体的体心填入
,该晶胞可看成由8个小立方体构成,其中4个小立方体的体心填入 ,另外4个小立方体的体心填入以四面体方式排列的
,另外4个小立方体的体心填入以四面体方式排列的 ,其余
,其余 占据晶胞的顶点和面心。
占据晶胞的顶点和面心。 与
与 的最短距离为
的最短距离为______  (用含
(用含 的代数式表示);若阿伏加德罗常数的值为
的代数式表示);若阿伏加德罗常数的值为 ,该合金晶体的密度为
,该合金晶体的密度为______  (列出含
(列出含 ,
, 的计算式)。
的计算式)。
(1)基态铜原子的核外电子有
 大的有
大的有(2)研究发现,以掺有镁的铜纳米合金电还原催化
 制
制 有较高的选择性,与氮气相比,
有较高的选择性,与氮气相比, 的键能较低
的键能较低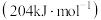 使其成为
使其成为 合成的理想来源。
合成的理想来源。①
 的中心原子的杂化类型为
的中心原子的杂化类型为②将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质。

 中
中 键角
键角 中
中 键角。
键角。(3)铜基单原子催化剂能将
 转化为
转化为 。
。①
 分子中含有
分子中含有 键。
键。②沸点:

 (填“>”或“<”)。
(填“>”或“<”)。(4)一种镁铜合金的晶胞结构如图所示,晶胞参数为
 ,该晶胞可看成由8个小立方体构成,其中4个小立方体的体心填入
,该晶胞可看成由8个小立方体构成,其中4个小立方体的体心填入 ,另外4个小立方体的体心填入以四面体方式排列的
,另外4个小立方体的体心填入以四面体方式排列的 ,其余
,其余 占据晶胞的顶点和面心。
占据晶胞的顶点和面心。
 与
与 的最短距离为
的最短距离为 (用含
(用含 的代数式表示);若阿伏加德罗常数的值为
的代数式表示);若阿伏加德罗常数的值为 ,该合金晶体的密度为
,该合金晶体的密度为 (列出含
(列出含 ,
, 的计算式)。
的计算式)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】一桥连三地,天堑变通途。举世瞩目的港珠澳大桥于2018年10月23日正式通车,体现了我国工程建设自主创新能力实现大跨越,尤其在新材料研究方面有重大突破,回答下列问题:
(1)钛是一种新兴的结构材料,比钢轻、比铝硬。
①基态钛原子的价电子排布式为______ ,与钛同周期的元素中,基态原子的未成对电子数与钛相同的有_____ 种
②钛的硬度比铝大的原因是_______________________________ 。
③工业上制金属钛采用金属还原四氧化钛。先将TiO2和足量炭粉混合加热至1000~1100K进行氯化处理,生成TiCl4。该反应的化学反应方程式为_______________________ 。
(2)跨海桥梁的主要结构材料为钢铁。铁能与三氮唑(Bipy,结构见图)形成多种配合物。

①1mol Bipy中所含 键
键_____ mol;碳原子杂化方式是___________________ 。
②Bipy的沸点为260℃、结构相似且相对分子质量接近的环戊二烯(结构见上图)的沸点为42.5℃.前者较大的原因是______________________________ 。
(3)碳化钨是耐高温耐磨材料。下图为化晶体的部分结构,碳原子嵌入金属的晶格间隙,并不破坏原有金属的晶格,形成填隙+固溶体、也称为填隙化合物。

①在该结构中,每个钨原子周围距离钨原子最近的碳原子有____ 个。
②假设该部分晶体的体积为d/cm3,碳化的摩尔质量为Mg/mol,密度为dg/cm3,则阿伏伽德罗常数NA用上述数据表示为______ 。
(1)钛是一种新兴的结构材料,比钢轻、比铝硬。
①基态钛原子的价电子排布式为
②钛的硬度比铝大的原因是
③工业上制金属钛采用金属还原四氧化钛。先将TiO2和足量炭粉混合加热至1000~1100K进行氯化处理,生成TiCl4。该反应的化学反应方程式为
(2)跨海桥梁的主要结构材料为钢铁。铁能与三氮唑(Bipy,结构见图)形成多种配合物。

①1mol Bipy中所含
 键
键②Bipy的沸点为260℃、结构相似且相对分子质量接近的环戊二烯(结构见上图)的沸点为42.5℃.前者较大的原因是
(3)碳化钨是耐高温耐磨材料。下图为化晶体的部分结构,碳原子嵌入金属的晶格间隙,并不破坏原有金属的晶格,形成填隙+固溶体、也称为填隙化合物。

①在该结构中,每个钨原子周围距离钨原子最近的碳原子有
②假设该部分晶体的体积为d/cm3,碳化的摩尔质量为Mg/mol,密度为dg/cm3,则阿伏伽德罗常数NA用上述数据表示为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】I、钢铁中加入少量镍铬等元素可制成不锈钢,东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是______________________ 。
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为_________ ,提供孤电子对的成键原子是________ 。
(2)铁元素有变价,试根据原子核外电子排布所遵循的原理解释Fe2+具有较强的还原性,易被氧化为Fe3+的原因______________________________ 。
(3)普鲁士蓝(Prussian Blue),即亚铁氰化铁,化学式Fe4[Fe(CN)6]3是一种配合物,其中含有的化学键有____________________ ;
a.共价键 b.离子键 c.配位键 d.金属键 e.氢键
II、钢铁分析中常用过硫酸盐氧化法测定钢中锰的含量,反应原理为2Mn2++5S2O82−+8H2O=2MnO4−+10SO42−+16H+
(4)写出基态锰原子的价电子排布的轨道表示式:________________ 。
(5)已知H2S2O8的结构如图:

①H2S2O8硫原子的轨道杂化方式为________________ 。
②上述反应每生成2 mol MnO4−,S2O82−断裂的共价键数目为_________ 。
③上述反应中被还原的元素为________________ 。
(1)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为
(2)铁元素有变价,试根据原子核外电子排布所遵循的原理解释Fe2+具有较强的还原性,易被氧化为Fe3+的原因
(3)普鲁士蓝(Prussian Blue),即亚铁氰化铁,化学式Fe4[Fe(CN)6]3是一种配合物,其中含有的化学键有
a.共价键 b.离子键 c.配位键 d.金属键 e.氢键
II、钢铁分析中常用过硫酸盐氧化法测定钢中锰的含量,反应原理为2Mn2++5S2O82−+8H2O=2MnO4−+10SO42−+16H+
(4)写出基态锰原子的价电子排布的轨道表示式:
(5)已知H2S2O8的结构如图:

①H2S2O8硫原子的轨道杂化方式为
②上述反应每生成2 mol MnO4−,S2O82−断裂的共价键数目为
③上述反应中被还原的元素为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】工业上用某矿渣(含有Cu2O、Al2O3、Fe2O3、SiO2)提取铜的操作流程如图(金属单质E可由滤液C制取):
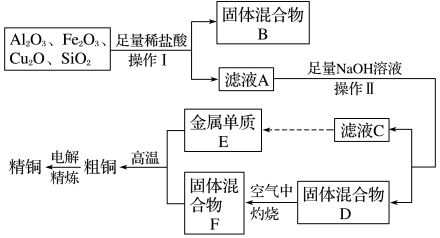
已知:Cu2O+2H+=Cu+Cu2++H2O
(1)固体混合物B的成分是_____ 。它与NaOH溶液反应的离子方程式为_____ 。
(2)滤液A中铁元素的存在形式为_____ (填离子符号),生成该离子与Fe元素有关的离子反应方程式为_____ 。要检验该铁元素的离子的实验_____
(3)在滤液C中通入足量CO2的离子方程式为_____
(4)金属单质E从固体混合物F中置换出Cu的化学方程式为_____

已知:Cu2O+2H+=Cu+Cu2++H2O
(1)固体混合物B的成分是
(2)滤液A中铁元素的存在形式为
(3)在滤液C中通入足量CO2的离子方程式为
(4)金属单质E从固体混合物F中置换出Cu的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】聚合氯化铝是一种新型、高效絮凝剂和净水剂,其单体是液态的碱式氯化铝[Al2(OH)nCl6-n]。
本实验采用铝盐溶液水解絮凝法制备碱式氯化铝。其制备原料为分布广、价格廉的高岭土,化学组成为:Al2O3(25%~34%)、SiO2(40%~50%)、Fe2O3(0.5%~3.0%)以及少量杂质和水分。已知氧化铝有多种不同的结构,化学性质也有差异,且一定条件下可相互转化;高岭土中的氧化铝难溶于酸。制备碱式氯化铝的实验流程如下:
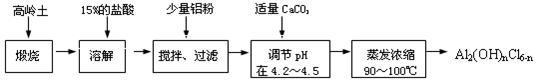
回答下列问题:
(1)“煅烧”的目的是_________________________________________ 。
(2)“溶解”过程中发生反应的离子方程式为_________________________________________________________________________________________
(3)加少量铝粉的主要作用是________________________________ 。
(4)“调节pH在4.2~4.5”的过程中,除添加必要的试剂,还需借助的实验用品是________________ ;“蒸发浓缩”需保持温度在90~100℃,控制温度的实验方法是________________________ 。
本实验采用铝盐溶液水解絮凝法制备碱式氯化铝。其制备原料为分布广、价格廉的高岭土,化学组成为:Al2O3(25%~34%)、SiO2(40%~50%)、Fe2O3(0.5%~3.0%)以及少量杂质和水分。已知氧化铝有多种不同的结构,化学性质也有差异,且一定条件下可相互转化;高岭土中的氧化铝难溶于酸。制备碱式氯化铝的实验流程如下:

回答下列问题:
(1)“煅烧”的目的是
(2)“溶解”过程中发生反应的离子方程式为
(3)加少量铝粉的主要作用是
(4)“调节pH在4.2~4.5”的过程中,除添加必要的试剂,还需借助的实验用品是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中Cr(Ⅲ)的处理工艺流程如下:
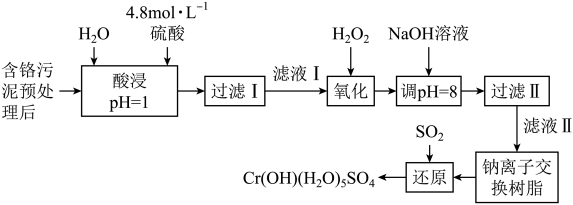
其中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
(1)实验室用18.4mol·L-1的浓硫酸配制480mL4.6mol·L-1的硫酸,需量取浓硫酸___________ mL;配制时所用玻璃仪器除量筒、烧杯和玻璃棒外,还需___________ 。
(2)酸浸时,为了提高浸取率可采取的措施有___________ 。(答出两点)
(3)H2O2的作用是将滤液Ⅰ中的Cr3+转化为 ,写出此反应的离子方程式
,写出此反应的离子方程式___________ 。
(4)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
加入NaOH溶液使溶液呈碱性,既可以除去某些杂质离子,同时使 转化为
转化为 ,但溶液的pH不能超过8,其理由是(用离子方程式表示)
,但溶液的pH不能超过8,其理由是(用离子方程式表示)___________ 。
(5)钠离子交换树脂的反应原理为Mn++nNaR→MRn+nNa+,利用钠离子交换树脂除去滤液Ⅱ中的金属阳离子是___________ 。
(6)写出上述流程中用SO2进行还原时发生反应的化学方程式:___________ 。

其中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
(1)实验室用18.4mol·L-1的浓硫酸配制480mL4.6mol·L-1的硫酸,需量取浓硫酸
(2)酸浸时,为了提高浸取率可采取的措施有
(3)H2O2的作用是将滤液Ⅰ中的Cr3+转化为
 ,写出此反应的离子方程式
,写出此反应的离子方程式(4)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
| 阳离子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
| 开始沉淀时的pH | 2.7 | — | — | — |
| 沉淀完全时的pH | 3.7 | 11.1 | 5.4(>8溶解) | 9(>9溶解) |
加入NaOH溶液使溶液呈碱性,既可以除去某些杂质离子,同时使
 转化为
转化为 ,但溶液的pH不能超过8,其理由是(用离子方程式表示)
,但溶液的pH不能超过8,其理由是(用离子方程式表示)(5)钠离子交换树脂的反应原理为Mn++nNaR→MRn+nNa+,利用钠离子交换树脂除去滤液Ⅱ中的金属阳离子是
(6)写出上述流程中用SO2进行还原时发生反应的化学方程式:
您最近一年使用:0次



