下列对生活、生产中的事实解释不正确 的是
选项 | 事实 | 解释 |
A | 铁盐用作净水剂 |  水解生成的 水解生成的 胶体具有吸附、絮凝作用 胶体具有吸附、絮凝作用 |
B | 工业合成氨反应温度控制在700K左右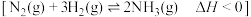 | 700K下, 的平衡转化率最高 的平衡转化率最高 |
C | 铁制锅炉内壁焊上锌片 | 利用牺牲阳极法延长锅炉的使用寿命 |
D | 保暖贴的主要成分是铁粉、水、食盐、活性炭等 | 形成原电池加速铁粉氧化,放出热量 |
| A.A | B.B | C.C | D.D |
更新时间:2024-05-14 08:44:11
|
相似题推荐
单选题
|
适中
(0.65)
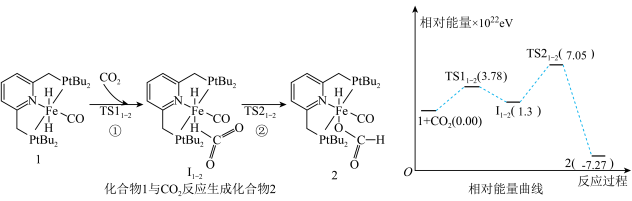
【推荐1】我国科学院化学研究所报道了化合物1催化 氢化机理。由化合物1(固体)→化合物2(固体)过程的机理和相对能量曲线如下图所示(已知
氢化机理。由化合物1(固体)→化合物2(固体)过程的机理和相对能量曲线如下图所示(已知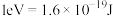 )。下列说法
)。下列说法错误 的是
 氢化机理。由化合物1(固体)→化合物2(固体)过程的机理和相对能量曲线如下图所示(已知
氢化机理。由化合物1(固体)→化合物2(固体)过程的机理和相对能量曲线如下图所示(已知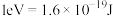 )。下列说法
)。下列说法
A.化合物1→化合物2的过程中包含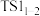 、 、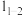 、 、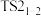 三个基元反应 三个基元反应 |
B.降低温度有利于提高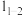 的平衡转化率 的平衡转化率 |
C.图中化合物1和 的总能量大于化合物2的总能量 的总能量大于化合物2的总能量 |
D.过程①的热化学方程式为: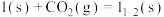 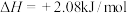 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列方案设计、现象和结论都正确的是
| 实验 | 目的 | 方案设计 | 现象和结论 |
| A | 比较H2SO3与H2CO3,的酸性强弱 | 向等体积的水中分别通入SO2、CO2至饱和,再测两溶液的pH | 通SO2后所得溶液的pH小,则H2SO3的酸性比H2CO3强 |
| B | 探究压强对化学平衡的影响 | 快速压缩装有NO2、N2O4平衡混合气体的针筒活塞 | 气体颜色变深,则增大压强,平衡向生成NO2的方向移动 |
| C | 比较Ksp(AgCl)与Ksp(AgBr)的大小 | 向AgNO3溶液中先加入少量NaCl溶液,再加入NaBr溶液 | 先生成白色沉淀,再生成淡黄色沉淀,则Ksp(AgCl)>Ksp(AgBr) |
| D | 验证Na2CO3溶液 中存在水解平衡 | 往2mL含有酚酞的Na2CO3溶液中,加入少量CaCl2晶体 | 溶液红色变浅,则Na2CO3溶液中存在水解平衡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】二氧化碳催化加氢可合成乙烯:
 。当原料初始组成
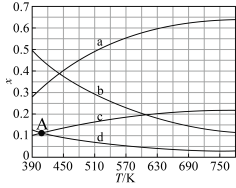
。当原料初始组成 ,体系压强为0.1MPa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。下列说法正确的是
,体系压强为0.1MPa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。下列说法正确的是

 。当原料初始组成
。当原料初始组成 ,体系压强为0.1MPa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。下列说法正确的是
,体系压强为0.1MPa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。下列说法正确的是
A.该反应 |
B.若A点对应温度为420K,此时 的转化率为66.7% 的转化率为66.7% |
C.表示 、 、 变化的曲线分别为b、c 变化的曲线分别为b、c |
| D.选择合适的催化剂可提高反应速率和乙烯的平衡产率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】现有下列实验探究摩尔盐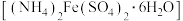 的化学性质。
的化学性质。
下列离子方程式不能准确解释相应实验现象的是
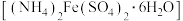 的化学性质。
的化学性质。| 装置 | 实验 | 试剂a | 现象 |
 | ① | 紫色石蕊溶液 | 溶液变红色 |
| ② |  溶液 溶液 | 产生白色沉淀 | |
| ③ | 稀硝酸溶液 | 溶液变黄色 | |
| ④ | 浓 溶液 溶液 | 产生具有刺激性气味的气体 |
A.①中溶液变红: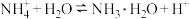 、 、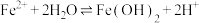 |
B.②中产生白色沉淀: |
C.③中溶液变黄: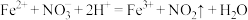 |
D.④中产生有刺激性气体: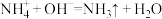 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在给定条件下,下列选项所示的物质间转化能实现的是
A.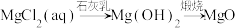 |
B.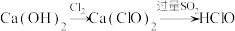 |
C.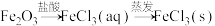 |
D.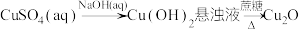 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列有关物质性质的应用错误的是
| A.明矾水解生成Al(OH)3胶体,用作净水剂 |
| B.SO2具有漂白性,常用来漂白纸浆 |
| C.碳酸钠溶液显碱性,可用热的纯碱溶液除去金属器件表面油污 |
| D.氮气化学性质通常不活泼,可将炽热的镁粉可放在氮气中冷却 |
您最近一年使用:0次
【推荐1】下列叙述中,正确的个数为
①电解池是将化学能转变为电能的装置;
②金属导电和电解质溶液导电均为物理变化;
③通过电解原理只能实现不能自发进行的氧化还原反应;
④电镀过程相当于金属的“迁移”,可视为物理变化;
⑤纯银质物品久置表面变暗,是由于发生了电化学腐蚀;
⑥为了防止钢铁锈蚀,在排放海水的钢铁阀门上用导线连接一块石墨一同浸入海水中;
⑦一般来说,带有盐桥的原电池比不带盐桥的原电池效率高。
①电解池是将化学能转变为电能的装置;
②金属导电和电解质溶液导电均为物理变化;
③通过电解原理只能实现不能自发进行的氧化还原反应;
④电镀过程相当于金属的“迁移”,可视为物理变化;
⑤纯银质物品久置表面变暗,是由于发生了电化学腐蚀;
⑥为了防止钢铁锈蚀,在排放海水的钢铁阀门上用导线连接一块石墨一同浸入海水中;
⑦一般来说,带有盐桥的原电池比不带盐桥的原电池效率高。
| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】如图所示的方案可以降低铁闸门的腐蚀速率。下列判断正确的是( )


| A.若X为导线,Y可以是锌 |
| B.若X为导线,铁闸门上的电极反应式为Fe-2e-=Fe2+ |
| C.若X为直流电源,铁闸门做负极 |
| D.若X为直流电源,Y极上发生还原反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】化学电源在日常生活和高科技领域中都有广泛应用。下列说法不正确的是( )


| A.甲:正极的电极反应式为Ag2O+2e−+H2O=2Ag+2OH− |
| B.乙:Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加 |
| C.丙:锌筒作负极,发生氧化反应,锌筒会变薄 |
D.丁:充电时,阳极的电极反应式为PbSO4+2H2O-2e-=PbO2+4H++SO |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】最早使用的化学电池是锌锰电池,即大家熟悉的干电池,其结构如图所示。
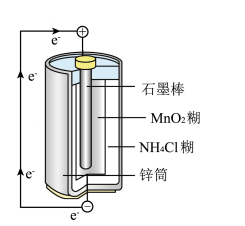
尽管这种电池的历史悠久,但对于它的化学过程人们尚未完全了解。一般认为,放电时,电池中的反应如下:
E极:2MnO2+2e-+2NH4+===Mn2O3+H2O+2NH3↑
F极:Zn-2e-===Zn2+
总反应式:2MnO2+Zn+2NH4+===Mn2O3+Zn2++2NH3↑+H2O
下列说法正确的是

尽管这种电池的历史悠久,但对于它的化学过程人们尚未完全了解。一般认为,放电时,电池中的反应如下:
E极:2MnO2+2e-+2NH4+===Mn2O3+H2O+2NH3↑
F极:Zn-2e-===Zn2+
总反应式:2MnO2+Zn+2NH4+===Mn2O3+Zn2++2NH3↑+H2O
下列说法正确的是
| A.E极是电池的正极,发生的是氧化反应 |
| B.F极是电池的负极,发生的是氧化反应 |
| C.从结构上分析,锌锰电池应属于可充电电池 |
| D.锌锰电池内部发生的氧化还原反应是可逆的 |
您最近一年使用:0次

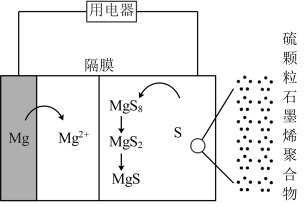
 电极流出
电极流出


