过渡性金属元素在工业生产中有很重要的作用,如金属钼用于制火箭、卫星的合金构件,钼酸钠晶体(Na2MoO4·2H2O)是一种重要的金属缓蚀剂。某工厂利用钼精矿(主要成分MoS2,还含少量钙、镁等元素)为原料冶炼金属钼和钼酸钠晶体(Na2MoO4·2H2O)的主要流程图如下:_______ ,已知Rb(铷)质子数为37,在第五周期ⅠA,Mo的质子数为42,那么Mo在周期表中的位置为第五周期_______ 族。
(2)用浓氨水溶解粗产品的离子方程式是_______ ,由图中信息可以判断MoO3是_______ 氧化物。(填“酸性”、“碱性”或“两性”)
(3)操作Ⅰ是_______ ,操作Ⅱ所得的钼酸要水洗,检验钼酸是否洗涤干净的方法是_______ 。
(4)采用NaClO氧化钼矿的方法将矿石中的钼浸出,该过程放热。①请配平以下化学反应:_______ 。
_______NaClO+_______MoS2+_______NaOH→_______Na2MoO4+_______Na2SO4+_______NaCl+_______H2O
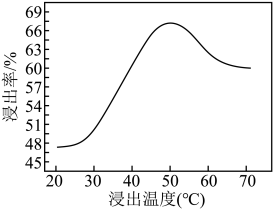
②钼的浸出率随着温度变化如图,当温度高于50℃后浸出率降低的可能原因是_______ (写一点)。 Lix(MoS2)n,则电池工作时正极上的电极反应式为
Lix(MoS2)n,则电池工作时正极上的电极反应式为_______ 。
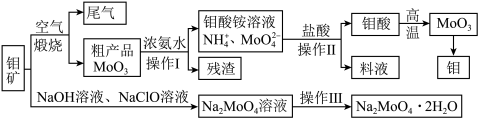
(2)用浓氨水溶解粗产品的离子方程式是
(3)操作Ⅰ是
(4)采用NaClO氧化钼矿的方法将矿石中的钼浸出,该过程放热。①请配平以下化学反应:
_______NaClO+_______MoS2+_______NaOH→_______Na2MoO4+_______Na2SO4+_______NaCl+_______H2O
②钼的浸出率随着温度变化如图,当温度高于50℃后浸出率降低的可能原因是
 Lix(MoS2)n,则电池工作时正极上的电极反应式为
Lix(MoS2)n,则电池工作时正极上的电极反应式为
更新时间:2024-05-18 11:53:43
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
名校
【推荐1】化合物A(200g•mol-1<M<300g•mol-1)由3种常见元素组成,某兴趣小组进行了如图实验:
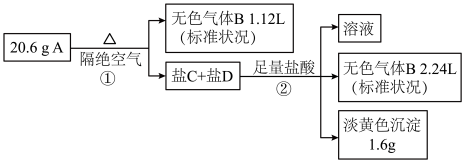
已知:A的焰色为紫色;气体B能使品红溶液褪色;盐C和盐D的组成元素和A相同,且C、D的物质的量之比为1:1。
请回答:
(1)组成A的元素有______ 。
(2)A的化学式为_______ 。
(3)A隔绝空气加热发生反应的化学方程式是_______ 。
(4)化合物A具有强还原性,在潮湿空气中可能转化为由两种酸式盐组成的混合物,反应的化学方程式是______ 。

已知:A的焰色为紫色;气体B能使品红溶液褪色;盐C和盐D的组成元素和A相同,且C、D的物质的量之比为1:1。
请回答:
(1)组成A的元素有
(2)A的化学式为
(3)A隔绝空气加热发生反应的化学方程式是
(4)化合物A具有强还原性,在潮湿空气中可能转化为由两种酸式盐组成的混合物,反应的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】 为紫色固体,易溶于水,微溶于
为紫色固体,易溶于水,微溶于 溶液,不溶于乙醇;有强氧化性,在0℃~5℃的强碱性溶液中较稳定,在酸性或中性溶液中快速产生
溶液,不溶于乙醇;有强氧化性,在0℃~5℃的强碱性溶液中较稳定,在酸性或中性溶液中快速产生 。
。
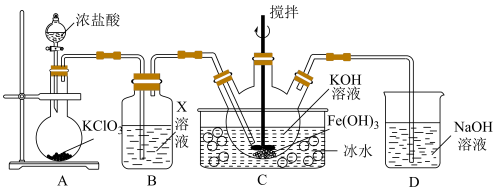
(1)A中发生反应的离子反应方程式是__________ 。
(2)下列试剂中,装置B的X溶液可以选用的是__________(填标号)。
(3)C中得到紫色固体和溶液,生成 的化学方程式是
的化学方程式是__________ ;若要从反应后的装置C中尽可能得到更多的 固体,可以采取的一种措施是
固体,可以采取的一种措施是__________ 。
(4)高铁酸钾与水反应的离子方程式是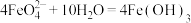 (胶体)
(胶体) ,则其作为水处理剂的原理是
,则其作为水处理剂的原理是__________ 、__________ 。
(5)某同学设计如图装置制备一定量的 ,并使其能在较长时间内存在。
,并使其能在较长时间内存在。
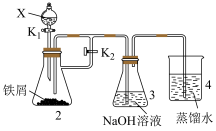
X不能是硝酸,原因是__________ ,装置4的作用是__________ 。
 为紫色固体,易溶于水,微溶于
为紫色固体,易溶于水,微溶于 溶液,不溶于乙醇;有强氧化性,在0℃~5℃的强碱性溶液中较稳定,在酸性或中性溶液中快速产生
溶液,不溶于乙醇;有强氧化性,在0℃~5℃的强碱性溶液中较稳定,在酸性或中性溶液中快速产生 。
。
(1)A中发生反应的离子反应方程式是
(2)下列试剂中,装置B的X溶液可以选用的是__________(填标号)。
| A.饱和食盐水 | B.浓盐酸 | C.饱和氯水 | D. 溶液 溶液 |
(3)C中得到紫色固体和溶液,生成
 的化学方程式是
的化学方程式是 固体,可以采取的一种措施是
固体,可以采取的一种措施是(4)高铁酸钾与水反应的离子方程式是
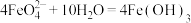 (胶体)
(胶体) ,则其作为水处理剂的原理是
,则其作为水处理剂的原理是(5)某同学设计如图装置制备一定量的
 ,并使其能在较长时间内存在。
,并使其能在较长时间内存在。
X不能是硝酸,原因是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】化合物X含四种元素,某实验小组按如下流程进行相关实验:

已知:①反应I为非氧化还原反应;②溶液D只含1种溶质;③气体F可使品红溶液褪色。请回答下列问题:
(1)X的组成元素为_______ (写元素符号);D中溶质的化学式为_______ 。
(2)金属C与HI溶液反应可生成黄色固体和无色气体,该反应的离子方程式为_______ 。
(3)X与稀硫酸反应也可得到A、E、F、G,且E、F的物质的量之比为1:1.写出对应的化学方程式:_______ 。
(4)将混合气体B通入足量的NaOH溶液中充分反应,试设计实验检验反应产物中的阴离子:_____ 。

已知:①反应I为非氧化还原反应;②溶液D只含1种溶质;③气体F可使品红溶液褪色。请回答下列问题:
(1)X的组成元素为
(2)金属C与HI溶液反应可生成黄色固体和无色气体,该反应的离子方程式为
(3)X与稀硫酸反应也可得到A、E、F、G,且E、F的物质的量之比为1:1.写出对应的化学方程式:
(4)将混合气体B通入足量的NaOH溶液中充分反应,试设计实验检验反应产物中的阴离子:
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】某可逆反应:X(g)+3Y(g)⇌2Z(g)平衡常数与温度关系如下表所示:
(1)根据上述数据判断,该可逆反应的正反应是________ (填“吸热”或“放热”)反应,理由是__________________________ 。
(2)为了增大X的转化率和反应速率,宜采用的措施是____
A.升高温度B.增大压强
C.加催化剂D.离Z
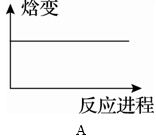
(3)在2 L密闭容器中充入Z气体,在一定条件下进行反应。下列图象不能表明该反应达到平衡状态的是________ 。
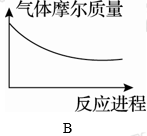


(4)440 ℃时,在2 L密闭容器中,开始充入1 mol X气体和3 mol Y气体进行反应。在某时刻测得c(X)=0.45 mol·L-1,此时,反应是否达到平衡状态________ (填“是”或“否”),简述理由:___________________________________ 。
(5)在某容积固定的容器中进行上述反应,当X、Y起始物质的量一定时,仅改变一个外界条件对Z体积分数的影响如图所示(曲线Ⅰ为标准):
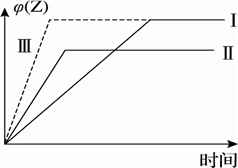
①曲线Ⅱ改变的条件是_______________________________ 。
② 曲线Ⅲ改变的条件是_______________________________ 。
| 温度(℃) | 360 | 440 | 520 |
| K | 0.036 | 0.010 | 0.0038 |
(1)根据上述数据判断,该可逆反应的正反应是
(2)为了增大X的转化率和反应速率,宜采用的措施是
A.升高温度B.增大压强
C.加催化剂D.离Z
(3)在2 L密闭容器中充入Z气体,在一定条件下进行反应。下列图象不能表明该反应达到平衡状态的是




(4)440 ℃时,在2 L密闭容器中,开始充入1 mol X气体和3 mol Y气体进行反应。在某时刻测得c(X)=0.45 mol·L-1,此时,反应是否达到平衡状态
(5)在某容积固定的容器中进行上述反应,当X、Y起始物质的量一定时,仅改变一个外界条件对Z体积分数的影响如图所示(曲线Ⅰ为标准):

①曲线Ⅱ改变的条件是
② 曲线Ⅲ改变的条件是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】研究氮氧化物污染的治理是环保的一项重要工作.合理应用和处理氨氧化物,在生产生活中有重要意义.
(1)已知:①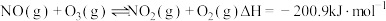 ;
;
② .
.
则由二氧化氮分解生成一氧化氮和氧气的热化学方程式为_______________________ .
(2)利用测压法在恒容刚性反应器中研究反应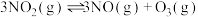 ,充入一定量
,充入一定量 ,T℃时,测得体系的总压强p随反应时间t的变化如表所示:
,T℃时,测得体系的总压强p随反应时间t的变化如表所示:
① 时,反应物的转化率
时,反应物的转化率
_____________ .若降低反应温度,则平衡后体系总压强小于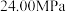 ,主要原因是
,主要原因是________________________ .
②T℃时反应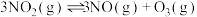 的平衡常数
的平衡常数
______ ( 为以分压表示的平衡常数).
为以分压表示的平衡常数).
(3)一定条件下,在体积为2L的密闭容器中充入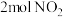 发生反应:
发生反应: 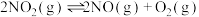 .实验测得
.实验测得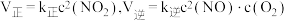 ,
, 是为速率常数,受温度影响.在温度为T℃时
是为速率常数,受温度影响.在温度为T℃时 的转化率随时间变化的情况如图所示.
的转化率随时间变化的情况如图所示.
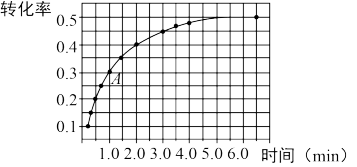
①要提高 的转化率,可采取的措施是
的转化率,可采取的措施是_____________ 、____________ (写两条).
②计算A点处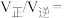
_____________ (保留一位小数).
(1)已知:①
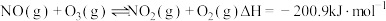 ;
;②
 .
.则由二氧化氮分解生成一氧化氮和氧气的热化学方程式为
(2)利用测压法在恒容刚性反应器中研究反应
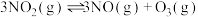 ,充入一定量
,充入一定量 ,T℃时,测得体系的总压强p随反应时间t的变化如表所示:
,T℃时,测得体系的总压强p随反应时间t的变化如表所示:| t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| p/MPa | 20.00 | 21.38 | 22.30 | 23.00 | 23.58 | 24.00 | 24.00 |
 时,反应物的转化率
时,反应物的转化率
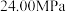 ,主要原因是
,主要原因是②T℃时反应
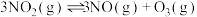 的平衡常数
的平衡常数
 为以分压表示的平衡常数).
为以分压表示的平衡常数).(3)一定条件下,在体积为2L的密闭容器中充入
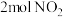 发生反应:
发生反应: 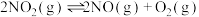 .实验测得
.实验测得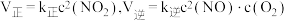 ,
, 是为速率常数,受温度影响.在温度为T℃时
是为速率常数,受温度影响.在温度为T℃时 的转化率随时间变化的情况如图所示.
的转化率随时间变化的情况如图所示.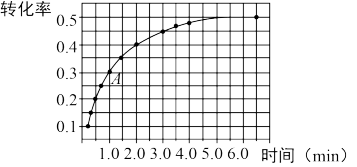
①要提高
 的转化率,可采取的措施是
的转化率,可采取的措施是②计算A点处
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】研发二氧化碳的利用技术,将二氧化碳转化为能源是减轻环境污染和解决能源问题的方案之一、回答下列问题:
(1)利用CO2合成二甲醚有两种工艺。
工艺1:
涉及以下主要反应:
反应Ⅰ.甲醇的合成:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1=-49.0kJ/mol
CH3OH(g)+H2O(g) △H1=-49.0kJ/mol
反应Ⅱ.逆水汽变换:CO2(g)+H2(g) CO(g)+H2O(g) △H2=+41.0kJ/mol
CO(g)+H2O(g) △H2=+41.0kJ/mol
反应Ⅲ.甲醇脱水:2CH3OH(g) CH3OCH3(g)+H2O(g) △H3=-23.5kJ/mol
CH3OCH3(g)+H2O(g) △H3=-23.5kJ/mol
工艺2:反应Ⅳ.2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) △H
CH3OCH3(g)+3H2O(g) △H
①△H=___________ kJ/mol,反应Ⅳ在___________ (填“低温”“高温”或“任意温度”)下自发进行。
②反应Ⅳ的活化能Ea(正)___________ (填“>”“<"或“=”)Ea(逆)。
③在恒温恒容的密闭容器中,下列说法能判断反应Ⅳ达到平衡的是___________ (填标号)。
A.气体物质中碳元素与氧元素的质量比不变
B.容器内CH3OCH3浓度保持不变
C.容器内气体密度不变
D.容器内气体的平均摩尔质量不变
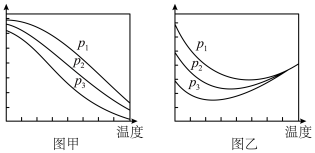
(2)在不同压强下,按照n(CO2):n(H2)=1:3投料合成甲醇(反应Ⅰ),实验测得CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如图甲、乙所示。___________ (填标号)。
A.图甲纵坐标表示CH3OH的平衡产率
B.p1<p2<p3
C.为了同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择低温、高压条件
D.一定温度、压强下,提高CO2的平衡转化率的主要方向是寻找活性更高的催化剂
②图乙中,某温度时,三条曲线几乎交于一点的原因是___________ 。
(3)在T1温度下,将3molCO2和7molH2充入2L的恒容密闭容器中发生反应Ⅰ和Ⅳ,达到平衡状态时CH3OH(g)和CH3OCH3(g)的物质的量分别为1mol和0.5mol。
①反应经过10min达到平衡,0~10min内CO2的平均反应速率v(CO2)=___________ mol/(L·min)。
②T1温度时反应Ⅰ的平衡常数K=___________ 。
(1)利用CO2合成二甲醚有两种工艺。
工艺1:
涉及以下主要反应:
反应Ⅰ.甲醇的合成:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1=-49.0kJ/mol
CH3OH(g)+H2O(g) △H1=-49.0kJ/mol反应Ⅱ.逆水汽变换:CO2(g)+H2(g)
 CO(g)+H2O(g) △H2=+41.0kJ/mol
CO(g)+H2O(g) △H2=+41.0kJ/mol反应Ⅲ.甲醇脱水:2CH3OH(g)
 CH3OCH3(g)+H2O(g) △H3=-23.5kJ/mol
CH3OCH3(g)+H2O(g) △H3=-23.5kJ/mol工艺2:反应Ⅳ.2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g) △H
CH3OCH3(g)+3H2O(g) △H①△H=
②反应Ⅳ的活化能Ea(正)
③在恒温恒容的密闭容器中,下列说法能判断反应Ⅳ达到平衡的是
A.气体物质中碳元素与氧元素的质量比不变
B.容器内CH3OCH3浓度保持不变
C.容器内气体密度不变
D.容器内气体的平均摩尔质量不变
(2)在不同压强下,按照n(CO2):n(H2)=1:3投料合成甲醇(反应Ⅰ),实验测得CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如图甲、乙所示。
A.图甲纵坐标表示CH3OH的平衡产率
B.p1<p2<p3
C.为了同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择低温、高压条件
D.一定温度、压强下,提高CO2的平衡转化率的主要方向是寻找活性更高的催化剂
②图乙中,某温度时,三条曲线几乎交于一点的原因是
(3)在T1温度下,将3molCO2和7molH2充入2L的恒容密闭容器中发生反应Ⅰ和Ⅳ,达到平衡状态时CH3OH(g)和CH3OCH3(g)的物质的量分别为1mol和0.5mol。
①反应经过10min达到平衡,0~10min内CO2的平均反应速率v(CO2)=
②T1温度时反应Ⅰ的平衡常数K=
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
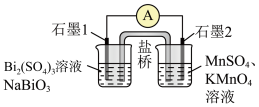
【推荐1】钨在自然界的储量只有620万吨,以钨冶炼渣(主要含 、
、 、
、 、CaO、MgO、Fe的氧化物以及少量重金属氧化物等)为原料,提炼制备电池级硫酸锰的工艺流程如下:
、CaO、MgO、Fe的氧化物以及少量重金属氧化物等)为原料,提炼制备电池级硫酸锰的工艺流程如下: 一般难溶于酸溶液。
一般难溶于酸溶液。
(1)第一步酸浸后所得浸出液中金属阳离子包括 ,写出对应的离子方程式
,写出对应的离子方程式_______ 。
(2)第二步中温度升高可以增大浸取速率,但高于50℃时浸取速率反而会下降,其可能的原因是_______ 。
(3)第四步中加MnS的目的是_______ 。
(4) 溶解度曲线如图。从酸溶后的溶液中提取
溶解度曲线如图。从酸溶后的溶液中提取 晶体的操作为
晶体的操作为_______ 、_______ ,然后可用_______ 洗涤再进行干燥和碾磨制得电池级硫酸锰。_______ 。
 、
、 、
、 、CaO、MgO、Fe的氧化物以及少量重金属氧化物等)为原料,提炼制备电池级硫酸锰的工艺流程如下:
、CaO、MgO、Fe的氧化物以及少量重金属氧化物等)为原料,提炼制备电池级硫酸锰的工艺流程如下:
 一般难溶于酸溶液。
一般难溶于酸溶液。(1)第一步酸浸后所得浸出液中金属阳离子包括
 ,写出对应的离子方程式
,写出对应的离子方程式(2)第二步中温度升高可以增大浸取速率,但高于50℃时浸取速率反而会下降,其可能的原因是
(3)第四步中加MnS的目的是
(4)
 溶解度曲线如图。从酸溶后的溶液中提取
溶解度曲线如图。从酸溶后的溶液中提取 晶体的操作为
晶体的操作为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】某煤矸石经化学成分分析可知,其含有大量的Al、Si、Li元素,还含有少量Fe、Mg等杂质。硝酸浸出铝、铁、锂等工业流程如下。按要求回答下列问题:
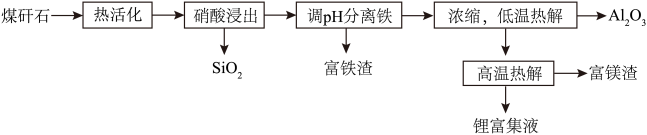
(1)在实验室模拟“硝酸浸出”分离出 的操作,要用到的玻璃仪器有
的操作,要用到的玻璃仪器有___________ 。
(2)富铁渣中的主要成分是___________ (填化学式)。
(3)“低温热解”过程中有红棕色气体放出,则铝盐发生反应的化学方程式为___________ (假设该过程中只有一种含氮化合物生成);此时热解温度不宜过高的原因是___________ 。
(4)“热活化”过程可在氮气( )或空气(Air)气氛中进行,其活化气氛在不同温度下对铝(图1)、铁(图2)浸出的影响,以及铁的活化产物与硝酸反应的
)或空气(Air)气氛中进行,其活化气氛在不同温度下对铝(图1)、铁(图2)浸出的影响,以及铁的活化产物与硝酸反应的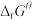 与温度的关系(图3)如下图所示。则“热活化”过程所选用的合适条件是
与温度的关系(图3)如下图所示。则“热活化”过程所选用的合适条件是___________ (填字母)。
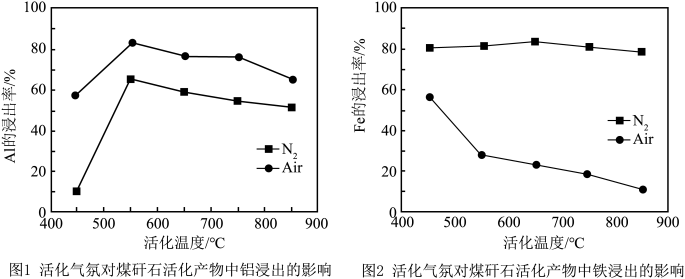

A.氮气气氛、650℃ B.空气气氛、650℃
C.氮气气氛、550℃ D.空气气氛、550℃
空气气氛中温度越高,铁的浸出率越小的原因可能是___________ 。
(5)该流程获得的锂富集液可广泛应用于电池行业。某锂离子电池电解液由六氟磷酸锂( )和碳酸酯类有机溶剂组成,充电过程中,石墨(
)和碳酸酯类有机溶剂组成,充电过程中,石墨(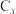 )电极发生阴离子插层反应得
)电极发生阴离子插层反应得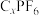 。则碳酸酯类为
。则碳酸酯类为___________ (填“极性”或“非极性”)溶剂,放电时,正极发生的电极反应方程式为___________ 。

(1)在实验室模拟“硝酸浸出”分离出
 的操作,要用到的玻璃仪器有
的操作,要用到的玻璃仪器有(2)富铁渣中的主要成分是
(3)“低温热解”过程中有红棕色气体放出,则铝盐发生反应的化学方程式为
(4)“热活化”过程可在氮气(
 )或空气(Air)气氛中进行,其活化气氛在不同温度下对铝(图1)、铁(图2)浸出的影响,以及铁的活化产物与硝酸反应的
)或空气(Air)气氛中进行,其活化气氛在不同温度下对铝(图1)、铁(图2)浸出的影响,以及铁的活化产物与硝酸反应的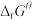 与温度的关系(图3)如下图所示。则“热活化”过程所选用的合适条件是
与温度的关系(图3)如下图所示。则“热活化”过程所选用的合适条件是

A.氮气气氛、650℃ B.空气气氛、650℃
C.氮气气氛、550℃ D.空气气氛、550℃
空气气氛中温度越高,铁的浸出率越小的原因可能是
(5)该流程获得的锂富集液可广泛应用于电池行业。某锂离子电池电解液由六氟磷酸锂(
 )和碳酸酯类有机溶剂组成,充电过程中,石墨(
)和碳酸酯类有机溶剂组成,充电过程中,石墨(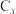 )电极发生阴离子插层反应得
)电极发生阴离子插层反应得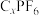 。则碳酸酯类为
。则碳酸酯类为
您最近一年使用:0次
【推荐3】甲醇是一种优质的液体燃料,CO和CO2均可用于合成甲醇。目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H1。
(1)已知:2CO(g)+O2(g)=2CO2(g) △H2
2H2(g)+O2(g)=2H2O(g) △H3
则CO(g)+2H2(g) CH3OH(g) △H=
CH3OH(g) △H=_______ 。
(2)由CO合成甲醇时,CO在不同温度下的平衡转化率与压强的关系如图所示。

该反应ΔH_______ 0(填“>”或“<”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是_______ 。
(3)一定温度下,向2L密闭容器中加入1molCH3OH(g),发生反应:CH3OH(g) CO(g)+2H2(g),H2物质的量随时间的变化如图所示。
CO(g)+2H2(g),H2物质的量随时间的变化如图所示。

0~2min内的平均反应速率v(CH3OH)=_______ 。该温度下,CO(g)+2H2(g) CH3OH(g)的平衡常数K=
CH3OH(g)的平衡常数K=_______ 。相同温度下,若开始加入CH3OH(g)的物质的量是原来的2倍,则_______ 是原来的2倍。
a.平衡常数 b.CH3OH的平衡浓度
c.达到平衡的时间 d.平衡时气体的密度
(4)以CH3OH为燃料(以KOH溶液作电解质溶液)可制成CH3OH燃料电池。
①充入CH3OH的电极为_______ 极。
②负极反应的电极反应式为_______ 。
(1)已知:2CO(g)+O2(g)=2CO2(g) △H2
2H2(g)+O2(g)=2H2O(g) △H3
则CO(g)+2H2(g)
 CH3OH(g) △H=
CH3OH(g) △H=(2)由CO合成甲醇时,CO在不同温度下的平衡转化率与压强的关系如图所示。

该反应ΔH
(3)一定温度下,向2L密闭容器中加入1molCH3OH(g),发生反应:CH3OH(g)
 CO(g)+2H2(g),H2物质的量随时间的变化如图所示。
CO(g)+2H2(g),H2物质的量随时间的变化如图所示。
0~2min内的平均反应速率v(CH3OH)=
 CH3OH(g)的平衡常数K=
CH3OH(g)的平衡常数K=a.平衡常数 b.CH3OH的平衡浓度
c.达到平衡的时间 d.平衡时气体的密度
(4)以CH3OH为燃料(以KOH溶液作电解质溶液)可制成CH3OH燃料电池。
①充入CH3OH的电极为
②负极反应的电极反应式为
您最近一年使用:0次



