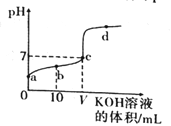
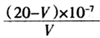用0.1000mol/L的标准盐酸分别滴定20.00mL的0.1000mol/L氨水和20.00mL的0.1000mol/L氢氧化钠溶液的滴定曲线如图所示,横坐标为滴定百分数(滴定用量/总滴定用量),纵坐标为滴定过程中溶液pH,甲基红是一种酸碱指示剂,变色范围为4.4-6.2,下列有关滴定过程说法正确的是


A.滴定氨水溶液当滴定分数为50%时,各离子浓度间存在关系:c( )+c(H+)=c(OH-) )+c(H+)=c(OH-) |
| B.滴定分数为100%时,即为滴定过程中反应恰好完全的时刻 |
| C.从滴定曲线可以判断,使用甲基橙作为滴定过程中的指示剂准确性更佳 |
D.滴定氨水溶液当滴定分数为150%时,所得溶液中离子浓度有大小关系c(Cl-)>c(H+)>c( )>c(OH-) )>c(OH-) |
更新时间:2017-03-15 16:50:23
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】实验室用标准NaOH溶液滴定食用白醋,测定所含醋酸的浓度,下列说法错误的是
| A.将NaOH固体放在烧杯中用托盘天平称量 |
| B.用量筒量取25.00mL NaOH标准溶液置于锥形瓶中 |
| C.滴定时眼睛一直注视锥形瓶中溶液颜色变化 |
| D.用酚酞作指示剂,滴定终点时溶液为浅红色 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】298K时,向体积均为15.0mL,浓度均为1.00mol/L的氨水和NaHCO3溶液中分别滴加1.00mol/L的盐酸,溶液的pH与所加盐酸体积的关系如图所示。下列有关叙述正确的是
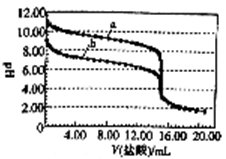
| A.曲线a是NaHCO3溶液的滴定曲线 |
| B.当V(盐酸)=4.00mL时,c(HCO3-)>c(NH4+)>c(CO32-) |
| C.当V(盐酸)=15.00mL时,c(Na+)=c(NH4+) |
| D.两个滴定过程均可选择酚酞作指示剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】 时,氯水中部分含氯的物种的分布分数
时,氯水中部分含氯的物种的分布分数 平衡时某物种的浓度占各物种浓度之和的百分数
平衡时某物种的浓度占各物种浓度之和的百分数 与pH的关系如图所示。下列叙述不正确的是( )
与pH的关系如图所示。下列叙述不正确的是( )

 时,氯水中部分含氯的物种的分布分数
时,氯水中部分含氯的物种的分布分数 平衡时某物种的浓度占各物种浓度之和的百分数
平衡时某物种的浓度占各物种浓度之和的百分数 与pH的关系如图所示。下列叙述不正确的是( )
与pH的关系如图所示。下列叙述不正确的是( )
A.新制氯水中持续通入 ,pH不断变小,溶液颜色不断变浅 ,pH不断变小,溶液颜色不断变浅 |
B.新制的 的氯水中, 的氯水中,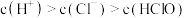 |
C. 时, 时, 的电离常数Ka的对数值为 的电离常数Ka的对数值为 |
D. 的氯水中加入NaOH溶液,主要发生的离子反应方程式为 的氯水中加入NaOH溶液,主要发生的离子反应方程式为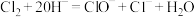 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】电位滴定法是根据滴定过程中指示电极电位的变化来确定滴定终点的一种滴定分析方法。在化学计量点附近,被测离子浓度发生突跃,指示电极电位也产生了突跃,进而确定滴定终点。常温下,利用盐酸滴定某溶液中碳酸钠的含量,其电位滴定曲线与pH曲线如图所示(已知碳酸的电离常数Ka1=10-6.35,Ka2=10-10.34。下列说法正确的是
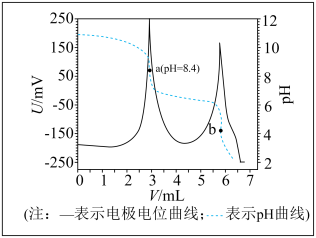

| A.该滴定过程需要两种指示剂 |
B.a点溶液中存在:c(Cl-)+c(H+)=c( )+c(OH-)+c( )+c(OH-)+c( ) ) |
C.a点溶液中c( ):c(H2CO3)=100.11 ):c(H2CO3)=100.11 |
| D.水的电离程度:a点<b点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】常温下,下列有关电解质溶液的说法正确的是
| A.相同浓度的HCOONa和NaF两溶液,前者的pH较大,则Ka(HCOOH)>Ka(HF) |
| B.相同浓度的CH3COOH和CH3COONa两溶液等体积混合后pH约为4.7,则溶液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| C.FeS溶于稀硫酸,而CuS不溶于稀硫酸,则Ksp(FeS)>Ksp(CuS) |
| D.在1mol/LNa2S溶液中,c(S2-)+c(HS-)+c(H2S)=0.5mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】常温下,在20 mL 0.1 mol·L-1 Na2CO3溶液中逐滴加入40 mL 0.1 mol·L-1稀盐酸,溶液中含碳元素各种微粒(CO2因逸出未画出)的物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。下列说法正确的是


| A.曲线a表示H2CO3的变化曲线 |
B.H2CO3、 、 、 可大量共存于同一溶液中 可大量共存于同一溶液中 |
C.pH=11时,c( )>c(Cl-) )>c(Cl-) |
| D.碳酸钠溶液的水解平衡常数为1.0×10-11 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,下列溶液中的微粒浓度关系错误的是
| A.氯水与NaOH溶液混合:c(Cl-)=c(HClO)+c(ClO-) |
| B.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
C.0.2mol·L-1NaHCO3溶液与0.1mol·L-1NaOH溶液等体积混合:c(CO )>c(HCO )>c(HCO )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
| D.物质的量浓度相等的NH3·H2O和NH4Cl溶液等体积混合:c(NH3·H2O)+c(OH-)=c(H+)+c(Cl-) |
您最近一年使用:0次


 )/c(
)/c( );B点>F点
);B点>F点 )>c(OH-)>c(H+)
)>c(OH-)>c(H+)