下列叙述中正确的是
A.若反应2A(S)+B(g) 2C(g)ΔH>0 能自发进行,原因是ΔS<0 2C(g)ΔH>0 能自发进行,原因是ΔS<0 |
| B.催化剂能改变反应的途径,但不能改变反应的ΔH |
| C.S(g)+O2(g)===SO2(g) ΔH1<0; S(s)+O2(g)===SO2(g) ΔH2<0,则ΔH1>ΔH2。 |
D.化学平衡CO(g)+H2O(g)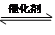 CO2(g)+H2(g),增加H2O的浓度H2O的转化率增大 CO2(g)+H2(g),增加H2O的浓度H2O的转化率增大 |
更新时间:2017-05-17 08:14:15
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列热化学方程式及有关应用的叙述中,不正确的是
| A.在同温同压下,热化学方程式2H2(g)+O2(g)==2H2O(l)ΔH1;2H2(g)+O2(g)==2H2O(g)ΔH2,反应热ΔH1˂ΔH2 |
B.已知强酸与强碱在稀溶液里反应的中和热为57.3kJ•mol-1,则 H2SO4(aq)+ H2SO4(aq)+ Ba(OH)2(aq)═ Ba(OH)2(aq)═ BaSO4(s)+H2O(l)△H˂-57.3kJ•mol-1 BaSO4(s)+H2O(l)△H˂-57.3kJ•mol-1 |
C.500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,则:N2(g)+3H2(g) 2NH3(g)△H˂-38.6kJ•mol-1 2NH3(g)△H˂-38.6kJ•mol-1 |
D.甲烷的燃烧热为890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+ O2(g)═CO(g)+2H2O(l)△H=-890.3kJ•mol-1 O2(g)═CO(g)+2H2O(l)△H=-890.3kJ•mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在同温同压下,下列各组热化学方程式中, 的是
的是
 的是
的是A.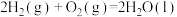  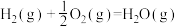  |
B.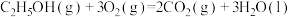  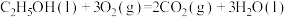  |
C.    |
D.    |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列实验操作不能达到实验目的的是
| A | B | C | D |
| 探究温度对化学平衡的影响 | 探究不同催化剂的催化能力 | 探究浓度对化学平衡的影响 | 验证Ksp(AgI)<Ksp(AgCl) |
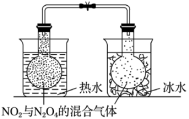 | 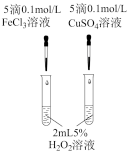 | 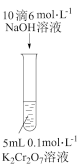 | 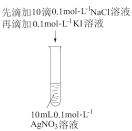 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】“接触法制硫酸”的主要反应是2SO2+O2 2SO3在催化剂表面的反应历程如下:
2SO3在催化剂表面的反应历程如下:
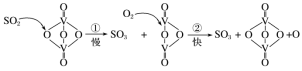
下列说法正确的是
 2SO3在催化剂表面的反应历程如下:
2SO3在催化剂表面的反应历程如下:
下列说法正确的是
| A.过程中既有V—O键的断裂,又有V—O键的形成 |
| B.反应②的活化能比反应①大 |
| C.该反应的催化剂是V2O4 |
| D.使用催化剂只能加快正反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列事实中,不能用勒夏特列原理来解释的是
| A.向新制氯水中加入小苏打固体后漂白性明显增强 |
| B.氢气、碘蒸气、碘化氢气体组成的平衡体系,压缩体积后气体颜色变深 |
| C.合成氨时将氨液化分离,可提高原料的利用率。 |
| D.可乐等碳酸饮料突然打开后泛起大量泡沫 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】氨基甲酸铵( )主要用作磷化铝中间体,也用于医药。在T℃时,将足量的
)主要用作磷化铝中间体,也用于医药。在T℃时,将足量的 固体置于恒温恒容容器中,存在如下化学平衡:
固体置于恒温恒容容器中,存在如下化学平衡: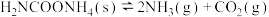 ,经t min达到平衡状态,平衡时体系的总浓度为
,经t min达到平衡状态,平衡时体系的总浓度为 。下列叙述正确的是
。下列叙述正确的是
 )主要用作磷化铝中间体,也用于医药。在T℃时,将足量的
)主要用作磷化铝中间体,也用于医药。在T℃时,将足量的 固体置于恒温恒容容器中,存在如下化学平衡:
固体置于恒温恒容容器中,存在如下化学平衡: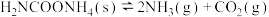 ,经t min达到平衡状态,平衡时体系的总浓度为
,经t min达到平衡状态,平衡时体系的总浓度为 。下列叙述正确的是
。下列叙述正确的是| A.当混合气体的平均摩尔质量不变时,说明反应达到平衡状态 |
B.T℃时,向平衡体系中加入适量 , , 增大 增大 |
C.在0~t min时间段内,平均反应速率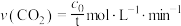 |
D.向平衡体系中充入适量的 ,逆反应速率增大 ,逆反应速率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
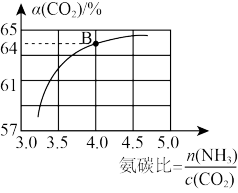
【推荐1】以CO2和NH3为原料,通过反应:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(l)合成尿素。该反应在一定温度和压强下,原料气中NH3和CO2的物质的量之比(氨碳比)与CO2平衡转化率(α)的关系如图所示。下列说法正确的是
CO(NH2)2(s)+H2O(l)合成尿素。该反应在一定温度和压强下,原料气中NH3和CO2的物质的量之比(氨碳比)与CO2平衡转化率(α)的关系如图所示。下列说法正确的是
 CO(NH2)2(s)+H2O(l)合成尿素。该反应在一定温度和压强下,原料气中NH3和CO2的物质的量之比(氨碳比)与CO2平衡转化率(α)的关系如图所示。下列说法正确的是
CO(NH2)2(s)+H2O(l)合成尿素。该反应在一定温度和压强下,原料气中NH3和CO2的物质的量之比(氨碳比)与CO2平衡转化率(α)的关系如图所示。下列说法正确的是
| A.图中B点处NH3的平衡转化率为32% |
B.该反应平衡常数的表达式为 |
| C.若开始投料按照n(NH3):n(CO2)为2∶1投料,平衡后若压缩容器的体积,则再次平衡时c(NH3)比压缩前大 |
| D.氨碳比越高,合成CO(NH2)2(s)时NH3的转化率越高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某温度下,在2L的恒容密闭容器中充入 与
与 的混合气体发生上述反应:
的混合气体发生上述反应: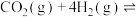
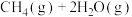 ,
, 与
与 的物质的量随时间的变化如图所示,下列说法正确的是
的物质的量随时间的变化如图所示,下列说法正确的是
 与
与 的混合气体发生上述反应:
的混合气体发生上述反应: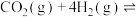
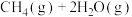 ,
, 与
与 的物质的量随时间的变化如图所示,下列说法正确的是
的物质的量随时间的变化如图所示,下列说法正确的是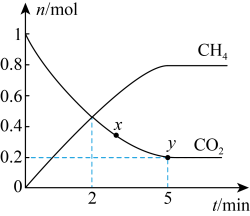
A.0-5min内,用 表示该反应的平均反应速率 表示该反应的平均反应速率 |
| B.2min时,v(正)=v(逆) |
| C.容器中混合气体的平均相对分子质量不再发生改变时,该反应达到平衡 |
D. 的转化率:x点>y点 的转化率:x点>y点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。下列描述错误的是
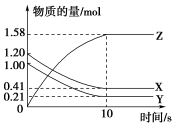

| A.反应开始到10 s,用Z表示的反应速率为0.079 mol·L-1·s-1 |
| B.反应开始到10 s,X的物质的量浓度减少了0.79 mol·L-1 |
| C.反应开始到10 s时,Y的转化率为79.0% |
D.反应的化学方程式为X(g)+Y(g) 2Z(g) 2Z(g) |
您最近一年使用:0次

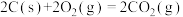
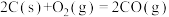


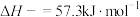 ,若将含1mol
,若将含1mol 的醋酸溶液与含1molNaOH的溶液混合,放出的热量小于57.3kJ
的醋酸溶液与含1molNaOH的溶液混合,放出的热量小于57.3kJ 完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为
完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为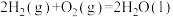
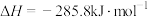

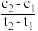
 溶液中存在水解平衡:
溶液中存在水解平衡: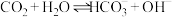 .下列说法正确的是
.下列说法正确的是 ,溶液
,溶液 增大
增大 固体,平衡向逆反应方向移动
固体,平衡向逆反应方向移动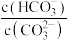 不变
不变

