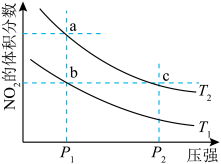
向甲、乙、丙三个恒容密闭容器中分别充入一定量的A和B,发生反应:A(g)+xB(g) 2C(g)。
2C(g)。
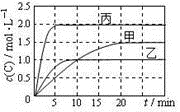
相关数据如下表,反应过程中C的浓度随时间变化关系如下图。下列说法正确的是
 2C(g)。
2C(g)。相关数据如下表,反应过程中C的浓度随时间变化关系如下图。下列说法正确的是
| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5L | 0.5L | 1.0L |
| 温度/℃ | T1 | T2 | T2 |
| 反应物 起始量 | 1.5molA 0.5molB | 1.5molA 0.5molB | 6molA 2molB |

| A.T1>T2,x=1 |
| B.T2℃时,该反应的平衡常数为0.8 |
| C.A的平衡转化率a(甲):a(乙)=2:3 |
| D.15~20min内C的平均反应速率v(乙)<v(丙) |
更新时间:2017-05-20 15:49:44
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验能达到预期目的是
| 选项 | 实验内容 | 实验目的 |
| A | 将 的 的 溶液和 溶液和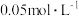 的 的 溶液等体积混合,充分反应后,取少许混合液滴加 溶液等体积混合,充分反应后,取少许混合液滴加 溶液 溶液 | 验证 与 与 的反应有一定限度 的反应有一定限度 |
| B | 相同温度下,分别向两支试管中加入 浓度均为 浓度均为 的草酸溶液,再分别加入 的草酸溶液,再分别加入 和 和 酸性高锰酸钾溶液,酸性高锰酸钾溶液褪色时间不同 酸性高锰酸钾溶液,酸性高锰酸钾溶液褪色时间不同 | 比较反应物浓度对反应速率的影响 |
| C | 相同条件下,向一支试管中加入 和 和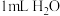 ,向另一支试管中加入 ,向另一支试管中加入 和 和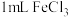 溶液,观察并比较实验现象 溶液,观察并比较实验现象 | 探究 对 对 分解速率的影响 分解速率的影响 |
| D | 向2支盛有 不同浓度 不同浓度 溶液的试管中,同时加入 溶液的试管中,同时加入 溶液,观察并比较实验现象 溶液,观察并比较实验现象 | 探究浓度对反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法正确的是
| A.食醋总酸含量测定时若没有控制好滴定终点,溶液显深红色,则必须重做实验 |
| B.配制一定物质的量浓度的稀硫酸时,用移液管量取浓硫酸可以提高实验精度 |
| C.探究温度对硫代硫酸钠与酸反应速率的影响时,应先将两种溶液混合后,再用水浴加热至设定温度 |
| D.在两支试管中分别加1mL无水乙醇和1.5g苯酚固体,再加等量等体积的钠,比较乙醇、苯酚羟基上氢原子的活泼性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】一定温度下,在密闭容器中发生反应:N2O4(g)⇌2NO2(g) ΔH>0,反应达到平衡时,下列说法不正确的是
| A.若缩小容器的体积,则容器中气体的颜色先变深后又变浅,且比原平衡颜色深 |
| B.若压强不变,向容器中再加入一定量的N2O4,再次达到平衡时各种物质的百分含量不变 |
| C.若体积不变,向容器中再加入一定量的N2O4,相对于原平衡,平衡向正反应方向移动,再次平衡时N2O4的转化率将升高 |
| D.若体积不变,升高温度,再次平衡时体系颜色加深 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】反应NH4HS(s) NH3(g)+H2S(g)在某温度下达到平衡,下列各种情况下,不会使平衡发生移动的是
NH3(g)+H2S(g)在某温度下达到平衡,下列各种情况下,不会使平衡发生移动的是
 NH3(g)+H2S(g)在某温度下达到平衡,下列各种情况下,不会使平衡发生移动的是
NH3(g)+H2S(g)在某温度下达到平衡,下列各种情况下,不会使平衡发生移动的是| A.温度、容积不变时,通入SO2气体 |
| B.将NH4HS固体全部移走 |
| C.保持温度和容器体积不变,充入氮气 |
| D.保持温度和压强不变,充入氮气 |
您最近一年使用:0次
【推荐1】一定温度下,在一个容积为1L的密闭容器中,充入1molH2(g)和1mol I2(g),发生反应H2(g)+I2(g) 2HI(g),经充分反应达到平衡后,生成的HI(g)占气体体积的50%,该温度下,在另一个容积为2L的密闭容器中充入1molHI(g)发生反应HI(g)
2HI(g),经充分反应达到平衡后,生成的HI(g)占气体体积的50%,该温度下,在另一个容积为2L的密闭容器中充入1molHI(g)发生反应HI(g)
 H2(g)+
H2(g)+ I2(g),则下列判断正确的是( )
I2(g),则下列判断正确的是( )
 2HI(g),经充分反应达到平衡后,生成的HI(g)占气体体积的50%,该温度下,在另一个容积为2L的密闭容器中充入1molHI(g)发生反应HI(g)
2HI(g),经充分反应达到平衡后,生成的HI(g)占气体体积的50%,该温度下,在另一个容积为2L的密闭容器中充入1molHI(g)发生反应HI(g)
 H2(g)+
H2(g)+ I2(g),则下列判断正确的是( )
I2(g),则下列判断正确的是( )| A.后一反应的平衡常数为1 |
| B.后一反应的平衡常数为0.5 |
| C.后一反应达到平衡时,H2的平衡浓度为0.25 mol·L-1 |
| D.后一反应达到平衡时,HI(g)的平衡浓度0.5 mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】Al3+与F-具有很强的亲和性,当F-的浓度过大时,还会形成AlF 。AlF3在一定溶剂中存在分步电离,常温下向某浓度的AlF3溶液中加入NaF,实验测定Al3+、AlF2+、AlF
。AlF3在一定溶剂中存在分步电离,常温下向某浓度的AlF3溶液中加入NaF,实验测定Al3+、AlF2+、AlF 、AlF3在所有含铝元素微粒中的百分含量随pF[
、AlF3在所有含铝元素微粒中的百分含量随pF[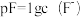 ]的变化如图所示,下列说法错误的是
]的变化如图所示,下列说法错误的是
 。AlF3在一定溶剂中存在分步电离,常温下向某浓度的AlF3溶液中加入NaF,实验测定Al3+、AlF2+、AlF
。AlF3在一定溶剂中存在分步电离,常温下向某浓度的AlF3溶液中加入NaF,实验测定Al3+、AlF2+、AlF 、AlF3在所有含铝元素微粒中的百分含量随pF[
、AlF3在所有含铝元素微粒中的百分含量随pF[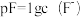 ]的变化如图所示,下列说法错误的是
]的变化如图所示,下列说法错误的是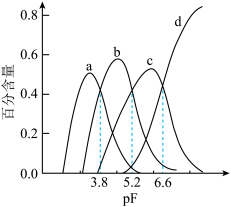
A.曲线b表示AlF |
B.pF=4时, |
C.Pf= 6.6时, 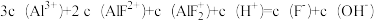 |
D.常温下, 的化学平衡常数为1015.6 的化学平衡常数为1015.6 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】某温度下,在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g)发生反应H2(g) + CO2(g)  H2O(g) + CO(g),其起始浓度如表所示,已知平衡时甲中H2的转化率为60%。下列判断正确的是
H2O(g) + CO(g),其起始浓度如表所示,已知平衡时甲中H2的转化率为60%。下列判断正确的是
 H2O(g) + CO(g),其起始浓度如表所示,已知平衡时甲中H2的转化率为60%。下列判断正确的是
H2O(g) + CO(g),其起始浓度如表所示,已知平衡时甲中H2的转化率为60%。下列判断正确的是 | 起始浓度 | 甲 | 乙 | 丙 |
| c(H2)[mol/L] | 0.010 | 0.020 | 0.020 |
| c(CO2)[mol/L] | 0.010 | 0.010 | 0.020 |
| A.刚开始反应时,乙中的反应速率最快,甲中的反应速率最慢 |
| B.平衡时,乙中H2的转化率大于60% |
| C.平衡时,丙中c(CO) = 0.008 mol/L |
| D.该温度下,平衡常数K=9/4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】乙醇催化合成乙酸乙酯的新方法为: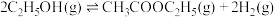 。在2L密闭容器中充入
。在2L密闭容器中充入
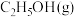 发生反应,乙醇的转化率
发生反应,乙醇的转化率 变化如图所示。下列分析正确的是
变化如图所示。下列分析正确的是
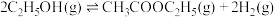 。在2L密闭容器中充入
。在2L密闭容器中充入
 发生反应,乙醇的转化率
发生反应,乙醇的转化率 变化如图所示。下列分析正确的是
变化如图所示。下列分析正确的是
| A.降低温度,有利于提高乙醇的平衡转化率 |
B.230℃,该反应的平衡常数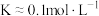 |
C.m、n两点中,乙酸乙酯的浓度均为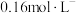 |
| D.反应在230℃、恒压容器中进行,达平衡时,乙醇的转化率小于48% |
您最近一年使用:0次
【推荐2】某恒定温度下,在一个2L的密闭容器中,加入4 mol A和2 mol B进行如下反应:3A (g)+2B (g)⇌4C (?)+2D (?),“?”代表状态不确定。反应一段时间后达到平衡,测得生成 1.6 mol C,且反应前后压强之比为5:4,则下列说法正确的是
| A.增加C,B的平衡转化率不变 |
| B.此时B的平衡转化率是35% |
| C.增大该体系的压强,平衡向右移动,化学平衡常数增大 |
D.该反应的化学平衡常数表达式是K=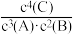 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】某温度下,在三个体积均为2L的恒容密闭容器中发生如下反应:PCl5(g)⇌PCl3(g)+Cl2(g),测得实验数据如表:下列说法正确的是
| 编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | 达到平衡所需时(s) | |
| PCl5(g) | PCl3(g) | Cl2(g) | |||
| Ⅰ | 320 | 0.40 | 0.10 | 0.10 | t1 |
| Ⅱ | 320 | 0.80 | a | a | t1 |
| Ⅲ | 410 | 0.40 | 0.15 | 0.15 | t1 |
| A.平衡常数K:容器Ⅱ>容器Ⅲ |
| B.反应到达平衡时,PCl5的转化率:容器Ⅰ>容器Ⅲ |
| C.反应到达平衡时,a>0.2 mol |
| D.起始时向容器Ⅲ中充入0.30 mol PCl5(g)、0.45 molPCl3(g)和0.10 mol Cl2(g),则反应朝逆向进行 |
您最近一年使用:0次


 和
和
 可能为铜与稀硝酸反应的催化剂
可能为铜与稀硝酸反应的催化剂