一定温度下,在密闭容器中发生反应:N2O4(g)⇌2NO2(g) ΔH>0,反应达到平衡时,下列说法不正确的是
| A.若缩小容器的体积,则容器中气体的颜色先变深后又变浅,且比原平衡颜色深 |
| B.若压强不变,向容器中再加入一定量的N2O4,再次达到平衡时各种物质的百分含量不变 |
| C.若体积不变,向容器中再加入一定量的N2O4,相对于原平衡,平衡向正反应方向移动,再次平衡时N2O4的转化率将升高 |
| D.若体积不变,升高温度,再次平衡时体系颜色加深 |
2021高二·全国·专题练习 查看更多[1]
(已下线)2.3.2 温度变化对化学平衡的影响(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)
更新时间:2022-01-17 09:06:36
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】在恒温恒容条件下,能使A(g)+B(g)  C(g)+D(g)逆反应速率增大且平衡向右移动的措施是
C(g)+D(g)逆反应速率增大且平衡向右移动的措施是
 C(g)+D(g)逆反应速率增大且平衡向右移动的措施是
C(g)+D(g)逆反应速率增大且平衡向右移动的措施是| A.减小C的浓度 | B.增大D的浓度 | C.减小B的浓度 | D.增大A的浓度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列变化不能用勒夏特列原理解释的是
| A.开启可乐瓶盖后,马上泛起大量泡沫 |
B. 溶液加热蒸干最终得不到 溶液加热蒸干最终得不到 固体 固体 |
C.合成氨工厂通常加入过量的 ,以提高 ,以提高 的转化率 的转化率 |
D.缩小平衡体系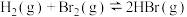 的体积,体系颜色变深 的体积,体系颜色变深 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】在密闭容器中发生储氢反应:
 。在一定温度下,达到平衡状态,测得氢气压强为2 MPa。下列说法正确的是
。在一定温度下,达到平衡状态,测得氢气压强为2 MPa。下列说法正确的是

 。在一定温度下,达到平衡状态,测得氢气压强为2 MPa。下列说法正确的是
。在一定温度下,达到平衡状态,测得氢气压强为2 MPa。下列说法正确的是| A.高温条件有利于该反应正向自发,利于储氢 |
| B.降低温度,v正增大,v逆减小,平衡正向移动 |
| C.缩小容器的容积,重新达到平衡时H2的浓度增大 |
| D.该温度下压缩体积至原来的一半,重新达到平衡时H2压强仍为2 MPa |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】图中装置不能完成的实验是
| A | B | C | D | |
| 装置 |  | 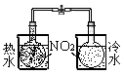 |  |  |
| 实验 | 结合秒表测量锌与硫酸的反应速率 | 验证温度对化学平衡的影响 | 验证化学能转化为电能 | 铁的析氢腐蚀实验 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
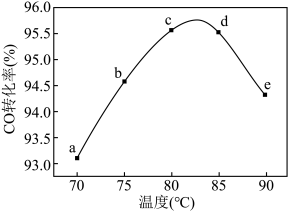
【推荐2】工业上可通过甲醇(CH3OH)羰基化法制取甲酸甲酯(HCOOCH3):CH3OH(g)+CO(g) HCOOCH3(g) △H<0。在容积固定的密闭容器中,投入等物质的量的CH3OH和CO及催化剂,测得相同时间内CO的转化率随温度变化如图所示。下列说法错误的是
HCOOCH3(g) △H<0。在容积固定的密闭容器中,投入等物质的量的CH3OH和CO及催化剂,测得相同时间内CO的转化率随温度变化如图所示。下列说法错误的是
 HCOOCH3(g) △H<0。在容积固定的密闭容器中,投入等物质的量的CH3OH和CO及催化剂,测得相同时间内CO的转化率随温度变化如图所示。下列说法错误的是
HCOOCH3(g) △H<0。在容积固定的密闭容器中,投入等物质的量的CH3OH和CO及催化剂,测得相同时间内CO的转化率随温度变化如图所示。下列说法错误的是
| A.a、b、c点一定没有达到平衡,不能确定d、e点是否达到平衡 |
| B.反应速率从快到慢依次为:e、d、c、b、a |
| C.e点的转化率低于d点,可能原因是催化剂中毒 |
| D.生产时反应温度控制在80~85℃为宜 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
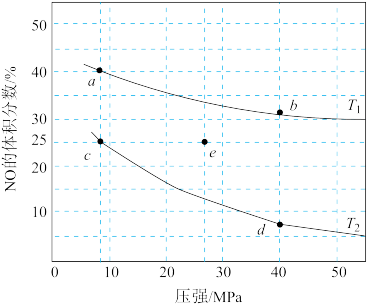
【推荐1】反应2NO(g) + 2CO(g) N2(g) + 2CO2(g)+Q(Q>0)可用于消除汽车尾气中的有害气体。在密闭容器中充入4 mol NO和5 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法错误的是
N2(g) + 2CO2(g)+Q(Q>0)可用于消除汽车尾气中的有害气体。在密闭容器中充入4 mol NO和5 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法错误的是
 N2(g) + 2CO2(g)+Q(Q>0)可用于消除汽车尾气中的有害气体。在密闭容器中充入4 mol NO和5 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法错误的是
N2(g) + 2CO2(g)+Q(Q>0)可用于消除汽车尾气中的有害气体。在密闭容器中充入4 mol NO和5 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法错误的是
| A.温度:T1>T2 |
| B.a点达到平衡所需时间比c点短 |
| C.c点NO的平衡转化率:50% |
| D.若在e点对反应容器升温的同时扩大体积使体系压强减小,重新达到的平衡状态可能是图中的c点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】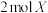 和
和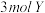 在容器中发生反应:
在容器中发生反应: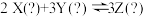 ,反应达到平衡状态时,若增大压强或降低温度,
,反应达到平衡状态时,若增大压强或降低温度,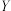 的体积分数都减小,则下列说法正确的是
的体积分数都减小,则下列说法正确的是
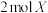 和
和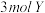 在容器中发生反应:
在容器中发生反应: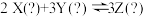 ,反应达到平衡状态时,若增大压强或降低温度,
,反应达到平衡状态时,若增大压强或降低温度,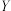 的体积分数都减小,则下列说法正确的是
的体积分数都减小,则下列说法正确的是A.可能 、 、 均是气体,也可能 均是气体,也可能 、 、 均不是气体,正反应放热 均不是气体,正反应放热 |
B.可能 是气体, 是气体, 不是气体,正反应放热 不是气体,正反应放热 |
C.可能 、 、 均是气体,正反应吸热 均是气体,正反应吸热 |
D. 、 、 一定都是气体,正反应放热 一定都是气体,正反应放热 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列叙述与图像相符的是
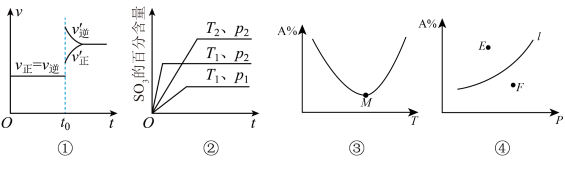

A.图①表示反应2SO2(g)+O2(g) 2SO3(g)达到平衡后在t0时刻充入了一定量的SO3 2SO3(g)达到平衡后在t0时刻充入了一定量的SO3 |
B.图②可满足反应2SO2(g)+O2(g) 2SO3(g) ΔH<0 2SO3(g) ΔH<0 |
C.图③表示反应aA(g)+bB(g) cC(g),在容器中充入1molA和1molB,经过相同时间容器中A的百分含量随温度的变化,可知反应ΔH>0 cC(g),在容器中充入1molA和1molB,经过相同时间容器中A的百分含量随温度的变化,可知反应ΔH>0 |
D.图④表示反应aA(g)+bB(g) cC(g)平衡时A的百分含量随压强的变化,可知E点v(逆)>v(正) cC(g)平衡时A的百分含量随压强的变化,可知E点v(逆)>v(正) |
您最近一年使用:0次




