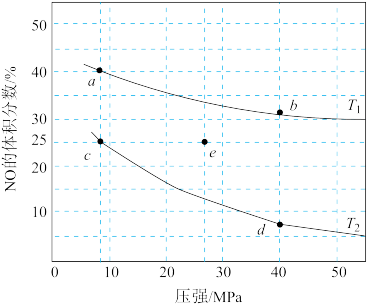
反应2NO(g) + 2CO(g) N2(g) + 2CO2(g)+Q(Q>0)可用于消除汽车尾气中的有害气体。在密闭容器中充入4 mol NO和5 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法错误的是
N2(g) + 2CO2(g)+Q(Q>0)可用于消除汽车尾气中的有害气体。在密闭容器中充入4 mol NO和5 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法错误的是
 N2(g) + 2CO2(g)+Q(Q>0)可用于消除汽车尾气中的有害气体。在密闭容器中充入4 mol NO和5 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法错误的是
N2(g) + 2CO2(g)+Q(Q>0)可用于消除汽车尾气中的有害气体。在密闭容器中充入4 mol NO和5 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法错误的是
| A.温度:T1>T2 |
| B.a点达到平衡所需时间比c点短 |
| C.c点NO的平衡转化率:50% |
| D.若在e点对反应容器升温的同时扩大体积使体系压强减小,重新达到的平衡状态可能是图中的c点 |
2020·北京朝阳·模拟预测 查看更多[10]
河南省南阳市第一中学校2023-2024学年高二上学期第一次月考化学试题甘肃省张掖市高台县第一中学2023-2024学年高二上学期开学(暑假学习效果)检测化学试题河南省汝州市第一高级中学2022-2023学年高二上学期11月月考化学试题河南省鹤壁市高中2022-2023学年高三上学期第三次模拟考试化学试题甘肃省张掖市高台县第一中学2022-2023学年高二上学期期中考试化学试题上海行知中学2022-2023学年高三上学期第一次月考化学试题黑龙江省嫩江市高级中学2021届高三上学期模拟考试化学试题上海市复旦大学附属中学2021届高三上学期第一次教学质量检测化学试题(已下线)北京市2019-2020学年高三各区一模化学考试分类汇编 选择题:化学平衡 离子平衡北京市朝阳区2020届高三学业水平等级性考试练习化学试题
更新时间:2022-10-13 11:29:13
|
相似题推荐
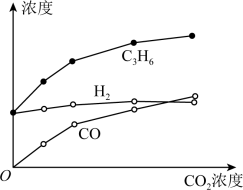
【推荐1】丙烷经催化脱氢制丙烯的反应为C3H8(g)=C3H6(g)+H2(g)。600℃,将固定浓度的C3H8通入有催化剂的恒容反应器,逐渐提高CO2浓度,经相同时间,测得出口处C3H6、CO和H2浓度随初始CO2浓度的变化关系如图所示。下列说法不正确的是

A.丙烷脱氢制丙烯反应的化学平衡常数K=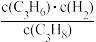 |
B.c(H2)和c(C3H6)变化差异的原因:CO2+H2 CO+H2O CO+H2O |
| C.其他条件不变,投料比c(C3H8)/c(CO2)越大,C3H8转化率越小 |
| D.若体系只有C3H6、H2、CO和H2O生成,则出口处物质浓度c之间一定存在关系:2c(C3H6)=2c(H2)+c(CO)+2c(H2O) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】 时,向
时,向 密闭容器中充入
密闭容器中充入 和
和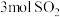 发生反应:
发生反应: 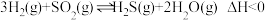 。部分物质的物质的量
。部分物质的物质的量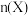 随时间t变化如图中实线所示,下列说法正确的是
随时间t变化如图中实线所示,下列说法正确的是
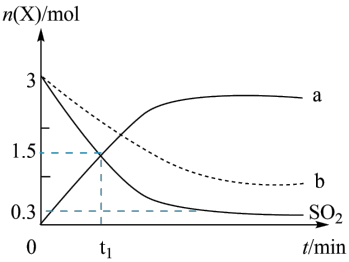
 时,向
时,向 密闭容器中充入
密闭容器中充入 和
和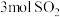 发生反应:
发生反应: 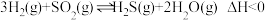 。部分物质的物质的量
。部分物质的物质的量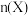 随时间t变化如图中实线所示,下列说法正确的是
随时间t变化如图中实线所示,下列说法正确的是
A.实线a代表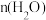 随时间变化的曲线 随时间变化的曲线 |
B. 时, 时, |
C.该反应的平衡常数计算式为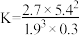 |
D.若该反应在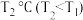 时进行,则虚线b可表示 时进行,则虚线b可表示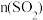 的变化 的变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】向某密闭容器中充入0.3mol A、0.1mol C和一定量的B三种气体。一定条件下发生反应,各物质的浓度随时间的变化如甲图所示[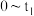 阶段的c(B)变化未画出]。乙图为
阶段的c(B)变化未画出]。乙图为 时刻后改变条件时平衡体系中正、逆反应速率随时间变化的情况,且四个阶段都各改变一种反应条件且互不相同,
时刻后改变条件时平衡体系中正、逆反应速率随时间变化的情况,且四个阶段都各改变一种反应条件且互不相同,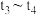 阶段改变的条件为使用催化剂。下列说法不正确的是
阶段改变的条件为使用催化剂。下列说法不正确的是
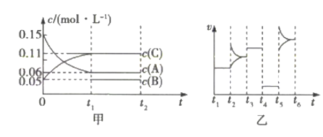
 阶段的c(B)变化未画出]。乙图为
阶段的c(B)变化未画出]。乙图为 时刻后改变条件时平衡体系中正、逆反应速率随时间变化的情况,且四个阶段都各改变一种反应条件且互不相同,
时刻后改变条件时平衡体系中正、逆反应速率随时间变化的情况,且四个阶段都各改变一种反应条件且互不相同,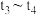 阶段改变的条件为使用催化剂。下列说法不正确的是
阶段改变的条件为使用催化剂。下列说法不正确的是
A.若 =15s,则用A的浓度变化表示的0~ =15s,则用A的浓度变化表示的0~ 阶段的平均反应速率为0.006 阶段的平均反应速率为0.006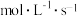 |
B. 阶段改变的条件一定为减小压强,即增大容器体积 阶段改变的条件一定为减小压强,即增大容器体积 |
| C.起始时该容器的容积为2 L,B的起始物质的量为0.02 mol |
D.该反应的化学方程式为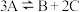 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】PCl3和PCl5都是重要的化工原料。将PCl3(g)和Cl2(g)充入体积不变的2 L密闭容器中,在一定条件下发生反应:PCl3(g)+Cl2(g)⇌PCl5(g) ΔH<0,并于10 min时达到平衡。有关数据如下:
下列判断不正确的是
| PCl3(g) | Cl2(g) | PCl5(g) | |
| 初始浓度/(mol·L-1) | 2.0 | 1.0 | 0 |
| 平衡浓度/(mol·L-1) | c1 | c2 | 0.4 |
| A.10 min内,v(Cl2)=0.04 mol·L-1·min-1 |
| B.当容器中Cl2为1.2 mol时,反应达到平衡 |
| C.升高温度,反应的平衡常数减小,则平衡时PCl3的转化率升高 |
| D.平衡后移走2.0 mol PCl3和1.0 mol Cl2,在相同条件下再达到平衡时,c(PCl5)<0.2 mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】将等物质的量的X、Y气体充入某密闭容器中,在一定条件下,发生如下反应并达到平衡:X(g)+3Y(g) 2Z(g) ΔH<0。当改变某个条件并维持新条件直至新的平衡时,下表中关于新平衡与原平衡的比较正确的是
2Z(g) ΔH<0。当改变某个条件并维持新条件直至新的平衡时,下表中关于新平衡与原平衡的比较正确的是
 2Z(g) ΔH<0。当改变某个条件并维持新条件直至新的平衡时,下表中关于新平衡与原平衡的比较正确的是
2Z(g) ΔH<0。当改变某个条件并维持新条件直至新的平衡时,下表中关于新平衡与原平衡的比较正确的是| 选项 | 改变条件 | 新平衡与原平衡比较 |
| A | 升高温度 | X的转化率变大 |
| B | 增大压强 | X的浓度变大 |
| C | 充入一定量Y | Y的转化率增大 |
| D | 使用适当催化剂 | X的体积分数变小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】在恒温恒容条件下,向容积为1L的密闭容器中充入一定量的SO3(g),发生下列反应: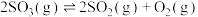
 。温度为T时,部分实验数据如表所示:
。温度为T时,部分实验数据如表所示:
下列说法错误的是
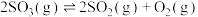
 。温度为T时,部分实验数据如表所示:
。温度为T时,部分实验数据如表所示: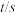 | 0 | 50 | 100 | 150 |
 | 4.00 | 2.50 | 2.00 | 2.00 |
A.前50s内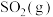 的平均生成速率为 的平均生成速率为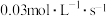 |
| B.容器内密度不再改变说明反应已达平衡 |
C.150s时,向容器中继续通入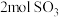 、 、 、 、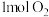 ,则此时反应将逆向进行 ,则此时反应将逆向进行 |
D.其他条件不变,若将恒容改为恒压,则平衡时 的转化率增大 的转化率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】室温下,下列探究方案能 达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 用不同浓度、等体积的 溶液分别与相同浓度相同体积的 溶液分别与相同浓度相同体积的 溶液反应,观察现象 溶液反应,观察现象 | 探究浓度对反应速率的影响 |
| B | 两支试管中先后分别加入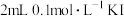 溶液和 溶液和 溶液及3滴淀粉溶液,再分别放入热水与冷水中,记录溶液变蓝的时间 溶液及3滴淀粉溶液,再分别放入热水与冷水中,记录溶液变蓝的时间 | 探究温度对化学反应速率的影响 |
| C | 先将注射器中充满 气体,然后将活塞往里推,压缩体积,观察注射器内气体颜色变化 气体,然后将活塞往里推,压缩体积,观察注射器内气体颜色变化 | 探究压强对化学平衡的影响 |
| D | 向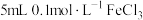 溶液中滴加 溶液中滴加 溶液,充分反应后,取少量反应后溶液于试管中,再滴入几滴 溶液,充分反应后,取少量反应后溶液于试管中,再滴入几滴 溶液,观察溶液颜色变化 溶液,观察溶液颜色变化 | 探究化学反应的限度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】将 4 mol A 气体和 2 mol B 气体在 2 L 的容器中混合并在一定条件下发生如下反应2A(g)+B(g) 2C(g)若经 2 s(秒)后测得 C 的浓度为 0.6 mol·L-1 ,现有下列几种说法:
2C(g)若经 2 s(秒)后测得 C 的浓度为 0.6 mol·L-1 ,现有下列几种说法:
① 用物质 A 表示的反应的平均速率为 0.3 mol·(L·s)-1
② 用物质 B 表示的反应的平均速率为 0.6 mol·(L·s)-1
③ 2 s 时物质 A 和 B 的转化率(发生反应的物质的量占总物质的量的百分数)一样
④ 2 s 时物质 B 的浓度为 0.3 mol·L-1
其中正确的是
 2C(g)若经 2 s(秒)后测得 C 的浓度为 0.6 mol·L-1 ,现有下列几种说法:
2C(g)若经 2 s(秒)后测得 C 的浓度为 0.6 mol·L-1 ,现有下列几种说法:① 用物质 A 表示的反应的平均速率为 0.3 mol·(L·s)-1
② 用物质 B 表示的反应的平均速率为 0.6 mol·(L·s)-1
③ 2 s 时物质 A 和 B 的转化率(发生反应的物质的量占总物质的量的百分数)一样
④ 2 s 时物质 B 的浓度为 0.3 mol·L-1
其中正确的是
| A.①③ | B.③④ | C.②③ | D.①④ |
您最近一年使用:0次
【推荐2】一定温度下,在一体积为2L的恒容密闭容器中充入2molSO2、1molO2,发生反应:2SO2(g)+O2(g)  2SO3(g) △H= - 196 kJ·mol-1,达到平衡后放出热量156.8kJ,下列说法不正确的是
2SO3(g) △H= - 196 kJ·mol-1,达到平衡后放出热量156.8kJ,下列说法不正确的是
 2SO3(g) △H= - 196 kJ·mol-1,达到平衡后放出热量156.8kJ,下列说法不正确的是
2SO3(g) △H= - 196 kJ·mol-1,达到平衡后放出热量156.8kJ,下列说法不正确的是| A.相同条件下初始若向容器中只充入2molSO3,达到平衡时吸收热量156.8kJ |
| B.若升高温度,该反应的平衡常数将减小 |
| C.反应过程中转移3.2mole- |
| D.平衡时SO2的转化率为80% |
您最近一年使用:0次

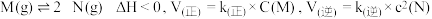 ,若该温度下的平衡常数
,若该温度下的平衡常数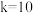 ,下列说法正确的是
,下列说法正确的是
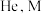 的转化率增大
的转化率增大
 的体积(已折算为标准状况下)如表。
的体积(已折算为标准状况下)如表。