氮氧化物和碳氧化合物的综合治理是当前的重要课题之一。
已知:ⅰ.NO(g)+CO2(g) NO2(g)+CO(g) △H1=+234kJ·mol-1
NO2(g)+CO(g) △H1=+234kJ·mol-1
ⅱ.2NO(g)+2CO(g) N2(g)+2CO2(g) △H2=-745kJ·mol-1
N2(g)+2CO2(g) △H2=-745kJ·mol-1
(1)NO2(g)与CO(g)反应生成两种无毒气体的热化学方程式为______________ 。
(2)反应ⅰ的正反应的活化能E_____ △H1(填“>”、“<”或“=”)。
(3)一定压强下,密闭容器中发生反应ⅰ和反应ⅱ。达到平衡后,保持其他条件不变,升高温度,CO(g)的体积分数________ (填“增大”、“减少”或“无法确定”),原因为_____________________ 。
(4)向起始温度为t℃、容积为10L的恒容绝热的密闭容器中充入2molNO(g)和1molCO2(g),发生反应ⅰ。5min时达到平衡。则:
①下列事实能说明该反应达到平衡状态的是________ (填选项字母)
A.混合气体温度不变 B.混合气体的压强不变
C. NO2和CO的浓度之比为1: 1 D.混合气体的平均相对分子质量不变
②t℃时,向另一容积为10 L的恒温恒容的密闭容器中充入2 mol NO(g)和1 mol CO2(g),发生反应i。达到平衡的时间______ 5 min(填“>”、“<”或“=”)。
(5)在某密闭容器中充有10 mol CO(g)和20 mol NO(g),发生反应ii,CO的平衡转化率(α)与温度(T)、压强(p)的关系如图所示。
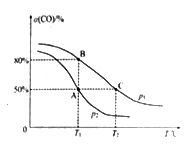
①A、B、C 三点的平衡常数KA、KB、KC的大小关系为________ ;p1和p2的大小关系为__________ 。
②A点时.测得容器的体积为10 L,则T1℃时,该反应平衡常数K的值为____________ 。
已知:ⅰ.NO(g)+CO2(g)
 NO2(g)+CO(g) △H1=+234kJ·mol-1
NO2(g)+CO(g) △H1=+234kJ·mol-1ⅱ.2NO(g)+2CO(g)
 N2(g)+2CO2(g) △H2=-745kJ·mol-1
N2(g)+2CO2(g) △H2=-745kJ·mol-1(1)NO2(g)与CO(g)反应生成两种无毒气体的热化学方程式为
(2)反应ⅰ的正反应的活化能E
(3)一定压强下,密闭容器中发生反应ⅰ和反应ⅱ。达到平衡后,保持其他条件不变,升高温度,CO(g)的体积分数
(4)向起始温度为t℃、容积为10L的恒容绝热的密闭容器中充入2molNO(g)和1molCO2(g),发生反应ⅰ。5min时达到平衡。则:
①下列事实能说明该反应达到平衡状态的是
A.混合气体温度不变 B.混合气体的压强不变
C. NO2和CO的浓度之比为1: 1 D.混合气体的平均相对分子质量不变
②t℃时,向另一容积为10 L的恒温恒容的密闭容器中充入2 mol NO(g)和1 mol CO2(g),发生反应i。达到平衡的时间
(5)在某密闭容器中充有10 mol CO(g)和20 mol NO(g),发生反应ii,CO的平衡转化率(α)与温度(T)、压强(p)的关系如图所示。

①A、B、C 三点的平衡常数KA、KB、KC的大小关系为
②A点时.测得容器的体积为10 L,则T1℃时,该反应平衡常数K的值为
更新时间:2017-05-29 11:46:48
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】CO2–CH4干气重整反应制合成气(H2、CO)是CO2资源化利用的重要研究方向。其反应主要包括:
反应I CH4(g)+CO2(g) 2H2(g)+2CO(g) ΔH1=+247.34 kJ·mol-1
2H2(g)+2CO(g) ΔH1=+247.34 kJ·mol-1
反应II H2(g)+CO2(g) H2O(g)+CO(g) ΔH2
H2O(g)+CO(g) ΔH2
回答下列问题:
(1)已知 H2(g)、CO(g) 的燃烧热分别为 285.8 kJ·mol-1 和 283 kJ·mol-1 ,水的汽化热为44 kJ·mol-1,则ΔH2=___________ kJ·mol-1;能同时提高CH4(g)的平衡转化率和反应速率的措施为___________ (写一条即可)。
(2)向T℃、2.8 MPa的恒压密闭容器中,充入1 mol CH4(g)和1 mol CO2(g)发生反应I和II。达到平衡时,CO2的转化率为80%,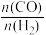 =3 ,则平衡时气体的总物质的量n总=
=3 ,则平衡时气体的总物质的量n总=___________ mol;反应I的压强平衡常数Kp=___________ (MPa)2;若反应在刚性容器中达到平衡,则CO2(g)的转化率___________ (填“>”、“=”或“<”)80%。
(3)实验研究发现,在(2)条件下,催化剂表面产生积碳与下列2个反应有关:
反应III CH4(g) C(s)+2H2(g) ΔH3=+74.87 kJ·mol-1
C(s)+2H2(g) ΔH3=+74.87 kJ·mol-1
反应IV 2CO(g) CO2(g)+C(s) ΔH4=–172.47 kJ·mol-1
CO2(g)+C(s) ΔH4=–172.47 kJ·mol-1
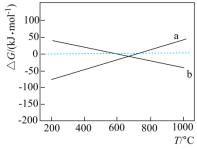
已知ΔG=ΔH–TΔS,ΔG的值只取决于反应体系的始态和终态,忽略ΔH、ΔS随温度的变化,反应Ⅲ和反应Ⅳ的ΔG与T的关系如图所示,其中表示反应III的曲线为___________ (填“a”或“b”);催化剂表面始终存在积碳的原因为___________ 。
反应I CH4(g)+CO2(g)
 2H2(g)+2CO(g) ΔH1=+247.34 kJ·mol-1
2H2(g)+2CO(g) ΔH1=+247.34 kJ·mol-1反应II H2(g)+CO2(g)
 H2O(g)+CO(g) ΔH2
H2O(g)+CO(g) ΔH2回答下列问题:
(1)已知 H2(g)、CO(g) 的燃烧热分别为 285.8 kJ·mol-1 和 283 kJ·mol-1 ,水的汽化热为44 kJ·mol-1,则ΔH2=
(2)向T℃、2.8 MPa的恒压密闭容器中,充入1 mol CH4(g)和1 mol CO2(g)发生反应I和II。达到平衡时,CO2的转化率为80%,
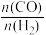 =3 ,则平衡时气体的总物质的量n总=
=3 ,则平衡时气体的总物质的量n总=(3)实验研究发现,在(2)条件下,催化剂表面产生积碳与下列2个反应有关:
反应III CH4(g)
 C(s)+2H2(g) ΔH3=+74.87 kJ·mol-1
C(s)+2H2(g) ΔH3=+74.87 kJ·mol-1反应IV 2CO(g)
 CO2(g)+C(s) ΔH4=–172.47 kJ·mol-1
CO2(g)+C(s) ΔH4=–172.47 kJ·mol-1已知ΔG=ΔH–TΔS,ΔG的值只取决于反应体系的始态和终态,忽略ΔH、ΔS随温度的变化,反应Ⅲ和反应Ⅳ的ΔG与T的关系如图所示,其中表示反应III的曲线为

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】甲醇是重要的绿色能源之一,目前科学家用水煤气(CO+H2)合成甲醇,其反应为:CO(g)+2H2(g)  CH3OH(g)△H=-128.1kJ·mol-1
CH3OH(g)△H=-128.1kJ·mol-1
回答下列问题:
(1)该反应是可逆反应,为使化学反应速率和CO的转化率都同时提高的措施有_____ 。
A、升高温度 B、增大压强 C、充入氢气 D、分离出甲醇
(2)恒温恒容条件能说明该可逆反应达平衡的是_________ ;
A.2v正(H2)=v逆(CH3OH)
B.n(CO):n(H2):n(CH3OH)=1:2:1
C.混合气体的密度不变
D.混合气体的平均相对分子质量不变
(3)若上述可逆反应在恒温恒容的密闭容器进行,起始时间向该容器中充入1molCO(g)和2molH2(g)。实验测得H2的平衡转化率随温度(T)、压强(P)的变化如图所示。
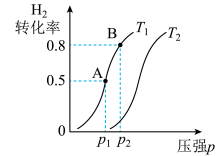
①该反应的△S____ 0,图中的T1___ T2(填“<”“>”或“=”)
②T1下到达平衡状态A时,容器的体积为2L,此时该反应的平衡常数为______ ,若达到平衡状态B时,则容器的体积V(B)=______ L。
(4) CO燃烧的热化学方程式:CO(g)+ 1/2 O2(g)═CO2(g)△H= —283.0kJ•mol-1
H2(g)+1/2 O2(g)═H2O(l)△H= —285.8 kJ•mol-1
CO(g)+2H2(g)═CH3OH(l)△H= —128.1KJ•mol-1
则CH3OH(g)燃烧热的热化学方程式是为___________ 。
 CH3OH(g)△H=-128.1kJ·mol-1
CH3OH(g)△H=-128.1kJ·mol-1回答下列问题:
(1)该反应是可逆反应,为使化学反应速率和CO的转化率都同时提高的措施有
A、升高温度 B、增大压强 C、充入氢气 D、分离出甲醇
(2)恒温恒容条件能说明该可逆反应达平衡的是
A.2v正(H2)=v逆(CH3OH)
B.n(CO):n(H2):n(CH3OH)=1:2:1
C.混合气体的密度不变
D.混合气体的平均相对分子质量不变
(3)若上述可逆反应在恒温恒容的密闭容器进行,起始时间向该容器中充入1molCO(g)和2molH2(g)。实验测得H2的平衡转化率随温度(T)、压强(P)的变化如图所示。

①该反应的△S
②T1下到达平衡状态A时,容器的体积为2L,此时该反应的平衡常数为
(4) CO燃烧的热化学方程式:CO(g)+ 1/2 O2(g)═CO2(g)△H= —283.0kJ•mol-1
H2(g)+1/2 O2(g)═H2O(l)△H= —285.8 kJ•mol-1
CO(g)+2H2(g)═CH3OH(l)△H= —128.1KJ•mol-1
则CH3OH(g)燃烧热的热化学方程式是为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】为有效控制雾霾,各地积极采取措施改善大气质量,有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要。
(1)在汽车排气管内按照催化转化器,可将汽车尾气中主要污染物转化为无毒的大气循环物质。
已知:① N2(g)+O2(g)=2NO(g) △H=+180.5kJ·mol-1
②C和CO的燃烧热(△H)分别为-393.5kJ·mol-1和-283kJ·mol-1
则2NO(g)+2CO(g)=N2(g)+2CO2(g)) △H=_______ kJ·mol-1
(2)将0.20molNO和0.10molCO充入一个容积为1L的密闭容器中,反应过程中物质浓度变化如图所示。
①CO在0-9min内的平均反应速率v(CO)=________ mol·L-1·min-1 (保留两位有效数字);第12 min时改变的反应条件可能为________ 。
A.升高温度 B.加入NO C.加催化剂 D.降低温度
②该反应在第18 min时达到平衡状态,CO2的体积分数为________ (保留三位有效数字),化学平衡常数K=________ (保留两位有效数字)。
(3)通过人工光合作用能将水与燃煤产生的CO2转化成HCOOH和O2。已知常温下0.1mol·L-2的
HCOONa溶液pH=10,则HCOOH的电离常数Ka=______________ 。
(1)在汽车排气管内按照催化转化器,可将汽车尾气中主要污染物转化为无毒的大气循环物质。
已知:① N2(g)+O2(g)=2NO(g) △H=+180.5kJ·mol-1
②C和CO的燃烧热(△H)分别为-393.5kJ·mol-1和-283kJ·mol-1
则2NO(g)+2CO(g)=N2(g)+2CO2(g)) △H=
(2)将0.20molNO和0.10molCO充入一个容积为1L的密闭容器中,反应过程中物质浓度变化如图所示。
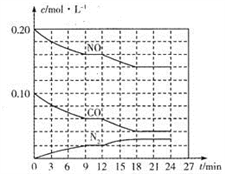
①CO在0-9min内的平均反应速率v(CO)=
A.升高温度 B.加入NO C.加催化剂 D.降低温度
②该反应在第18 min时达到平衡状态,CO2的体积分数为
(3)通过人工光合作用能将水与燃煤产生的CO2转化成HCOOH和O2。已知常温下0.1mol·L-2的
HCOONa溶液pH=10,则HCOOH的电离常数Ka=
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】柳酸甲酯( )常用于医药制剂的赋香剂,实验小组利用邻羟基苯甲酸(
)常用于医药制剂的赋香剂,实验小组利用邻羟基苯甲酸( )和甲醇在浓硫酸催化下合成少量柳酸甲酯。
)和甲醇在浓硫酸催化下合成少量柳酸甲酯。
I.实验原理:
II.相关数据如下表:
III.实验步骤:
合成:向A中加入6.9g邻羟基苯甲酸、适量固态酸性催化剂、24g甲醇,10mL甲苯(甲苯与水能形成的共沸物,沸点为85℃,易将水蒸出)加热回流1.5小时;
提纯:反应完毕,待装置冷却后,分离出固态催化剂,依次用水洗、5%的NaHCO3溶液洗、水洗,将产物移至干燥的烧杯中加入0.5g无水氯化钙,一段时间后,过滤,蒸馏有机层获得4.5g纯品。

回答下列问题:
(1)甲苯蒸气、甲醇蒸气、水蒸气冷凝为液体,然后通过分水器,甲苯、甲醇重新流回到A中,打开活塞将水从下口放出。下列有关说法中错误的是___________(填字母)。
(2)在提纯步骤中,一定没有用到下列仪器中的___________ (填仪器名称)。
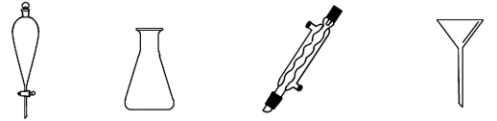
(3)提纯步骤中第二次水洗的目的是___________ ;无水氯化钙的作用是___________ 。
(4)本实验的产率为___________ %(保留三位有效数字)。
(5)实验小组为了探究影响产率的因素,采集了如下数据(邻羟基苯甲酸易溶于甲醇):
①实验IV中x=___________ ;设计实验IV是为了探究___________ 对产率的影响。
②增加甲醇的体积会提高产率,但甲醇超过一定量时,反应时间相同的情况下,产率反而下降,试从速率角度分析产率下降的主要原因:___________ 。
 )常用于医药制剂的赋香剂,实验小组利用邻羟基苯甲酸(
)常用于医药制剂的赋香剂,实验小组利用邻羟基苯甲酸( )和甲醇在浓硫酸催化下合成少量柳酸甲酯。
)和甲醇在浓硫酸催化下合成少量柳酸甲酯。I.实验原理:

II.相关数据如下表:
| 名称 | 分子量 | 颜色状态 | 相对密度 | 熔点(℃) | 沸点(℃) | 溶解性(中) |
| 柳酸甲酯 | 152 | 无色液体 | 1.18 | -8.6 | 224 | 微溶 |
| 邻羟基苯甲酸 | 138 | 白色晶体 | 1.44 | 158 | 210 | 不溶 |
| 甲醇 | 32 | 无色液体 | 0.792 | -97 | 64.7 | 互溶 |
合成:向A中加入6.9g邻羟基苯甲酸、适量固态酸性催化剂、24g甲醇,10mL甲苯(甲苯与水能形成的共沸物,沸点为85℃,易将水蒸出)加热回流1.5小时;
提纯:反应完毕,待装置冷却后,分离出固态催化剂,依次用水洗、5%的NaHCO3溶液洗、水洗,将产物移至干燥的烧杯中加入0.5g无水氯化钙,一段时间后,过滤,蒸馏有机层获得4.5g纯品。

回答下列问题:
(1)甲苯蒸气、甲醇蒸气、水蒸气冷凝为液体,然后通过分水器,甲苯、甲醇重新流回到A中,打开活塞将水从下口放出。下列有关说法中错误的是___________(填字母)。
| A.使用分水器能提高反应物的利用率 |
| B.使用分水器能够促使反应正向进行 |
| C.分水器中的水面不再变化时,反应达到最大限度 |
| D.10mL甲苯也可用四氯化碳代替 |

(3)提纯步骤中第二次水洗的目的是
(4)本实验的产率为
(5)实验小组为了探究影响产率的因素,采集了如下数据(邻羟基苯甲酸易溶于甲醇):
| 编号 | 邻羟基苯甲酸/g | 甲醇/mL | 反应时间/min | 催化剂用量/g | 产率/% |
| I | 4.8 | 4.0 | 8 | 1.4 | 61.67 |
| II | 4.8 | 4.0 | 8 | 1.0 | 55.42 |
| III | 4.8 | 5.0 | 8 | 1.4 | 65.42 |
| IV | 4.8 | x | 4 | 1.4 | — |
②增加甲醇的体积会提高产率,但甲醇超过一定量时,反应时间相同的情况下,产率反而下降,试从速率角度分析产率下降的主要原因:
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】异丁烯为重要的化工原料,工业上可采用叔丁醇(TBA)气相脱水法制备高纯异丁烯产品,主要涉及以下反应:
反应1(主反应):
反应2(副反应):
(1)副反应产物 的系统命名为
的系统命名为___________ 。
(2)标准摩尔生成焓是指由稳态单质生成1mol该化合物的焓变,几种物质的标准生成焓如表,求反应1的
___________  。
。
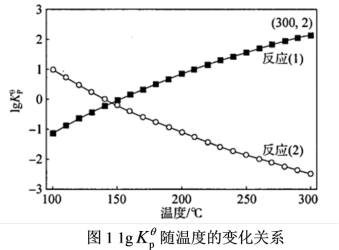
(3)根据,该脱水反应的标准平衡常数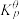 随温度的变化关系如图1所示,则反应2的
随温度的变化关系如图1所示,则反应2的
___________ 0(填“<”或“>”),向体积可变容器中充入1mol的叔丁醇,容器体积为1L,保持300℃100kPa条件,反应一段时间后达到平衡(忽略副反应),则
___________ (已知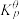 为以标准分压表示的平衡常数,各组分的标准分压
为以标准分压表示的平衡常数,各组分的标准分压 ,
,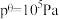 )。
)。
(4)理论计算反应条件对叔丁醇转化率的影响如图2、3所示,脱水反应温度 ℃时,N2/叔丁醇摩尔比对叔丁醇转化率有影响,试从平衡移动的角度分析充入N2的原因
℃时,N2/叔丁醇摩尔比对叔丁醇转化率有影响,试从平衡移动的角度分析充入N2的原因___________ 。根据图示该脱水反应适宜采用条件为 ℃,P=
℃,P=___________ MPa,N2/叔丁醇摩尔比=3/1。


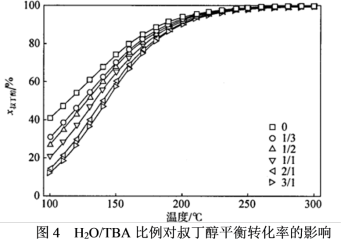
(5)已知工业原料叔丁醇中存在不同含量的水分,相同温度下不同初始原料中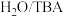 比例对叔丁醇平衡转化率的影响如图4所示,实际生产最佳工艺条件为
比例对叔丁醇平衡转化率的影响如图4所示,实际生产最佳工艺条件为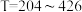 ℃,请从
℃,请从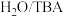 比例角度分析该条件下的优点
比例角度分析该条件下的优点___________ 。
反应1(主反应):

反应2(副反应):

(1)副反应产物
 的系统命名为
的系统命名为(2)标准摩尔生成焓是指由稳态单质生成1mol该化合物的焓变,几种物质的标准生成焓如表,求反应1的

 。
。| 组分 |  | 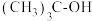 | 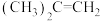 |
焓变/ | -241.83 | -339.21 | -17.1 |
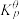 随温度的变化关系如图1所示,则反应2的
随温度的变化关系如图1所示,则反应2的

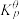 为以标准分压表示的平衡常数,各组分的标准分压
为以标准分压表示的平衡常数,各组分的标准分压 ,
,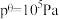 )。
)。
(4)理论计算反应条件对叔丁醇转化率的影响如图2、3所示,脱水反应温度
 ℃时,N2/叔丁醇摩尔比对叔丁醇转化率有影响,试从平衡移动的角度分析充入N2的原因
℃时,N2/叔丁醇摩尔比对叔丁醇转化率有影响,试从平衡移动的角度分析充入N2的原因 ℃,P=
℃,P=

(5)已知工业原料叔丁醇中存在不同含量的水分,相同温度下不同初始原料中
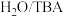 比例对叔丁醇平衡转化率的影响如图4所示,实际生产最佳工艺条件为
比例对叔丁醇平衡转化率的影响如图4所示,实际生产最佳工艺条件为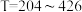 ℃,请从
℃,请从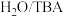 比例角度分析该条件下的优点
比例角度分析该条件下的优点
您最近一年使用:0次
【推荐3】铬是用途广泛的金属,但在生产过程中易产生有害的含铬工业废水。
I.还原沉淀法是处理含CrO42-和Cr2O72-工业废水的一种常用方法,其工艺流程如下:
其中,第I步存在平衡:2CrO42-(黄色)+2H+ Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O
(1)若平衡体系中,pH=0时溶液呈______ 色。
(2)以石墨为电极,电解Na2CrO4制备Na2CrO7的装置如图所示,a极的名称是_______ ;第I步中b极直接相连一极的反应式为_______________ 。
(3)第II步的离子方程式为______________ ;向第II步反应后的溶液中加入一定量烧碱,若溶液中c(Fe3+)=2.0×10-12mol/L,则溶液中c(Cr3+)=_______ mol/L。
(已知:Ksp[Fe(OH)3]=4.0×10-38mol/L,Ksp[Cr(OH)3]=6.0×10-31mol/L)
II.探究CrO3的强氧化性和热稳定性
(4)CrO3遇有机物(如酒精)时猛然反应以至着火。若该过程中乙醇被氧化成乙酸,CrO3被还原成绿色的Cr2(SO4)3。补充并配平下列反应式:a CrO3+bC2H5OH+cH2SO4=d Cr2(SO4)3+eCH3COOH+fR
b:c:f=_________ 。
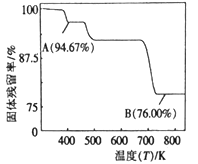
(5)CrO3的热稳定性差,加热时逐步分解,其固体残解率随温度的变化如图所示。B点时生成固体的化学式为______ 。( )。
)。
I.还原沉淀法是处理含CrO42-和Cr2O72-工业废水的一种常用方法,其工艺流程如下:

其中,第I步存在平衡:2CrO42-(黄色)+2H+
 Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O(1)若平衡体系中,pH=0时溶液呈
(2)以石墨为电极,电解Na2CrO4制备Na2CrO7的装置如图所示,a极的名称是

(3)第II步的离子方程式为
(已知:Ksp[Fe(OH)3]=4.0×10-38mol/L,Ksp[Cr(OH)3]=6.0×10-31mol/L)
II.探究CrO3的强氧化性和热稳定性
(4)CrO3遇有机物(如酒精)时猛然反应以至着火。若该过程中乙醇被氧化成乙酸,CrO3被还原成绿色的Cr2(SO4)3。补充并配平下列反应式:a CrO3+bC2H5OH+cH2SO4=d Cr2(SO4)3+eCH3COOH+fR
b:c:f=
(5)CrO3的热稳定性差,加热时逐步分解,其固体残解率随温度的变化如图所示。B点时生成固体的化学式为
 )。
)。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】氮的氧化物是大气污染物之一,研究它们的反应机理,对于消除环境污染,促进社会可持续发展有重要意义。回答下列问题:
(1)碘蒸气的存在能大幅度提高 的分解速率,反应历程为:
的分解速率,反应历程为:
第一步: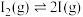 (快反应)
(快反应)
第二步: (慢反应)
(慢反应)
第三步: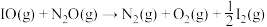 (快反应)
(快反应)
实验表明,含碘时 分解速率方程
分解速率方程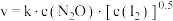 (
( 为速率常数)。下列表述正确的是___________
为速率常数)。下列表述正确的是___________
(2)对反应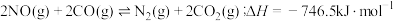 ,分别在不同温度、不同催化剂下,保持其它初始条件不变,重复实验,在相同时间内测得NO转化率与温度的关系如图所示。
,分别在不同温度、不同催化剂下,保持其它初始条件不变,重复实验,在相同时间内测得NO转化率与温度的关系如图所示。
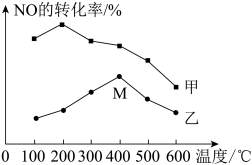
图中M点对应的速率(对应温度 )
)
___________  (填“>”、“<”或“=”),温度高于
(填“>”、“<”或“=”),温度高于 ,NO转化率降低的原因可能是
,NO转化率降低的原因可能是___________ 。
(3)在密闭容器中充入 和
和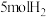 ,发生反应:
,发生反应: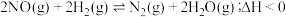 。平衡时NO的体积分数随温度、压强的变化关系如图。
。平衡时NO的体积分数随温度、压强的变化关系如图。

①下列物理量中,图中d点大于b点的是___________ (填字母)。
A.正反应速率 B.逆反应速率
C. 的浓度 D.对应温度的平衡常数
的浓度 D.对应温度的平衡常数
②c点NO的平衡转化率为___________ 。
③若在M点对反应容器升温的同时扩大容器体积使体系压强减小,重新达到的平衡状态可能是图中a、b、c、d中的___________ 点。
(4) 时,向容积为2L的恒容容器中充入
时,向容积为2L的恒容容器中充入 、
、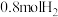 ,发生反应:
,发生反应: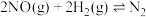
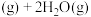 ,体系的总压强P随时间t的变化如下表所示:
,体系的总压强P随时间t的变化如下表所示:
①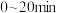 内该反应的平均反应速率
内该反应的平均反应速率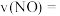
___________  。
。
②该温度下反应的平衡常数
___________  (用平衡分压代替平衡浓度,平衡分压=总压×物质的量分数,列出计算式即可)。
(用平衡分压代替平衡浓度,平衡分压=总压×物质的量分数,列出计算式即可)。
(1)碘蒸气的存在能大幅度提高
 的分解速率,反应历程为:
的分解速率,反应历程为:第一步:
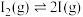 (快反应)
(快反应)第二步:
 (慢反应)
(慢反应)第三步:
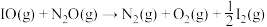 (快反应)
(快反应)实验表明,含碘时
 分解速率方程
分解速率方程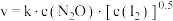 (
( 为速率常数)。下列表述正确的是___________
为速率常数)。下列表述正确的是___________| A.升高温度,第一步向右进行的程度变大 |
| B.第二步的活化能比第三步小 |
C. 为反应的催化剂 为反应的催化剂 |
D. 分解反应的速率与是否含碘蒸气有关 分解反应的速率与是否含碘蒸气有关 |
(2)对反应
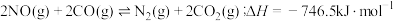 ,分别在不同温度、不同催化剂下,保持其它初始条件不变,重复实验,在相同时间内测得NO转化率与温度的关系如图所示。
,分别在不同温度、不同催化剂下,保持其它初始条件不变,重复实验,在相同时间内测得NO转化率与温度的关系如图所示。
图中M点对应的速率(对应温度
 )
)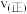
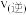 (填“>”、“<”或“=”),温度高于
(填“>”、“<”或“=”),温度高于 ,NO转化率降低的原因可能是
,NO转化率降低的原因可能是(3)在密闭容器中充入
 和
和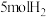 ,发生反应:
,发生反应: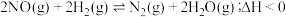 。平衡时NO的体积分数随温度、压强的变化关系如图。
。平衡时NO的体积分数随温度、压强的变化关系如图。
①下列物理量中,图中d点大于b点的是
A.正反应速率 B.逆反应速率
C.
 的浓度 D.对应温度的平衡常数
的浓度 D.对应温度的平衡常数②c点NO的平衡转化率为
③若在M点对反应容器升温的同时扩大容器体积使体系压强减小,重新达到的平衡状态可能是图中a、b、c、d中的
(4)
 时,向容积为2L的恒容容器中充入
时,向容积为2L的恒容容器中充入 、
、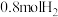 ,发生反应:
,发生反应: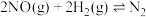
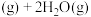 ,体系的总压强P随时间t的变化如下表所示:
,体系的总压强P随时间t的变化如下表所示: | 0 | 10 | 20 | 30 | 40 |
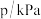 | 240 | 226 | 216 | 210 | 210 |
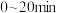 内该反应的平均反应速率
内该反应的平均反应速率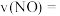
 。
。②该温度下反应的平衡常数

 (用平衡分压代替平衡浓度,平衡分压=总压×物质的量分数,列出计算式即可)。
(用平衡分压代替平衡浓度,平衡分压=总压×物质的量分数,列出计算式即可)。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】研究CO2的回收利用既可变废为宝,又可减少碳的排放。回答下列问题;
二甲醚(CH3OCH3)被誉为“21世纪的清洁燃料,由CO2和H2制备二甲醚的反应原理如下:
反应Ⅰ:
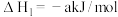 (a>0)
(a>0)
反应Ⅱ: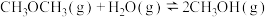
 (b>0)
(b>0)
反应Ⅲ:

(1) =
=_______ kJ/mol,据此判断反应Ⅲ在_______ (填“低温”、“高温”或“任意温度”)条件下能自发进行。
(2)恒温恒压条件下,在密闭容器中通入等物质的量的CO2和H2发生反应I,能说明反应I达到平衡状态的是_______ (填字母序号)。
a.平衡常数保持不变 b.生成3molH—H键的同时断裂1molC—O键
c.容器内混合气体的密度保持不变 d.CO2和H2O的物质的量之比保持不变
(3)T1℃时,将1mol二甲醚充入某恒容密闭容器中,发生如下分解反应:
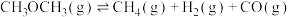 ,在不同时间测定容器内的总压,所得数据见下表:
,在不同时间测定容器内的总压,所得数据见下表:
由表中数据计算:反应达平衡时,二甲醚的分解率为_______ ,该温度下的平衡常数
_______  (
( 为用气体平衡分压代替气体平衡浓度表示的平衡常数,分压=总压×气体的物质的量分数)。
为用气体平衡分压代替气体平衡浓度表示的平衡常数,分压=总压×气体的物质的量分数)。
(4)恒压下将CO2和氢气按体积比1:3混合,在不同催化剂作用下发生反应I和反应Ⅲ,在相同的时间段内CH3OH的选择性和产率随温度的变化如下图。其中:CH3OH的选择性=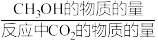 ×100%
×100%

①在上述条件下,结合图象分析,合成甲醇的最佳温度是_______ ,最佳催化剂是_______ 。
②温度高于230℃,CH3OH产率随温度升高而下降的原因是_______ 。
二甲醚(CH3OCH3)被誉为“21世纪的清洁燃料,由CO2和H2制备二甲醚的反应原理如下:
反应Ⅰ:

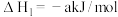 (a>0)
(a>0)反应Ⅱ:
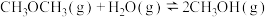
 (b>0)
(b>0)反应Ⅲ:


(1)
 =
=(2)恒温恒压条件下,在密闭容器中通入等物质的量的CO2和H2发生反应I,能说明反应I达到平衡状态的是
a.平衡常数保持不变 b.生成3molH—H键的同时断裂1molC—O键
c.容器内混合气体的密度保持不变 d.CO2和H2O的物质的量之比保持不变
(3)T1℃时,将1mol二甲醚充入某恒容密闭容器中,发生如下分解反应:
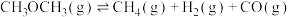 ,在不同时间测定容器内的总压,所得数据见下表:
,在不同时间测定容器内的总压,所得数据见下表:| 反应时间t/min | 0 | 5 | 10 | 15 | 20 |  |
| 气体总压p总/kPa | p0 | 1.4p0 | 1.6p0 | 1.8p0 | 1.9p0 | 2p0 |

 (
( 为用气体平衡分压代替气体平衡浓度表示的平衡常数,分压=总压×气体的物质的量分数)。
为用气体平衡分压代替气体平衡浓度表示的平衡常数,分压=总压×气体的物质的量分数)。(4)恒压下将CO2和氢气按体积比1:3混合,在不同催化剂作用下发生反应I和反应Ⅲ,在相同的时间段内CH3OH的选择性和产率随温度的变化如下图。其中:CH3OH的选择性=
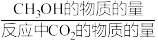 ×100%
×100%
①在上述条件下,结合图象分析,合成甲醇的最佳温度是
②温度高于230℃,CH3OH产率随温度升高而下降的原因是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】 常用于玻璃、陶瓷中作染色剂,含铝合金钢具有韧性好、高温塑性强等优点,可用于制造机床结构部件。工业上常用铝钒混合矿(主要成分为
常用于玻璃、陶瓷中作染色剂,含铝合金钢具有韧性好、高温塑性强等优点,可用于制造机床结构部件。工业上常用铝钒混合矿(主要成分为 、
、 ,还含
,还含 、
、 、
、 、
、 等杂质)提取高熔点金属单质钼和
等杂质)提取高熔点金属单质钼和 ,其工艺流程如图所示。
,其工艺流程如图所示。 、
、 、
、 、
、 和
和 均可与纯碱反应生成对应的钠盐,而
均可与纯碱反应生成对应的钠盐,而 不行。
不行。
②“气体X”为混合气体,经处理后得“气体Y”。
③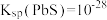 ,
, ,
,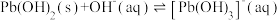
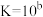 。
。
④“滤渣Ⅳ”主要成分是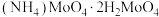 。
。
回答下列问题:
(1)“焙烧”时,采用逆流式投料,且分批加入铝钒混合矿、碳酸钠粉末,其目的是_______ , 参与反应的化学方程式为
参与反应的化学方程式为_______ 。
(2)“气体X”经洗气操作可获得较纯净的“气体Y”,洗气时选择的试剂是_______ ,“滤渣Ⅲ”的主要成分是_______ (填化学式)。
(3)“沉铅”过程中,总反应为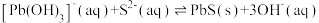 则该反应的平衡常数
则该反应的平衡常数
_______ 。
(4)“沉钒”后,经过滤、洗涤、干燥,将所得固体进行煅烧,当固体质量减少16.8t时,理论上制得 的质量为
的质量为_______ t。
(5)“滤渣Ⅳ”中需要加入稍过量的 还原
还原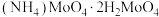 制
制 ,加入稍过量
,加入稍过量 的原因是
的原因是_______ 。
 常用于玻璃、陶瓷中作染色剂,含铝合金钢具有韧性好、高温塑性强等优点,可用于制造机床结构部件。工业上常用铝钒混合矿(主要成分为
常用于玻璃、陶瓷中作染色剂,含铝合金钢具有韧性好、高温塑性强等优点,可用于制造机床结构部件。工业上常用铝钒混合矿(主要成分为 、
、 ,还含
,还含 、
、 、
、 、
、 等杂质)提取高熔点金属单质钼和
等杂质)提取高熔点金属单质钼和 ,其工艺流程如图所示。
,其工艺流程如图所示。
 、
、 、
、 、
、 和
和 均可与纯碱反应生成对应的钠盐,而
均可与纯碱反应生成对应的钠盐,而 不行。
不行。②“气体X”为混合气体,经处理后得“气体Y”。
③
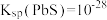 ,
, ,
,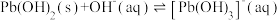
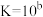 。
。④“滤渣Ⅳ”主要成分是
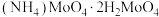 。
。回答下列问题:
(1)“焙烧”时,采用逆流式投料,且分批加入铝钒混合矿、碳酸钠粉末,其目的是
 参与反应的化学方程式为
参与反应的化学方程式为(2)“气体X”经洗气操作可获得较纯净的“气体Y”,洗气时选择的试剂是
(3)“沉铅”过程中,总反应为
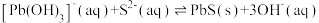 则该反应的平衡常数
则该反应的平衡常数
(4)“沉钒”后,经过滤、洗涤、干燥,将所得固体进行煅烧,当固体质量减少16.8t时,理论上制得
 的质量为
的质量为(5)“滤渣Ⅳ”中需要加入稍过量的
 还原
还原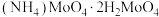 制
制 ,加入稍过量
,加入稍过量 的原因是
的原因是
您最近一年使用:0次



