(1)将下列符合要求的组别字母填入相应位置
A.O2和O3 B.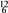 C和
C和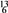 C C.CH3CH2CH2CH3和
C C.CH3CH2CH2CH3和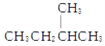
D. E.CH3CH2CH2CH3和
E.CH3CH2CH2CH3和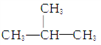
①___________ 组两种微粒互为同位素。②__________ 组两种物质互为同素异形体。
③___________ 组两种物质属于同系物。④___________ 组两物质互为同分异构体。
⑤___________ 组两物质是同一物质。
(2)一定温度下,将3 molA气体和1mol B气体通入一容积固定为2L的密闭容器中,发生如下反应:3A(g)+B(g) xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为
xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为__________________ ;X为________ ;若反应经2min达到平衡,平衡时C的浓度________ 0.8mol/L(填“大于,小于或等于”)。
A.O2和O3 B.
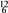 C和
C和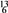 C C.CH3CH2CH2CH3和
C C.CH3CH2CH2CH3和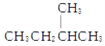
D.
 E.CH3CH2CH2CH3和
E.CH3CH2CH2CH3和
①
③
⑤
(2)一定温度下,将3 molA气体和1mol B气体通入一容积固定为2L的密闭容器中,发生如下反应:3A(g)+B(g)
 xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为
xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为
更新时间:2017-06-16 20:15:21
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】氢气是未来非常理想的能源,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O 2H2+O2。制得的氢气可用于燃料电池、合成氨工业。回答下列问题:
2H2+O2。制得的氢气可用于燃料电池、合成氨工业。回答下列问题:
(1)分解海水时,________ 能转变为________ 能。生成的氢气用于燃料电池时,________ 能转变为________ 能。
(2)某种氢氧燃料电池是用NaOH溶液作电解质,正极的电极反应式为________ ;若把燃料改为甲烷,负极的电极反应式为________ 。
(3)氢气可用于合成氨。一定温度下,向2L 的密闭容器中加入1 molN2和 3molH2发生反应 N2(g)+3H2(g) 2NH3(g),2min时测得N2的浓度为0.3mol/L,5min时达到平衡,此时测得压强为开始时的
2NH3(g),2min时测得N2的浓度为0.3mol/L,5min时达到平衡,此时测得压强为开始时的 。则前2min用NH3表示的化学反应速率为
。则前2min用NH3表示的化学反应速率为________ ;平衡时,N2的转化率为________ ,混合气体的平均相对分子质量为________ 。
 2H2+O2。制得的氢气可用于燃料电池、合成氨工业。回答下列问题:
2H2+O2。制得的氢气可用于燃料电池、合成氨工业。回答下列问题:(1)分解海水时,
(2)某种氢氧燃料电池是用NaOH溶液作电解质,正极的电极反应式为
(3)氢气可用于合成氨。一定温度下,向2L 的密闭容器中加入1 molN2和 3molH2发生反应 N2(g)+3H2(g)
 2NH3(g),2min时测得N2的浓度为0.3mol/L,5min时达到平衡,此时测得压强为开始时的
2NH3(g),2min时测得N2的浓度为0.3mol/L,5min时达到平衡,此时测得压强为开始时的 。则前2min用NH3表示的化学反应速率为
。则前2min用NH3表示的化学反应速率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】I.工业上用丙烯加成法制备1,2-二氯丙烷(CH2ClCHClCH3),主要副产物为3-氯丙烯,反应原理为:
①CH2=CHCH3(g)+Cl2(g) CH2ClCHClCH3(g) ΔH1=-134 kJ·mol-1
CH2ClCHClCH3(g) ΔH1=-134 kJ·mol-1
②CH2=CHCH3(g)+Cl2(g) CH2=CHCH2Cl(g)+HCl(g) ΔH2=-102 kJ·mol-1
CH2=CHCH2Cl(g)+HCl(g) ΔH2=-102 kJ·mol-1
(1)一定温度下,向恒容密闭容器中充入等物质的量的CH2=CHCH3(g)和Cl2(g),在催化剂作用下发生反应①②,容器内气体的压强随时间的变化如下表所示。
用单位时间内气体分压的变化来表示反应速率,即v=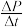 ,则反应①前180 min内平均反应速率v(CH2ClCHClCH3)=
,则反应①前180 min内平均反应速率v(CH2ClCHClCH3)=_______ kPa·min-1(保留小数点后2位)。
II.丙烯的制备方法
方法一:丙烷无氧脱氢法制备丙烯反应:C3H8(g) C3H6(g)+H2(g) ΔH=+124 kJ·mol-1
C3H6(g)+H2(g) ΔH=+124 kJ·mol-1
(2)①某温度下,在刚性容器中充入C3H8,起始压强为10 kPa,平衡时总压强为14 kPa,C3H8的平衡转化率为_______ 。该反应的平衡常数Kp=_______ kPa(保留小数点后2位)。
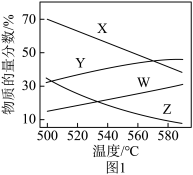
②总压分别为100 kPa和10 kPa时发生该反应,平衡体系中C3H8和C3H6的物质的量分数随温度变化关系如图1所示。_______ 、_______ 。
方法二:丙烷氧化脱氢法制备丙烯还生成CO、CO2等副产物,制备丙烯的反应: C3H8(g)+ O2(g)
O2(g)  C3H6(g)+H2O(g) ΔH=-118 kJ·mol-1,在催化剂的作用下C3H8的转化率和C3H6的产率随温度变化关系如图2所示。
C3H6(g)+H2O(g) ΔH=-118 kJ·mol-1,在催化剂的作用下C3H8的转化率和C3H6的产率随温度变化关系如图2所示。_______ ,观察图2,回答能提高C3H6选择性的措施是_______ 。(C3H6的选择性=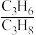 ×100%)
×100%)
①CH2=CHCH3(g)+Cl2(g)
 CH2ClCHClCH3(g) ΔH1=-134 kJ·mol-1
CH2ClCHClCH3(g) ΔH1=-134 kJ·mol-1②CH2=CHCH3(g)+Cl2(g)
 CH2=CHCH2Cl(g)+HCl(g) ΔH2=-102 kJ·mol-1
CH2=CHCH2Cl(g)+HCl(g) ΔH2=-102 kJ·mol-1(1)一定温度下,向恒容密闭容器中充入等物质的量的CH2=CHCH3(g)和Cl2(g),在催化剂作用下发生反应①②,容器内气体的压强随时间的变化如下表所示。
| 时间/min | 0 | 60 | 120 | 180 | 240 | 300 | 360 |
| 压强/kPa | 80 | 74.2 | 69.4 | 65.2 | 61.6 | 57.6 | 57.6 |
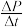 ,则反应①前180 min内平均反应速率v(CH2ClCHClCH3)=
,则反应①前180 min内平均反应速率v(CH2ClCHClCH3)=II.丙烯的制备方法
方法一:丙烷无氧脱氢法制备丙烯反应:C3H8(g)
 C3H6(g)+H2(g) ΔH=+124 kJ·mol-1
C3H6(g)+H2(g) ΔH=+124 kJ·mol-1(2)①某温度下,在刚性容器中充入C3H8,起始压强为10 kPa,平衡时总压强为14 kPa,C3H8的平衡转化率为
②总压分别为100 kPa和10 kPa时发生该反应,平衡体系中C3H8和C3H6的物质的量分数随温度变化关系如图1所示。
方法二:丙烷氧化脱氢法制备丙烯还生成CO、CO2等副产物,制备丙烯的反应: C3H8(g)+
 O2(g)
O2(g)  C3H6(g)+H2O(g) ΔH=-118 kJ·mol-1,在催化剂的作用下C3H8的转化率和C3H6的产率随温度变化关系如图2所示。
C3H6(g)+H2O(g) ΔH=-118 kJ·mol-1,在催化剂的作用下C3H8的转化率和C3H6的产率随温度变化关系如图2所示。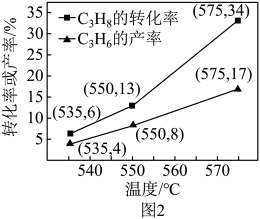
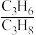 ×100%)
×100%)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】我国提出2030年实现“碳达峰”,2060年实现“碳中和”,CO2的再利用成为热门话题。工业上可用CO2来生产燃料甲醇(CH3OH,无色液体),实验室模拟该过程,在体积为2L的密闭容器中,充入2mol CO2和6mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示:
CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示:
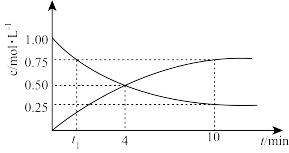
(1)t1时刻,正、逆反应速率大小:v(正)_______ (填“>”“=”或“<”)v(逆),达到平衡的点为_______ 时刻(填选项)。
a.t1 b.4min c.10min
(2)在0min到4min时间段,v(H2)=_______ mol·L-1·min-1;从开始到平衡,CH3OH的平均反应速率v(CH3OH)=_______ mol·L-1·min-1。
(3)下列措施能增大反应速率的是_______(填字母)。
(4)能说明上述反应达到平衡状态的是_______ (填字母)。
a.3v正(H2)=v逆(CH3OH)
b.H2的体积分数不再变化
c.容器内气体的压强不随时间的变化而变化
d.单位时间内,每生成1mol CH3OH,同时生成3mol H2
e.c(CO2):c(H2):c(CH3OH):c(H2O)=1:3:1:1
 CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示:
CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示:
(1)t1时刻,正、逆反应速率大小:v(正)
a.t1 b.4min c.10min
(2)在0min到4min时间段,v(H2)=
(3)下列措施能增大反应速率的是_______(填字母)。
| A.升高温度 | B.扩大容器体积 | C.充入一定量氦气 | D.加入催化剂 |
a.3v正(H2)=v逆(CH3OH)
b.H2的体积分数不再变化
c.容器内气体的压强不随时间的变化而变化
d.单位时间内,每生成1mol CH3OH,同时生成3mol H2
e.c(CO2):c(H2):c(CH3OH):c(H2O)=1:3:1:1
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
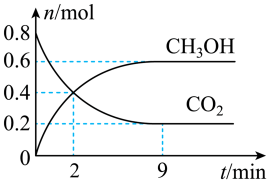
【推荐1】某温度下CO2加氢制甲醇的的总反应为CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),该反应为放热反应,在固定容积为2.0 L的密闭容器中充入0.8 mol的CO2和2.4 mol的H2,测得CO2和CH3OH的物质的量随时间变化如图。
(1)对于该反应,反应物的化学键断裂要吸收的能量_______ (填“大于”、“小于”或“等于”)生成物的化学键形成要放出的能量。
(2)下列措施能加快反应速率的是_______ (填序号,下同)。
A.往容器中充入N2
B.往容器充入H2
C.及时分离出CH3OH
D.减小容器体积
E.选择高效的催化剂
(3)2 min内CH3OH的反应速率为_______ ,2 min末时v正_______ v逆(填“<”“>”或“=”)。
(4)恒温恒容条件下,能说明反应已达平衡状态的是_______ 。
A.CO2(g)体积分数保持不变
B.容器中气体压强保持不变
C.容器中CH3OH浓度与H2O浓度之比为1∶1
D.混合气体的密度保持不变
E.H2的生成速率是H2O生成速率的3倍
(5)该反应平衡时CO2的转化率为_______ 。
(6)甲醇是优质的清洁燃料,可制作碱性甲醇燃料电池,其工作原理如图所示,其总反应式为:2CH3OH+3O2+4OH−=2 +6H2O,则电极A的反应式为
+6H2O,则电极A的反应式为_______ 。
(1)对于该反应,反应物的化学键断裂要吸收的能量
(2)下列措施能加快反应速率的是
A.往容器中充入N2
B.往容器充入H2
C.及时分离出CH3OH
D.减小容器体积
E.选择高效的催化剂
(3)2 min内CH3OH的反应速率为
(4)恒温恒容条件下,能说明反应已达平衡状态的是
A.CO2(g)体积分数保持不变
B.容器中气体压强保持不变
C.容器中CH3OH浓度与H2O浓度之比为1∶1
D.混合气体的密度保持不变
E.H2的生成速率是H2O生成速率的3倍
(5)该反应平衡时CO2的转化率为
(6)甲醇是优质的清洁燃料,可制作碱性甲醇燃料电池,其工作原理如图所示,其总反应式为:2CH3OH+3O2+4OH−=2
 +6H2O,则电极A的反应式为
+6H2O,则电极A的反应式为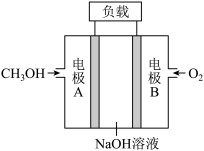
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】通过以下示例分析是哪些因素影响了化学反应速率?
(1)Na 、Mg分别与水反应时,钠与水反应更为剧烈;_______
(2)带火星的木条能在纯氧中复燃;_______
(3)新鲜水果和食物保存在冰箱里能存放得更久;_______
(4)实验室用H2O2制氧气时,使用二氧化锰作催化剂反应更快;_______
(5)木材劈得小一些烧得更快。_______
(1)Na 、Mg分别与水反应时,钠与水反应更为剧烈;
(2)带火星的木条能在纯氧中复燃;
(3)新鲜水果和食物保存在冰箱里能存放得更久;
(4)实验室用H2O2制氧气时,使用二氧化锰作催化剂反应更快;
(5)木材劈得小一些烧得更快。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某化学课外小组的同学,通过实验室制备铁和稀盐酸的反应探究外界条件对化学反应速率的影响,下表是实验过程中的数据及相关信息:
(注:气体体积均在相同条件下测得)
(1)实验①和②表明,________ 对反应速率有影响;实验①和③表明________ 对反应速率的影响。
(2)实验室在制氢气时,可在锌和盐酸反应的容器中加入少量硫酸铜固体,原因是________ 。(用文字表达)
(3)若四组实验均反应进行1分钟(铁有剩余),则以上实验需要测出的数据是________ 。
序号 | 反应温度/℃ | c(HCl)/(mol·L-1) | V(HCl)/mL | 10 g Fe的形状 | t/min |
① | 20 | 2 | 10 | 块状 | 1 |
② | 20 | 4 | 10 | 块状 | 1 |
③ | 20 | 2 | 10 | 粉末 | 1 |
④ | 40 | 2 | 10 | 粉末 | 1 |
⑤ | 40 | 4 | 10 | 粉末 | 1 |
(1)实验①和②表明,
(2)实验室在制氢气时,可在锌和盐酸反应的容器中加入少量硫酸铜固体,原因是
(3)若四组实验均反应进行1分钟(铁有剩余),则以上实验需要测出的数据是
您最近一年使用:0次
【推荐1】已知:①O2和O3 ②CH3CH3和CH3CH2CH2CH3 ③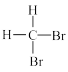 和
和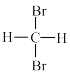 ④金刚石和石墨 ⑤氕、氘和氚 ⑥CH3CH2CH2CH2CH(CH3)CH3和CH3CH2CH(CH3)CH(CH3)CH3
④金刚石和石墨 ⑤氕、氘和氚 ⑥CH3CH2CH2CH2CH(CH3)CH3和CH3CH2CH(CH3)CH(CH3)CH3
(1)上述各组物质属于同位素的是____ ,属于同素异形体的是____ ,属于同系物的是____ ,属于同分异构体的是____ ,属于同种物质的是____ 。(以上各空均填序号)
(2)烷烃的通式为____ 。
(3)相对分子质量为58的烷烃的分子式为____ ,写出它所有同分异构体的结构简式____ 。
(4)分子式为C5H12的烷烃,其一氯代物只有一种,该烷烃的结构简式为____ 。
 和
和 ④金刚石和石墨 ⑤氕、氘和氚 ⑥CH3CH2CH2CH2CH(CH3)CH3和CH3CH2CH(CH3)CH(CH3)CH3
④金刚石和石墨 ⑤氕、氘和氚 ⑥CH3CH2CH2CH2CH(CH3)CH3和CH3CH2CH(CH3)CH(CH3)CH3(1)上述各组物质属于同位素的是
(2)烷烃的通式为
(3)相对分子质量为58的烷烃的分子式为
(4)分子式为C5H12的烷烃,其一氯代物只有一种,该烷烃的结构简式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】有下列8种有机物:① ;②
;② ;③
;③ ;④
;④ ;⑤
;⑤ ;⑥
;⑥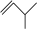 ;⑦
;⑦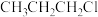 ;⑧
;⑧ 。回答下列问题:
。回答下列问题:
(1)上述有机物中,互为同分异构体的是___________ (填标号,下同);互为同系物的是___________ ;属于醚类的是___________ 。
(2)⑧的化学名称为___________ 。
(3)⑤在稀硫酸、加热条件下反应的化学方程式为___________ ,该反应中稀硫酸的作用为___________ ,该反应的反应类型为___________ 。
(4)一定条件下,①可形成一种高分子化合物(R),R的结构简式为___________ 。
 ;②
;② ;③
;③ ;④
;④ ;⑤
;⑤ ;⑥
;⑥ ;⑦
;⑦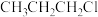 ;⑧
;⑧ 。回答下列问题:
。回答下列问题:(1)上述有机物中,互为同分异构体的是
(2)⑧的化学名称为
(3)⑤在稀硫酸、加热条件下反应的化学方程式为
(4)一定条件下,①可形成一种高分子化合物(R),R的结构简式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】将下列物质进行分类(填序号):①O2与O3;② C与
C与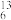 C;③H2O和D2O;④冰与干冰;⑤H2、D2、T2;⑥乙醇与甲醚(CH3-O-CH3);⑦CH3CH2CH2CH2CH3和CH3(CH2)3CH3
C;③H2O和D2O;④冰与干冰;⑤H2、D2、T2;⑥乙醇与甲醚(CH3-O-CH3);⑦CH3CH2CH2CH2CH3和CH3(CH2)3CH3
(1)互为同位素的是_______ ;
(2)互为同素异形体的是_______ ;
(3)互为同分异构体的是_______ ;
(4)属于同一化合物的是_______ 。
(5)下列各图均能表示甲烷的分子结构,按要求回答下列问题。
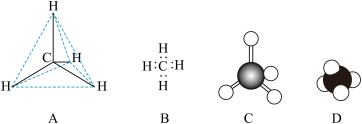
①甲烷的球棍模型是_______ ,甲烷的电子式是_______ (填序号)。
②写出甲烷在氧气中燃烧的化学方程式:_______
③相对分子质量为30的烷烃的分子式是_______ 。
④甲烷与丙烷互为_________
A.同位素 B.同素异形体 C.同系物 D.同分异构体
 C与
C与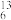 C;③H2O和D2O;④冰与干冰;⑤H2、D2、T2;⑥乙醇与甲醚(CH3-O-CH3);⑦CH3CH2CH2CH2CH3和CH3(CH2)3CH3
C;③H2O和D2O;④冰与干冰;⑤H2、D2、T2;⑥乙醇与甲醚(CH3-O-CH3);⑦CH3CH2CH2CH2CH3和CH3(CH2)3CH3(1)互为同位素的是
(2)互为同素异形体的是
(3)互为同分异构体的是
(4)属于同一化合物的是
(5)下列各图均能表示甲烷的分子结构,按要求回答下列问题。

①甲烷的球棍模型是
②写出甲烷在氧气中燃烧的化学方程式:
③相对分子质量为30的烷烃的分子式是
④甲烷与丙烷互为
A.同位素 B.同素异形体 C.同系物 D.同分异构体
您最近一年使用:0次



