如图所示,已知A元素的最低化合价为-3价,D元素和B元素可形成2种化合物。试回答下列问题(均用具体的元素符号回答):
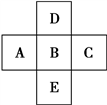
(1)写出它们的元素符号:
A______ ,B________ ,C__________ ,D_______ ;
(2)A、B、C、D的气态氢化物稳定性最差的是_____ ;
(3)A、B、C的原子半径由小到大的顺序是_________ ;
(4)A、B、C三元素最高价氧化物对应水化物的酸性由强到弱的顺序是:_____ ;
(5)用化学方程式表示元素C的非金属性大于B元素;__________ 。

(1)写出它们的元素符号:
A
(2)A、B、C、D的气态氢化物稳定性最差的是
(3)A、B、C的原子半径由小到大的顺序是
(4)A、B、C三元素最高价氧化物对应水化物的酸性由强到弱的顺序是:
(5)用化学方程式表示元素C的非金属性大于B元素;
更新时间:2017-09-07 10:50:18
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题。
(1)写出下列元素的符号②____ ③____ ⑥____ ⑧___ ⑩___ 。
(2)非金属性最强的元素是___ ,化合物种类最多的元素是___ 。(填元素符号)
(3)第三周期元素除⑩外原子半径最小的是___ ,元素①-⑨中原子半径最大的是___ 。(填元素符号)
(4)这些元素的最高价氧化物对应水化物中碱性最强的是___ ,具有两性的是___ 。(填化学式)
(5)写出⑤的最高价氧化物对应的水化物与⑧的最高价氧化物的水化物反应的化学反应方程式___ 。
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)写出下列元素的符号②
(2)非金属性最强的元素是
(3)第三周期元素除⑩外原子半径最小的是
(4)这些元素的最高价氧化物对应水化物中碱性最强的是
(5)写出⑤的最高价氧化物对应的水化物与⑧的最高价氧化物的水化物反应的化学反应方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】有X、Y、Z、M、R、Q六种短周期的主族元素,部分信息如下表所示:
请回答下列问题:
(1)R在元素周期表中的位置是_____ 。
(2)M元素简单氢化物的结构式为_____ 。
(3)Z、M、Q的简单离子的半径由大到小的顺序为_____ (用离子符号表示)
(4)由元素X、M、Z组成的化合物所含的化学键类型为_____ 。写出 的电子式
的电子式_____ 。
(5)物质的量各0.1mol的Z单质和Q单质,分别与100mL0.1mol/L的XR溶液反应,生成气体在相同条件下的体积之比为_____ 。
(6)下列事实能作为比较元素Y与R的非金属性相对强弱依据的是_____(选填字母序号)
(7)用电子式表示ZR的形成过程_____ 。
(8)写出R的单质与Z的最高价氧化物对应水化物的水溶液反应的离子方程式_____ 。
| X | Y | Z | M | R | Q | |
| 原子半径/nm | 0.186 | 0.074 | 0.099 | 0.160 | ||
| 主要化合价 | -4、+4 | -2 | -1、+7 | |||
| 其它信息 | 某种核素无中子 | 常用的半导体材料 | 短周期主族元素中原子半径最大 | 次外层电子数是最外层电子数的4倍 |
(1)R在元素周期表中的位置是
(2)M元素简单氢化物的结构式为
(3)Z、M、Q的简单离子的半径由大到小的顺序为
(4)由元素X、M、Z组成的化合物所含的化学键类型为
 的电子式
的电子式(5)物质的量各0.1mol的Z单质和Q单质,分别与100mL0.1mol/L的XR溶液反应,生成气体在相同条件下的体积之比为
(6)下列事实能作为比较元素Y与R的非金属性相对强弱依据的是_____(选填字母序号)
| A.常温下Y的单质呈固态,R的单质呈气态 |
B.稳定性: |
| C.Y与R形成的化合物中Y呈正价 |
D.酸性 |
(8)写出R的单质与Z的最高价氧化物对应水化物的水溶液反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】随原子序数的递增,八种短周期元素原子半径的相对大小、最高正价或最低负价的变化如图所示,根据判断出的元素回答问题:
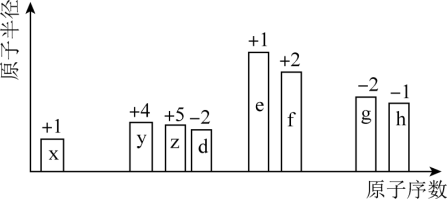
(1)g在元素周期表中的位置是_______ 。
(2)元素y的一种核素可测定文物年代,该核素的符号为_______ 。
(3)在上述元素中,原子半径最大的是_______ (填元素名称),e、f、d三元素形成的简单离子,它们的离子半径由大到小顺序是 用离子符号表示
用离子符号表示
_______ 。
(4)元素g与元素h相比,非金属性较强的是_______ (填元素符号),下列表述中能证明这一事实的是_______ (填序号)。
a.常温下g的单质和h的单质状态不同
b.h的气态氢化物比g的气态氢化物稳定
c.h的最高价氧化物的水化物酸性比g的最高价氧化物的水化物酸性强
(5)f、h 两种元素组成的化合物的电子式为:_______ 。
(6)在最高价氧化物对应的水化物中,酸性最强的化合物的化学式是_______  填化学式
填化学式 ,最高价氧化物对应的水化物是两性的元素是
,最高价氧化物对应的水化物是两性的元素是_______  填元素符号
填元素符号 ,写出它的氢氧化物与e的氢氧化物反应的离子方程式
,写出它的氢氧化物与e的氢氧化物反应的离子方程式_______ 。
(7)g、h两元素原子得电子能力较强的是_______ (元素符号),请从原子结构得角度解释其原因_______ 。

(1)g在元素周期表中的位置是
(2)元素y的一种核素可测定文物年代,该核素的符号为
(3)在上述元素中,原子半径最大的是
 用离子符号表示
用离子符号表示
(4)元素g与元素h相比,非金属性较强的是
a.常温下g的单质和h的单质状态不同
b.h的气态氢化物比g的气态氢化物稳定
c.h的最高价氧化物的水化物酸性比g的最高价氧化物的水化物酸性强
(5)f、h 两种元素组成的化合物的电子式为:
(6)在最高价氧化物对应的水化物中,酸性最强的化合物的化学式是
 填化学式
填化学式 ,最高价氧化物对应的水化物是两性的元素是
,最高价氧化物对应的水化物是两性的元素是 填元素符号
填元素符号 ,写出它的氢氧化物与e的氢氧化物反应的离子方程式
,写出它的氢氧化物与e的氢氧化物反应的离子方程式(7)g、h两元素原子得电子能力较强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表是元素周期表的一部分。
请回答下列问题。
(1)非金属性最强的元素名称为___________ ,它位于元素周期表中的位置___________ 。
(2)硅元素的原子结构示意图是____________ ,其最高价氧化物是____________ (填“酸性”或“碱性”)氧化物。
(3)硼酸(H3BO3)的酸性_________ (填“>” 或“<”)碳酸(H2CO3)的酸性,说明你判断的理由:__________________________ 。
(4)NH3的电子式为________________ ,它属于____________ (填“离子”或“共价”)化合物。NH3的还原性_________ (填“>” 或“<”)PH3的还原性。
(5)第三周期元素的最高价氧化物对应的水化物中,有一种物质既能与强酸反应又能与强碱反应,写出这种物质跟氢氧化钠溶液反应的化学方程式______________ 。
| H | He | ||||||
| Li | Be | B | C | N | O | F | Ne |
| Na | Mg | Al | Si | P | S | Cl | Ar |
(1)非金属性最强的元素名称为
(2)硅元素的原子结构示意图是
(3)硼酸(H3BO3)的酸性
(4)NH3的电子式为
(5)第三周期元素的最高价氧化物对应的水化物中,有一种物质既能与强酸反应又能与强碱反应,写出这种物质跟氢氧化钠溶液反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】如表为元素周期表的一部分,请回答有关问题:
(1)已知元素⑩的一种核素,其中子数为45,用原子符号表示该核素为___ 。
(2)由元素②和④形成的三核直线形分子的结构式为___ 。
(3)由上述元素①和④形成的一种绿色氧化剂的电子式为___ ,该化合物所含的化学键类型为___ (填“离子键”、“极性键”或“非极性键”)。
(4)若将元素④和⑤组成的一种淡黄色固体投入到含有下列离子的溶液中: 、
、 、
、 、Na+。反应完毕后,溶液中上述离子数目几乎不变的有
、Na+。反应完毕后,溶液中上述离子数目几乎不变的有__ (填离子符号)。
(5)能比较元素⑦和⑧非金属性强弱的实验事实是__ (填字母序号)。
a.⑦的氢化物的酸性比⑧的氢化物的酸性弱
b.⑧的单质R2与H2化合比⑦的单质Q与H2化合容易,且HR的稳定性比H2Q强
c.在⑦的氢化物H2Q的水溶液中通少量⑧的单质R2气体可置换出单质Q
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
(2)由元素②和④形成的三核直线形分子的结构式为
(3)由上述元素①和④形成的一种绿色氧化剂的电子式为
(4)若将元素④和⑤组成的一种淡黄色固体投入到含有下列离子的溶液中:
 、
、 、
、 、Na+。反应完毕后,溶液中上述离子数目几乎不变的有
、Na+。反应完毕后,溶液中上述离子数目几乎不变的有(5)能比较元素⑦和⑧非金属性强弱的实验事实是
a.⑦的氢化物的酸性比⑧的氢化物的酸性弱
b.⑧的单质R2与H2化合比⑦的单质Q与H2化合容易,且HR的稳定性比H2Q强
c.在⑦的氢化物H2Q的水溶液中通少量⑧的单质R2气体可置换出单质Q
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】金属镓(Ga)应用广泛,在半导体和光电材料、合金、磁性材料等领域都有重要应用。镓与铝是同主族元素,性质相似。
(1)铝在元素周期表中的位置是_________________ 。
(2)GaAs是共价化合物,一种重要的半导体材料。As 与 Ga 同周期,As 与 N 同主族。
①下列事实不能用元素周期律解释的是_______________ (填字母)。
a.碱性:Ga (OH)3> Al (OH)3
b.非金属性:As>Ga
c.酸性:H3AsO4>H3AsO3
②GaAs 中,As 元素化合价为-3 价,用原子结构理论解释 As 元素显负价的原因______________________________ 。
③废弃含 GaAs 半导体材料可以用浓硝酸溶解 GaAs,生成 H3AsO4 和 Ga3+,写出该反应的化学方程式________________________________________ 。
(1)铝在元素周期表中的位置是
(2)GaAs是共价化合物,一种重要的半导体材料。As 与 Ga 同周期,As 与 N 同主族。
①下列事实不能用元素周期律解释的是
a.碱性:Ga (OH)3> Al (OH)3
b.非金属性:As>Ga
c.酸性:H3AsO4>H3AsO3
②GaAs 中,As 元素化合价为-3 价,用原子结构理论解释 As 元素显负价的原因
③废弃含 GaAs 半导体材料可以用浓硝酸溶解 GaAs,生成 H3AsO4 和 Ga3+,写出该反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】现有部分短周期元素的性质或原子结构如表:
用化学用语回答下列问题:
(1)A元素在周期表中的位置__________________ ;
(2)C单质分子的结构式______________________ ;
(3)元素D与元素A相比,非金属性较强的是______ (用元素符号表示),下列表述中能证明这一事实的是 ______ (填选项序号)。
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A最高价含氧酸的酸性弱于D最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
(4)X是由A、B、C、D四种元素中的某种元素组成的单质,能经图所示的过程转化为(其他条件略去)。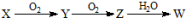
①若Y是有刺激性气味的无色气体,把Y通入BaCl2溶液中,无现象,然后滴加适量H2O2溶液,有白色沉淀生成,则该白色沉淀为_______________ ,试写出Y与H2O2溶液反应的化学方程式: __________________________________________ ;
②若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂物质的量之比为_________ 。
| 元素编号 | 元素性质或原子结构 |
| A | 有3个电子层,K、M层电子数之和等于L层电子数 |
| B | 短周期中金属性最强 |
| C | 常温下单质为双原子分子,氢化物的水溶液呈碱性 |
| D | 元素最高正价是+7价 |
(1)A元素在周期表中的位置
(2)C单质分子的结构式
(3)元素D与元素A相比,非金属性较强的是
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A最高价含氧酸的酸性弱于D最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
(4)X是由A、B、C、D四种元素中的某种元素组成的单质,能经图所示的过程转化为(其他条件略去)。
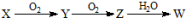
①若Y是有刺激性气味的无色气体,把Y通入BaCl2溶液中,无现象,然后滴加适量H2O2溶液,有白色沉淀生成,则该白色沉淀为
②若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】如图为元素周期表的一部分,请参照元素①~⑩在表中的位置,回答下列问题:
(1)元素⑩在周期表中的位置是_____ ,⑦的原子结构示意图为_____ 。
(2)④⑤⑥的简单离子半径由大到小的顺序为_____ (用离子符号和“>”表示)。
(3)④⑧⑨的气态氢化物中,最稳定的是_____ (用化学式表示)。
(4)④与⑥两种元素组成的化合物电子式为_____ 。
(5)用电子式表示⑥和⑨组成的化合物的形成过程:_____ 。
(6)第三周期中,原子半径(稀有气体元素除外)最小的元素是_____ ,非金属性最强的元素是_____ 。(填元素符号,下同),最高价氧化物对应水化物呈两性的元素是_____ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||||||||||||
| ⑩ |
(2)④⑤⑥的简单离子半径由大到小的顺序为
(3)④⑧⑨的气态氢化物中,最稳定的是
(4)④与⑥两种元素组成的化合物电子式为
(5)用电子式表示⑥和⑨组成的化合物的形成过程:
(6)第三周期中,原子半径(稀有气体元素除外)最小的元素是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表是元素周期表的一部分,表中每一个字母分别代表一种元素,请从A~J这十种元素中选择适当的元素回答下列问题。
(1)物质熔沸点比较: BD2_______ HD2; A2D_______ A2I。 (填“>”、“=”或“<”):
(2)物质的键角比较: A2D_______ CA3; A2D_______ DK2(填“>”、“=”或“<”):
(3)B、C、D三种元素电负性由大到小的顺序_______ (用对应元素的符号表示);E、F、G三种元素第一电离能由大到小的顺序_______ (用对应元素的符号表示)
(4)D、E、 J的离子半径由大到小的顺序为_______ 。(用所对应元素的离子符号表示);B、H、I的最高价含氧酸的酸性由强到弱的顺序是_______ 。(用化学式表示)
(5)A、C、D三种元素形成的一种离子化合物的化学式_______ 。
(6)I的氧化物与J的单质溶于水反应生成两种强酸的方程式_______ 。
| 族 周期 | IA | 0 | ||||||
| 1 | A | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | B | C | D | K | ||||
| 3 | E | F | G | H | I | J |
(2)物质的键角比较: A2D
(3)B、C、D三种元素电负性由大到小的顺序
(4)D、E、 J的离子半径由大到小的顺序为
(5)A、C、D三种元素形成的一种离子化合物的化学式
(6)I的氧化物与J的单质溶于水反应生成两种强酸的方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】化学学习和研究离不开元素周期表。下表为元素周期表的一部分,表中①-⑩分别代表一种元素。回答下列问题:
(1)上述元素中,有一种元素在自然界中形成的物质种类最多,该元素在周期表中的位置是_______ 。
(2)⑧、⑨、⑩元素的离子半径由大到小的顺序为________________ (用离子符号表示)。
(3)写出由①、⑥、⑧三种元素形成的一种离子化合物的电子式__________________ 。
(4)上述元素中有一种元素的氧化物和氢氧化物都有两性,面出该元素的原子结构示意图______________ ;高温条件下,该元素的单质与铁红能发生反应,此反应常用于野外焊接钢轨,则该反应的能量变化可用图__________________ 表示。(填“甲“或“乙”)

(5)已知W+X→Y+Z,且W、X、Y、Z分别是由①、⑤、⑥三种元素中的两种形成的10电子粒子,写出并配平上述反应式_________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ||
| 3 | ⑧ | ⑨ | ⑩ |
(2)⑧、⑨、⑩元素的离子半径由大到小的顺序为
(3)写出由①、⑥、⑧三种元素形成的一种离子化合物的电子式
(4)上述元素中有一种元素的氧化物和氢氧化物都有两性,面出该元素的原子结构示意图

(5)已知W+X→Y+Z,且W、X、Y、Z分别是由①、⑤、⑥三种元素中的两种形成的10电子粒子,写出并配平上述反应式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下表为周期表前20号元素中某些元素的有关数据:
试回答下列问题:(用对应的元素符号或物质的化学式表示)
(1)写出⑧的原子结构示意图:________ ;
(2)上述⑤、⑥、⑦号元素中某2种元素形成的化合物中,每一个原子都满足最外层为8电子稳定结构的物质可能是______ 、____ ;
(3)某元素R的原子半径为1.04×10-10m,该元素在周期表中的位置是___________ 。
(4)以上10种元素的原子中,还原性最强的是__________ (元素符号)。
(5)③、⑦、①、⑩四种元素形成的离子,其半径由小到大的顺序为___________ 。
| 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径(10-10m) | 1.86 | 1.52 | 0.66 | 0.53 | 0.77 | 1.10 | 0.99 | 2.31 | 0.70 | 0.64 |
| 最高价态 | +1 | +1 | —— | +1 | +4 | +5 | +7 | +1 | +5 | —— |
| 最低价态 | —— | —— | -2 | -1 | -4 | -3 | -1 | —— | -3 | -1 |
试回答下列问题:(用对应的元素符号或物质的化学式表示)
(1)写出⑧的原子结构示意图:
(2)上述⑤、⑥、⑦号元素中某2种元素形成的化合物中,每一个原子都满足最外层为8电子稳定结构的物质可能是
(3)某元素R的原子半径为1.04×10-10m,该元素在周期表中的位置是
(4)以上10种元素的原子中,还原性最强的是
(5)③、⑦、①、⑩四种元素形成的离子,其半径由小到大的顺序为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】如图是元素周期表的一部分。表中所列的字母分别代表某一元素。

(1) mol A与
mol A与 的简单氢化物完全反应时可产生标准状况下气体的体积为
的简单氢化物完全反应时可产生标准状况下气体的体积为___________ 。
(2)写出 的最高价氧化物对应的水化物的化学式
的最高价氧化物对应的水化物的化学式___________ 。
(3)其中含元素E化合物是一种白色胶状沉淀,可用于净水,则该物质的化学式为___________ ; 与
与 的氢氧化物水溶液反应的化学方程式为
的氢氧化物水溶液反应的化学方程式为___________ 。C的简单氢化物的电子式___________ 。
(4) 、E、F、
、E、F、 形成的简单离子半径由大到小顺序(用离子符合表示)
形成的简单离子半径由大到小顺序(用离子符合表示)___________ 。

(1)
 mol A与
mol A与 的简单氢化物完全反应时可产生标准状况下气体的体积为
的简单氢化物完全反应时可产生标准状况下气体的体积为(2)写出
 的最高价氧化物对应的水化物的化学式
的最高价氧化物对应的水化物的化学式(3)其中含元素E化合物是一种白色胶状沉淀,可用于净水,则该物质的化学式为
 与
与 的氢氧化物水溶液反应的化学方程式为
的氢氧化物水溶液反应的化学方程式为(4)
 、E、F、
、E、F、 形成的简单离子半径由大到小顺序(用离子符合表示)
形成的简单离子半径由大到小顺序(用离子符合表示)
您最近一年使用:0次



