题型:填空题
难度:0.65
引用次数:201
题号:5571498
当前材料科学的发展方兴未艾。B、N、Ti、Fe都是重要的材料元素,其单质及化合物在诸多领域中都有广泛的应用。
(1)基态Fe2+的电子排布式为_____________________________
(2)BF3分子空间结构为___________ ;在NH3中N原子的杂化方式为_______ 。
(3)科学家目前合成了N4分子,结合等电子体相关内容判断该分子中N—N键的键角为__________ 。
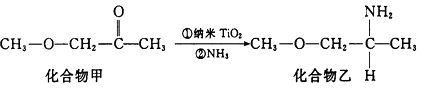
(4)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下图所示。化合物乙的沸点明显高于化合物甲,主要原因是_________________________________________
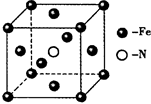
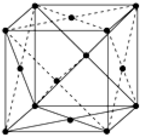
(5)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构如右上图所示。若该晶体的密度是ρ g·cm-3,则两个最近的Fe原子间的距离为_____________ cm。(阿伏伽德罗常数用NA表示)
(1)基态Fe2+的电子排布式为
(2)BF3分子空间结构为
(3)科学家目前合成了N4分子,结合等电子体相关内容判断该分子中N—N键的键角为
(4)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下图所示。化合物乙的沸点明显高于化合物甲,主要原因是


(5)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构如右上图所示。若该晶体的密度是ρ g·cm-3,则两个最近的Fe原子间的距离为
更新时间:2017/11/04 21:45:13
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)Cu+基态核外电子排布式为__________ 。
(2)基态Fe原子有______ 个未成对电子,Fe3+的电子排布式为__________ 。
(3)S的基态原子核外有_____ 个未成对电子;Si的基态原子核外电子排布式为_______________ 。
(4)Cu的价层电子轨道示意图为_____ 。
(5)基态Si原子中,电子占据的最高能层符号为_____ ,该能层具有的原子轨道数为_____ ,电子数为_____ 。
(2)基态Fe原子有
(3)S的基态原子核外有
(4)Cu的价层电子轨道示意图为
(5)基态Si原子中,电子占据的最高能层符号为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】原子结构与性质
(1)元素As与N同族。As的氢化物沸点比NH3的___ (填“高”或“低”),其判断理由是______ 。
(2)铜原子在基态时的价电子排布式为______ 。
(3)Fe是人体需要补充的元素之一,试写出Fe2+的核外电子排布式:_____ 。与Al同一周期的Na、Mg元素也是人体所需元素,Na、Mg、Al基态原子第一电离能的大小关系____ 。某同学所画基态镁原子的核外电子排布图如图 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了______ 。
(4)K元素处于元素周期表的____ 区,其基态原子中,核外电子占据的电子云轮廓图为球形的能级有____ 个。
(1)元素As与N同族。As的氢化物沸点比NH3的
(2)铜原子在基态时的价电子排布式为
(3)Fe是人体需要补充的元素之一,试写出Fe2+的核外电子排布式:
 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了(4)K元素处于元素周期表的
您最近一年使用:0次
【推荐3】依据原子结构知识回答下列问题。
(1)下列有关说法错误的是_______。
(2)基态氟原子的第一电离能_______ 基态氮原子的第一电离能(填大于、小于或等于)的原因是_______ 。
(3)基态Mn2+的价电子排布式为_______ 。
(4)Li2O是离子晶体,其形成过程中的能量变化如图(a)所示。_______ kJ·mol-1,O=O键键能为_______ kJ·mol-1。
(1)下列有关说法错误的是_______。
| A.简单离子的还原性: P3->O2->F- |
| B.在元素周期表第二周期中元素原子的第一电离能介于硼和氮之间的元素有两种 |
| C.焰色试验与电子跃迁有关 |
| D.基态铝原子占据的最高能级的电子云轮廓图的形状为球形 |
(3)基态Mn2+的价电子排布式为
(4)Li2O是离子晶体,其形成过程中的能量变化如图(a)所示。
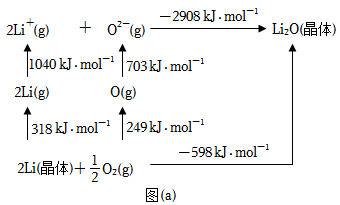
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】冰晶体不能形成最密堆积结构的原因是___________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】四种短周期主族元素W、X、Y、Z原子序数依次增大,请结合表中信息回答下列问题:
(1)Y元素在周期表中的位置为___________
(2)W与X可形成10电子分子A,也可形成10电子阳离子B,画出阳离子B的电子式______ ;W与Z在一定条件下可以形成极不稳定的原子个数比为1∶1的化合物,该化合物分子中既有极性键又有非极性键,写出该分子的结构式__________ 。
(3)工业上制粗Y的化学方程式为___________ 。
(4)在25℃、101kPa下,8.5g 在足量的氧气中完全燃烧后恢复至原状态,放出的热量为356.8kJ,写出表示
在足量的氧气中完全燃烧后恢复至原状态,放出的热量为356.8kJ,写出表示 燃烧热的热化学方程式
燃烧热的热化学方程式____________ 。
(5)元素As与X同族。As的简单氢化物分子为_________ (填“极性”成“非极性”)分子,其沸点比 的
的________ (填“高”或“低”),其判断理由是______________ 。
元素 | W | X | Y | Z |
| 结构或性质 | W的单质为密度最小的气体 | X的氢化物的水溶液显碱性 | Y的单质晶体是应用最广泛的半导体材料 | Z的单质为淡黄色固体,常存在于火山喷口附近 |
(2)W与X可形成10电子分子A,也可形成10电子阳离子B,画出阳离子B的电子式
(3)工业上制粗Y的化学方程式为
(4)在25℃、101kPa下,8.5g
 在足量的氧气中完全燃烧后恢复至原状态,放出的热量为356.8kJ,写出表示
在足量的氧气中完全燃烧后恢复至原状态,放出的热量为356.8kJ,写出表示 燃烧热的热化学方程式
燃烧热的热化学方程式(5)元素As与X同族。As的简单氢化物分子为
 的
的
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】甲醛是重要的化工原料,合理利用甲醛对工业生产和人们的生活有重要意义。已知甲烷分子的结构简式为HCHO,对甲醛的认识可以按照以下顺序:
Ⅰ.从空间结构认识甲醛
(1)甲醛分子的空间结构是_____ ,中心原子的杂化类型是_____ ,请用杂化轨道理论解释甲醛分子中的共价键类型_____ 。
Ⅱ.从分子结构认识甲醛的性质:蛋白质可以与甲醛发生反应而失活,所以37%的甲醛水溶液(福尔马林)是医学和畜牧业常用的杀菌防腐剂。
(2)请解释甲醛可溶于水的原因_____ 。
(3)蛋白质分子中的 可以与甲醛发生加成反应,但
可以与甲醛发生加成反应,但 很难与乙烯发生加成反应,说明
很难与乙烯发生加成反应,说明_____ 在影响物质的化学性质。
Ⅲ.从甲醛性质认识甲醛的回收利用
(4)活性炭主要由碳原子构成,可以吸附一定量的甲醛,但吸附效果一般。有同学提出可以通过化学反应,在活性炭表面引入一些基团来增加吸附效果,你认为可引入的基团有_____ 。
a. b.
b. c.
c.
Ⅰ.从空间结构认识甲醛
(1)甲醛分子的空间结构是
Ⅱ.从分子结构认识甲醛的性质:蛋白质可以与甲醛发生反应而失活,所以37%的甲醛水溶液(福尔马林)是医学和畜牧业常用的杀菌防腐剂。
(2)请解释甲醛可溶于水的原因
(3)蛋白质分子中的
 可以与甲醛发生加成反应,但
可以与甲醛发生加成反应,但 很难与乙烯发生加成反应,说明
很难与乙烯发生加成反应,说明Ⅲ.从甲醛性质认识甲醛的回收利用
(4)活性炭主要由碳原子构成,可以吸附一定量的甲醛,但吸附效果一般。有同学提出可以通过化学反应,在活性炭表面引入一些基团来增加吸附效果,你认为可引入的基团有
a.
 b.
b. c.
c.
您最近一年使用:0次
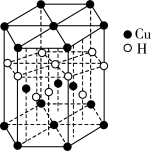
【推荐1】(1)Cu元素与H元素可形成一种红色化合物,其晶体结构单元如图所示。则该化合物的化学式为________ 。
(2)如图是由Q、R、G三种元素组成的一种高温超导体的晶胞结构,其中R为+2价,G为-2价,则Q的化合价为________ 。
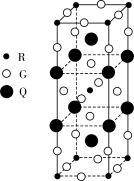
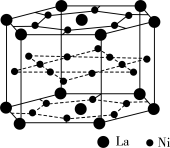
(3)已知镧镍合金LaNin的晶胞结构如图,则LaNin中n=________ 。
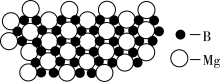
(4)硼化镁晶体在39 K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,下图是该晶体微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为________ 。
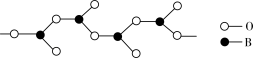
(5)在硼酸盐中,阴离子有链状、环状等多种结构形式。下图是一种链状结构的多硼酸根,则多硼酸根离子符号为________ 。
(6)Cu与F形成的化合物的晶胞结构如图所示,若晶体密度为a g·cm-3,则Cu与F最近距离为________ pm。(阿伏加 德罗常数用NA表示,列出计算表达式,不用化简;图中 为Cu,
为Cu, 为F)
为F)
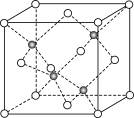
(7)如图为Na2S的晶胞,该晶胞与CaF2晶胞结构相似,设晶体密度是ρ g·cm-3,试计算Na+与S2-的最短距离为________ cm(阿伏加 德罗常数用NA表示 ,只写出计算式)。
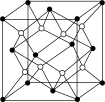
(8)用晶体的X射线衍射法对Cu的测定得到以下结果:Cu的晶胞为面心立方最密堆积(如图),已知该晶体的密度为9.00 g·cm-3,晶胞中该原子的配位数为________ ;Cu的原子半径为________ cm(阿伏加 德罗常数为NA,要求列式计算)。
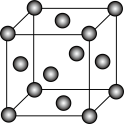
(9)Na和O能够形成化合物,其晶胞结构如图所示,晶胞参数a=0.566 nm,化合物的化学式为________ ;晶胞中A原子的配位数为________ ;列式计算晶体F的密度(g·cm-3 )_____ 。
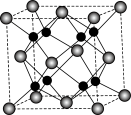
(10)下图所示的CaF2晶体中与Ca2+最近且等距离的F-数为________ ,已知,两个距离最近的Ca2+核间距离为a×10-8 cm,计算CaF2晶体的密度为________________ 。
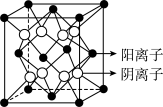
(11)Cu( )与Cl(
)与Cl( )形成的一种化合物的立方晶胞如图所示。该化合物的化学式为
)形成的一种化合物的立方晶胞如图所示。该化合物的化学式为________ ,已知晶胞参数a=0.542 nm,此晶体的密度为__________ g·cm-3。(写出计算式,不要求计算结果。阿伏加 德罗常数为NA)
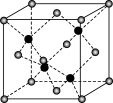
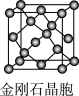
(12)金刚石晶胞含有________ 个碳原子。若碳原子半径为r,金刚石晶胞的边长为a,根据硬球接触模型,则r=______ a,列式表示碳原子在晶胞中的空间占有率_________ (不要求计算结果)。

(2)如图是由Q、R、G三种元素组成的一种高温超导体的晶胞结构,其中R为+2价,G为-2价,则Q的化合价为

(3)已知镧镍合金LaNin的晶胞结构如图,则LaNin中n=

(4)硼化镁晶体在39 K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,下图是该晶体微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为

(5)在硼酸盐中,阴离子有链状、环状等多种结构形式。下图是一种链状结构的多硼酸根,则多硼酸根离子符号为

(6)Cu与F形成的化合物的晶胞结构如图所示,若晶体密度为a g·cm-3,则Cu与F最近距离为
 为Cu,
为Cu, 为F)
为F)
(7)如图为Na2S的晶胞,该晶胞与CaF2晶胞结构相似,设晶体密度是ρ g·cm-3,试计算Na+与S2-的最短距离为

(8)用晶体的X射线衍射法对Cu的测定得到以下结果:Cu的晶胞为面心立方最密堆积(如图),已知该晶体的密度为9.00 g·cm-3,晶胞中该原子的配位数为

(9)Na和O能够形成化合物,其晶胞结构如图所示,晶胞参数a=0.566 nm,化合物的化学式为

(10)下图所示的CaF2晶体中与Ca2+最近且等距离的F-数为

(11)Cu(
 )与Cl(
)与Cl( )形成的一种化合物的立方晶胞如图所示。该化合物的化学式为
)形成的一种化合物的立方晶胞如图所示。该化合物的化学式为
(12)金刚石晶胞含有

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下图为几种晶体或晶胞的示意图:
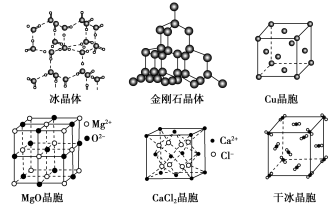
请回答下列问题:
(1)上述晶体中,粒子之间以共价键结合形成的晶体是___________ 。
(2)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为___________ 。
(3)NaCl晶胞与MgO晶胞相同,NaCl晶体的晶格能___________ (填“大于”或“小于”)MgO晶体。
(4)每个Cu晶胞中实际占有___________ 个Cu原子,晶胞中Cu原子配位数为___________ 。
(5)冰的熔点远高于干冰,除H2O是极性分子、CO2是非极性分子外,还有一个重要的原因是___________ 。

请回答下列问题:
(1)上述晶体中,粒子之间以共价键结合形成的晶体是
(2)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为
(3)NaCl晶胞与MgO晶胞相同,NaCl晶体的晶格能
(4)每个Cu晶胞中实际占有
(5)冰的熔点远高于干冰,除H2O是极性分子、CO2是非极性分子外,还有一个重要的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】甲醇(CH3OH)有很多用途。回答下列问题:
I.甲醇可用于制取甲醛(HCHO)。
(1)甲醇的沸点为64 ℃,甲醛的沸点为-21 ℃,甲醇的沸点较高的原因是__________ 。
(2)甲醇分子中采用sp3杂化的原子有____________ (填元素符号);甲醛分子中σ键与π键之比为_______ 。
II.直接甲醇燃料电池(DMFC)因其具有质量轻、体积小、结构简单、比能量密度高、低温操作等优点,DMFC阳极普遍采用以铂(Pt)为基础 的二元催化剂,如Pt-Cr合金等。
(3)基态Cr原子的未成对电子数为______________ 。
(4)与铬同周期的所有元素中基态原子最外层电子数与铬原子相同的元素是_______ 。(填元素符号)
(5)已知金属铂晶胞结构如图所示。催化剂的XRD图谱分析认为:当铂中掺入Cr原子后,Cr替代了晶胞面心位置上的Pt,该催化剂的化学式为_______ ,晶体中与1个Pt原子相紧邻的Cr原子有_____ 个。
(6)若铂原子半径为r pm,铂摩尔质量为M g·mol-1,铂晶体的密度为ρ g·cm-3,则阿伏伽德罗常数NA为_____ mol-1(用有关字母列出计算式即可)。
I.甲醇可用于制取甲醛(HCHO)。
(1)甲醇的沸点为64 ℃,甲醛的沸点为-21 ℃,甲醇的沸点较高的原因是
(2)甲醇分子中采用sp3杂化的原子有
II.直接甲醇燃料电池(DMFC)因其具有质量轻、体积小、结构简单、比能量密度高、低温操作等优点,DMFC阳极普遍采用以铂(Pt)为基础 的二元催化剂,如Pt-Cr合金等。
(3)基态Cr原子的未成对电子数为
(4)与铬同周期的所有元素中基态原子最外层电子数与铬原子相同的元素是
(5)已知金属铂晶胞结构如图所示。催化剂的XRD图谱分析认为:当铂中掺入Cr原子后,Cr替代了晶胞面心位置上的Pt,该催化剂的化学式为
(6)若铂原子半径为r pm,铂摩尔质量为M g·mol-1,铂晶体的密度为ρ g·cm-3,则阿伏伽德罗常数NA为
您最近一年使用:0次



