硒元素(selenium)是第四周期、VIA族元素,单质有红硒、黑硒和灰硒,其中灰硒有良好的导热导电性,且有显著的光电效应,可应用于光电半导体材料。请回答下列问题:
(1)Se原子的核外电子排布式为[Ar]___________ 。
(2)As和Se是同一周期的元素,As的第一电离能比Se大,原因是____________ 。
(3) 中Se―O的键角比SeO3的键角
中Se―O的键角比SeO3的键角_______ (填“大”或“小”),原因是____________________________________________ 。
(4)H2Se比H2S水溶液的酸性强,原因是__________________________________ 。
(5)灰硒的晶体为六方晶胞结构,原子排列为无限螺旋链,分布在六方晶格上,同一条链内原子作用很强,相邻链之间原子作用较弱,其螺旋链状图、晶胞结构图和晶胞俯视图如下。

①螺旋链中Se原子的杂化方式为______________ 。
②已知正六棱柱的边长为acm,高为bcm,阿伏伽德罗常数为NAmol-l,则该晶胞中含有的Se原子个数为__________ ,该晶体的密度为_____________ g/cm3(用含NA、a、b的式子表示)。
(1)Se原子的核外电子排布式为[Ar]
(2)As和Se是同一周期的元素,As的第一电离能比Se大,原因是
(3)
 中Se―O的键角比SeO3的键角
中Se―O的键角比SeO3的键角(4)H2Se比H2S水溶液的酸性强,原因是
(5)灰硒的晶体为六方晶胞结构,原子排列为无限螺旋链,分布在六方晶格上,同一条链内原子作用很强,相邻链之间原子作用较弱,其螺旋链状图、晶胞结构图和晶胞俯视图如下。

①螺旋链中Se原子的杂化方式为
②已知正六棱柱的边长为acm,高为bcm,阿伏伽德罗常数为NAmol-l,则该晶胞中含有的Se原子个数为
17-18高三上·四川成都·阶段练习 查看更多[2]
更新时间:2017-11-05 16:29:23
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
【推荐1】早期发现的一种天然二十面体准晶颗粒由Al、Ca、Cu、Fe 四种金属元素组成。
(1)基态 Fe原子有___________ 个未成对电子,Fe2+的价电子排布式为___________ 。
(2)配合物[Cu(NH3)4](OH)2中含有的化学键类型有___________ ,其中非金属元素电负性由大到小顺序是___________ ,配体是___________ ,配位原子最高能级的电子云轮廓图为___________ 。
(3)Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有___________ 个铜原子;金属铜采取如图甲所示堆积方式,可称为___________ 堆积。

(4)CaCl2熔点高于AlCl3的原因___________ 。
(5)CaF2晶胞如图乙所示,已知:氟化钙晶体密度为ρg·cm-3, NA代表阿伏加德罗常数的值。氟化钙晶体中Ca2+和F-之间最近核间距(d)为___________ cm(只要求列出计算式即可)。

(1)基态 Fe原子有
(2)配合物[Cu(NH3)4](OH)2中含有的化学键类型有
(3)Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有

(4)CaCl2熔点高于AlCl3的原因
(5)CaF2晶胞如图乙所示,已知:氟化钙晶体密度为ρg·cm-3, NA代表阿伏加德罗常数的值。氟化钙晶体中Ca2+和F-之间最近核间距(d)为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】Fritz Haber在合成氨领域的贡献距今已经110周年,氮族元素及其化合物应用广泛。
(1)在基态13N原子中,核外存在__________ 对自旋相反的电子,核外电子占据的最高能级的电子云轮廓图为__________ 形。
(2)根据价层电子对互斥理论,NH3、NO3-、NO2-中,中心原子价层电子对数不同于其他两种粒子的是________ ,与NO3-互为等电子体的分子为__________ 。液氨中存在电离平衡2NH3 NH4++NH2-,根据价层电子对互斥理论,可推知NH2-的空间构型为
NH4++NH2-,根据价层电子对互斥理论,可推知NH2-的空间构型为__________ ,液氨体系内,氮原子的杂化轨道类型为________ 。NH3比PH3更容易液化的原因为__________________ 。
(3)我国科学工作者实现世界首次全氮阴离子(N5-)金属盐Co(N5)2(H2O)4·4H2O的合成,其结构如图所示,可知N5-的化学键类型有______________ 。

(4)把特定物质的量之比的NH4Cl和HgCl2在密封管中一起加热时,生成晶体X,其晶胞的结构图及晶胞参数如图所示。则晶体X的化学式为__________ ,其晶体密度为__________ (设阿伏伽德罗常数的值为NA,列出计算式)g·cm-3。
(1)在基态13N原子中,核外存在
(2)根据价层电子对互斥理论,NH3、NO3-、NO2-中,中心原子价层电子对数不同于其他两种粒子的是
 NH4++NH2-,根据价层电子对互斥理论,可推知NH2-的空间构型为
NH4++NH2-,根据价层电子对互斥理论,可推知NH2-的空间构型为(3)我国科学工作者实现世界首次全氮阴离子(N5-)金属盐Co(N5)2(H2O)4·4H2O的合成,其结构如图所示,可知N5-的化学键类型有

(4)把特定物质的量之比的NH4Cl和HgCl2在密封管中一起加热时,生成晶体X,其晶胞的结构图及晶胞参数如图所示。则晶体X的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】钙钛矿(CaTiO3)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料。回答下列问题:
(1)Ti的基态原子的核外电子排布式为___________ 。
(2)Ti的四卤化物熔点如表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高;上述情况的原因是___________ 。
(3)CaTiO3的晶胞如图(a)所示,其组成元素的电负性大小顺序是___________ ;金属离子与氧离子间的作用力为___________ ,与Ca2+、Ti4+最近的O2﹣的数目分别是___________ 。
(4)一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I-和有机碱离子CH3NH ,其晶胞如图(b)所示。其中Pb2+与图(a)中
,其晶胞如图(b)所示。其中Pb2+与图(a)中___________ 的空间位置相同,有机碱CH3NH 中,N原子的杂化轨道类型是
中,N原子的杂化轨道类型是___________ ;若晶胞参数为anm,则晶体密度为___________ g•cm-3(列出计算式)。
(5)用上述金属卤化物光电材料制作的太阳能电池在使用过程中会产生单质铅和碘,降低了器件效率和使用寿命。我国科学家巧妙地在此材料中引入稀土铕(Eu)盐,提升了太阳能电池的效率和使用寿命,其作用原理如图(c)所示,用离子方程式表示该原理___________ 。

(1)Ti的基态原子的核外电子排布式为
(2)Ti的四卤化物熔点如表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高;上述情况的原因是
| 化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | -24.12 | 38.3 | 155 |
(3)CaTiO3的晶胞如图(a)所示,其组成元素的电负性大小顺序是
(4)一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I-和有机碱离子CH3NH
 ,其晶胞如图(b)所示。其中Pb2+与图(a)中
,其晶胞如图(b)所示。其中Pb2+与图(a)中 中,N原子的杂化轨道类型是
中,N原子的杂化轨道类型是(5)用上述金属卤化物光电材料制作的太阳能电池在使用过程中会产生单质铅和碘,降低了器件效率和使用寿命。我国科学家巧妙地在此材料中引入稀土铕(Eu)盐,提升了太阳能电池的效率和使用寿命,其作用原理如图(c)所示,用离子方程式表示该原理

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】I.新型储氢材料是开发利用氢能的重要研究方向,Ti(BH4)3是一种储氢材料,可由LiBH4和TiCl4反应制得。
(1)基态Cl原子有_______ 种运动状态的电子,属于_______ 区(填“s”或“p”或“d”或“f”);
(2)LiBH4由Li+和 构成,
构成, 的立体结构是
的立体结构是_______ ,与 互为等电子体的分子为
互为等电子体的分子为_______ ,Li、Be、B元素的第一电离能由大到小排列顺序为_______ ;
(3)某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
M是_______ (填元素符号)。
II.叠氮化合物是一类重要的化合物,其中氢叠氮酸(HN3)是一种弱酸,其分子结构可表示为H—N=N≡N,肼(N2H4)被亚硝酸氧化时便可得到氢叠氮酸(HN3),发生的反应为:N2H4+HNO2=2H2O+HN3。HN3的酸性和醋酸相近,可微弱电离出H+和 。试回答下列问题:
。试回答下列问题:
(4)下列有关说法正确的是_______(填序号);
(5)叠氮酸根能与许多金属离子等形成配合物,如[Co(N3)(NH3)5]SO4,在该配合物中钴显_______ 价;根据价层电子对互斥理论判断 的空间构型为
的空间构型为_______ ;
(6)与 互为等电子体的分子有
互为等电子体的分子有_______ (写两种即可)。
(1)基态Cl原子有
(2)LiBH4由Li+和
 构成,
构成, 的立体结构是
的立体结构是 互为等电子体的分子为
互为等电子体的分子为(3)某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
| I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 | I4/kJ·mol-1 | I5/kJ·mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
II.叠氮化合物是一类重要的化合物,其中氢叠氮酸(HN3)是一种弱酸,其分子结构可表示为H—N=N≡N,肼(N2H4)被亚硝酸氧化时便可得到氢叠氮酸(HN3),发生的反应为:N2H4+HNO2=2H2O+HN3。HN3的酸性和醋酸相近,可微弱电离出H+和
 。试回答下列问题:
。试回答下列问题:(4)下列有关说法正确的是_______(填序号);
| A.HN3中含有5个σ键 |
| B.HN3中的三个氮原子均采用sp2杂化 |
| C.HN3、HNO2、H2O、N2H4都是极性分子 |
| D.N2H4沸点高达113.5℃,说明肼分子间可形成氢键 |
 的空间构型为
的空间构型为(6)与
 互为等电子体的分子有
互为等电子体的分子有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】张亭栋研究小组受民间中医启发,发现As2O3(俗称砒霜)对白血病有明显的治疗作用。氮(N)、磷(P)、砷(As)等都是VA族的元素,该族元素的化合物在研究和生产中有许多重要用途。回答下列问题:
(1)N、P、As的第一电离能由大到小的顺序为___ ;基态As原子的核外电子排布式为___ 。
(2)NH3的沸点比PH3的___ (填“高”或低”),原因是___ 。
(3)Na3AsO4中含有的化学键类型包括___ ,AsO43-的空间构型为___ 。
(4)白磷(P4)晶体属于分子晶体,其晶胞结构如图所示(小圆圈表示白磷分子)。已知晶胞的边长为acm,阿伏加 德罗常数为NAmol-1,则该晶胞中含有的P原子的个数为___ ,该晶胞的密度为___ g·cm-3(用含NA、a的式子表示)。

(1)N、P、As的第一电离能由大到小的顺序为
(2)NH3的沸点比PH3的
(3)Na3AsO4中含有的化学键类型包括
(4)白磷(P4)晶体属于分子晶体,其晶胞结构如图所示(小圆圈表示白磷分子)。已知晶胞的边长为acm,阿伏加 德罗常数为NAmol-1,则该晶胞中含有的P原子的个数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】铁(Fe)、钴(Co)、镍(Ni)是第四周期第Ⅷ族的元素,在化学上称为铁系元素,其化合物在生产生活中应用广泛。
(1)铁系元素能与CO形成Fe(CO)5、Ni(CO)4等金属羰基化合物。已知室温时Fe(CO)5为浅黄色液体,沸点103℃,则Fe(CO)5中含有的化学键类型包括___________(填字母)。
(2)镍能形成多种配合物,如Ni(CO)4、[Ni(CN)4]2-、[Ni(NH3)6]2+等,下列有关说法正确的是________(填选项字母)。
(3)Fe、Co、Ni与Ca都位于第四周期且最外层电子数相同,但相应单质的熔点,Fe、Co、Ni明显高于Ca,其原因是___________ 。
(4)CoxNi(1-x)Fe2O4中Co、Ni的化合价都是+2,则Fe的化合价是___________ 。Fe3+比Fe2+更稳定的原因是___________ 。
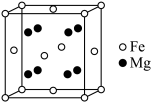
(5)铁镁合金储氢材料,晶胞结构如图所示,晶胞参数为apm,储氢后H原子以正八面体的配位模式有序分布在Fe原子的周围,H原子与Fe原子之间的最短距离为晶胞参数的 。储氢后晶体的化学式为
。储氢后晶体的化学式为___________ ,Mg原子占据Fe原子形成的___________ 空隙,两个H原子之间的最短距离为___________ 。
(1)铁系元素能与CO形成Fe(CO)5、Ni(CO)4等金属羰基化合物。已知室温时Fe(CO)5为浅黄色液体,沸点103℃,则Fe(CO)5中含有的化学键类型包括___________(填字母)。
| A.极性共价键 | B.离子键 | C.配位键 | D.金属键 |
(2)镍能形成多种配合物,如Ni(CO)4、[Ni(CN)4]2-、[Ni(NH3)6]2+等,下列有关说法正确的是________(填选项字母)。
| A.[Ni(NH3)6]2+中含有共价键和离子键 |
| B.CO与N2互为等电子体,其中CO分子内σ键和π键的个数比为1:2 |
| C.NH3中N原子为sp3杂化,其空间构型为正四面体形 |
| D.Ni2+在形成配合物时其配位数只能为4,Fe在形成配合物时其配位数只能为6 |
(3)Fe、Co、Ni与Ca都位于第四周期且最外层电子数相同,但相应单质的熔点,Fe、Co、Ni明显高于Ca,其原因是
(4)CoxNi(1-x)Fe2O4中Co、Ni的化合价都是+2,则Fe的化合价是
(5)铁镁合金储氢材料,晶胞结构如图所示,晶胞参数为apm,储氢后H原子以正八面体的配位模式有序分布在Fe原子的周围,H原子与Fe原子之间的最短距离为晶胞参数的
 。储氢后晶体的化学式为
。储氢后晶体的化学式为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐1】W、X、Y、Z为原子序数依次增大的前四周期元素,元素W是宇宙中最丰富的元素,元素X的原子最外层电子数是其内层的3倍,元素Z的基态原子核外电子有24种运动状态,Y、X、Z不在同一周期,且Y原子核外p电子比s电子多5个。
(1)Z基态原子的核外电子排布式为____________ 。
(2)Z的氧化物是石油化工中重要的催化剂之一,如催化异丙苯( )裂化生成苯和丙烯。
)裂化生成苯和丙烯。
①1 mol丙烯分子中含有σ键与π键的数目之比为________ 。
②苯分子中碳原子轨道的杂化类型为________ 。
③Z的一种氧化物ZO5中,Z的化合价为+6,则其中过氧键的数目为________ 个。
(3)W、X、Y三种元素的电负性由小到大的顺序为________ 。(请用元素符号回答)
(4)ZY3熔点为1152 ℃,熔融状态下能够导电,据此可判断ZY3晶体属于________ (填晶体类型)。
(1)Z基态原子的核外电子排布式为
(2)Z的氧化物是石油化工中重要的催化剂之一,如催化异丙苯(
 )裂化生成苯和丙烯。
)裂化生成苯和丙烯。①1 mol丙烯分子中含有σ键与π键的数目之比为
②苯分子中碳原子轨道的杂化类型为
③Z的一种氧化物ZO5中,Z的化合价为+6,则其中过氧键的数目为
(3)W、X、Y三种元素的电负性由小到大的顺序为
(4)ZY3熔点为1152 ℃,熔融状态下能够导电,据此可判断ZY3晶体属于
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表为元素周期表的一部分,a、b、c…为部分元素。回答下列问题:
(1)请写出上述元素d3+的核外电子排布式____________________ ;
(2)请写出e元素的原子电子轨道表示式_____________ ;
(3)ya3分子的电子式________ ,其分子的空间构型是____________ ;
(4)b、e两种元素中,金属性较强的是_______ ,第一电离能大的是___________ (填元素符号);
(5)h的i形成hi2分子杂化类型是____________ ;fh32-的空间构型为_____________ 。
| a | |||||||||||||||||
| f | y | h | i | ||||||||||||||
| b | e | j | |||||||||||||||
| c | d | g | l | ||||||||||||||
(1)请写出上述元素d3+的核外电子排布式
(2)请写出e元素的原子电子轨道表示式
(3)ya3分子的电子式
(4)b、e两种元素中,金属性较强的是
(5)h的i形成hi2分子杂化类型是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1) 分子中所有原子均满足8电子构型,
分子中所有原子均满足8电子构型, 分子中
分子中 键和
键和 键的个数比为
键的个数比为_______ ,中心原子的杂化方式为_______ 。
(2) 的分子结构如图所示,其中
的分子结构如图所示,其中 原子的杂化方式为
原子的杂化方式为_______ 。
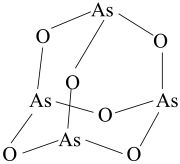
(3) 中,
中, 原子的杂化方式为
原子的杂化方式为_______ ;列举与 立体构型相同的一种离子和一种分子
立体构型相同的一种离子和一种分子_______ 、_______ (填化学式)。
(4)用价层电子对互斥理论推断 分子中,
分子中, 价层电子对数为
价层电子对数为_______ , 的VSEPR模型名称是
的VSEPR模型名称是_______ ;属于_______ 分子(填“极性”或“非极性”)分子中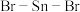 的键角
的键角_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(1)
 分子中所有原子均满足8电子构型,
分子中所有原子均满足8电子构型, 分子中
分子中 键和
键和 键的个数比为
键的个数比为(2)
 的分子结构如图所示,其中
的分子结构如图所示,其中 原子的杂化方式为
原子的杂化方式为
(3)
 中,
中, 原子的杂化方式为
原子的杂化方式为 立体构型相同的一种离子和一种分子
立体构型相同的一种离子和一种分子(4)用价层电子对互斥理论推断
 分子中,
分子中, 价层电子对数为
价层电子对数为 的VSEPR模型名称是
的VSEPR模型名称是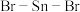 的键角
的键角 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】比亚迪采用磷酸亚铁锂技术的刀片电池,大幅度提高了电动汽车的续航里程。以硫铁矿(主要成分是 ,含少量
,含少量 、
、 和
和 )为原料制备
)为原料制备 的流程如下:
的流程如下:
请回答下列问题:
(1) 分子的空间结构为
分子的空间结构为_______ 形。基态Fe原子的电子排布式为_______ 。
(2)“还原”反应的离子方程式为_______ 。
(3)“试剂R”是一种绿色氧化剂,其中心原子杂化方式为_______ 。
(4)从平衡的角度解析加FeO“除铝”的原因(结合离子方程式说明)_______ 。
(5)常温下,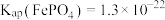 ,“沉铁”中为了使
,“沉铁”中为了使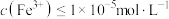 ,
,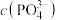 最小为
最小为_______  。
。
(6)流程中在“高温煅烧”条件下,由 制备
制备 的化学方程式为:
的化学方程式为:_______ 。
(7)磷酸亚铁锂的晶胞结构如图所示: 为阿伏加德罗常数,晶体密度为
为阿伏加德罗常数,晶体密度为_______  。
。
 ,含少量
,含少量 、
、 和
和 )为原料制备
)为原料制备 的流程如下:
的流程如下: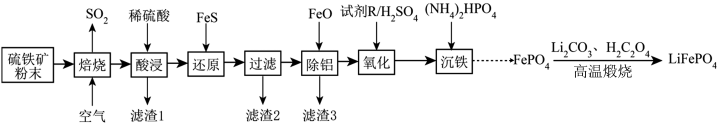
| 金属氢氧化物 |  |  |  |
| 开始沉淀的pH | 2.3 | 7.5 | 4.0 |
| 完全沉淀的pH | 4.1 | 9.7 | 5.2 |
(1)
 分子的空间结构为
分子的空间结构为(2)“还原”反应的离子方程式为
(3)“试剂R”是一种绿色氧化剂,其中心原子杂化方式为
(4)从平衡的角度解析加FeO“除铝”的原因(结合离子方程式说明)
(5)常温下,
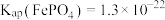 ,“沉铁”中为了使
,“沉铁”中为了使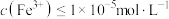 ,
,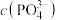 最小为
最小为 。
。(6)流程中在“高温煅烧”条件下,由
 制备
制备 的化学方程式为:
的化学方程式为:(7)磷酸亚铁锂的晶胞结构如图所示:
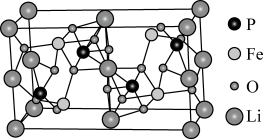
 为阿伏加德罗常数,晶体密度为
为阿伏加德罗常数,晶体密度为 。
。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】炼铅烟尘的主要成分为铅的氧化物(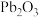 、
、 、
、 )及
)及 ,其杂质主要为含镉
,其杂质主要为含镉 化合物,回收处理炼铅烟尘可实现资源再生。某工艺流程如图:
化合物,回收处理炼铅烟尘可实现资源再生。某工艺流程如图:

已知:ⅰ. ;
;
ⅱ. 易溶于水,热稳定性好;
易溶于水,热稳定性好;
ⅲ. ;
;
 ;
;
ⅳ.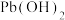 为两性氢氧化物。
为两性氢氧化物。
(1)步骤①中焙烧的目的是__________ 。在此过程中 与浓硫酸发生反应的化学方程式为
与浓硫酸发生反应的化学方程式为__________ 。
(2)滤液Ⅰ的主要成分是__________ 。
(3)相同反应时间,步骤①中焙烧温度和酸料比对 、
、 去除率的影响如下表所示(均未达到平衡状态):
去除率的影响如下表所示(均未达到平衡状态):
应选择的焙烧温度和酸料比为__________ 。
(4)步骤③中 溶液的作用是
溶液的作用是__________ 。
(5)步骤④的操作是__________ 。
(6)下列说法正确的是______(填字母)。
(7)一种立方钙钛矿结构的金属卤化物光电材料的组成为 、
、 和有机碱离子
和有机碱离子 ,其晶胞如图(b)所示。其中
,其晶胞如图(b)所示。其中 与图(a)中
与图(a)中__________ 的空间位置相同,若该光电材料的晶胞参数为 ,则其晶体密度为
,则其晶体密度为__________  (列出计算式)。
(列出计算式)。

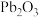 、
、 、
、 )及
)及 ,其杂质主要为含镉
,其杂质主要为含镉 化合物,回收处理炼铅烟尘可实现资源再生。某工艺流程如图:
化合物,回收处理炼铅烟尘可实现资源再生。某工艺流程如图:
已知:ⅰ.
 ;
;ⅱ.
 易溶于水,热稳定性好;
易溶于水,热稳定性好;ⅲ.
 ;
; ;
;ⅳ.
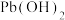 为两性氢氧化物。
为两性氢氧化物。(1)步骤①中焙烧的目的是
 与浓硫酸发生反应的化学方程式为
与浓硫酸发生反应的化学方程式为(2)滤液Ⅰ的主要成分是
(3)相同反应时间,步骤①中焙烧温度和酸料比对
 、
、 去除率的影响如下表所示(均未达到平衡状态):
去除率的影响如下表所示(均未达到平衡状态):焙烧温度/℃ | 各元素的去除率/% | 酸料比 | 各元素的去除率/% | ||
|
|
|
| ||
100 | 2.57 | 56.63 | 0.3 | 2.57 | 74.12 |
200 | 2.62 | 89.30 | 0.4 | 2.67 | 85.10 |
500 | 2.67 | 96.98 | 0.5 | 2.72 | 92.48 |
600 | 2.87 | 95.42 | 0.6 | 2.67 | 96.98 |
900 | 2.88 | 40.15 | 0.7 | 2.65 | 95.13 |
应选择的焙烧温度和酸料比为
(4)步骤③中
 溶液的作用是
溶液的作用是(5)步骤④的操作是
(6)下列说法正确的是______(填字母)。
| A.步骤①中浓硫酸作氧化剂 |
B.步骤③中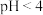 的目的是防止 的目的是防止 水解 水解 |
C.步骤④的滤液可循环利用以提高 的回收率 的回收率 |
D.步骤⑤中增大 溶液浓度可使 溶液浓度可使 沉淀完全 沉淀完全 |
 、
、 和有机碱离子
和有机碱离子 ,其晶胞如图(b)所示。其中
,其晶胞如图(b)所示。其中 与图(a)中
与图(a)中 ,则其晶体密度为
,则其晶体密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】如图所示是金刚石的晶胞结构,除顶点和面心上有碳原子外,4 条体对角线的  处还各有 1 个碳原子。回答下列问题:
处还各有 1 个碳原子。回答下列问题:___________ 。若金刚石的晶胞参数为a1pm ,则其中最近的两个碳原子之间的核间距为___________ pm (用含a1 的代数式表示)。
(2)面心立方ZnS 晶胞与金刚石的晶胞结构类似,阴、阳离子各占晶胞所含微粒数的一半。
①S 元素及其同周期的相邻元素第一电离能由小到大的顺序是___________ ;二氯化硫(SCl2 )分子中 S 原子的杂化轨道类型是___________ 。
②写出基态 Zn2+电子排布式:___________ 。___________ 个σ键。(易错)
④若该ZnS晶胞的晶胞参数为 a2pm,阿伏加德罗常数的值为NA ,则晶体的密度为___________ g.cm-3 (列出计算式)。
 处还各有 1 个碳原子。回答下列问题:
处还各有 1 个碳原子。回答下列问题:
(2)面心立方ZnS 晶胞与金刚石的晶胞结构类似,阴、阳离子各占晶胞所含微粒数的一半。
①S 元素及其同周期的相邻元素第一电离能由小到大的顺序是
②写出基态 Zn2+电子排布式:

④若该ZnS晶胞的晶胞参数为 a2pm,阿伏加德罗常数的值为NA ,则晶体的密度为
您最近一年使用:0次




