I.新型储氢材料是开发利用氢能的重要研究方向,Ti(BH4)3是一种储氢材料,可由LiBH4和TiCl4反应制得。
(1)基态Cl原子有_______ 种运动状态的电子,属于_______ 区(填“s”或“p”或“d”或“f”);
(2)LiBH4由Li+和 构成,
构成, 的立体结构是
的立体结构是_______ ,与 互为等电子体的分子为
互为等电子体的分子为_______ ,Li、Be、B元素的第一电离能由大到小排列顺序为_______ ;
(3)某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
M是_______ (填元素符号)。
II.叠氮化合物是一类重要的化合物,其中氢叠氮酸(HN3)是一种弱酸,其分子结构可表示为H—N=N≡N,肼(N2H4)被亚硝酸氧化时便可得到氢叠氮酸(HN3),发生的反应为:N2H4+HNO2=2H2O+HN3。HN3的酸性和醋酸相近,可微弱电离出H+和 。试回答下列问题:
。试回答下列问题:
(4)下列有关说法正确的是_______(填序号);
(5)叠氮酸根能与许多金属离子等形成配合物,如[Co(N3)(NH3)5]SO4,在该配合物中钴显_______ 价;根据价层电子对互斥理论判断 的空间构型为
的空间构型为_______ ;
(6)与 互为等电子体的分子有
互为等电子体的分子有_______ (写两种即可)。
(1)基态Cl原子有
(2)LiBH4由Li+和
 构成,
构成, 的立体结构是
的立体结构是 互为等电子体的分子为
互为等电子体的分子为(3)某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
| I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 | I4/kJ·mol-1 | I5/kJ·mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
II.叠氮化合物是一类重要的化合物,其中氢叠氮酸(HN3)是一种弱酸,其分子结构可表示为H—N=N≡N,肼(N2H4)被亚硝酸氧化时便可得到氢叠氮酸(HN3),发生的反应为:N2H4+HNO2=2H2O+HN3。HN3的酸性和醋酸相近,可微弱电离出H+和
 。试回答下列问题:
。试回答下列问题:(4)下列有关说法正确的是_______(填序号);
| A.HN3中含有5个σ键 |
| B.HN3中的三个氮原子均采用sp2杂化 |
| C.HN3、HNO2、H2O、N2H4都是极性分子 |
| D.N2H4沸点高达113.5℃,说明肼分子间可形成氢键 |
 的空间构型为
的空间构型为(6)与
 互为等电子体的分子有
互为等电子体的分子有
更新时间:2022-04-14 15:22:53
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】中科院大连化学物理研究所科学家用Ni-BaH3/Al2O3、Ni-LiH等作催化剂,实现了在常压、100~300℃的条件下合成氨,这一成果发表在《Nature Energy》杂志上。
(1)基态 的核外电子排布式为
的核外电子排布式为___________ ,若该离子核外电子空间运动状态有15种,则该离子处于___________ (填“基”或“激发”)态。
(2)氨在粮食生产、国防中有着无可替代的地位,也是重要的化工原料,可用于合成氨基酸、硝酸、TNT等。甘氨酸(NH2CH2COOH)是组成最简单的氨基酸,熔点为182℃,沸点为233℃。
①硝酸溶液中 的空间构型为
的空间构型为___________ 。
②甘氨酸的晶体类型是___________ ,其熔、沸点远高于相对分子质量几乎相等的丙酸(熔点为-21℃,沸点为141℃)的主要原因:一是甘氨酸能形成内盐;二是___________ 。
(3)比较NH3分子(前者)和在 中NH3(后者)分子中∠H-N-H的键角大小,前者
中NH3(后者)分子中∠H-N-H的键角大小,前者______ 后者。(填“>”、“<”或“=”)
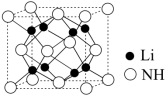
(4)亚氨基锂(Li2NH,摩尔质量为M g/mol),是一种储氢容量高、安全性能好的固体储氢材料,其晶胞结构如图所示,若晶胞参数为d pm,密度为ρ g/cm3,则阿伏加德罗常数
_______  (列出表达式)。
(列出表达式)。
(1)基态
 的核外电子排布式为
的核外电子排布式为(2)氨在粮食生产、国防中有着无可替代的地位,也是重要的化工原料,可用于合成氨基酸、硝酸、TNT等。甘氨酸(NH2CH2COOH)是组成最简单的氨基酸,熔点为182℃,沸点为233℃。
①硝酸溶液中
 的空间构型为
的空间构型为②甘氨酸的晶体类型是
(3)比较NH3分子(前者)和在
 中NH3(后者)分子中∠H-N-H的键角大小,前者
中NH3(后者)分子中∠H-N-H的键角大小,前者(4)亚氨基锂(Li2NH,摩尔质量为M g/mol),是一种储氢容量高、安全性能好的固体储氢材料,其晶胞结构如图所示,若晶胞参数为d pm,密度为ρ g/cm3,则阿伏加德罗常数

 (列出表达式)。
(列出表达式)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】N元素能形成多种化合物,它们之间可以发生相互转化,如:N2H4+HNO2=2H2O+HN3。请回答下列问题:
(1)N与O的电负性较小的是_____ 。
(2)N的基态原子的电子排布中,有____ 个运动状态不同的未成对电子。
(3)HNO2原子的杂化类型是____ 。
(4)NO 与钴盐通过配位键形成的[Co(NO2)6]3-能与K+结合生成黄色K3[Co(NO2)6]沉淀,此方法可用于检验溶液中的K+,写出该配合物中钴离子的电子排布式:
与钴盐通过配位键形成的[Co(NO2)6]3-能与K+结合生成黄色K3[Co(NO2)6]沉淀,此方法可用于检验溶液中的K+,写出该配合物中钴离子的电子排布式:____ 。
(1)N与O的电负性较小的是
(2)N的基态原子的电子排布中,有
(3)HNO2原子的杂化类型是
(4)NO
 与钴盐通过配位键形成的[Co(NO2)6]3-能与K+结合生成黄色K3[Co(NO2)6]沉淀,此方法可用于检验溶液中的K+,写出该配合物中钴离子的电子排布式:
与钴盐通过配位键形成的[Co(NO2)6]3-能与K+结合生成黄色K3[Co(NO2)6]沉淀,此方法可用于检验溶液中的K+,写出该配合物中钴离子的电子排布式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】CH4、NH3、H2O和HF均为含10e-的分子。
(1)C、N、O、F四种元素中,与C基态原子的核外未成对电子数相等的元素是_______ (写元素名称),其基态原子的核外电子排布式为_____________ 。
(2)C、N、O、F四种元素第电一离能由大到小的顺序是__________ (用元素符号表示)
(3)CH4、NH3和H2O分子中,从原子轨道的重叠方向来说.三种分子的中心原子的杂化轨道类型均为__________ 。
(4)CH4燃烧生成 CO、CO2和H2O
①在CO气流中轻微加热金属镍(Ni),生成无色挥发性液态Ni(CO)4, 423K时 Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉..试推测四碳基镍的晶体类型为_________ 。
②CO2、H2O和NH3反应生成(NH4)2CO3,根据电子对互斥理论知CO32-的空间构型为_____ 。
(5)CH4、H2O和HF三种物质中H2O的熔沸点最高,其原因是__________ 。
(6)硅晶体的结构跟金刚石的结构相似.而SiO2的结构相当于在硅晶体结构中每个硅与硅 化学键之间插入一个O原子。观察下图金刚石的结构,分析SiO2的空间结构中,Si,O形成的最小环上O原子的数目是_______________ 。

(1)C、N、O、F四种元素中,与C基态原子的核外未成对电子数相等的元素是
(2)C、N、O、F四种元素第电一离能由大到小的顺序是
(3)CH4、NH3和H2O分子中,从原子轨道的重叠方向来说.三种分子的中心原子的杂化轨道类型均为
(4)CH4燃烧生成 CO、CO2和H2O
①在CO气流中轻微加热金属镍(Ni),生成无色挥发性液态Ni(CO)4, 423K时 Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉..试推测四碳基镍的晶体类型为
②CO2、H2O和NH3反应生成(NH4)2CO3,根据电子对互斥理论知CO32-的空间构型为
(5)CH4、H2O和HF三种物质中H2O的熔沸点最高,其原因是
(6)硅晶体的结构跟金刚石的结构相似.而SiO2的结构相当于在硅晶体结构中每个硅与硅 化学键之间插入一个O原子。观察下图金刚石的结构,分析SiO2的空间结构中,Si,O形成的最小环上O原子的数目是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】已知四种短周期元素的原子序数的大小顺序为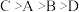 ;D和氢原子可形成4核10电子分子,该分子可使湿润的红色石器试纸变蓝:A、C同周期,B和C同主族;A与B可形成两种离子化合物
;D和氢原子可形成4核10电子分子,该分子可使湿润的红色石器试纸变蓝:A、C同周期,B和C同主族;A与B可形成两种离子化合物 、
、 ,氢原子与B可形成两种共价化合物
,氢原子与B可形成两种共价化合物 、
、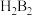 。试回答下列问题:
。试回答下列问题:
(1)C元素的元素符号为_____ ;写出A的电子排布式______ 。
(2)写出D元素形成的 分子的结构式
分子的结构式____ ,其中 键与
键与 键的数目比为
键的数目比为______ 。
(3)B、D元素的第一电离能大小关系为:B_______ D(填“<”或“>”)。
(4) 对应的水化物的碱性比
对应的水化物的碱性比
______ (填“强”或“弱”);写出 的电子式
的电子式________ 。
(5)化合物 、
、 它们结构与组成相似,热稳定性更强的是
它们结构与组成相似,热稳定性更强的是__________ (填化学式), 的沸点比
的沸点比 高得多的原因是
高得多的原因是_______________ 。
(6)下列选项能作为C元素和氧元素非金属性强弱比较的依据的是_________ 。
a.C的氧化物对应的水化物的酸性弱于盐酸
b.C元素的电负性小于氯的电负性
c.化学反应: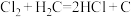
(7)B和C可以形成化合物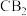 ,
,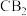 分子中空间结构为
分子中空间结构为___ (填“V型”成“直线型”)。中心原子C采用____ 杂化。
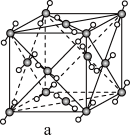
(8)元素B和铜原子形成的化合物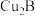 晶体结构可能是
晶体结构可能是______ (填字母)。
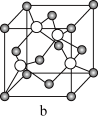
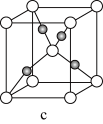
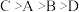 ;D和氢原子可形成4核10电子分子,该分子可使湿润的红色石器试纸变蓝:A、C同周期,B和C同主族;A与B可形成两种离子化合物
;D和氢原子可形成4核10电子分子,该分子可使湿润的红色石器试纸变蓝:A、C同周期,B和C同主族;A与B可形成两种离子化合物 、
、 ,氢原子与B可形成两种共价化合物
,氢原子与B可形成两种共价化合物 、
、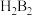 。试回答下列问题:
。试回答下列问题:(1)C元素的元素符号为
(2)写出D元素形成的
 分子的结构式
分子的结构式 键与
键与 键的数目比为
键的数目比为(3)B、D元素的第一电离能大小关系为:B
(4)
 对应的水化物的碱性比
对应的水化物的碱性比
 的电子式
的电子式(5)化合物
 、
、 它们结构与组成相似,热稳定性更强的是
它们结构与组成相似,热稳定性更强的是 的沸点比
的沸点比 高得多的原因是
高得多的原因是(6)下列选项能作为C元素和氧元素非金属性强弱比较的依据的是
a.C的氧化物对应的水化物的酸性弱于盐酸
b.C元素的电负性小于氯的电负性
c.化学反应:
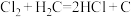
(7)B和C可以形成化合物
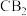 ,
,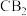 分子中空间结构为
分子中空间结构为(8)元素B和铜原子形成的化合物
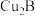 晶体结构可能是
晶体结构可能是


您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】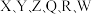 均为前四周期原子序数依次增大的六种元素,其中前4种为同周期相邻元素。
均为前四周期原子序数依次增大的六种元素,其中前4种为同周期相邻元素。 的基态原子
的基态原子 能级有1个未成对电子,
能级有1个未成对电子, 是周期表中族序数最大但核电荷数最小的,
是周期表中族序数最大但核电荷数最小的, 原子核内有29个质子。请回答(用相应元素符号表示):
原子核内有29个质子。请回答(用相应元素符号表示):
(1)2021年3月20日三星堆考古揭晓了最新发掘的大量珍贵文物,考古学家可利用 的一种核素来鉴定其年代,该核素的符号为
的一种核素来鉴定其年代,该核素的符号为___________ 。
(2)与 同周期的所有元素中,第一电离能大于Z的有
同周期的所有元素中,第一电离能大于Z的有___________ 种。
(3)请写一个能证明非金属性Q强于Z的化学反应方程式___________ 。
(4)Y的一种氢化物分子中共有18个电子,其电子式是___________ 。
(5) 离子的空间结构是
离子的空间结构是___________ ,中心原子的杂化方式是___________ ,与其互为等电子体的有___________ (任写一种分子和一种阳离子)。
(6)向 的硫酸盐中加入过量氨水,再加入一定乙醇,析出晶体的化学式是
的硫酸盐中加入过量氨水,再加入一定乙醇,析出晶体的化学式是___________ 。
(7) 元素位于周期表的
元素位于周期表的___________ 区,基态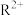 的价层电子轨道表示式是
的价层电子轨道表示式是___________ 。化合物 中与
中与 直接结合的原子是
直接结合的原子是 而不是
而不是 的可能原因是
的可能原因是___________ ,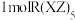 含有的
含有的 键数目是
键数目是___________ 。
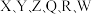 均为前四周期原子序数依次增大的六种元素,其中前4种为同周期相邻元素。
均为前四周期原子序数依次增大的六种元素,其中前4种为同周期相邻元素。 的基态原子
的基态原子 能级有1个未成对电子,
能级有1个未成对电子, 是周期表中族序数最大但核电荷数最小的,
是周期表中族序数最大但核电荷数最小的, 原子核内有29个质子。请回答(用相应元素符号表示):
原子核内有29个质子。请回答(用相应元素符号表示):(1)2021年3月20日三星堆考古揭晓了最新发掘的大量珍贵文物,考古学家可利用
 的一种核素来鉴定其年代,该核素的符号为
的一种核素来鉴定其年代,该核素的符号为(2)与
 同周期的所有元素中,第一电离能大于Z的有
同周期的所有元素中,第一电离能大于Z的有(3)请写一个能证明非金属性Q强于Z的化学反应方程式
(4)Y的一种氢化物分子中共有18个电子,其电子式是
(5)
 离子的空间结构是
离子的空间结构是(6)向
 的硫酸盐中加入过量氨水,再加入一定乙醇,析出晶体的化学式是
的硫酸盐中加入过量氨水,再加入一定乙醇,析出晶体的化学式是(7)
 元素位于周期表的
元素位于周期表的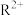 的价层电子轨道表示式是
的价层电子轨道表示式是 中与
中与 直接结合的原子是
直接结合的原子是 而不是
而不是 的可能原因是
的可能原因是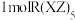 含有的
含有的 键数目是
键数目是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】Ⅰ、锂一磷酸氧铜电池正极的活性物质是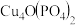 可通过下列反应制备:
可通过下列反应制备:
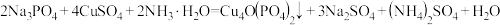 。
。
(1)写出基态 的电子排布式:
的电子排布式:___________ 。
(2)P、S元素第一电离能大小关系为___________ ,原因是___________ 。
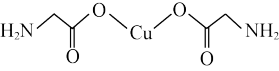
(3)氨基乙酸铜分子结构如图所示,碳原子的杂化方式为___________ ,基态碳原子核外电子有___________ 种运动状态。
(4)在硫酸铜溶液中加入过量KCN,生成配合物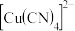 ,则1mol该配合物含有
,则1mol该配合物含有 键的数目为
键的数目为___________ ( 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
Ⅱ、苯的含氧衍生物A的相对分子质量为180,其中碳元素的质量分数为60%,A完全燃烧消耗 的物质的量与生成
的物质的量与生成 的物质的量相等。请回答下列问题:
的物质的量相等。请回答下列问题:
(5)A的分子式为___________ 。
(6)已知A的苯环上取代基彼此相间,A能发生银镜反应,也能与 溶液反应生成
溶液反应生成 ,还能与
,还能与 溶液发生显色反应,则A含有的官能团名称是
溶液发生显色反应,则A含有的官能团名称是___________ ,满足上述条件的A的结构可能有___________ 种。
(7)A的一种同分异构体B是邻位二取代苯,其中一个取代基是羧基。B能发生如图所示转化。
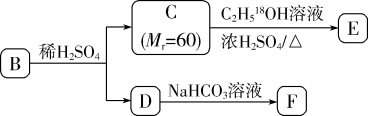
回答下列问题:
①C→E的反应类型为___________ 。
②D与浓溴水反应的主要产物的结构简式为___________ 。
③F可发生的化学反应类型有___________ (填字母)。
A取代反应B.加成反应C.消去反应D.加聚反应
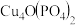 可通过下列反应制备:
可通过下列反应制备: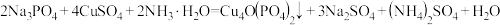 。
。(1)写出基态
 的电子排布式:
的电子排布式:(2)P、S元素第一电离能大小关系为
(3)氨基乙酸铜分子结构如图所示,碳原子的杂化方式为

(4)在硫酸铜溶液中加入过量KCN,生成配合物
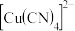 ,则1mol该配合物含有
,则1mol该配合物含有 键的数目为
键的数目为 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。Ⅱ、苯的含氧衍生物A的相对分子质量为180,其中碳元素的质量分数为60%,A完全燃烧消耗
 的物质的量与生成
的物质的量与生成 的物质的量相等。请回答下列问题:
的物质的量相等。请回答下列问题:(5)A的分子式为
(6)已知A的苯环上取代基彼此相间,A能发生银镜反应,也能与
 溶液反应生成
溶液反应生成 ,还能与
,还能与 溶液发生显色反应,则A含有的官能团名称是
溶液发生显色反应,则A含有的官能团名称是(7)A的一种同分异构体B是邻位二取代苯,其中一个取代基是羧基。B能发生如图所示转化。

回答下列问题:
①C→E的反应类型为
②D与浓溴水反应的主要产物的结构简式为
③F可发生的化学反应类型有
A取代反应B.加成反应C.消去反应D.加聚反应
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】氧缺位体(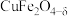 )是热化学循环分解水制氢的催化剂。一种以黄铜矿(主要成分是
)是热化学循环分解水制氢的催化剂。一种以黄铜矿(主要成分是 ,含
,含 、
、 等杂质)为原料制备
等杂质)为原料制备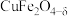 的流程如下:
的流程如下:
①酸浸后溶液中的金属离子有 、
、 、
、 和
和
②25°℃时已知几种金属离子沉淀的 如表所示:
如表所示:
回答下列问题:
(1) 位于元素周期表
位于元素周期表___________ 区。
(2) “焙烧”时生成三种氧化物(其中
“焙烧”时生成三种氧化物(其中 的氧化物形式为
的氧化物形式为 ),其化学方程式为
),其化学方程式为___________ 。
(3)加 “还原”的目的是
“还原”的目的是___________ 。
(4)滤渣2的主要成分为___________ 。
(5)已知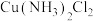 C有两种同分异构体,则“沉铁”过程中生成的
C有两种同分异构体,则“沉铁”过程中生成的 的空间构型是
的空间构型是___________ 。
(6)充分“煅烧”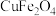 得到的氧缺位体(
得到的氧缺位体(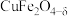 )的质量为原质量的98%,则
)的质量为原质量的98%,则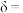
___________ 。
(7)氧缺位体分解水制氢分两步:
第一步___________ (完成方程式);
第二步: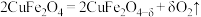 。
。
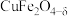 )是热化学循环分解水制氢的催化剂。一种以黄铜矿(主要成分是
)是热化学循环分解水制氢的催化剂。一种以黄铜矿(主要成分是 ,含
,含 、
、 等杂质)为原料制备
等杂质)为原料制备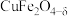 的流程如下:
的流程如下: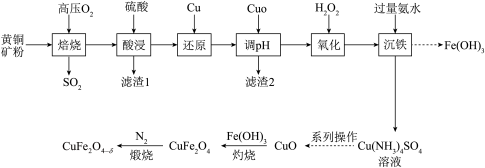
①酸浸后溶液中的金属离子有
 、
、 、
、 和
和
②25°℃时已知几种金属离子沉淀的
 如表所示:
如表所示:| 金属氢氧化物 |  |  |  |  |
开始沉淀的 | 1.9 | 3.4 | 6.4 | 7.0 |
完全沉淀的 | 3.2 | 4.7 | 7.6 | 9.0 |
(1)
 位于元素周期表
位于元素周期表(2)
 “焙烧”时生成三种氧化物(其中
“焙烧”时生成三种氧化物(其中 的氧化物形式为
的氧化物形式为 ),其化学方程式为
),其化学方程式为(3)加
 “还原”的目的是
“还原”的目的是(4)滤渣2的主要成分为
(5)已知
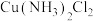 C有两种同分异构体,则“沉铁”过程中生成的
C有两种同分异构体,则“沉铁”过程中生成的 的空间构型是
的空间构型是(6)充分“煅烧”
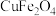 得到的氧缺位体(
得到的氧缺位体(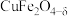 )的质量为原质量的98%,则
)的质量为原质量的98%,则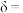
(7)氧缺位体分解水制氢分两步:
第一步
第二步:
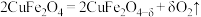 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】E、G、M、Q、T是五种原子序数依次增大的前四周期元素。E、G、M是位于p区的同一周期的元素,M的价层电子排布为ns2np2n,E与M原子核外的未成对电子数相等;QM2与GM2−具有相等的价电子总数;T为过渡元素,其原子核外没有未成对电子。请回答下列问题:
(1)T元素原子的价电子排布式是___ 。
(2)E、G、M三种元素的第一电离能由大到小的顺序为___ (用元素符号表示),其原因为___ 。
(3)G的最简单氢化物的分子立体构型名称为___ ,M的最简单氢化物的分子中中心原子的杂化类型为___ 。M和Q的最简单氢化物的沸点大小顺序为___ (写化学式)。
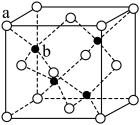
(4)TQ在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方TQ晶体结构如图所示,该晶体的密度为pg·cm−3。如果TQ的摩尔质量为Mg·mol−1,阿伏加 德罗常数为NAmol−1,则a、b之间的距离为___ cm。
(1)T元素原子的价电子排布式是
(2)E、G、M三种元素的第一电离能由大到小的顺序为
(3)G的最简单氢化物的分子立体构型名称为
(4)TQ在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方TQ晶体结构如图所示,该晶体的密度为pg·cm−3。如果TQ的摩尔质量为Mg·mol−1,阿伏加 德罗常数为NAmol−1,则a、b之间的距离为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】A、B、C、D、E为前四周期元素,且原子序数依次增大
(1)C元素的位置_______ ,E元素的价电子排布图为_______ 。
(2)B的氢化物由固体变为气态所需克服的微粒间的作用有_______ 。在二氧化碳分子中σ键和 键之比是
键之比是_______ 。
(3)A的简单氢化物的空间构型为_______ ,其中A原子的杂化方式:_______ 。
(4)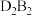 的电子式为
的电子式为_______ ,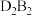 与
与 反应生成B的单质的化学方程式为:
反应生成B的单质的化学方程式为:_______ 。
(5)A和 形成的一种化合物的晶胞结构如图所示,该晶胞的化学式为
形成的一种化合物的晶胞结构如图所示,该晶胞的化学式为_______ 。若晶胞边长为 ,则该晶体的密度是
,则该晶体的密度是_______  。
。
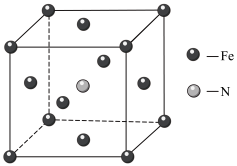
| A | 第二周期中一种非金属元素,第一电离能大于相邻元素 |
| B | 地壳中含量最多的元素, 轨道上有二个孤电子 轨道上有二个孤电子 |
| C | 与B同主族 |
| D | 前四周期中金属性最强的元素 |
| E | 前四周期中原子核外孤电子数最多 |
(2)B的氢化物由固体变为气态所需克服的微粒间的作用有
 键之比是
键之比是(3)A的简单氢化物的空间构型为
(4)
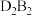 的电子式为
的电子式为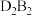 与
与 反应生成B的单质的化学方程式为:
反应生成B的单质的化学方程式为:(5)A和
 形成的一种化合物的晶胞结构如图所示,该晶胞的化学式为
形成的一种化合物的晶胞结构如图所示,该晶胞的化学式为 ,则该晶体的密度是
,则该晶体的密度是 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)根据价层电子对互斥理论,H2S、SO2、SO3的气态分中,中心原子价层电子对数不同于其他分子的是___________ 。气态三氧化硫以单分子形式存在,其分子的空间结构为___________ 形;固体三氧化硫中存在如图所示的三聚分子,该分子中S原子的杂化轨道类型为___________ 。

(2)分子中的大π键可用符号 表示,其中m代表参与形成大键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ),已知SO2分子中含有5对孤电子对,则SO2中的大π键应表示为
),已知SO2分子中含有5对孤电子对,则SO2中的大π键应表示为___________ 。SO2分子中键角∠OSO___________  中键角∠ONO(填“>”、“<”、“=”)。
中键角∠ONO(填“>”、“<”、“=”)。
(3)乙烯酮在室温下可聚合成二聚乙烯酮(结构简式为 ),二聚乙烯酮分子中含有的π键与σ键的数目之比为
),二聚乙烯酮分子中含有的π键与σ键的数目之比为___________ 。下图中表示的碳原子能量最高的是___________ (填字母)。
A. B.
B.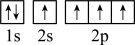
C. D.
D.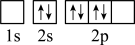
(4)三甲胺 和乙二胺
和乙二胺 均属于胺,但三甲胺比乙二胺的沸点低得多,原因是
均属于胺,但三甲胺比乙二胺的沸点低得多,原因是___________ 。C60的熔点比金刚石、石墨熔点低的原因是___________ 。
(5)在冰晶体中除氢键外,还存在范德华力 。已知冰的升华热是
。已知冰的升华热是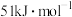 ,请估算冰中氢键的作用能为多少
,请估算冰中氢键的作用能为多少___________  。
。
(1)根据价层电子对互斥理论,H2S、SO2、SO3的气态分中,中心原子价层电子对数不同于其他分子的是

(2)分子中的大π键可用符号
 表示,其中m代表参与形成大键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ),已知SO2分子中含有5对孤电子对,则SO2中的大π键应表示为
),已知SO2分子中含有5对孤电子对,则SO2中的大π键应表示为 中键角∠ONO(填“>”、“<”、“=”)。
中键角∠ONO(填“>”、“<”、“=”)。(3)乙烯酮在室温下可聚合成二聚乙烯酮(结构简式为
 ),二聚乙烯酮分子中含有的π键与σ键的数目之比为
),二聚乙烯酮分子中含有的π键与σ键的数目之比为A.
 B.
B.
C.
 D.
D.
(4)三甲胺
 和乙二胺
和乙二胺 均属于胺,但三甲胺比乙二胺的沸点低得多,原因是
均属于胺,但三甲胺比乙二胺的沸点低得多,原因是(5)在冰晶体中除氢键外,还存在范德华力
 。已知冰的升华热是
。已知冰的升华热是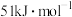 ,请估算冰中氢键的作用能为多少
,请估算冰中氢键的作用能为多少 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】我国科学家设计了一种钝化剂三氟乙脒来抑制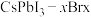 薄膜缺陷,提高无机钙钛矿太阳能电池的功率转换效率。回答下列问题:
薄膜缺陷,提高无机钙钛矿太阳能电池的功率转换效率。回答下列问题:
(1)基态碘原子的价层电子的运动状态有_______ 种,基态 原子的价层电子排布式为
原子的价层电子排布式为_______ 。
(2) 、
、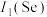 、
、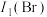 的第一电离能由大到小顺序为:
的第一电离能由大到小顺序为:_______ 。
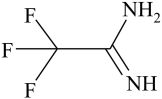
(3)①三氟乙脒的结构如图所示,碳原子的杂化类型为_______ ;测量 相对分子质量测量值经常偏大的原因是
相对分子质量测量值经常偏大的原因是_______ 。
②已知:F—F的键能为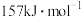 ,Br—Br的键能为
,Br—Br的键能为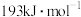 ,结合原子结构,对键能数据给予合理解释:
,结合原子结构,对键能数据给予合理解释:_______ 。
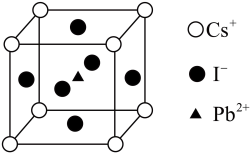
(4)某种金属卤化物无机钙钛矿的晶胞结构如图所示,晶胞的边长 ,晶体中
,晶体中 与
与 最短距离为
最短距离为_______ pm;晶体的密度
_______  (设阿伏加德罗常数的值为
(设阿伏加德罗常数的值为 ,用含a、
,用含a、 的代数式表示;可能用到相对原子质量:
的代数式表示;可能用到相对原子质量:
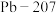
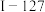 )
)
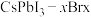 薄膜缺陷,提高无机钙钛矿太阳能电池的功率转换效率。回答下列问题:
薄膜缺陷,提高无机钙钛矿太阳能电池的功率转换效率。回答下列问题:(1)基态碘原子的价层电子的运动状态有
 原子的价层电子排布式为
原子的价层电子排布式为(2)
 、
、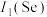 、
、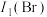 的第一电离能由大到小顺序为:
的第一电离能由大到小顺序为:(3)①三氟乙脒的结构如图所示,碳原子的杂化类型为
 相对分子质量测量值经常偏大的原因是
相对分子质量测量值经常偏大的原因是
②已知:F—F的键能为
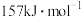 ,Br—Br的键能为
,Br—Br的键能为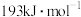 ,结合原子结构,对键能数据给予合理解释:
,结合原子结构,对键能数据给予合理解释:(4)某种金属卤化物无机钙钛矿的晶胞结构如图所示,晶胞的边长
 ,晶体中
,晶体中 与
与 最短距离为
最短距离为
 (设阿伏加德罗常数的值为
(设阿伏加德罗常数的值为 ,用含a、
,用含a、 的代数式表示;可能用到相对原子质量:
的代数式表示;可能用到相对原子质量:
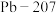
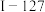 )
)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】宁德时代发布的NCM811是指正极材料中镍钴锰的含量比例为8:1:1的三元锂电池。
(1)基态镍原子的电子排布式为_______ ,基态锰原子有_______ 种能量不同的电子。
(2)Co3+可形成配合物[Co(N3)(NH3)5]Cl2,配位数为_______ ,配体中心原子的杂化类型为_______ ,1 mol该配合物中含有的σ键数目为_______ 。
(3)CO也是常见配体,CO中提供孤电子对的原子为_______ ,写出与CO互为等电子体的分子和离子各一种_______ 。
(4)镍、镁与碳构成的晶胞结构如图,该晶体的化学式为_______ ,与镁原子等距离且最近的镍原子个数为_______ ,已知该晶体密度为ρ g/cm3,NA为阿伏加德罗常数,则晶胞参数为_______ nm(列出计算式即可)。

(1)基态镍原子的电子排布式为
(2)Co3+可形成配合物[Co(N3)(NH3)5]Cl2,配位数为
(3)CO也是常见配体,CO中提供孤电子对的原子为
(4)镍、镁与碳构成的晶胞结构如图,该晶体的化学式为

您最近一年使用:0次



