E、G、M、Q、T是五种原子序数依次增大的前四周期元素。E、G、M是位于p区的同一周期的元素,M的价层电子排布为ns2np2n,E与M原子核外的未成对电子数相等;QM2与GM2−具有相等的价电子总数;T为过渡元素,其原子核外没有未成对电子。请回答下列问题:
(1)T元素原子的价电子排布式是___ 。
(2)E、G、M三种元素的第一电离能由大到小的顺序为___ (用元素符号表示),其原因为___ 。
(3)G的最简单氢化物的分子立体构型名称为___ ,M的最简单氢化物的分子中中心原子的杂化类型为___ 。M和Q的最简单氢化物的沸点大小顺序为___ (写化学式)。
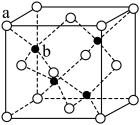
(4)TQ在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方TQ晶体结构如图所示,该晶体的密度为pg·cm−3。如果TQ的摩尔质量为Mg·mol−1,阿伏加 德罗常数为NAmol−1,则a、b之间的距离为___ cm。
(1)T元素原子的价电子排布式是
(2)E、G、M三种元素的第一电离能由大到小的顺序为
(3)G的最简单氢化物的分子立体构型名称为
(4)TQ在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方TQ晶体结构如图所示,该晶体的密度为pg·cm−3。如果TQ的摩尔质量为Mg·mol−1,阿伏加 德罗常数为NAmol−1,则a、b之间的距离为

更新时间:2019-12-28 11:26:16
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】按照要求完成填空(共计14分)。
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为__ ;其价层电子排布图为__ 。
(2)A-的电子排布式为1s22s22p63s23p6,第__ 周期第__ 族。
(3)B元素的正三价离子的3d能级为半充满,B的元素符号为__ ,其基态原子的电子排布式为__ ,检验该离子的方法是___ 。
(4)现向蓝色的硫酸铜溶液中,加入少量稀氨水,得到蓝色絮状沉淀,继续加入氨水后,蓝色沉淀溶解,得到深蓝色透明溶液,写出划线部分现象对应的离子方程式___ 。1mol[Cu(H2O)4]2+中含有___ molσ键。
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为
(2)A-的电子排布式为1s22s22p63s23p6,第
(3)B元素的正三价离子的3d能级为半充满,B的元素符号为
(4)现向蓝色的硫酸铜溶液中,加入少量稀氨水,得到蓝色絮状沉淀,继续加入氨水后,蓝色沉淀溶解,得到深蓝色透明溶液,写出划线部分现象对应的离子方程式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】我国科学家受中医启发,发现As2O3(俗称砒霜)对白血病有疗效。氮、磷、砷(As)是VA族、第二至第四周期的元素,这些元素的化合物在研究和生产中有许多重要用途。

完成下列填空:
(1)As原子最外层电子的轨道表示式为_____________ ;砷蒸气的分子式:As4,其分子结构与白磷(P4)相似,也是正四面体,则As4中砷砷键的键角是__________ 。
(2)P的非金属性比As强,从原子结构的角度解释其原因_______ ;如图是元素周期表的一部分,请推测砷的单质或其化合物可能具有的性质_______________ (写出两条即可)
(3)NH4NO3可做化肥,但易爆,300℃发生爆炸:2NH4NO3→2N2↑+O2↑+4H2O。每生成2molN2,反应中转移的电子为_____ mol,氧化产物与还原产物的质量之比为_____ 。
(4)发电厂常用氨气吸收烟气中的CO2。常温下,当CO2不断通入pH=11的氨水中时会产生微量的新离子:NH2COO-。
(i)写出NH2COO-的电子式___________ 。
(ii)计算原氨水中c(NH4+)=_______ mol/L。

完成下列填空:
(1)As原子最外层电子的轨道表示式为
(2)P的非金属性比As强,从原子结构的角度解释其原因
(3)NH4NO3可做化肥,但易爆,300℃发生爆炸:2NH4NO3→2N2↑+O2↑+4H2O。每生成2molN2,反应中转移的电子为
(4)发电厂常用氨气吸收烟气中的CO2。常温下,当CO2不断通入pH=11的氨水中时会产生微量的新离子:NH2COO-。
(i)写出NH2COO-的电子式
(ii)计算原氨水中c(NH4+)=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】1915年诺贝尔物理学奖授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献。科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如图,其中配位键和氢键均采用虚线表示。

(1)写出基态Cu原子的核外电子排布式____ ,S原子的价层电子排布图______
(2)写出胆矾晶体中水合铜离子的结构简式_____ (必须将配位键表示出来)。
(3)向CuSO4溶液中滴加氨水,可以得到深蓝色的溶液,再加入乙醇后析出深蓝色晶体,写出深蓝色晶体的化学式_____ 。比较NH3和[Cu(NH3)4]2+中H-N-H中键角的大小:NH3_____ [Cu(NH3)4]2+(填“ ” “
” “ ”或“=”)。
”或“=”)。
(4)已知H2O2的结构如图:
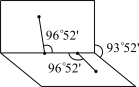
H2O2分子不是直线形的,两个H原子犹如在半展开的书的两面纸上,书页角为93°52′,而两个O—H键与O—O键的夹角均为96°52′,估计它难溶于CS2,简要说明原因______ 。
(5)分析下表中两种物质的键能数据(单位:kJ/mol)。
结合数据说明CO比N2活泼的原因:_________ 。

(1)写出基态Cu原子的核外电子排布式
(2)写出胆矾晶体中水合铜离子的结构简式
(3)向CuSO4溶液中滴加氨水,可以得到深蓝色的溶液,再加入乙醇后析出深蓝色晶体,写出深蓝色晶体的化学式
 ” “
” “ ”或“=”)。
”或“=”)。(4)已知H2O2的结构如图:

H2O2分子不是直线形的,两个H原子犹如在半展开的书的两面纸上,书页角为93°52′,而两个O—H键与O—O键的夹角均为96°52′,估计它难溶于CS2,简要说明原因
(5)分析下表中两种物质的键能数据(单位:kJ/mol)。
| A—B | A=B | A=B | |
| CO | 357.7 | 798.9 | 1 071.9 |
| N2 | 154.8 | 418.4 | 941.7 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】铜单质及其化合物在很多领域有重要用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂。
(1)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为_____________________________ ,Cu位于元素周期表第ⅠB族。Cu 2+的核外电子排布式为____________________ 。
(2)胆矾CuSO4·5H2O可写成[Cu(H2O) 4 ]SO4 ·H2O,其结构示意图如下:
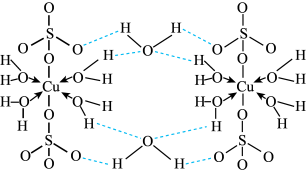
下列说法正确的是________ (填字母)。
A.水中的氧原子采用sp3杂化
B.氧原子参与形成配位键和氢键两种化学键
C.Cu2+的价电子排布式为3d84s1
D.胆矾中的水在不同温度下会分步失去
(1)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为
(2)胆矾CuSO4·5H2O可写成[Cu(H2O) 4 ]SO4 ·H2O,其结构示意图如下:

下列说法正确的是
A.水中的氧原子采用sp3杂化
B.氧原子参与形成配位键和氢键两种化学键
C.Cu2+的价电子排布式为3d84s1
D.胆矾中的水在不同温度下会分步失去
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】科学研究发现铁氮化合物具有非常优异的磁性能、机械性能和耐腐蚀性,因此受到研究人员的广泛关注。γ−Fe4N是一种性能优异的铁氮化合物,其可由氨气与羰基铁粉[Fe(CO)5]反应得到。
(1)Fe变为Fe2+时是失去_______ 轨道电子。
(2)NH3中H−N−H的键角比NH 中H−N−H的键角
中H−N−H的键角_______ (填“大”或“小”)。
(3)羰基铁粉[Fe(CO)5]中配位原子为_______ 。
(4)氨气与羰基铁粉的反应中涉及元素电负性由大到小的顺序为_______ 。
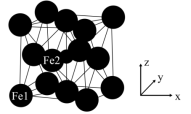
(5)γ−Fe4N的晶胞如图所示,设晶胞中Fe1点的原子坐标为(0,0,0),N点的原子坐标为( ,
, ,
, ),则Fe2点的原子坐标为
),则Fe2点的原子坐标为_______ 。已知该晶体的密度为d g/cm3,阿伏加德罗常数的值为NA,则晶胞参数a为_______ nm(用含d和NA的代数式表示)。
(1)Fe变为Fe2+时是失去
(2)NH3中H−N−H的键角比NH
 中H−N−H的键角
中H−N−H的键角(3)羰基铁粉[Fe(CO)5]中配位原子为
(4)氨气与羰基铁粉的反应中涉及元素电负性由大到小的顺序为
(5)γ−Fe4N的晶胞如图所示,设晶胞中Fe1点的原子坐标为(0,0,0),N点的原子坐标为(
 ,
, ,
, ),则Fe2点的原子坐标为
),则Fe2点的原子坐标为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为Fe−Sm−As−F−O组成的化合物。回答下列问题:
(1)AsH3的中心原子的杂化轨道类型为___________ ,H2O沸点比H2S的___________ (填“高”或“低”),其判断理由是___________ ,BF3的立体构型为___________ 。
(2)Sm的价层电子排布式为4f66s2,Sm3+的价层电子排布式为___________ 。
(3)一种四方结构的超导化合物的晶胞结构如图1所示,晶胞中Sm和As原子的投影位置如图2所示。图中F−和O2−共同占据晶胞的上下底面位置,若两者的比例依次用x和1−x代表,则该化合物的化学式表示为___________ 。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图1中原子1的坐标为( ),则原子3的坐标分别为
),则原子3的坐标分别为___________ 。

(1)AsH3的中心原子的杂化轨道类型为
(2)Sm的价层电子排布式为4f66s2,Sm3+的价层电子排布式为
(3)一种四方结构的超导化合物的晶胞结构如图1所示,晶胞中Sm和As原子的投影位置如图2所示。图中F−和O2−共同占据晶胞的上下底面位置,若两者的比例依次用x和1−x代表,则该化合物的化学式表示为
 ),则原子3的坐标分别为
),则原子3的坐标分别为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】在人类文明的历程中,改变世界的事物很多,其中铁、硝酸钾、青霉素、氨、乙醇、二氧化碳等17种“分子”改变过人类的世界。
(1)铁原子在基态时,价层电子排布式为___ 。
(2)硝酸钾中NO3-的空间构型为___ 。
(3)1molCO2分子中含有σ键的数目为___ 。乙醇的相对分子质量比氯乙烷小,但其沸点比氯乙烷高,其原因是___ 。
(4)6-氨基青霉烷酸的结构如图1所示,其中采用sp3杂化的原子有___ 。

(5)铁和氨气在640℃可发生置换反应,产物之-的晶胞结构如图2所示,写出该反应的化学方程式___ 。

(6)晶胞有两个基本要素:
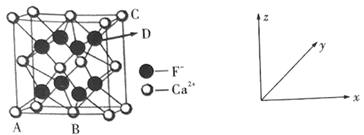
①原子坐标参数:表示晶胞内部各微粒的相对位置。如图是CaF2的晶胞,其中原子坐标参数A处为(0,0,0);B处为( ,
, ,0);C处为(1,1,1)。则D处微粒的坐标参数为
,0);C处为(1,1,1)。则D处微粒的坐标参数为___ 。
②晶胞参数:描述晶胞的大小和形状。已知CaF2晶体的密度为ρg·cm-3,则晶胞参数a为___ pm(设NA为阿伏加 德罗常数的值,用含ρ、NA的式子表示)。
(1)铁原子在基态时,价层电子排布式为
(2)硝酸钾中NO3-的空间构型为
(3)1molCO2分子中含有σ键的数目为
(4)6-氨基青霉烷酸的结构如图1所示,其中采用sp3杂化的原子有

(5)铁和氨气在640℃可发生置换反应,产物之-的晶胞结构如图2所示,写出该反应的化学方程式

(6)晶胞有两个基本要素:
①原子坐标参数:表示晶胞内部各微粒的相对位置。如图是CaF2的晶胞,其中原子坐标参数A处为(0,0,0);B处为(
 ,
, ,0);C处为(1,1,1)。则D处微粒的坐标参数为
,0);C处为(1,1,1)。则D处微粒的坐标参数为
②晶胞参数:描述晶胞的大小和形状。已知CaF2晶体的密度为ρg·cm-3,则晶胞参数a为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】砷(As)在地壳中含量不高,但砷的化合物却是丰富多彩。回答下列问题:
(1)砷的基态原子简化电子排布式为__________________ ;第一电离能:砷______ 硒(填“>”或“<”)
(2)目前市售发光二极管材质以砷化镓(CaAs)为主。Ga和As相比,电负性较大的是____________ ,CaAs中Ga元素的化合价为____________ 。
(3)AsH3是无色、稍有大蒜味气体。AsH3空间构型为____________ 。AsH3的沸点高于PH3,低于NH3,其原因是_________________________________ 。
(4)Na3AsO4可作杀虫剂。 AsO43− 中As原子杂化轨道类型为__________ 。与AsO43−互为等电子体 分子和离子各填一种___________ 、__________ 。
(5)H3AsO4和H3AsO3是砷的两种含氧酸,根据物质结构与性质的关系,解释H3AsO4比H3AsO3酸性强的原因_____________________________________________________ 。
(6)磷和砷同主族。磷的一种单质白磷(P4)属于分子晶体,其晶胞结构如图所示。若其晶胞边长为a pm,则白磷的密度为_______________ g·cm-3(列出计算式即可)。

 1个 代表一个白磷分子
1个 代表一个白磷分子
(1)砷的基态原子简化电子排布式为
(2)目前市售发光二极管材质以砷化镓(CaAs)为主。Ga和As相比,电负性较大的是
(3)AsH3是无色、稍有大蒜味气体。AsH3空间构型为
(4)Na3AsO4可作杀虫剂。 AsO43− 中As原子杂化轨道类型为
(5)H3AsO4和H3AsO3是砷的两种含氧酸,根据物质结构与性质的关系,解释H3AsO4比H3AsO3酸性强的原因
(6)磷和砷同主族。磷的一种单质白磷(P4)属于分子晶体,其晶胞结构如图所示。若其晶胞边长为a pm,则白磷的密度为

 1个 代表一个白磷分子
1个 代表一个白磷分子
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】无水四氯化锡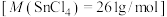 是一种重要的工业原料,其在常温下为无色液体,沸点114℃,在空气中极易水解生成
是一种重要的工业原料,其在常温下为无色液体,沸点114℃,在空气中极易水解生成 ,液态四氯化锡对很多非极性分子有一定的溶解度。实验室可选用以下装置用熔融的锡与氯气反应制备无水
,液态四氯化锡对很多非极性分子有一定的溶解度。实验室可选用以下装置用熔融的锡与氯气反应制备无水 ,请回答有关问题:
,请回答有关问题:______ 。
(2)A中盛放 晶体的仪器名称为
晶体的仪器名称为______ ,在其中发生反应的化学方程式是______ 。
(3)整个实验装置的连接顺序是A→______ →B→C→______ (装置可重复选用),若缺少装置F,则收集器C中发生反应的化学方程式为______ 。
(4)收集器C中收集到的液体略显黄色,原因是______ ,C中上方冷水的作用是______ 。
(5)除氯后测定最后产品的纯度。量取 ,ag/mL的样品,置于已称重含20mL水的称量瓶中,混合后,移入锥形瓶,加入200mL水和2滴1%甲基橙指示液,用b mol/L的NaOH标准液滴定,消耗标准液
,ag/mL的样品,置于已称重含20mL水的称量瓶中,混合后,移入锥形瓶,加入200mL水和2滴1%甲基橙指示液,用b mol/L的NaOH标准液滴定,消耗标准液 (接近终点时,每滴加一滴标准液须待沉淀沉降后观察澄清液体的颜色)。滴定到达终点的实验现象为
(接近终点时,每滴加一滴标准液须待沉淀沉降后观察澄清液体的颜色)。滴定到达终点的实验现象为______ ,产品的纯度为______ %。
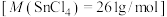 是一种重要的工业原料,其在常温下为无色液体,沸点114℃,在空气中极易水解生成
是一种重要的工业原料,其在常温下为无色液体,沸点114℃,在空气中极易水解生成 ,液态四氯化锡对很多非极性分子有一定的溶解度。实验室可选用以下装置用熔融的锡与氯气反应制备无水
,液态四氯化锡对很多非极性分子有一定的溶解度。实验室可选用以下装置用熔融的锡与氯气反应制备无水 ,请回答有关问题:
,请回答有关问题:
(2)A中盛放
 晶体的仪器名称为
晶体的仪器名称为(3)整个实验装置的连接顺序是A→
(4)收集器C中收集到的液体略显黄色,原因是
(5)除氯后测定最后产品的纯度。量取
 ,ag/mL的样品,置于已称重含20mL水的称量瓶中,混合后,移入锥形瓶,加入200mL水和2滴1%甲基橙指示液,用b mol/L的NaOH标准液滴定,消耗标准液
,ag/mL的样品,置于已称重含20mL水的称量瓶中,混合后,移入锥形瓶,加入200mL水和2滴1%甲基橙指示液,用b mol/L的NaOH标准液滴定,消耗标准液 (接近终点时,每滴加一滴标准液须待沉淀沉降后观察澄清液体的颜色)。滴定到达终点的实验现象为
(接近终点时,每滴加一滴标准液须待沉淀沉降后观察澄清液体的颜色)。滴定到达终点的实验现象为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】据世界权威刊物《自然》最近报道,我国科学家选择碲化锆(ZrTe2)和砷化镉(Cd3As2)为材料验证了三维量子霍尔效应,并发现了金属-绝缘体的转换。回答下列问题:
(1)锌原子的价电子排布图:____________________________________________
(2)硫和碲位于同主族,H2S的分解温度高于H2Te,其主要原因是________________
(3)Cd2+与NH3等配体形成配离子。1 mol [Cd(NH3)4]2+含___________ mol σ键。该配离子中三种元素的电负性大小关系是:_______________________
(4)砷与卤素形成多种卤化物。AsCl3、AsF3、AsBr3的熔点由高到低的排序为________
(5)锆晶胞如图1所示,这种堆积方式称为______________________ ,镉晶胞如图2所示。已知:NA是阿伏加 德罗常数的值,晶体密度为d g·cm3。在该晶胞中两个镉原子最近核间距为______ nm(用含NA、d的代数式表示),镉晶胞中原子空间利用率为________ (用含π的代数式表示)。

(1)锌原子的价电子排布图:
(2)硫和碲位于同主族,H2S的分解温度高于H2Te,其主要原因是
(3)Cd2+与NH3等配体形成配离子。1 mol [Cd(NH3)4]2+含
(4)砷与卤素形成多种卤化物。AsCl3、AsF3、AsBr3的熔点由高到低的排序为
(5)锆晶胞如图1所示,这种堆积方式称为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】镓及其化合物在合金工业、制药工业和电池工业中应用广泛。回答下列问题:
(1)写出基态Ga原子的核外电子排布式:_______ 。
(2)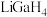 是一种温和的还原剂,可由
是一种温和的还原剂,可由 和过量的LiH反应制得,该反应的化学方程式:
和过量的LiH反应制得,该反应的化学方程式:_______ 。
(3)①已知 的熔点为77.9°C,LiCl的熔点为605°C,两者熔点差异较大的原因是
的熔点为77.9°C,LiCl的熔点为605°C,两者熔点差异较大的原因是_____ 。
② 的空间结构为
的空间结构为_______ 。
(4)砷化镓是第二代半导体,熔点为1238°C,具有共价键三维骨架结构。其晶胞结构为平行六面体,如图所示。_______ 。
②已知Ga和As的摩尔质量分别为 和
和 ,晶胞的边长为
,晶胞的边长为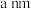 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则砷化镓晶胞的密度为
,则砷化镓晶胞的密度为_______  。
。
③若A点分数坐标为 ,B点分数坐标为
,B点分数坐标为 ,则W点分数坐标为
,则W点分数坐标为_______ 。
(1)写出基态Ga原子的核外电子排布式:
(2)
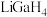 是一种温和的还原剂,可由
是一种温和的还原剂,可由 和过量的LiH反应制得,该反应的化学方程式:
和过量的LiH反应制得,该反应的化学方程式:(3)①已知
 的熔点为77.9°C,LiCl的熔点为605°C,两者熔点差异较大的原因是
的熔点为77.9°C,LiCl的熔点为605°C,两者熔点差异较大的原因是②
 的空间结构为
的空间结构为(4)砷化镓是第二代半导体,熔点为1238°C,具有共价键三维骨架结构。其晶胞结构为平行六面体,如图所示。

②已知Ga和As的摩尔质量分别为
 和
和 ,晶胞的边长为
,晶胞的边长为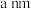 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则砷化镓晶胞的密度为
,则砷化镓晶胞的密度为 。
。③若A点分数坐标为
 ,B点分数坐标为
,B点分数坐标为 ,则W点分数坐标为
,则W点分数坐标为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】氢能被视为最具发展潜力的清洁能源,开发新型储氯材料是氢能利用的重要研究方向。请回答下列问题:
Ⅰ.化合物A(H3BNH3)是一种潜在的储氢材料,可由六元环状物质(HB=NH)3通过如下反应制得:3CH4+2 (HB=NH)3+6H2O=3CO2+6H3BNH3
(1)基态B原子的价电子排布式为___________ ,B、C,N,O第一电离能由大到小的顺序为_________ ,CH4、H2O、CO2的键角按照由大到小的顺序排列为___________ 。
(2)与(HB=NH)3,互为等电子体的有机分子为___________ (填分子式)。
Ⅱ.氢气的安全贮存和运输是氢能应用的关键。
(1)印度尼赫鲁先进科学研究中心的Datta和Pati等人借助ADF软件对一种新型环烯类储氢材料(C16S8)进行研究,从理论角度证明这种材料的分子呈平面结构(如图),每个杂环平面上下两侧最多可吸附10个H2分子。

①C16S8分子中C原子和S原子的杂化轨道类型分别为___________ 。
②相关键长数据如表所示:
从表中数据看出,C16S8中碳硫键键长介于C—S键与C=S键之间,原因可能______________________ 。
③C16S8与H2微粒间的作用力是___________ 。
(2)有储氢功能的铜合金晶体具有立方最密堆积结构,晶胞中Cu原子位于面心,Ag原子位于顶点,氢原子可进到由Cu原子与Ag原子构成的四面体空隙中。该晶体储氢后的晶胞结构与CaF2(如图)相似,该晶体储氢后的化学式为___________ 。


(3)MgH2是金属氢化物储氢材料,其晶胞如上图所示,该晶体的密度为ag•cm-3,则晶胞的体积为___________ cm3(用含a、NA的代数式表示,NA表示阿伏伽德罗常数的值)。
Ⅰ.化合物A(H3BNH3)是一种潜在的储氢材料,可由六元环状物质(HB=NH)3通过如下反应制得:3CH4+2 (HB=NH)3+6H2O=3CO2+6H3BNH3
(1)基态B原子的价电子排布式为
(2)与(HB=NH)3,互为等电子体的有机分子为
Ⅱ.氢气的安全贮存和运输是氢能应用的关键。
(1)印度尼赫鲁先进科学研究中心的Datta和Pati等人借助ADF软件对一种新型环烯类储氢材料(C16S8)进行研究,从理论角度证明这种材料的分子呈平面结构(如图),每个杂环平面上下两侧最多可吸附10个H2分子。

①C16S8分子中C原子和S原子的杂化轨道类型分别为
②相关键长数据如表所示:
| 化学键 | C-S | C=S | C16S8中碳硫键 |
| 键长/pm | 181 | 155 | 176 |
③C16S8与H2微粒间的作用力是
(2)有储氢功能的铜合金晶体具有立方最密堆积结构,晶胞中Cu原子位于面心,Ag原子位于顶点,氢原子可进到由Cu原子与Ag原子构成的四面体空隙中。该晶体储氢后的晶胞结构与CaF2(如图)相似,该晶体储氢后的化学式为


(3)MgH2是金属氢化物储氢材料,其晶胞如上图所示,该晶体的密度为ag•cm-3,则晶胞的体积为
您最近一年使用:0次



