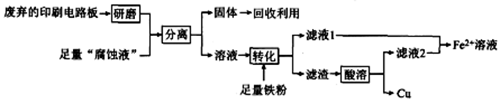
印刷电路板在科技领域具有不可替代的作用,它的制备方法为高分子化合物和铜箔压合,通过FeCl3溶液“腐蚀”而成。某实验小组在实验室用废弃的印刷电路板和“腐蚀液”提取铜的一种工艺流程如下:
请回答下列问题:
(1)检验“腐蚀液”中含有Fe3+的方法为_____________________________ 。
(2)“分离”所用的操作名称为________ 。该操作所用的主要玻璃仪器除了有烧杯还有_______ 。
(3)Fe2+溶液有很多重要用途。
①已知:常温下Ksp[Fe(OH)2]=1.8×10-16。保存1.8mol·L-1的FeSO4溶液时,为确保溶液中不出现浑浊,应调节溶液的pH不超过_______________ 。
②Fe2+转化为Fe3+后,可用于制备高铁酸盐。向FeCl3溶液中加入NaOH、NaClO溶液制备Na2FeO4的化学方程式为____________________________________________ 。
③一定温度下,向0.1 mol•L-1的Fe(NO3)2溶液中加入AgNO3 固体忽略溶液体积的变化,平衡c(Fe3+)与c(Ag+)的关系如图所示:Fe2++Ag+ Fe3++Ag
Fe3++Ag
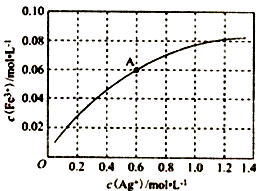
该温度下,A 点溶液中以上反应的化学平衡常数为__________ (溶液体积变化忽略不计);若将0.6 mol•L-1 Fe(NO3)2 溶液、0.15 mol•L-1Fe(NO3)3 溶液、0.06mol•L-1AgNO3溶液等体积混合后,再加入1.08gAg,可观察到的现象为_________________________________ 。

请回答下列问题:
(1)检验“腐蚀液”中含有Fe3+的方法为
(2)“分离”所用的操作名称为
(3)Fe2+溶液有很多重要用途。
①已知:常温下Ksp[Fe(OH)2]=1.8×10-16。保存1.8mol·L-1的FeSO4溶液时,为确保溶液中不出现浑浊,应调节溶液的pH不超过
②Fe2+转化为Fe3+后,可用于制备高铁酸盐。向FeCl3溶液中加入NaOH、NaClO溶液制备Na2FeO4的化学方程式为
③一定温度下,向0.1 mol•L-1的Fe(NO3)2溶液中加入AgNO3 固体忽略溶液体积的变化,平衡c(Fe3+)与c(Ag+)的关系如图所示:Fe2++Ag+
 Fe3++Ag
Fe3++Ag
该温度下,A 点溶液中以上反应的化学平衡常数为
更新时间:2018-01-18 10:27:58
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】I.钛冶炼厂与氯碱厂、甲醇厂组成一个产业链(如图所示),将大大提高资源的利用率,减少环境污染。
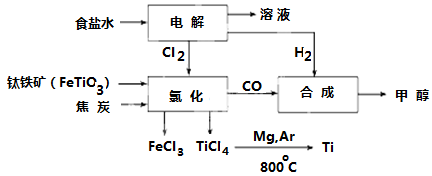
请回答下列问题:
(1)Fe位于元素周期表中第________ 周期,第________ 族。
(2)写出钛铁矿在高温下与焦炭经氯化得到四氯化钛的化学方程式______________ 。
Ⅱ.A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)。
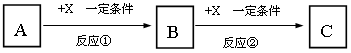
试回答:
(1)若X是强氧化性单质,则A不可能是________________ 。
A.S B.N2 C.Na D.Mg E.Al
(2)若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则B的化学式为____________ ;C溶液在贮存时应加入少量X,理由是(用必要的文字和离子方程式表示)____________ 。
(3)A还可以是氨气,氨气分子的空间构型是____________________ 。

请回答下列问题:
(1)Fe位于元素周期表中第
(2)写出钛铁矿在高温下与焦炭经氯化得到四氯化钛的化学方程式
Ⅱ.A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)。

试回答:
(1)若X是强氧化性单质,则A不可能是
A.S B.N2 C.Na D.Mg E.Al
(2)若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则B的化学式为
(3)A还可以是氨气,氨气分子的空间构型是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】含镍催化剂在有机合成中应用广泛。某油脂厂制硬化油废弃的镍催化剂(主要含有 ,还含有
,还含有 、
、 )为原料制备
)为原料制备 ,及
,及 的工艺流程如下:
的工艺流程如下:
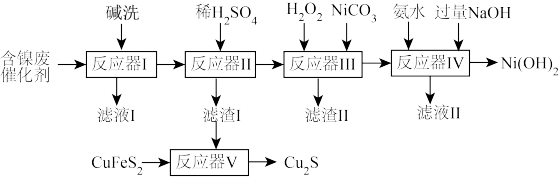
已知:①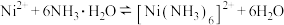
②制备过程中,降低 沉淀速率,可以避免沉淀团聚,提升产品性能回答下列问题:
沉淀速率,可以避免沉淀团聚,提升产品性能回答下列问题:
(1)反应器1中进行碱洗的主要目的是_______ 。
(2)保持其它条件不变,在不同温度下进行稀 溶浸,镍浸出率随时间变化如图。酸浸的最佳条件是
溶浸,镍浸出率随时间变化如图。酸浸的最佳条件是_______ 。

(3)反应器Ⅲ中加入 发生反应的离子方程式为
发生反应的离子方程式为_______ 。加入 的作用
的作用_______ 。
(4)反应器Ⅳ中,需先加氨水,再加过量 ,先加氨水的目的是
,先加氨水的目的是_______ 。
(5) 是一种不溶于水的黑色固体,但可溶于
是一种不溶于水的黑色固体,但可溶于 溶液,有研究指出
溶液,有研究指出 是该反应的催化剂,该过程的反应原理可用化学方程式表示为①
是该反应的催化剂,该过程的反应原理可用化学方程式表示为①_______ ;② 。
。
 ,还含有
,还含有 、
、 )为原料制备
)为原料制备 ,及
,及 的工艺流程如下:
的工艺流程如下:
已知:①
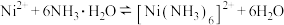
②制备过程中,降低
 沉淀速率,可以避免沉淀团聚,提升产品性能回答下列问题:
沉淀速率,可以避免沉淀团聚,提升产品性能回答下列问题:(1)反应器1中进行碱洗的主要目的是
(2)保持其它条件不变,在不同温度下进行稀
 溶浸,镍浸出率随时间变化如图。酸浸的最佳条件是
溶浸,镍浸出率随时间变化如图。酸浸的最佳条件是
(3)反应器Ⅲ中加入
 发生反应的离子方程式为
发生反应的离子方程式为 的作用
的作用(4)反应器Ⅳ中,需先加氨水,再加过量
 ,先加氨水的目的是
,先加氨水的目的是(5)
 是一种不溶于水的黑色固体,但可溶于
是一种不溶于水的黑色固体,但可溶于 溶液,有研究指出
溶液,有研究指出 是该反应的催化剂,该过程的反应原理可用化学方程式表示为①
是该反应的催化剂,该过程的反应原理可用化学方程式表示为① 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某同学类比镁在二氧化碳中的燃烧反应:2Mg+CO2=2MgO+C,认为钠和二氧化碳也可以发生反应,他在实验室中选择以下装置对该反应能否发生进行了实验探究。
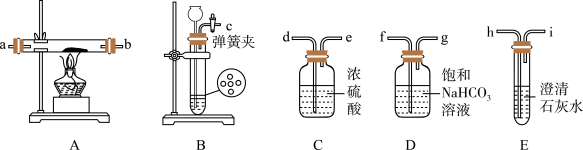
依据要求回答问题:
(1)二氧化碳的发生装置应选用上述装置中的__ (填装置下方对应字母),反应的离子方程式为___ 。
(2)为达到实验目的,选择上图中的装置,其连接顺序为:二氧化碳的发生装置→___ 。(按气流方向,用小写字母表示)。
(3)检查装置气密性良好,装好药品后,打开弹簧夹,待装置中的空气排净后才能点燃酒精灯。能说明装置中空气已经排净的现象是___ 。
(4)若反应过程中CO2足量,反应结束后,该同学对硬质玻璃管中生成的固体提出了以下猜想:①生成的固体物质为Na2CO3,②生成的固体物质为Na2CO3和C的混合物,③生成的固体物质为Na2CO3和Na2O的混合物,④生成的固体物质为Na2O和C的混合物。报告给老师后,老师认为可以排除其中的3种情况,老师排除的理由是___ ;则钠与CO2反应的化学方程式为___ 。
(5)该同学经过反思,认为上述实验设计中存在缺陷。他查阅资料后得知,PdCl2溶液可以吸收CO,同时得到黑色的Pd。于是他在装置后加装一个盛PdCl2溶液的吸收装置,该装置中发生反应的化学方程式为___ 。

依据要求回答问题:
(1)二氧化碳的发生装置应选用上述装置中的
(2)为达到实验目的,选择上图中的装置,其连接顺序为:二氧化碳的发生装置→
(3)检查装置气密性良好,装好药品后,打开弹簧夹,待装置中的空气排净后才能点燃酒精灯。能说明装置中空气已经排净的现象是
(4)若反应过程中CO2足量,反应结束后,该同学对硬质玻璃管中生成的固体提出了以下猜想:①生成的固体物质为Na2CO3,②生成的固体物质为Na2CO3和C的混合物,③生成的固体物质为Na2CO3和Na2O的混合物,④生成的固体物质为Na2O和C的混合物。报告给老师后,老师认为可以排除其中的3种情况,老师排除的理由是
(5)该同学经过反思,认为上述实验设计中存在缺陷。他查阅资料后得知,PdCl2溶液可以吸收CO,同时得到黑色的Pd。于是他在装置后加装一个盛PdCl2溶液的吸收装置,该装置中发生反应的化学方程式为
您最近一年使用:0次
【推荐1】I.以铝土矿的烧渣(主要成分为Al2O3、Fe2O3、SiO2)为原料,生产Fe3O4的工艺流程如下:
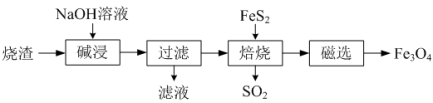
(1)“碱浸”时将烧渣粉碎的目的是_______
(2)“过滤”时用到的玻璃仪器除烧杯外,还有_______
(3)“滤液”中含有的溶质为_______ (填化学式),可以往滤液中通入过量二氧化碳,经过滤、灼烧生产氧化铝。
(4)“过滤”得到的滤渣中含大量的Fe2O3,Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,写出焙烧时发生反应的化学方程式_______
II.热化学铁氧化合物循环制H2具有成本低、产物易分离等优点。以太阳能为热源,经由铁氧化合物循环分解液态水的过程如下图所示:
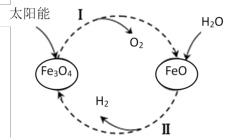
已知:①过程I:2Fe3O4(s)=6FeO(s)+O2(g) ΔH=+313.2kJ/mol
②2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ/mol
③H2O(g)=H2O(l) ΔH=-44kJ/mol
请回答下列问题3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=+129.2kJ/mol
(5)氢气的燃烧热ΔH=_______
(6)过程II的热化学方程式_______ 。

(1)“碱浸”时将烧渣粉碎的目的是
(2)“过滤”时用到的玻璃仪器除烧杯外,还有
(3)“滤液”中含有的溶质为
(4)“过滤”得到的滤渣中含大量的Fe2O3,Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,写出焙烧时发生反应的化学方程式
II.热化学铁氧化合物循环制H2具有成本低、产物易分离等优点。以太阳能为热源,经由铁氧化合物循环分解液态水的过程如下图所示:

已知:①过程I:2Fe3O4(s)=6FeO(s)+O2(g) ΔH=+313.2kJ/mol
②2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ/mol
③H2O(g)=H2O(l) ΔH=-44kJ/mol
请回答下列问题3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=+129.2kJ/mol
(5)氢气的燃烧热ΔH=
(6)过程II的热化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下:
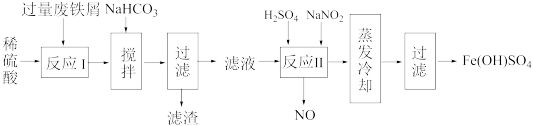
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如表。
完成下列填空:
(1)反应Ⅰ后的溶液中存在的阳离子有___________ 。
(2)加入少量 的目的是将溶液的pH调节在
的目的是将溶液的pH调节在___________ 范围内,从而使溶液中的 沉淀完全而
沉淀完全而 不沉淀,该工艺中“搅拌”的作用是
不沉淀,该工艺中“搅拌”的作用是___________ 。
(3)反应Ⅱ加入 的目的是氧化
的目的是氧化 ,反应的离子方程式为
,反应的离子方程式为___________ 。在实际生产中,反应Ⅱ常同时通入O2以减少 的用量,若参与反应的O2有11.2L(标准状况),则相当于节约了
的用量,若参与反应的O2有11.2L(标准状况),则相当于节约了
___________ g。
(4)碱式硫酸铁溶于水后产生的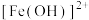 可部分水解生成
可部分水解生成 聚合离子,该水解反应的离子方程式为
聚合离子,该水解反应的离子方程式为___________ 。

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如表。
| 沉淀物 |  |  |  |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
(1)反应Ⅰ后的溶液中存在的阳离子有
(2)加入少量
 的目的是将溶液的pH调节在
的目的是将溶液的pH调节在 沉淀完全而
沉淀完全而 不沉淀,该工艺中“搅拌”的作用是
不沉淀,该工艺中“搅拌”的作用是(3)反应Ⅱ加入
 的目的是氧化
的目的是氧化 ,反应的离子方程式为
,反应的离子方程式为 的用量,若参与反应的O2有11.2L(标准状况),则相当于节约了
的用量,若参与反应的O2有11.2L(标准状况),则相当于节约了
(4)碱式硫酸铁溶于水后产生的
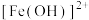 可部分水解生成
可部分水解生成 聚合离子,该水解反应的离子方程式为
聚合离子,该水解反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】工业上以碳酸锰矿(主要含 ,还含有
,还含有 、
、 、
、 等杂质)为原料制备
等杂质)为原料制备 的工艺流程如下图所示。
的工艺流程如下图所示。

已知:常温下,溶液中金属离子开始沉淀和完全沉淀时的pH如表所示。
回答下列问题:
(1)“酸浸”前将碳酸锰矿粉碎的目的是_______ 。
(2)“氧化”时 将
将 氧化成
氧化成 的离子方程式为
的离子方程式为_______ 。
(3)“调pH”时应控制pH范围为_______ ,滤渣2的主要成分为 和
和_______ 。
(4)“沉锰”得到 ,该过程需控制在较低温度下的原因是
,该过程需控制在较低温度下的原因是_______ 。要使 沉淀完全(通常认为溶液中离子浓度小于
沉淀完全(通常认为溶液中离子浓度小于 为沉淀完全),溶液中
为沉淀完全),溶液中 的浓度应大于
的浓度应大于_______ 。[25℃时,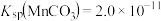 ]。
]。
(5)“氧化焙烧”的化学方程式为_______ 。
(6)若以125kg该碳酸锰矿为原料制备 ,得到产品质量为87kg,则该碳酸锰矿的纯度是
,得到产品质量为87kg,则该碳酸锰矿的纯度是_______ 。(忽略流程中锰元素的损失)。
 ,还含有
,还含有 、
、 、
、 等杂质)为原料制备
等杂质)为原料制备 的工艺流程如下图所示。
的工艺流程如下图所示。
已知:常温下,溶液中金属离子开始沉淀和完全沉淀时的pH如表所示。
| 金属离子 |  |  |  |  |
| 开始沉淀pH | 1.5 | 6.5 | 3.3 | 8.3 |
| 完全沉淀pH | 3.7 | 9.7 | 5.2 | 9.8 |
回答下列问题:
(1)“酸浸”前将碳酸锰矿粉碎的目的是
(2)“氧化”时
 将
将 氧化成
氧化成 的离子方程式为
的离子方程式为(3)“调pH”时应控制pH范围为
 和
和(4)“沉锰”得到
 ,该过程需控制在较低温度下的原因是
,该过程需控制在较低温度下的原因是 沉淀完全(通常认为溶液中离子浓度小于
沉淀完全(通常认为溶液中离子浓度小于 为沉淀完全),溶液中
为沉淀完全),溶液中 的浓度应大于
的浓度应大于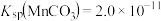 ]。
]。(5)“氧化焙烧”的化学方程式为
(6)若以125kg该碳酸锰矿为原料制备
 ,得到产品质量为87kg,则该碳酸锰矿的纯度是
,得到产品质量为87kg,则该碳酸锰矿的纯度是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)①CH3COONa 溶液呈碱性,原因是____________________ (用化学用语表达) 。
②在CH3COONa 溶液中,各个离子浓度大小关系为_________________________
③写出碳酸钠溶液中电荷守恒关系式_________________________________________
(2)已知:C(s)+H2O(g)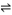 CO(g)+H2(g) △H=+131.3 kJ/mol。
CO(g)+H2(g) △H=+131.3 kJ/mol。
①该反应是________ (填“吸热”或“放热”)反应。
②它若反应消耗24g C(s),则反应吸收的热量为___________ 。
(3)在一定温度下,将CO(g)和H2O(g)各0.16 mol 通入容积为2.0 L的恒容密闭容器中,发生反应CO(g)+H2O(g)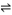 CO2(g)+H2(g),得到下表中数据:
CO2(g)+H2(g),得到下表中数据:
①2 min 内,v(CO)=________ 。
②该温度下,此反应的平衡常数的值是________ 。
③其他条件不变,再充入0.1mol CO 和0.mol H2O(g),达到平衡时CO 的体积分数_____ (填“增大”“减小”或“不变”)。
(4)下图为直流电源电解CuSO4 溶液的装置,C1和C2都为石墨电极。请回答下列问题:
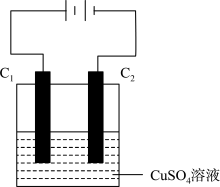
①C1作______ (填“ 阳极”或“阴极” )。
②C2 电极的电极反应式为___________ 。
③惰性电极电解CuSO4 溶液的化学方程式是_________________________
②在CH3COONa 溶液中,各个离子浓度大小关系为
③写出碳酸钠溶液中电荷守恒关系式
(2)已知:C(s)+H2O(g)
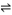 CO(g)+H2(g) △H=+131.3 kJ/mol。
CO(g)+H2(g) △H=+131.3 kJ/mol。①该反应是
②它若反应消耗24g C(s),则反应吸收的热量为
(3)在一定温度下,将CO(g)和H2O(g)各0.16 mol 通入容积为2.0 L的恒容密闭容器中,发生反应CO(g)+H2O(g)
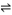 CO2(g)+H2(g),得到下表中数据:
CO2(g)+H2(g),得到下表中数据:  /min /min | 2 | 4 | 7 | 9 |
 (H (H O)/mol O)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
②该温度下,此反应的平衡常数的值是
③其他条件不变,再充入0.1mol CO 和0.mol H2O(g),达到平衡时CO 的体积分数
(4)下图为直流电源电解CuSO4 溶液的装置,C1和C2都为石墨电极。请回答下列问题:

①C1作
②C2 电极的电极反应式为
③惰性电极电解CuSO4 溶液的化学方程式是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】在一密闭容器中,起始时向该容器中充入H2S和CH4且n(H2S)∶n(CH4)=2∶1,发生反应:CH4(g)+2H2S(g)  CS2(g)+4H2(g)。0.1 MPa时,温度变化对平衡时产物的物质的量分数的影响如图所示:
CS2(g)+4H2(g)。0.1 MPa时,温度变化对平衡时产物的物质的量分数的影响如图所示:
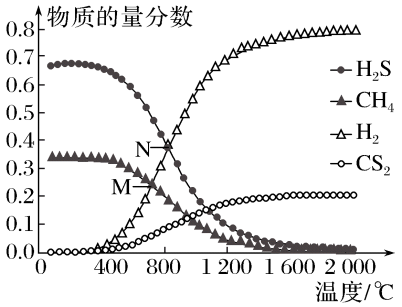
(1)该反应ΔH___________ (填“>”或“<”)0
(2)M点,H2S的平衡转化率为___________ ,为提高H2S的平衡转化率,除改变温度外,还可采取的措施是___________ (列举一条)
(3)N点,平衡分压p(CS2)=___________ MPa,对应温度下,该反应的KP =___________ (MPa)2 (KP为以分压表示的平衡常数)
 CS2(g)+4H2(g)。0.1 MPa时,温度变化对平衡时产物的物质的量分数的影响如图所示:
CS2(g)+4H2(g)。0.1 MPa时,温度变化对平衡时产物的物质的量分数的影响如图所示:
(1)该反应ΔH
(2)M点,H2S的平衡转化率为
(3)N点,平衡分压p(CS2)=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】Ⅰ.一定量的 与足量的
与足量的 在恒压密闭容器中发生反应:
在恒压密闭容器中发生反应: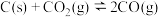
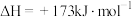 ,若压强为
,若压强为 ,平衡时体系中气体体积分数与温度的关系如图所示,回答下列问题:
,平衡时体系中气体体积分数与温度的关系如图所示,回答下列问题:
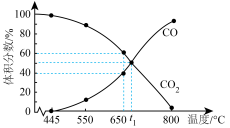
(1)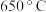 时
时 的平衡转化率为
的平衡转化率为_______ 。
(2)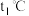 时压强平衡常数
时压强平衡常数
_______ 。(用平衡分压代替平衡浓度计算,分压=总压 物质的量分数);该温度下达平衡后若再充入等物质的量的
物质的量分数);该温度下达平衡后若再充入等物质的量的 和
和 气体,则平衡
气体,则平衡_______ (填“正向”“逆向”“不”)移动。
Ⅱ.一定温度下,向一容积为 的恒容密闭容器中充入
的恒容密闭容器中充入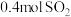 和
和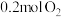 ,发生反应:
,发生反应:
 。当反应达到平衡时,容器内压强变为起始时的
。当反应达到平衡时,容器内压强变为起始时的 。请回答下列问题:
。请回答下列问题:
(3)判断该反应达到平衡状态的标志是_______ (填字母)。
a.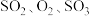 三者的浓度之比为2:1:2
三者的浓度之比为2:1:2
b.容器内气体的压强不变
c.容器内混合气体的密度保持不变
d. 的物质的量不再变化
的物质的量不再变化
e. 的生成速率和
的生成速率和 的生成速率相等
的生成速率相等
f.容器内混合气体的平均分子量保持不变
(4)①此温度下该反应的平衡常数
_______ 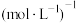 ;
;
②达到平衡时反应放出的热量为_______  。
。
(5)一定条件下反应达到平衡,在 和
和 时刻分别只改变一个条件(温度或压强),反应过程中正反应速率如图所示,下列说法正确的是_______。
时刻分别只改变一个条件(温度或压强),反应过程中正反应速率如图所示,下列说法正确的是_______。
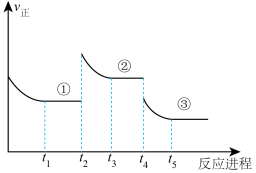
(注: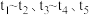 之后各时间段表示达到平衡状态①、②、③。)
之后各时间段表示达到平衡状态①、②、③。)
 与足量的
与足量的 在恒压密闭容器中发生反应:
在恒压密闭容器中发生反应: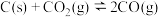
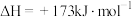 ,若压强为
,若压强为 ,平衡时体系中气体体积分数与温度的关系如图所示,回答下列问题:
,平衡时体系中气体体积分数与温度的关系如图所示,回答下列问题:
(1)
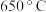 时
时 的平衡转化率为
的平衡转化率为(2)
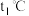 时压强平衡常数
时压强平衡常数
 物质的量分数);该温度下达平衡后若再充入等物质的量的
物质的量分数);该温度下达平衡后若再充入等物质的量的 和
和 气体,则平衡
气体,则平衡Ⅱ.一定温度下,向一容积为
 的恒容密闭容器中充入
的恒容密闭容器中充入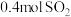 和
和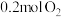 ,发生反应:
,发生反应:
 。当反应达到平衡时,容器内压强变为起始时的
。当反应达到平衡时,容器内压强变为起始时的 。请回答下列问题:
。请回答下列问题:(3)判断该反应达到平衡状态的标志是
a.
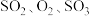 三者的浓度之比为2:1:2
三者的浓度之比为2:1:2b.容器内气体的压强不变
c.容器内混合气体的密度保持不变
d.
 的物质的量不再变化
的物质的量不再变化e.
 的生成速率和
的生成速率和 的生成速率相等
的生成速率相等f.容器内混合气体的平均分子量保持不变
(4)①此温度下该反应的平衡常数

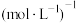 ;
;②达到平衡时反应放出的热量为
 。
。(5)一定条件下反应达到平衡,在
 和
和 时刻分别只改变一个条件(温度或压强),反应过程中正反应速率如图所示,下列说法正确的是_______。
时刻分别只改变一个条件(温度或压强),反应过程中正反应速率如图所示,下列说法正确的是_______。
(注:
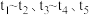 之后各时间段表示达到平衡状态①、②、③。)
之后各时间段表示达到平衡状态①、②、③。)A. 时间段平衡向正反应方向移动 时间段平衡向正反应方向移动 | B.平衡状态的平衡常数 ①大于② ①大于② |
C.平衡状态①和②时 转化率相同 转化率相同 | D. 时刻改变的条件是降低温度 时刻改变的条件是降低温度 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】工业上以菱锰矿(主要成分为 ,还含少量的
,还含少量的 、
、 、
、 、
、 、
、 、
、 等杂质)为原料制备高纯度碳酸锰的工艺流程如下。
等杂质)为原料制备高纯度碳酸锰的工艺流程如下。
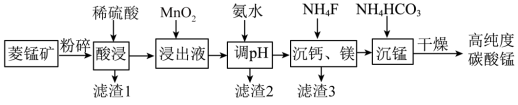
已知:①该工艺中,相关金属离子 形成
形成 沉淀的pH如下表:
沉淀的pH如下表:
 时可认为沉淀完全
时可认为沉淀完全
②常温下, ,
,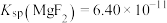
回答下列问题:
(1)为了提高酸浸速率,除粉碎菱锰矿外还可采取的措施有___________ (任写两条)。
(2)滤渣1的主要成分是___________ 、___________ 。
(3)在浸出液中加入 的作用为
的作用为___________ 。
(4)滤渣2为 和
和 ,加入氨水调节溶液pH范围为:
,加入氨水调节溶液pH范围为:___________ 。
(5)加入 的目的是将
的目的是将 、
、 沉淀除去,常温下,当溶液中
沉淀除去,常温下,当溶液中 、
、 完全除去时,则
完全除去时,则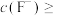
___________  。
。
(6)沉锰时, 溶液中加入
溶液中加入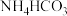 得到
得到 沉淀并有气泡产生,该反应的离子方程式为
沉淀并有气泡产生,该反应的离子方程式为___________ 。
 ,还含少量的
,还含少量的 、
、 、
、 、
、 、
、 、
、 等杂质)为原料制备高纯度碳酸锰的工艺流程如下。
等杂质)为原料制备高纯度碳酸锰的工艺流程如下。
已知:①该工艺中,相关金属离子
 形成
形成 沉淀的pH如下表:
沉淀的pH如下表:金属离子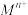 |  |  |  |  |  |
| 开始沉淀的pH | 3.4 | 1.9 | 7.0 | 8.1 | 9.1 |
| 沉淀完全的pH | 4.7 | 3.2 | 9.0 | 10.1 | 11.1 |
 时可认为沉淀完全
时可认为沉淀完全②常温下,
 ,
,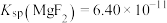
回答下列问题:
(1)为了提高酸浸速率,除粉碎菱锰矿外还可采取的措施有
(2)滤渣1的主要成分是
(3)在浸出液中加入
 的作用为
的作用为(4)滤渣2为
 和
和 ,加入氨水调节溶液pH范围为:
,加入氨水调节溶液pH范围为:(5)加入
 的目的是将
的目的是将 、
、 沉淀除去,常温下,当溶液中
沉淀除去,常温下,当溶液中 、
、 完全除去时,则
完全除去时,则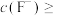
 。
。(6)沉锰时,
 溶液中加入
溶液中加入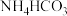 得到
得到 沉淀并有气泡产生,该反应的离子方程式为
沉淀并有气泡产生,该反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】孔雀石主要成分是 ,还含少量
,还含少量 及硅的氧化物,实验室以孔雀石为原料制备硫酸铜晶体的步骤如下:
及硅的氧化物,实验室以孔雀石为原料制备硫酸铜晶体的步骤如下:

有关物质沉淀的pH数据如下:
(1)步骤Ⅰ加稀硫酸充分反应,提高步骤Ⅰ反应速率的措施是_______ (写一条即可)。
(2)步骤Ⅱ中试剂①应选用试剂_______ (填代号)。
a. b.稀
b.稀 c.双氧水 d.氯水
c.双氧水 d.氯水
相关反应的离子方程式为:_______ 。
(3)步骤Ⅲ加入CuO调节溶液的pH至_______ (填写范围),目的是_______ 。
(4)从滤液3中获得干燥的硫酸铜晶体的操作是_______ 。
(5)常温下 的
的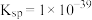 ,若要将溶液中的
,若要将溶液中的 转化为
转化为 沉淀,使溶液中
沉淀,使溶液中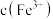 降低至
降低至 ,必须将溶液调节至
,必须将溶液调节至
_______ 。
(6)用 和孔雀石反应可以制得金属铜,已知1mol氨气通过灼热的
和孔雀石反应可以制得金属铜,已知1mol氨气通过灼热的 可以产生
可以产生 金属铜,则该反应的化学方程式为
金属铜,则该反应的化学方程式为_______ 。
 ,还含少量
,还含少量 及硅的氧化物,实验室以孔雀石为原料制备硫酸铜晶体的步骤如下:
及硅的氧化物,实验室以孔雀石为原料制备硫酸铜晶体的步骤如下:
有关物质沉淀的pH数据如下:
| 物质 |  开始沉淀 开始沉淀 |  完全沉淀 完全沉淀 |
 | 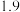 |  |
 | 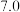 |  |
 |  | 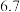 |
(1)步骤Ⅰ加稀硫酸充分反应,提高步骤Ⅰ反应速率的措施是
(2)步骤Ⅱ中试剂①应选用试剂
a.
 b.稀
b.稀 c.双氧水 d.氯水
c.双氧水 d.氯水相关反应的离子方程式为:
(3)步骤Ⅲ加入CuO调节溶液的pH至
(4)从滤液3中获得干燥的硫酸铜晶体的操作是
(5)常温下
 的
的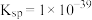 ,若要将溶液中的
,若要将溶液中的 转化为
转化为 沉淀,使溶液中
沉淀,使溶液中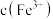 降低至
降低至 ,必须将溶液调节至
,必须将溶液调节至
(6)用
 和孔雀石反应可以制得金属铜,已知1mol氨气通过灼热的
和孔雀石反应可以制得金属铜,已知1mol氨气通过灼热的 可以产生
可以产生 金属铜,则该反应的化学方程式为
金属铜,则该反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】利用某钒废渣(主要成分为 、
、 、
、 、
、 、
、 等)制备
等)制备 的工艺流程如下:
的工艺流程如下: 溶于酸后以
溶于酸后以 的形式存在;过量
的形式存在;过量 可氧化
可氧化 ;
;
Ⅱ. 。
。
回答下列问题:
(1)为加快“氧化1”速率,可以采取的措施有____________________ (写出一条即可),该过程发生反应的离子方程式为______________________________ 。
(2)滤渣2的主要成分为____________________ 。
(3)实验室进行萃取、分液操作时,需要的玻璃仪器有____________________ 。
(4)“氧化2”中发生反应的离子方程式为______________________________ 。
(5)“沉钒”前若滤液中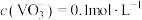 ,“沉钒”完成时,若上层清液中
,“沉钒”完成时,若上层清液中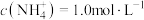 ,则钒元素的沉降率=
,则钒元素的沉降率=__________ %[ ,反应过程中溶液的体积不变]。
,反应过程中溶液的体积不变]。
(6)在Ar气氛中“煅烧” 生成
生成 ,分解产物中还含有氮气和一种氮的氢化物,发生反应的化学方程式
,分解产物中还含有氮气和一种氮的氢化物,发生反应的化学方程式______________________________ 。
 、
、 、
、 、
、 、
、 等)制备
等)制备 的工艺流程如下:
的工艺流程如下: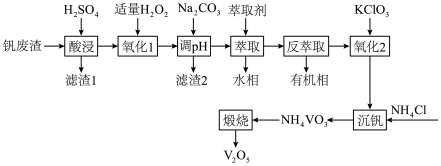
 溶于酸后以
溶于酸后以 的形式存在;过量
的形式存在;过量 可氧化
可氧化 ;
;Ⅱ.
 。
。回答下列问题:
(1)为加快“氧化1”速率,可以采取的措施有
(2)滤渣2的主要成分为
(3)实验室进行萃取、分液操作时,需要的玻璃仪器有
(4)“氧化2”中发生反应的离子方程式为
(5)“沉钒”前若滤液中
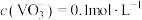 ,“沉钒”完成时,若上层清液中
,“沉钒”完成时,若上层清液中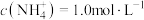 ,则钒元素的沉降率=
,则钒元素的沉降率= ,反应过程中溶液的体积不变]。
,反应过程中溶液的体积不变]。(6)在Ar气氛中“煅烧”
 生成
生成 ,分解产物中还含有氮气和一种氮的氢化物,发生反应的化学方程式
,分解产物中还含有氮气和一种氮的氢化物,发生反应的化学方程式
您最近一年使用:0次



