活性炭可处理大气污染物NO。为模拟该过程,T℃时,在3L密闭容器中加入NO和活性炭粉,反应体系中各物质的量变化如下表所示。下列说法正确的是
| 活性炭/mol | NO/mol | X/mol | Y/mol | |
| 起始时 | 2.030 | 0.100 | 0 | 0 |
| 10min达平衡 | 2.000 | 0.040 | 0.030 | 0.030 |
| A.X一定是N2,Y一定是CO2 |
| B.10min后增大压强,NO的吸收率增大 |
| C.10min后加入活性炭,平衡向正反应方向移动 |
| D.0~10min的平均反应速率v(NO)=0.002 mol/(L•min) |
18-19高三上·北京东城·期末 查看更多[5]
北京市东城区2018届高三第一学期期末考化学试试题(已下线)【中等生百日捷进提升系列-技能方法】专题09 化学反应速率化学平衡类选择题解题方法和策略陕西省汉中市龙岗中学2020届高三第七次质量检测化学试题2020年北京高二下学期 复习模拟试题二(选修4人教版)湖北省孝感市高级中学2020—2021学年高二下学期2月调研考试化学试题
更新时间:2018-01-20 12:37:29
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】某温度下,往2L的密闭容器中加入一定量的A和B,发生反应:2A(g)+B(g)⇌C(g)。物质C的浓度随反应时间(t)的变化如表。在0-6s内,A的平均反应速率为
| t/s | 2 | 4 | 6 | 8 |
| C的物质的量(mol) | 2.2 | 3.6 | 4.2 | 4.6 |
| A.0.70mol·L-1·s-1 | B.1.4mol·L-1·s-1 |
| C.0.35mol·L-1·s-1 | D.4.2mol·L-1·s-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
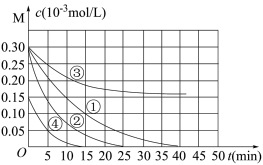
【推荐2】用Na2FeO4 溶液氧化废水中的还原性污染物 M,为研究降解效果。设计如下对比实验探究温度、浓度、pH 对降解速率和效果的影响,实验测得 M 的浓度与时间关系如图所示,下列说法错误的是

| 实验编号 | 温度℃ | pH |
| ① | 25 | 1 |
| ② | 45 | 1 |
| ③ | 25 | 7 |
| ④ | 25 | 1 |
| A.实验①在 15min 内 M 的降解速率为 1.33×10-5mol/(L·min) |
| B.实验①②说明升高温度,M 降解速率增大 |
| C.实验①③证明 pH 越高,越不利于 M 的降解 |
| D.实验②④说明 M 的浓度越小,降解的速率越慢 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】反应4NH3 + 5O2 === 4NO + 6H2O 在5L的密闭容器中进行,30s后,NO的物质的量增加了0.3mol,则此反应的平均速率可表示为:
| A.v (O2)=0.01 mol/(L·s) | B.v (NO)=0.008 mol/(L·s) |
| C.v (H2O)=0.015 mol/(L·s) | D.v (NH3)=0.002 mol/(L·s) |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】某温度时,浓度均为 的两种气体
的两种气体 和
和 ,在体积恒定的密闭容器中反应生成气体
,在体积恒定的密闭容器中反应生成气体 ,4s时
,4s时 、
、 、
、 的浓度分别是
的浓度分别是 、
、 、
、 ,若
,若 用
用 、
、 表示,则该反应的化学方程式可表示为
表示,则该反应的化学方程式可表示为
 的两种气体
的两种气体 和
和 ,在体积恒定的密闭容器中反应生成气体
,在体积恒定的密闭容器中反应生成气体 ,4s时
,4s时 、
、 、
、 的浓度分别是
的浓度分别是 、
、 、
、 ,若
,若 用
用 、
、 表示,则该反应的化学方程式可表示为
表示,则该反应的化学方程式可表示为A. | B. |
C. | D. |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】不能用勒夏特列原理解释的是
| A.用排饱和食盐水的方法收集氯气 |
B.HI、 、 、 形成的平衡混合气,加压时颜色变深 形成的平衡混合气,加压时颜色变深 |
| C.可用浓氨水和氢氧化钠固体,快速制取氨气 |
D.加压条件下有利于 和 和 反应生成 反应生成 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列实验的操作、现象和结论(或解释)均正确的是( )
| 操作 | 现象 | 结论(或解释) | |
| A | 向某溶液中滴加Ba(NO3)2溶液和稀盐酸 | 生成白色沉淀 | 原溶液中有SO42- |
| B | 密闭容器中有反应:A(g)+B(g) xC(g)达到平衡时测得c(C)为0.5 mol·L-1,将容器容积缩小至原来的一半 xC(g)达到平衡时测得c(C)为0.5 mol·L-1,将容器容积缩小至原来的一半 | 再次达到平衡时测得c(C)为0.8mol·L-1 | x=l,增大压强平衡正向移动 |
| C | 往试管中加入2mL 10%的CuSO4溶液,再滴入4~6滴2%的NaOH溶液,振荡后加入2mL葡萄糖溶液,加热煮沸 | 产生砖红色沉淀 | 葡萄糖分子结构中有醛基 |
| D | 向某溶液中滴加新制氯水和CCl4,振荡、静置 | 下层溶液显紫红色 | 原溶液中有I- |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
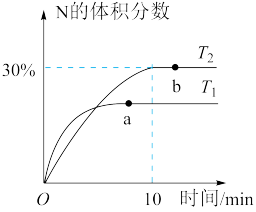
【推荐1】将2 mol X和0.8 mol Y置于体积为2 L的恒容密闭容器中,发生反应:2X(g)+Y(s)  M(g)+N(g) ΔH。反应过程中测得N的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是
M(g)+N(g) ΔH。反应过程中测得N的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是
 M(g)+N(g) ΔH。反应过程中测得N的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是
M(g)+N(g) ΔH。反应过程中测得N的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是
| A.无论温度为T1还是T2,当容器中气体密度和压强不变时,反应均达平衡状态 |
B.温度为T2时,X的平衡转化率为60%,平衡常数K=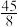 |
| C.若a、b两点的平衡常数分别为K1、K2,则K1<K2 |
| D.降低温度、增大压强、及时分离出产物均有利于提高反应物的平衡转化率 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】一定温度下,在三个体积均为1L的恒容密闭容器中发生反应:2CH3OH(g) CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
下列说法正确的是
 CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)| 容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
| CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
| ① | 387 | 0.20 | 0.080 | 0.080 |
| ② | 387 | 0.40 | ||
| ③ | 207 | 0.20 | 0.090 | 0.090 |
| A.该反应的正反应为吸热反应 |
| B.达到平衡时,容器①中的CH3OH体积分数比容器②中的小 |
| C.若容器①中反应达到平衡时增大压强,则各物质浓度保持增大 |
| D.若起始向容器①中充入CH3OH 0.10mol、CH3OCH30.10mol、H2O 0.10mol,则反应将向逆反应方向进行 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐3】在体积可变的密闭容器中投入0.5molO2和1molSO2,不同条件下发生反应:O2(g)+2SO2(g)  2SO3(g) ΔH。实验测得平衡时SO2的转化率[α(SO2)]随温度、压强的变化如图所示。下列说法错误的是
2SO3(g) ΔH。实验测得平衡时SO2的转化率[α(SO2)]随温度、压强的变化如图所示。下列说法错误的是

 2SO3(g) ΔH。实验测得平衡时SO2的转化率[α(SO2)]随温度、压强的变化如图所示。下列说法错误的是
2SO3(g) ΔH。实验测得平衡时SO2的转化率[α(SO2)]随温度、压强的变化如图所示。下列说法错误的是
| A.Y代表压强,且Y1>Y2,X代表温度,且ΔH<0 |
| B.M点反应物转化率之比α(O2):α(SO2)=1:1,N点该比例减小 |
| C.若M、N两点对应的容器体积均为5L,则N点的平衡常数K=20 |
| D.M、N两点对应的平均摩尔质量:M(M)>M(N) |
您最近一年使用:0次

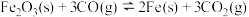 。一定温度下,在2L的密闭容器中加入
。一定温度下,在2L的密闭容器中加入 粉末和一定量的CO气体模拟炼铁的反应,测得容器内固体的质量随时间的变化如下:
粉末和一定量的CO气体模拟炼铁的反应,测得容器内固体的质量随时间的变化如下:
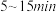 的平均速率v(CO)为
的平均速率v(CO)为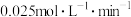

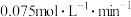
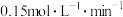

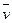
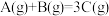 ;(正反应为放热反应)某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:下列判断
;(正反应为放热反应)某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:下列判断