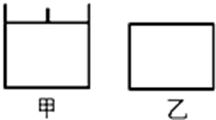
已知甲为恒压容器、乙为恒容容器.相同条件下充入等物质的量的NO2气体,且起始时体积相同,发生反应:2NO2(g)⇌N2O4(g)△H<0.一段时间后相继达到平衡状态..下列说法中错误的是

| A.该反应的平衡常数表达式K=c(N2O4)/c2(NO2) |
| B.若乙容器内气体的压强保持不变,说明反应已达到平衡状态 |
| C.平衡时NO2体积分数:甲>乙 |
| D.达到平衡所需时间,甲所需时间短 |
更新时间:2018-04-23 06:11:57
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】已知Ⅰ容器恒压,Ⅱ容器恒容,其它条件相同时,在Ⅰ、Ⅱ中分别加入3molZ,起始时容积相同,发生反应2X(g)+2Y(s)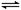 3Z(g)并达平衡。下列说法正确的是
3Z(g)并达平衡。下列说法正确的是

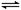 3Z(g)并达平衡。下列说法正确的是
3Z(g)并达平衡。下列说法正确的是
| A.从起始到平衡所需时间:Ⅰ>Ⅱ |
| B.平衡时Z的转化率:Ⅰ<Ⅱ |
| C.平衡后若在Ⅰ中再加入0.1molY,则X的物质的量将减少 |
| D.平衡后若在Ⅱ中再加入2molZ,则新平衡时Z的体积分数变小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在相同温度和压强下,对反应X(g)+Y(g) Z(g)+W(g)进行四组实验,实验起始时放入容器内各组分的物质的量见表:
Z(g)+W(g)进行四组实验,实验起始时放入容器内各组分的物质的量见表:
上述四种情况达到平衡后,n(Z)的大小顺序是( )
 Z(g)+W(g)进行四组实验,实验起始时放入容器内各组分的物质的量见表:
Z(g)+W(g)进行四组实验,实验起始时放入容器内各组分的物质的量见表:| 实验 | X | Y | Z | W |
| ① | amol | amol | 0mol | 0mol |
| ② | 3amol | amol | 0mol | 0mol |
| ③ | 0mol | 0mol | amol | amol |
| ④ | 2amol | 0mol | amol | amol |
上述四种情况达到平衡后,n(Z)的大小顺序是( )
| A.②=④>①=③ | B.②>④>①>③ |
| C.④>②>①=③ | D.④>③>②>① |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】工业制氢气的一个重要反应是:CO(g)+H2O(g)=CO2(g)+H2(g)。
已知在25℃时:①C(s)+ O2(g)
O2(g) CO(g) ∆H4=-111kJ/mol
CO(g) ∆H4=-111kJ/mol
②H2(g)+ O2(g)=H2(g) ∆H2=-242kJ/mol
O2(g)=H2(g) ∆H2=-242kJ/mol
③C(s)+O2(g)=CO2(g) ∆H2=-394kJ/mol
下列说法不正确的是( )
已知在25℃时:①C(s)+
 O2(g)
O2(g) CO(g) ∆H4=-111kJ/mol
CO(g) ∆H4=-111kJ/mol②H2(g)+
 O2(g)=H2(g) ∆H2=-242kJ/mol
O2(g)=H2(g) ∆H2=-242kJ/mol③C(s)+O2(g)=CO2(g) ∆H2=-394kJ/mol
下列说法不正确的是( )
A.25℃时,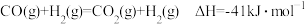 |
| B.增大压强,反应①的平衡向逆反应方向移,平衡常数K减小 |
C.反应①达到平衡时,每生成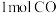 的同时生成0.5molO2 的同时生成0.5molO2 |
| D.反应②断开2molH2和1molO2中的化学键所吸收的能量比形成4molO-H键所放出的能量少484kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】硫酸是重要的化工原料。稀硫酸具有酸的通性;浓硫酸具有很强的氧化性,能氧化大多数金属单质和部分非金属单质。金属冶炼时产生的含SO2废气经回收处理、催化氧化、吸收后可制得硫酸。2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6kJ·mol-1。工业制硫酸尾气中的SO2可用氨水吸收,吸收液经处理后释放出的SO2又可循环利用。对于反应2SO2(g)+O2(g)
2SO3(g) ΔH=-196.6kJ·mol-1。工业制硫酸尾气中的SO2可用氨水吸收,吸收液经处理后释放出的SO2又可循环利用。对于反应2SO2(g)+O2(g) 2SO3(g),下列说法正确的是
2SO3(g),下列说法正确的是
 2SO3(g) ΔH=-196.6kJ·mol-1。工业制硫酸尾气中的SO2可用氨水吸收,吸收液经处理后释放出的SO2又可循环利用。对于反应2SO2(g)+O2(g)
2SO3(g) ΔH=-196.6kJ·mol-1。工业制硫酸尾气中的SO2可用氨水吸收,吸收液经处理后释放出的SO2又可循环利用。对于反应2SO2(g)+O2(g) 2SO3(g),下列说法正确的是
2SO3(g),下列说法正确的是| A.反应的ΔS>0 |
B.反应的平衡常数可表示为K=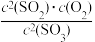 |
| C.增大体系的压强能提高SO2的反应速率和转化率 |
| D.使用催化剂能改变反应路径,提高反应的活化能 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某温度下,反应ClF(g)+F2(g)  ClF3(g) △H = -268 kJ·mol-1 在密闭容器中达到平衡。下列说法正确的是
ClF3(g) △H = -268 kJ·mol-1 在密闭容器中达到平衡。下列说法正确的是
 ClF3(g) △H = -268 kJ·mol-1 在密闭容器中达到平衡。下列说法正确的是
ClF3(g) △H = -268 kJ·mol-1 在密闭容器中达到平衡。下列说法正确的是 | A.温度不变,缩小体积,ClF的转化率增大 |
| B.温度不变,增大体积,ClF3产率提高 |
| C.升高温度,增大体积,有利于平衡向正反应方向移动 |
| D.降低温度,体积不变,F2转化率降低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】高温下,某反应达平衡,平衡常数K= ,恒容时,温度升高,B的浓度减小,下列说法正确的是
,恒容时,温度升高,B的浓度减小,下列说法正确的是
①该反应的焓变为正值
②恒温恒容下,增大压强B浓度一定增大
③升高温度,平衡常数K值减小
④该反应化学方程式为C(g)+D(g) A(g)+B(g)
A(g)+B(g)
⑤增加A的量,A的转化率减小
⑥加入催化剂,平衡不移动,V(正)、V(逆)都不变
 ,恒容时,温度升高,B的浓度减小,下列说法正确的是
,恒容时,温度升高,B的浓度减小,下列说法正确的是①该反应的焓变为正值
②恒温恒容下,增大压强B浓度一定增大
③升高温度,平衡常数K值减小
④该反应化学方程式为C(g)+D(g)
 A(g)+B(g)
A(g)+B(g)⑤增加A的量,A的转化率减小
⑥加入催化剂,平衡不移动,V(正)、V(逆)都不变
| A.①③⑥ | B.①⑤ | C.①④⑤ | D.①②⑤ |
您最近一年使用:0次
【推荐1】在一定温度下,将气体 X和气体Y各0.16mol充入 10L恒容密闭容器中,发生反应: X(g) + Y(g) ⇌ 2Z(g) △ H < 0.一段时间后达到平衡,反应过程中测定的数据如表,下列说法正确的是
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A.反应前 2 min 的平均速率v(Z) > 2.0 × 10−3 mol·L-1·min-1 |
| B.其他条件不变,降低温度,反应达到新平衡前:v(逆) > v(正) |
| C.保持其他条件不变,起始时向容器中充入0.32 mol气体 X和0.32 mol气体Y,到达平衡时,c(Z) > 0.24 mol·L-1 |
| D.该温度下此反应的平衡常数:K = 1.44 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应2SO2(g)+O2(g) 2SO3(g)(正反应放热),测得反应的相关数据如下:
2SO3(g)(正反应放热),测得反应的相关数据如下:
下列说法正确的是
 2SO3(g)(正反应放热),测得反应的相关数据如下:
2SO3(g)(正反应放热),测得反应的相关数据如下:| 容器1 | 容器2 | 容器3 | |
| 反应温度T/K | 700 | 700 | 800 |
| 反应物投入量 | 2 mol SO2、 1 mol O2 | 4 mol SO3 | 2 mol SO2、 1 mol O2 |
| 平衡v正(SO2)/mol·L-1·s-1 | v1 | v2 | v3 |
| 平衡c(SO3)/mol·L-1 | c1 | c2 | c3 |
| 平衡体系总压强p/Pa | p1 | p2 | p3 |
| 物质的平衡转化率α | α1(SO2) | α2(SO3) | α3(SO2) |
| 平衡常数K | K1 | K2 | K3 |
| A.v1<v2,c2<2c1 |
| B.K1>K3,p2>2p3 |
| C.v1<v3,α1(SO2)>α3(SO2) |
| D.c2>2c3,α2(SO3)+α3(SO2)=1 |
您最近一年使用:0次




 ,下列有关说法正确的是
,下列有关说法正确的是 2NO2(g)ΔH<0的速率方程为v正=k正cα(NO)cβ(O2),在T℃下测定了不同初始浓度及正反应速率的关系,数据如下表。下列说法错误的是
2NO2(g)ΔH<0的速率方程为v正=k正cα(NO)cβ(O2),在T℃下测定了不同初始浓度及正反应速率的关系,数据如下表。下列说法错误的是
 是一种新型硝化剂,在一定温度下可发生如下反应:
是一种新型硝化剂,在一定温度下可发生如下反应: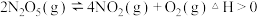 ,
, 温度时,向密闭容器中通入
温度时,向密闭容器中通入
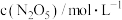

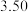
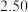
 的生成速率为
的生成速率为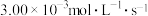

 ,
,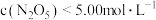
 ,
, 温度下的平衡常数为
温度下的平衡常数为 ,若
,若 ,则
,则


