现将0.4 mol A气体和0.2 mol B气体充入10 L的密闭容器中,在一定条件下使其发生反应生成气体C,其物质的量的变化如图:

(1)若t1=10 min,则0至t1时间内C物质的平均反应速率为________ ;该反应在t1时达到平衡,其化学方程式为____________________________________ 。
(2)据图中曲线变化情况分析,t1时刻改变的反应条件可能是________ 。
A.加入了催化剂 B.降低了反应温度
C.向容器中充入了C D.缩小了容器体积

(1)若t1=10 min,则0至t1时间内C物质的平均反应速率为
(2)据图中曲线变化情况分析,t1时刻改变的反应条件可能是
A.加入了催化剂 B.降低了反应温度
C.向容器中充入了C D.缩小了容器体积
更新时间:2018-10-20 23:06:43
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.700℃时,若向2L恒容的密闭容器中充入一定量N2和CO2发生反应:N2(g)+CO2(g) C(s)+2NO(g);其中N2、NO物质的量随时间变化的曲线如图所示。
C(s)+2NO(g);其中N2、NO物质的量随时间变化的曲线如图所示。

(1)0~10min 内的 CO2平均反应速率v( CO2)=___________
(2)图中A点v正___________ v逆(填“>”“<”或“=”)。
(3)下列叙述中能说明上述反应达到平衡状态的是___________ 。
A.反应中CO2与N2的物质的量之比为1∶1
B.混合气体的总物质的量不随时间的变化而变化
C.单位时间内每消耗a mol N2,同时消耗2a mol NO
D.N2的质量分数在混合气体中保持不变
E.混合气体的密度不随时间的变化而变化
Ⅱ.氢氧燃料电池的电解质溶液为KOH溶液,电池总反应为2H2+O2=2H2O。回答下列问题:
(4)该电池的负极反应式为___________ 。
(5)电池工作一段时间后电解质溶液的
___________ (填“增大”“减小”或“不变”)。
 C(s)+2NO(g);其中N2、NO物质的量随时间变化的曲线如图所示。
C(s)+2NO(g);其中N2、NO物质的量随时间变化的曲线如图所示。
(1)0~10min 内的 CO2平均反应速率v( CO2)=
(2)图中A点v正
(3)下列叙述中能说明上述反应达到平衡状态的是
A.反应中CO2与N2的物质的量之比为1∶1
B.混合气体的总物质的量不随时间的变化而变化
C.单位时间内每消耗a mol N2,同时消耗2a mol NO
D.N2的质量分数在混合气体中保持不变
E.混合气体的密度不随时间的变化而变化
Ⅱ.氢氧燃料电池的电解质溶液为KOH溶液,电池总反应为2H2+O2=2H2O。回答下列问题:
(4)该电池的负极反应式为
(5)电池工作一段时间后电解质溶液的

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化学与生产生活紧密联系,人们通过研究化学变化以达到控制化学反应的目的。
(1)叠氮化钠( )可作为汽车安全气囊的气体发生剂。当汽车发生碰撞时,气体发生剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
)可作为汽车安全气囊的气体发生剂。当汽车发生碰撞时,气体发生剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
① 是
是_______ (填“离子”或“共价”)化合物。
②汽车受到猛烈碰撞时,点火器点火引发迅速分解释放大量的热。下列可表示该反应过程中能量变化的是_______ 。(填字母)
a.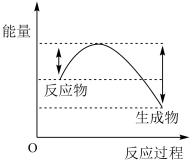 b.
b. 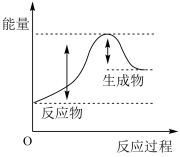 c.
c. 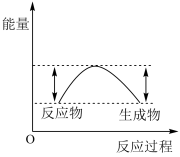
③安全气囊的气体发生剂中含有 固体。已知
固体。已知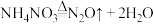 ,推测安全气囊中
,推测安全气囊中 的作用为
的作用为_______ 。
(2)一定温度下,2L密闭刚性容器内发生反应: ,
,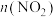 随时间变化如下表:
随时间变化如下表:
①在0~2s内, 的反应速率为
的反应速率为_______ 。
②平衡时容器的压强与起始时的压强之比为_______ 。
③下列叙述中能说明上述反应达到平衡状态的是_______ 。(填字母)
a. 与
与 的反应速率之比为2:1
的反应速率之比为2:1
b.体系的颜色保持不变
c.混合气体的压强不随时间的变化而变化
d.混合气体的密度不随时间的变化而变化
e.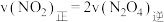
④下列措施可加快该反应速率的是_______ 。(填字母)
a.适当升高温度 b.恒容时充入Ne c.增大容器的体积 d.选择高效催化剂
(1)叠氮化钠(
 )可作为汽车安全气囊的气体发生剂。当汽车发生碰撞时,气体发生剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
)可作为汽车安全气囊的气体发生剂。当汽车发生碰撞时,气体发生剂产生大量气体使气囊迅速膨胀,从而起到保护作用。①
 是
是②汽车受到猛烈碰撞时,点火器点火引发迅速分解释放大量的热。下列可表示该反应过程中能量变化的是
a.
 b.
b.  c.
c. 
③安全气囊的气体发生剂中含有
 固体。已知
固体。已知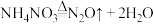 ,推测安全气囊中
,推测安全气囊中 的作用为
的作用为(2)一定温度下,2L密闭刚性容器内发生反应:
 ,
,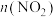 随时间变化如下表:
随时间变化如下表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
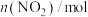 | 0.40 | 0.20 | 0.10 | 0.05 | 0.05 | 0.05 |
①在0~2s内,
 的反应速率为
的反应速率为②平衡时容器的压强与起始时的压强之比为
③下列叙述中能说明上述反应达到平衡状态的是
a.
 与
与 的反应速率之比为2:1
的反应速率之比为2:1 b.体系的颜色保持不变
c.混合气体的压强不随时间的变化而变化
d.混合气体的密度不随时间的变化而变化
e.
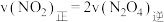
④下列措施可加快该反应速率的是
a.适当升高温度 b.恒容时充入Ne c.增大容器的体积 d.选择高效催化剂
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.草酸与高锰酸钾在酸性条件下能够发生如下反应:Mn +H2C2O4+H+→Mn2++CO2↑+H2O(未配平),用4 mL 0.001 mol·L-1 KMnO4溶液与2 mL 0.01 mol·L-1 H2C2O4溶液研究不同条件对化学反应速率的影响。改变的条件如下:
+H2C2O4+H+→Mn2++CO2↑+H2O(未配平),用4 mL 0.001 mol·L-1 KMnO4溶液与2 mL 0.01 mol·L-1 H2C2O4溶液研究不同条件对化学反应速率的影响。改变的条件如下:
(1)该反应中氧化剂和还原剂的物质的量之比为_______ 。
(2)如果研究催化剂对化学反应速率的影响,使用实验_______ 和_______ (用Ⅰ~Ⅳ表示,下同);如果研究温度对化学反应速率的影响,使用实验_______ 和_______ 。
(3)对比实验Ⅰ和Ⅳ,可以研究_______ 对化学反应速率的影响,实验Ⅳ加入1 mL蒸馏水的目的是_______ 。
II.某可逆反应在容积为5 L的密闭容器中进行,在从0~3 min内各物质的量的变化情况如图所示(A、B、C均为气体)。
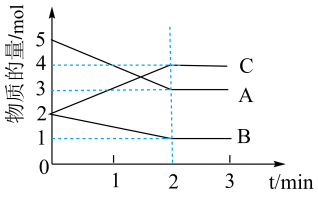
(4)该反应的化学方程式为_______ 。
(5)反应开始至2分钟时,B的平均反应速率为_______ 。
(6)在密闭容器里,通入a mol A(g)、b mol B(g)、c mol C(g),发生上述反应,当改变下列条件时,反应速率会减小的是_______ (填序号)。
①降低温度 ②加入催化剂 ③增大容器体积
 +H2C2O4+H+→Mn2++CO2↑+H2O(未配平),用4 mL 0.001 mol·L-1 KMnO4溶液与2 mL 0.01 mol·L-1 H2C2O4溶液研究不同条件对化学反应速率的影响。改变的条件如下:
+H2C2O4+H+→Mn2++CO2↑+H2O(未配平),用4 mL 0.001 mol·L-1 KMnO4溶液与2 mL 0.01 mol·L-1 H2C2O4溶液研究不同条件对化学反应速率的影响。改变的条件如下:| 实验编号 | 10%硫酸溶液的体积/mL | 温度/℃ | 其他物质 |
| Ⅰ | 2 | 20 | — |
| Ⅱ | 2 | 20 | 10滴饱和MnSO4溶液 |
| Ⅲ | 2 | 30 | — |
| Ⅳ | 1 | 20 | 1 mL蒸馏水 |
(2)如果研究催化剂对化学反应速率的影响,使用实验
(3)对比实验Ⅰ和Ⅳ,可以研究
II.某可逆反应在容积为5 L的密闭容器中进行,在从0~3 min内各物质的量的变化情况如图所示(A、B、C均为气体)。

(4)该反应的化学方程式为
(5)反应开始至2分钟时,B的平均反应速率为
(6)在密闭容器里,通入a mol A(g)、b mol B(g)、c mol C(g),发生上述反应,当改变下列条件时,反应速率会减小的是
①降低温度 ②加入催化剂 ③增大容器体积
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】一定条件下,某可逆反应在密闭容器中建立化学平衡,在t1时刻改变某一个条件,建立新的平衡,其v-t图像如下:
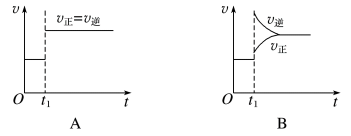
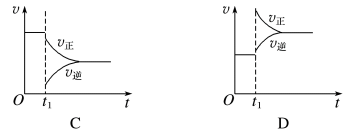
(1)对于反应:2SO2(g)+O2(g)⇌2SO3(g),t1时刻增大压强,其图像为___________ ,平衡___________ (填“向正反应方向”“向逆反应方向”或“不”,下同)移动。
(2)对于反应2NH3(g)⇌N2(g)+3H2(g),t1时刻增大容器体积,其图像为___________ ,平衡___________ 移动。
(3)对于反应N2(g)+3H2(g)⇌2NH3(g) ΔH=-92kJ·mol-1,达到平衡t1时刻其图像为B,则改变的反应条件是___________
(4)对于反应H2(g)+I2(g)⇌2HI(g),t1时刻缩小容器体积,其图像为___________ ,平衡___________ 移动。


(1)对于反应:2SO2(g)+O2(g)⇌2SO3(g),t1时刻增大压强,其图像为
(2)对于反应2NH3(g)⇌N2(g)+3H2(g),t1时刻增大容器体积,其图像为
(3)对于反应N2(g)+3H2(g)⇌2NH3(g) ΔH=-92kJ·mol-1,达到平衡t1时刻其图像为B,则改变的反应条件是
(4)对于反应H2(g)+I2(g)⇌2HI(g),t1时刻缩小容器体积,其图像为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】为了防止枪支生锈,常将枪支的钢铁零件放在NaNO2和NaOH的混合液中进行化学处理经处理后钢铁零件表面生成Fe3O4的致密的保护层——“发蓝”。主要反应如①②③:
①3Fe+NaNO2+5NaOH→3NaFeO2+NH3+H2O
②Na2FeO2+NaNO2+H2O→Na2Fe2O4+NH3+NaOH
③Na2FeO2+Na2Fe2O4+2H2O Fe3O4+4NaOH
Fe3O4+4NaOH
(1)配平化学方程式②,标出电子转移方向和数目。
______________________________________________________________________
(2)上述反应②中还原剂为___________ ,被还原物质是__________ 。
若有1mol Na2Fe2O4生成,则反应中有____ mol电子转移。
(3)当NaOH溶液浓度过大,“发蓝”的厚度会变小,其原因是:________ 。
①3Fe+NaNO2+5NaOH→3NaFeO2+NH3+H2O
②Na2FeO2+NaNO2+H2O→Na2Fe2O4+NH3+NaOH
③Na2FeO2+Na2Fe2O4+2H2O
 Fe3O4+4NaOH
Fe3O4+4NaOH(1)配平化学方程式②,标出电子转移方向和数目。
(2)上述反应②中还原剂为
若有1mol Na2Fe2O4生成,则反应中有
(3)当NaOH溶液浓度过大,“发蓝”的厚度会变小,其原因是:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】甲醛(HCHO)在化工、医药、农药等方面有广泛的应用。利用甲醛一定条件下直接脱氢可制甲醛,反应方程式:CH3OH(g) HCHO(g)+H2(g) △H1
HCHO(g)+H2(g) △H1
实验测得随温度升高,平衡常数如下表所示。
(1)甲醛分子中所有原子都达到稳定结构,甲醛的电子式为_____________ 。
(2) 若在恒温恒压容器中进行上述反应,可判断反应到达平衡状态的是_______________ 。
A.混合气体的密度不变
B.CH3OH、HCHO的物质的量浓度之比为1:1
C.H2的体积分数不再改变
D.单位时间内甲醛的生成量与氢气的消耗量相等
(3)T1时,CH3OH、HCHO、H2 起始浓度(mol·L-1)分别为1.0、0.50 、1.0,反应达到平衡时,HCHO 的体积分数___________ 20% (填“>”、“ =”、“ <”)。
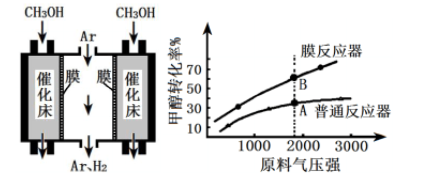
(4)工业上采用膜分离器(对氢气具有很高的选择性和透过率)催化脱氢,装置如下图。为探究转化率变化,分别在普通反应器和膜反应器中,改变原料气压强,控制相同温度,经过相同反应时间,测定甲醇转化率,实验结果如下图。
①A点:v正______ v逆(填“>”、“ =”、“ <”),理由是____________ ;
②B点比A点转化率高的原因是_______________ 。
(5)体系中加入一定量氧气有利于甲醛的生成。反应体系中存在下列反应:
CH3OH(g)+1/2O2(g) HCHO(g)+H2O(g) △H2
HCHO(g)+H2O(g) △H2
H2(g)+12O2(g) H2O(g) △H3
H2O(g) △H3
则△H2、△H3的大小关系是△H2________ △H3(填“>”、“ =”、“ <”)。
 HCHO(g)+H2(g) △H1
HCHO(g)+H2(g) △H1实验测得随温度升高,平衡常数如下表所示。
温度(K) | 500 | 700 | T1 | T2 | T3 |
平衡常数 | 7.13×10-4 | 3.30×10-1 | 2.00 | 9.00 | 10.00 |
(2) 若在恒温恒压容器中进行上述反应,可判断反应到达平衡状态的是
A.混合气体的密度不变
B.CH3OH、HCHO的物质的量浓度之比为1:1
C.H2的体积分数不再改变
D.单位时间内甲醛的生成量与氢气的消耗量相等
(3)T1时,CH3OH、HCHO、H2 起始浓度(mol·L-1)分别为1.0、0.50 、1.0,反应达到平衡时,HCHO 的体积分数
(4)工业上采用膜分离器(对氢气具有很高的选择性和透过率)催化脱氢,装置如下图。为探究转化率变化,分别在普通反应器和膜反应器中,改变原料气压强,控制相同温度,经过相同反应时间,测定甲醇转化率,实验结果如下图。
①A点:v正
②B点比A点转化率高的原因是

(5)体系中加入一定量氧气有利于甲醛的生成。反应体系中存在下列反应:
CH3OH(g)+1/2O2(g)
 HCHO(g)+H2O(g) △H2
HCHO(g)+H2O(g) △H2H2(g)+12O2(g)
 H2O(g) △H3
H2O(g) △H3则△H2、△H3的大小关系是△H2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】I. 在一定条件下,可逆反应A+B mC变化如图所示。已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后向容器加压的变化情况。
mC变化如图所示。已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后向容器加压的变化情况。
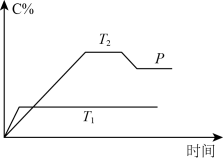
(1)温度T1________ T2(填“大于”“等于”或“小于”)。
(2)正反应是________ 反应(填“吸热”或“放热”)。
(3)如果A、B、C均为气体,则m________ 2(填“大于”“等于”或“小于”)。
(4)当温度和容积不变时,如在平衡体系中加入一定量的某稀有气体,则体系的压强________ (填“增大”“减小”或“不变”),平衡_________________ 移动(填“向正反应方向”“向逆反应方向”或“不”)。
II. CO是生产羰基化学品的基本原料, 850℃时,在恒容密闭容器中通入CO和H2O(g),发生:CO(g)+H2O(g) H2(g)+CO2(g)
H2(g)+CO2(g)  H<0,测定浓度随时间关系如下表:
H<0,测定浓度随时间关系如下表:
回答下列问题
(1)t=3min时,υ(正)____________ υ(逆)(选填:“>”,“<”,“=”)。
(2)0~2min,CO的平均反应速率为____________ 。
(3)上述反应中的CO平衡转化率为____________ 。
(4)在一定条件下,发生下列反应:CO(g)+H2O(g) H2(g)+CO2(g),其逆反应的速率随时间变化曲线如图所示,则t1时改变的某种反应条件可能是
H2(g)+CO2(g),其逆反应的速率随时间变化曲线如图所示,则t1时改变的某种反应条件可能是_____ (填序号)。
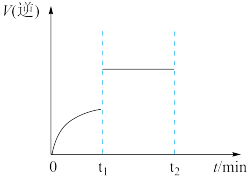
a.增大CO浓度
b.加压
c.恒容时充入氩气
d.使用催化剂
 mC变化如图所示。已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后向容器加压的变化情况。
mC变化如图所示。已知纵坐标表示在不同温度和压强下生成物C在混合物中的质量分数,p为反应在T2温度时达到平衡后向容器加压的变化情况。
(1)温度T1
(2)正反应是
(3)如果A、B、C均为气体,则m
(4)当温度和容积不变时,如在平衡体系中加入一定量的某稀有气体,则体系的压强
II. CO是生产羰基化学品的基本原料, 850℃时,在恒容密闭容器中通入CO和H2O(g),发生:CO(g)+H2O(g)
 H2(g)+CO2(g)
H2(g)+CO2(g)  H<0,测定浓度随时间关系如下表:
H<0,测定浓度随时间关系如下表:| t/min | c(CO)/ mol·L-1 | c(H2O)/ mol·L-1 |
| 0 | 0.30 | 0.20 |
| 2 | \ | 0.10 |
| 3 | 0.18 | \ |
| 4 | \ | 0.08 |
回答下列问题
(1)t=3min时,υ(正)
(2)0~2min,CO的平均反应速率为
(3)上述反应中的CO平衡转化率为
(4)在一定条件下,发生下列反应:CO(g)+H2O(g)
 H2(g)+CO2(g),其逆反应的速率随时间变化曲线如图所示,则t1时改变的某种反应条件可能是
H2(g)+CO2(g),其逆反应的速率随时间变化曲线如图所示,则t1时改变的某种反应条件可能是
a.增大CO浓度
b.加压
c.恒容时充入氩气
d.使用催化剂
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】向1L的密闭容器中加入1molX、0.3molZ和0.5molY三种气体。一定条件下发生反应,各物质的浓度随时间的变化如图甲所示。图乙为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件,且没有使用催化剂。
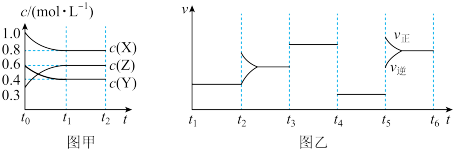
(1)请写出该反应的化学方程式___________ 。
(2)图乙中处于平衡的时间段是___________
(3)t3、t4、t5时刻改变的条件分别是___________ 、___________ 、___________ ,该反应
___________ 0(填“<”或“>”)。
(4)已知反应 ,改变下列条件,平衡如何移动(填“正向”“逆向”或“不”)。
,改变下列条件,平衡如何移动(填“正向”“逆向”或“不”)。
①增加反应物的浓度,平衡___________ 移动;
②增大压强,平衡___________ 移动;
③降低温度,平衡___________ 移动。

(1)请写出该反应的化学方程式
(2)图乙中处于平衡的时间段是___________
| A.t1-t2 | B.t2-t3 | C.t3-t5 | D.t5-t6 |
(3)t3、t4、t5时刻改变的条件分别是

(4)已知反应
 ,改变下列条件,平衡如何移动(填“正向”“逆向”或“不”)。
,改变下列条件,平衡如何移动(填“正向”“逆向”或“不”)。①增加反应物的浓度,平衡
②增大压强,平衡
③降低温度,平衡
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】亚硝酰氯(C1NO,黄色)是有机物合成中的重要试剂,常用于合成洗涤剂。在温度500 K时,向盛有食盐的恒容密闭容器中加入NO2、NO和Cl2,发生如下两个反应:
Ⅰ.2NO2(g)+NaCl(s)⇌NaNO3(s)+ClNO(g) ∆H1
Ⅱ.2NO(g)+Cl2(g)⇌2ClNO(g) ∆H2
(1)反应Ⅱ在一定条件下能自发进行,判断该反应的热效应,并说明理由______ 。
(2)关于恒温恒容密闭容器中进行的反应Ⅰ和Ⅱ的下列说法中,正确的是______ (填标号)。
a.反应体系中混合气体的颜色保持不变,说明反应Ⅰ达到平衡状态
b.∆H1和∆H2不再变化,可以作为判断反应Ⅰ和Ⅱ是否达到平衡状态的标志
c.同等条件下,反应Ⅰ的速率远远大于反应Ⅱ,说明反应Ⅰ的活化能小,∆H1<∆H2
d.达平衡后,向反应体系中再通入一定量C1NO(g),NO2(g)和NO(g)的百分含量均减小
(3)向2L恒容密闭容器中加入0.2 mol NO和0.1 mol Cl2发生反应Ⅱ,起始总压为p0。10分钟后达到平衡,用ClNO(g)表示平均反应速率v平(ClNO)=0.008mol·L-1·min-1。
①平衡时Cl2的压强为______ 。
②NO的平衡转化率α=______ ,影响α的因素有______ 。
③该反应的平衡常数Kp=______ (以分压表示,分压=总压×物质的量分数)。
(4)假设反应Ⅱ的速率方程为: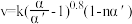 ,式中:k为反应速率常数,随温度t升高而增大;α为NO平衡转化率,α′为某时刻NO转化率,n为常数。在α′=0.8时,将一系列温度下的k、α值代入上述速率方程,得到v~t曲线如图所示。
,式中:k为反应速率常数,随温度t升高而增大;α为NO平衡转化率,α′为某时刻NO转化率,n为常数。在α′=0.8时,将一系列温度下的k、α值代入上述速率方程,得到v~t曲线如图所示。
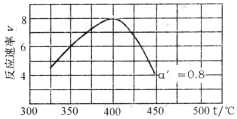
曲线上v最大值所对应温度称为该α'下反应的最适宜温度tm,t<tm时,v逐渐提高;t>tm后,v逐渐下降。原因是______ 。
Ⅰ.2NO2(g)+NaCl(s)⇌NaNO3(s)+ClNO(g) ∆H1
Ⅱ.2NO(g)+Cl2(g)⇌2ClNO(g) ∆H2
(1)反应Ⅱ在一定条件下能自发进行,判断该反应的热效应,并说明理由
(2)关于恒温恒容密闭容器中进行的反应Ⅰ和Ⅱ的下列说法中,正确的是
a.反应体系中混合气体的颜色保持不变,说明反应Ⅰ达到平衡状态
b.∆H1和∆H2不再变化,可以作为判断反应Ⅰ和Ⅱ是否达到平衡状态的标志
c.同等条件下,反应Ⅰ的速率远远大于反应Ⅱ,说明反应Ⅰ的活化能小,∆H1<∆H2
d.达平衡后,向反应体系中再通入一定量C1NO(g),NO2(g)和NO(g)的百分含量均减小
(3)向2L恒容密闭容器中加入0.2 mol NO和0.1 mol Cl2发生反应Ⅱ,起始总压为p0。10分钟后达到平衡,用ClNO(g)表示平均反应速率v平(ClNO)=0.008mol·L-1·min-1。
①平衡时Cl2的压强为
②NO的平衡转化率α=
③该反应的平衡常数Kp=
(4)假设反应Ⅱ的速率方程为:
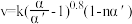 ,式中:k为反应速率常数,随温度t升高而增大;α为NO平衡转化率,α′为某时刻NO转化率,n为常数。在α′=0.8时,将一系列温度下的k、α值代入上述速率方程,得到v~t曲线如图所示。
,式中:k为反应速率常数,随温度t升高而增大;α为NO平衡转化率,α′为某时刻NO转化率,n为常数。在α′=0.8时,将一系列温度下的k、α值代入上述速率方程,得到v~t曲线如图所示。
曲线上v最大值所对应温度称为该α'下反应的最适宜温度tm,t<tm时,v逐渐提高;t>tm后,v逐渐下降。原因是
您最近一年使用:0次



