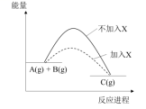
某反应A(g) + B(g) C(g)的能量变化如图所示,由图像可知,加入X后
C(g)的能量变化如图所示,由图像可知,加入X后
 C(g)的能量变化如图所示,由图像可知,加入X后
C(g)的能量变化如图所示,由图像可知,加入X后 
| A.反应速率不变 |
| B.反应物转化率增大 |
| C.生成物的能量降低 |
| D.反应的热效应不变 |
更新时间:2018-12-09 14:21:03
|
相似题推荐
单选题
|
容易
(0.94)
【推荐1】已知 键的键能为436kJ·mol
键的键能为436kJ·mol ,
, 键的键能为391kJ·mol
键的键能为391kJ·mol ,
, 键的键能是941.69kJ⋅mol
键的键能是941.69kJ⋅mol ,下列热化学方程式正确的是
,下列热化学方程式正确的是
 键的键能为436kJ·mol
键的键能为436kJ·mol ,
, 键的键能为391kJ·mol
键的键能为391kJ·mol ,
, 键的键能是941.69kJ⋅mol
键的键能是941.69kJ⋅mol ,下列热化学方程式正确的是
,下列热化学方程式正确的是A.  kJ⋅mol kJ⋅mol |
B. 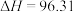 kJ⋅mol kJ⋅mol |
C.  kJ⋅mol kJ⋅mol |
D.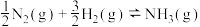  kJ⋅mol kJ⋅mol |
您最近一年使用:0次
单选题
|
容易
(0.94)
解题方法
【推荐2】乙醇未来理想的绿色燃料之一,可以由石油裂解来合成。已知:
则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的△H为
| 物质(状态) | H2(g) | C2H4(g) | C2H5OH(l) |
| 燃烧热△H/kJ•mol-1 | -285.8 | -1411.0 | -1366.8 |
| A.-44.2kJ•mol-1 | B.+44.2kJ•mol-1 | C.-330kJ•mol-1 | D.+330kJ•mol-1 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐3】工业上,以煤炭为原料,通入一定比例的空气,经过系列反应可以得到满足不同需求的原料气。在C和O2的反应体系中发生如下反应:
反应ⅠC(s)+O2(g)=CO2(g) △H1=-394kJ·mol-l
反应Ⅱ2CO(g)+O2(g)=2CO2(g) △H2=-566kJ·mol-l
反应Ⅲ2C(s)+O2(g)=2CO(g) △H3
设y=△H-T△S,反应Ⅰ、Ⅱ和Ⅲ的y随温度的变化关系如图所示。

下列说法正确的是
反应ⅠC(s)+O2(g)=CO2(g) △H1=-394kJ·mol-l
反应Ⅱ2CO(g)+O2(g)=2CO2(g) △H2=-566kJ·mol-l
反应Ⅲ2C(s)+O2(g)=2CO(g) △H3
设y=△H-T△S,反应Ⅰ、Ⅱ和Ⅲ的y随温度的变化关系如图所示。

下列说法正确的是
| A.反应Ⅲ低温能自发进行,高温下不能自发进行 |
| B.图中对应于反应Ⅱ的线条是a |
| C.一定温度下,增大压强,O2浓度增大,说明在此条件下反应Ⅱ变化的幅度小于反应Ⅲ变化的幅度 |
| D.一定压强下,随着温度的升高,气体中CO与CO2的物质的量之比增大 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐1】下列说法正确的是( )
| A.因为反应物浓度越大,反应速率越快,所以常温下,相同的铝片中分别加入足量的浓硝酸、稀硝酸中,浓硝酸中铝片先溶解完 |
| B.增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应能增大生成H2的速率 |
C.N2(g)+3H2(g) 2NH3(g)ΔH<0,其他条件不变时升高温度,反应速率v(H2)和H2的转化率均增大 2NH3(g)ΔH<0,其他条件不变时升高温度,反应速率v(H2)和H2的转化率均增大 |
| D.对于反应2H2O2===2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率 |
您最近一年使用:0次
单选题
|
容易
(0.94)
解题方法
【推荐2】在2SO2+O2 2SO3的反应中为加快该反应的速率,下列措施可行的是
2SO3的反应中为加快该反应的速率,下列措施可行的是
 2SO3的反应中为加快该反应的速率,下列措施可行的是
2SO3的反应中为加快该反应的速率,下列措施可行的是| A.降低温度 | B.使用更高效的催化剂 |
| C.减小SO2的浓度 | D.减小O2的浓度 |
您最近一年使用:0次
【推荐1】某 的多孔材料刚好可将N2O4“固定”,实现了NO2与N2O4分离并制备HNO3,如图所示:
的多孔材料刚好可将N2O4“固定”,实现了NO2与N2O4分离并制备HNO3,如图所示: N2O4(g) ΔH<0
N2O4(g) ΔH<0
下列说法不正确的是
 的多孔材料刚好可将N2O4“固定”,实现了NO2与N2O4分离并制备HNO3,如图所示:
的多孔材料刚好可将N2O4“固定”,实现了NO2与N2O4分离并制备HNO3,如图所示: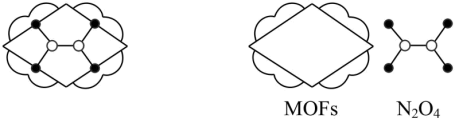
 N2O4(g) ΔH<0
N2O4(g) ΔH<0下列说法不正确的是
| A.气体温度升高后,不利于N2O4的固定 |
| B.N2O4被固定后,平衡正移,有利于NO2的去除 |
| C.制备HNO3的原理为:2N2O4+O2+2H2O=4HNO3 |
D.每制备0.4molHNO3,转移电子数约为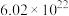 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐2】下列关于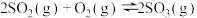
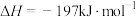 的说法,正确的是
的说法,正确的是
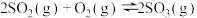
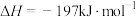 的说法,正确的是
的说法,正确的是A.该反应的 |
B.根据 ,低温条件下反应可以自发进行 ,低温条件下反应可以自发进行 |
| C.升高温度,逆反应速率增大,正反应速率减小,平衡逆向移动 |
| D.其他条件不变,增大压强,平衡右移,平衡常数增大 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐3】表中实验操作、现象与结论对应关系均正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 等体积pH=2的两种酸HX和HY分别与足量的锌反应 | HX溶液中放出的H2多 | HX的酸性比HY强 |
| B | 用广泛pH试纸测定1mol/LNaHSO3溶液的酸碱性 | 测得pH=3.2 | NaHSO3溶液呈酸性,证明HSO 在水中的电离程度小于水解程度 在水中的电离程度小于水解程度 |
| C | 在KSCN与FeCl3的混合液中再加入KCl固体 | 溶液颜色变浅 | 增大生成物浓度,平衡逆向移动 |
| D | 向浓度均为0.1mol/L的NaCl和NaI的混合溶液中滴加少量0.1mol/L的AgNO3溶液 | 产生黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐1】空气中的CO是大气污染物之一,常用碘量法测定,其反应原理是 。一定温度下,向某恒容密闭容器中加入足量的
。一定温度下,向某恒容密闭容器中加入足量的 和CO,发生上述反应。下列图像正确且在
和CO,发生上述反应。下列图像正确且在 时反应达到平衡状态的是
时反应达到平衡状态的是
 。一定温度下,向某恒容密闭容器中加入足量的
。一定温度下,向某恒容密闭容器中加入足量的 和CO,发生上述反应。下列图像正确且在
和CO,发生上述反应。下列图像正确且在 时反应达到平衡状态的是
时反应达到平衡状态的是A. | B. |
C. | D. |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐2】工业上合成尿素的反应为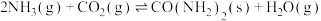
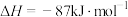 ,氨气的平衡转化率随着条件甲和条件乙的变化曲线如图所示,条件甲和条件乙表示温度或压强。
,氨气的平衡转化率随着条件甲和条件乙的变化曲线如图所示,条件甲和条件乙表示温度或压强。

下列说法正确的是
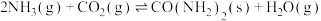
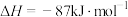 ,氨气的平衡转化率随着条件甲和条件乙的变化曲线如图所示,条件甲和条件乙表示温度或压强。
,氨气的平衡转化率随着条件甲和条件乙的变化曲线如图所示,条件甲和条件乙表示温度或压强。
下列说法正确的是
| A.条件甲是温度 | B.条件乙1>条件乙2 |
| C.a、b、c三点中,b点反应速率最大 | D.a、c点的平衡常数相等 |
您最近一年使用:0次

 分解制取
分解制取 时,添加少量
时,添加少量
 在
在 ,用镁粉代替镁条
,用镁粉代替镁条 与稀盐酸反应生成
与稀盐酸反应生成 时,加入蒸馏水
时,加入蒸馏水 时,适当升温
时,适当升温