A、B、C、W、M、N为原子序数依次增大的前四周期元素。A、C的基态原子中都有两个未成对电子,W是短周期中原子半径最大的金属元素,M为其所在周期中电负性最大的元素,基态N原子的3d轨道上有6个电子。请回答下列问题:
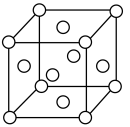
(1)N在周期表中的位置是__________ ;N的单质的一种晶胞如图,该晶胞为___ 堆积。
(2)A、B、C第一电离能由小到大的顺序为________ 。
(3)(AB)2中所有原子均满足8电子结构,则(AB)2中σ键与π键个数之比为___ 。
(4)C的简单氢化物在同主族元素的简单氢化物中沸点反常,其原因是________ 。
(5)与B3-互为等电子体的分子为__________ (写出一种)。依据价层电子对互斥理论,BC3-的空间构型为___ 。
(6)BM3中B原子的杂化轨道类型是_________ 。
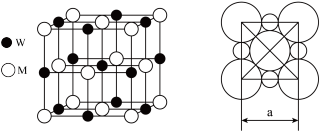
(7)如图所示为W、M两种元素形成的化合物的晶胞结构图以及晶胞的剖面图,若a=5.6×10-8 cm,,则该晶体的密度为______ g·cm-3(精确到小数点后1位)。
(1)N在周期表中的位置是

(2)A、B、C第一电离能由小到大的顺序为
(3)(AB)2中所有原子均满足8电子结构,则(AB)2中σ键与π键个数之比为
(4)C的简单氢化物在同主族元素的简单氢化物中沸点反常,其原因是
(5)与B3-互为等电子体的分子为
(6)BM3中B原子的杂化轨道类型是
(7)如图所示为W、M两种元素形成的化合物的晶胞结构图以及晶胞的剖面图,若a=5.6×10-8 cm,,则该晶体的密度为

更新时间:2018/12/24 21:52:35
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】下表列出了①~⑨九种元素在周期表中的位置元素,完成下列各小题。
(1)第3周期中金属性最强的元素是_______ (填元素名称)。
(2)⑧原子结构示意图为_______ 。
(3)第3周期元素中,最高价氧化物对应水化物酸性最强的是_______ (填化学式)。
(4)①、②和③原子半径由小到大的顺序是_______ 。
(5)第3周期中气态氢化物最稳定的是_______ (填化学式)。
(6)⑦是带来人类文明的重要元素之一,其氧化物化学式是_______ ,常用于制造_______ (填一种高性能的现代通信材料的名称)。
(7)⑥是大自然赐予人类的宝物。它其中的一个用途是作为铝热剂,该反应的化学方程式为_______ 。
(8)②元素形成的一种氢化物的化学式是_______ ,俗话说“雷雨发庄稼”,请写出二氧化氮溶于水的化学反应方程式_______ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)⑧原子结构示意图为
(3)第3周期元素中,最高价氧化物对应水化物酸性最强的是
(4)①、②和③原子半径由小到大的顺序是
(5)第3周期中气态氢化物最稳定的是
(6)⑦是带来人类文明的重要元素之一,其氧化物化学式是
(7)⑥是大自然赐予人类的宝物。它其中的一个用途是作为铝热剂,该反应的化学方程式为
(8)②元素形成的一种氢化物的化学式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】几种短周期元素的原子半径及主要化合价如下表:
请用化学用语回答下列问题:
(1)金属性①________ ②(填>或<)
(2)④元素的最高价氧化物对应的水化物与其简单氢化物能生成盐M,M中含有的化学键类型有_______________ ;
(3)写出元素⑥和⑦的单质在加热条件下反应生成的化合物的电子式:_________ 。
(4)①、②、④、⑥所形成的离子,其半径由小到大的顺序是___________ (填离子符号)
(5)①~⑦中元素最高价氧化物对应的水化物中酸性最强的是_____________ (填物质化学式);呈两性的氢氧化物是_________ (填物质化学式),该化合物与NaOH溶液反应的离子方程式为__________________ 。
(6)用电子式表示元素①与⑤形成化合物的过程___________________ 。
| 元素代号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.078 | 0.099 | 0.074 | 0.186 |
| 主要化合价 | +2 | +3 | +6、-2 | +5、-3 | +7、﹣1 | -2 | +1 |
请用化学用语回答下列问题:
(1)金属性①
(2)④元素的最高价氧化物对应的水化物与其简单氢化物能生成盐M,M中含有的化学键类型有
(3)写出元素⑥和⑦的单质在加热条件下反应生成的化合物的电子式:
(4)①、②、④、⑥所形成的离子,其半径由小到大的顺序是
(5)①~⑦中元素最高价氧化物对应的水化物中酸性最强的是
(6)用电子式表示元素①与⑤形成化合物的过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】有某固体化合物X(含有三种短周期元素)是一种络合氢化物储氢材料,X中某种元素的单质可用于制造信号弹。某实验员对固体化合物X作如图实验: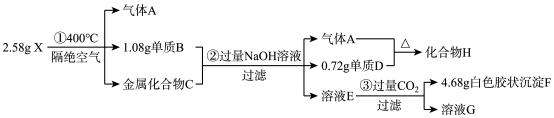
其中:X由三种短周期元素组成,且阴、阳离子个数比为2:1;金属互化物——全部由金属元素组成的化合物。请回答:
(1)化合物X的组成元素___________ ,写出H的电子式___________ 。
(2)X在400℃分解的化学方程式___________ 。
(3)溶液E和过量CO2发生反应的离子方程式为___________ 。
(4)金属互化物C分别与足量盐酸和足量氢氧化钠溶液反应产生的气体物质的量之比为___________ 。
(5)气体A与单质D制备化合物H的过程中,通常产物中会夹杂单质D,请设计实验方案,检验产品中是否含有单质D:___________ 。

其中:X由三种短周期元素组成,且阴、阳离子个数比为2:1;金属互化物——全部由金属元素组成的化合物。请回答:
(1)化合物X的组成元素
(2)X在400℃分解的化学方程式
(3)溶液E和过量CO2发生反应的离子方程式为
(4)金属互化物C分别与足量盐酸和足量氢氧化钠溶液反应产生的气体物质的量之比为
(5)气体A与单质D制备化合物H的过程中,通常产物中会夹杂单质D,请设计实验方案,检验产品中是否含有单质D:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z三种常见的短周期元素可以形成XY2、Z2Y、XY3、Z2Y2、Z2X等化合物,已知Y的离子和Z的离子有相同的电子层结构,X离子比Y离子多一个电子层。试回答:
(1)写出X、Y、Z三种元素的符号和名称:_____________ 、_______ 、_______ ;
(2)分析Z2Y2中含有的化学键类型:_______ ;
(3)写出Z2Y2与二氧化碳反应的方程式:_____________________ ;
(4)用电子式表示X和Z两元素形成化合物的过程:__________________ 。
(1)写出X、Y、Z三种元素的符号和名称:
(2)分析Z2Y2中含有的化学键类型:
(3)写出Z2Y2与二氧化碳反应的方程式:
(4)用电子式表示X和Z两元素形成化合物的过程:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】X、Y、Z、W是短周期元素,原子序数递增。X与Z位于同一主族,Y元素的单质既能与盐酸反应,也能与NaOH溶液反应,Z原子的最外层电子数是次外层电子数的一半,Y、Z、W原子的最外层电子数之和为14.
(1)HWO的结构式为___________ 。
(2)①X、Y、Z、W原子半径由大到小依次是___________ (填元素符号)。
②X、Z、W最高价氧化物对应水化物的酸性由强到弱依次是___________ (填化学式)。
(3)含Y元素的盐与小苏打溶液可用作泡沫灭火剂,写出灭火时发生反应的离子方程式:___________ 。
(4)NW3是黄色油状液体,无漂白性,在热水中会发生水解。NW3的电子式为___________ 。若取该液体滴入50℃左右的热水中,片刻后取该热溶液滴到干燥的红色石蕊试纸上,试纸先变蓝后褪色。写出NW3在热水中发生水解的化学方程式:___________ 。
(1)HWO的结构式为
(2)①X、Y、Z、W原子半径由大到小依次是
②X、Z、W最高价氧化物对应水化物的酸性由强到弱依次是
(3)含Y元素的盐与小苏打溶液可用作泡沫灭火剂,写出灭火时发生反应的离子方程式:
(4)NW3是黄色油状液体,无漂白性,在热水中会发生水解。NW3的电子式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知:A~H均为短周期元素,它们的最高(或最低)化合价与原子序数的关系如下图。

(1)画出F元素的原子结构示意图___ ,元素B的最高价氧化物的电子式为____ ,元素C、D、H的简单离子的半径由大到小顺序为____ (用离子符号表示)。
(2)C元素的气态氢化物与其最高价氧化物对应的水化物反应生成的化合物中存在化学键的类型为___ 。请从原子结构的角度说明元素H的得电子能力比G强的原因是___ 。
(3)C和F组成的化合物FC被大量用于制造电子元件。工业上用F的氧化物、B单质和C单质在高温下制备FC,其中F的氧化物和B单质的物质的量之比为1∶3,则该反应的化学方程式为___ 。
(4)已知X、Y、Z三种物质中均至少含有上述A~H元素中的一种元素,它们之间存在转化关系:X Y
Y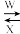 Z。
Z。
①X、Y、Z均含有上述元素中的同一种金属元素,若W固体俗称干冰,则反应Y→Z的离子方程式为___ 。
②X、Y、Z均为上述元素中的同一种非金属元素的化合物,W是一种常见金属单质,且上述转化均在常温条件下完成,则反应Z→Y的离子方程式为__ 。

(1)画出F元素的原子结构示意图
(2)C元素的气态氢化物与其最高价氧化物对应的水化物反应生成的化合物中存在化学键的类型为
(3)C和F组成的化合物FC被大量用于制造电子元件。工业上用F的氧化物、B单质和C单质在高温下制备FC,其中F的氧化物和B单质的物质的量之比为1∶3,则该反应的化学方程式为
(4)已知X、Y、Z三种物质中均至少含有上述A~H元素中的一种元素,它们之间存在转化关系:X
 Y
Y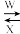 Z。
Z。①X、Y、Z均含有上述元素中的同一种金属元素,若W固体俗称干冰,则反应Y→Z的离子方程式为
②X、Y、Z均为上述元素中的同一种非金属元素的化合物,W是一种常见金属单质,且上述转化均在常温条件下完成,则反应Z→Y的离子方程式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】NH3和CO均具有还原性,均能被CuO氧化,反应涉及H、C、N、O、Cu元素。回答下列问题:
(1)基态氧原子价电子排布图为___________ , 基态铜原子最外层电子数为___________ 。
(2)C、N、O的第一电离能从大到小的顺序为___________ (填元素符号,下同);H、C、N三种元素的电负性从小到大的顺序为___________ 。
(3)CO分子中σ键与π键的数目比为___________ ;NH3分子中N原子的杂化方式为___________ 。
(4)已知Cu2O的熔点为1235℃,Cu2S的熔点为1130℃,Cu2O熔点较高的原因是___________ 。
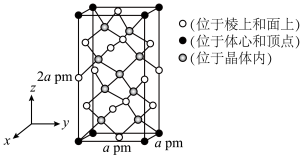
(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。一种热电材料的四方晶系晶胞结构如图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如下表所示:
该晶体的化学式为___________ ,该晶体中与单个Cu键合的S最多有___________ 个,找出一个距离Sb(0,0,0)最近的Cu:___________ (用分数坐标表示)。
(1)基态氧原子价电子排布图为
(2)C、N、O的第一电离能从大到小的顺序为
(3)CO分子中σ键与π键的数目比为
(4)已知Cu2O的熔点为1235℃,Cu2S的熔点为1130℃,Cu2O熔点较高的原因是
(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。一种热电材料的四方晶系晶胞结构如图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如下表所示:
| 坐标原子 | x | y | z |
| Sb(●) | 0 | 0 | 0 |
| Cu | 0 | 0 | 0.5 |
| S | 0.25 | 0.25 | 0.125 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】Fe是一种重要的金属元素,工业上用黄铁矿(主要成分为FeS2)来制备硫酸,用铁、硫酸、柠檬酸、双氧水、氨水等来制备(NH4)3Fe(C6H5O7)2(柠檬酸铁铵)。回答下列问题:
(1)FeS2中阴离子的电子式为_______ 。
(2)O和Cl的电负性相差不大,但Fe2O3的熔点为1565℃,而FeCl3的熔点为306℃,且很容易升华,Fe2O3与FeCl3熔点差别较大的原因是_______ ;FeCl3的蒸气中存在双聚分子(含有两个配位键),该双聚分子的结构式为_______ 。(配位键须用→表示)
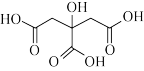
(3)柠檬酸的结构简式如图所示,其分子中碳原子的杂化方式为_______ ;柠檬酸、乙醇、水均可互溶,主要的原因是_______ ,(NH4)3Fe(C6H5O7)2中 的空间构型为
的空间构型为_______ 。
(4)铁和镍两种元素的第三电离能大小关系是I3(Fe)_______ I3(Ni),原因是_______ 。
(1)FeS2中阴离子的电子式为
(2)O和Cl的电负性相差不大,但Fe2O3的熔点为1565℃,而FeCl3的熔点为306℃,且很容易升华,Fe2O3与FeCl3熔点差别较大的原因是
(3)柠檬酸的结构简式如图所示,其分子中碳原子的杂化方式为
 的空间构型为
的空间构型为
(4)铁和镍两种元素的第三电离能大小关系是I3(Fe)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】W、X、Y、Z、M、N六种元素的原子序数依次递增,其中W、X、Y、Z为短周期元素,六种元素的元素性质或原子结构特征如下表,回答下列问题。
(1)写出元素Z元素周期表中的位置___________ 。
(2)W、X、Y三种元素的电负性数值由大到小的顺序为___________ (用元素符号作答,下同),这三种元素的第一电离能由大到小的顺序为___________ 。
(3)写出元素M的价层电子排布式___________ 。
(4)写出元素N的N3+最外层电子排布式___________ 。
| 元素 | 元素性质或原子结构特征 |
| W | 原子p轨道的电子数为2 |
| X | 原子中最高能级的不同轨道都有电子,且自旋方向相同 |
| Y | 最外能层电子数是最内能层电子数的3倍 |
| Z | 原子核外s能级上的电子总数与p能级上的电子总数相等,但第一电离能都高于同周期相邻元素 |
| M | 第24号元素 |
| N | 一种常见的金属元素,正三价离子遇硫氰化钾显红色 |
(2)W、X、Y三种元素的电负性数值由大到小的顺序为
(3)写出元素M的价层电子排布式
(4)写出元素N的N3+最外层电子排布式
您最近一年使用:0次
【推荐1】 是重要的电子工业原料,可用于半导体电子材料、三元电池材料、锰酸锂电池材料、锌锰电池材料、玻璃等的制造。以菱锰矿(主要成分为
是重要的电子工业原料,可用于半导体电子材料、三元电池材料、锰酸锂电池材料、锌锰电池材料、玻璃等的制造。以菱锰矿(主要成分为 ,含
,含 和少量Fe、Cu、Ni、Ca、Mg等元素)为原料制备
和少量Fe、Cu、Ni、Ca、Mg等元素)为原料制备 的一种工艺流程如图所示。
的一种工艺流程如图所示。
(1)基态Mn原子的价电子的轨道表示式为_______ 。
(2)“酸浸”时加快反应速率,提高浸取率可采取的措施有_______ (写两种)。
(3)滤渣2的主要成分为_______ (填化学式)。
(4)福美钠的化学式为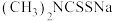 ,其中N、S、Na三种元素的简单离子半径从大到小顺序为
,其中N、S、Na三种元素的简单离子半径从大到小顺序为_______ (填写离子符号)。
(5)已知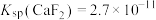 ,
,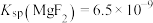 ,当
,当 沉淀完全时(浓度为
沉淀完全时(浓度为 mol⋅L
mol⋅L ),溶液中
),溶液中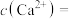
_______ mol⋅L (结果保留三位有效数字)。
(结果保留三位有效数字)。
(6)“沉锰”中生成的 在“氧化”时控制温度为50℃,反应的化学方程式为
在“氧化”时控制温度为50℃,反应的化学方程式为_______ 。
(7) 晶体温度高于1170℃时属于立方晶体,其中
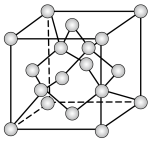
晶体温度高于1170℃时属于立方晶体,其中 与金刚石晶胞中碳原子占据的位置相似(金刚石晶胞如图所示)。若
与金刚石晶胞中碳原子占据的位置相似(金刚石晶胞如图所示)。若 晶体的晶胞参数为apm,则晶体密度为
晶体的晶胞参数为apm,则晶体密度为_______ g⋅cm-3(列出计算式,阿伏加德罗常数的值为 )。
)。
 是重要的电子工业原料,可用于半导体电子材料、三元电池材料、锰酸锂电池材料、锌锰电池材料、玻璃等的制造。以菱锰矿(主要成分为
是重要的电子工业原料,可用于半导体电子材料、三元电池材料、锰酸锂电池材料、锌锰电池材料、玻璃等的制造。以菱锰矿(主要成分为 ,含
,含 和少量Fe、Cu、Ni、Ca、Mg等元素)为原料制备
和少量Fe、Cu、Ni、Ca、Mg等元素)为原料制备 的一种工艺流程如图所示。
的一种工艺流程如图所示。 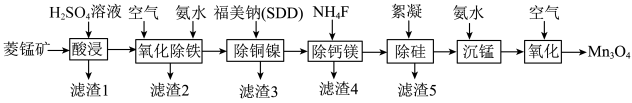
(1)基态Mn原子的价电子的轨道表示式为
(2)“酸浸”时加快反应速率,提高浸取率可采取的措施有
(3)滤渣2的主要成分为
(4)福美钠的化学式为
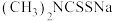 ,其中N、S、Na三种元素的简单离子半径从大到小顺序为
,其中N、S、Na三种元素的简单离子半径从大到小顺序为(5)已知
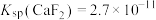 ,
,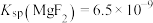 ,当
,当 沉淀完全时(浓度为
沉淀完全时(浓度为 mol⋅L
mol⋅L ),溶液中
),溶液中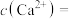
 (结果保留三位有效数字)。
(结果保留三位有效数字)。(6)“沉锰”中生成的
 在“氧化”时控制温度为50℃,反应的化学方程式为
在“氧化”时控制温度为50℃,反应的化学方程式为(7)
 晶体温度高于1170℃时属于立方晶体,其中
晶体温度高于1170℃时属于立方晶体,其中 与金刚石晶胞中碳原子占据的位置相似(金刚石晶胞如图所示)。若
与金刚石晶胞中碳原子占据的位置相似(金刚石晶胞如图所示)。若 晶体的晶胞参数为apm,则晶体密度为
晶体的晶胞参数为apm,则晶体密度为 )。
)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】金属锂及其化合物因独特的性质而具有重要的应用价值。例如:锰酸锂可用于电池; Li2O 可用于特种玻璃、陶瓷、医药等领域: LiH、LiBH4、LiNH2为常见的储氢材料等。回答下列问题:
(1)Mn2+最外层电子排布式___________
(2)LiH、LiBH4、 LiNH2中所含非金属元素的电负性由小到大的顺序为___________ (用元素符号表示); LiBH4中阴离子的空间构型为___________
(3)Li2O的熔点(1567℃)高于LiCl的熔点(605℃)的原因是___________ 。
(4)Li2O立方晶胞结构如图所示,晶胞边长为anm。Li+在晶胞中的配位数为___________ ;Li+和O2-的最短距离为___________ nm。

(1)Mn2+最外层电子排布式
(2)LiH、LiBH4、 LiNH2中所含非金属元素的电负性由小到大的顺序为
(3)Li2O的熔点(1567℃)高于LiCl的熔点(605℃)的原因是
(4)Li2O立方晶胞结构如图所示,晶胞边长为anm。Li+在晶胞中的配位数为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
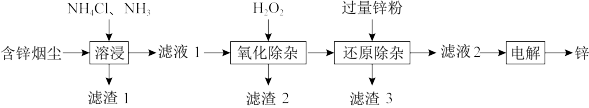
【推荐3】锌是冶金、化工、纺织等行业应用广泛的重要金属之一,一种以含锌烟尘(主要成分是ZnO,还含有少量Si、Cu、Cd、Pb、Sb等元素的氧化物)制备金属锌的工艺流程如下:
回答下列问题:
(1)基态锌原子的价层电子轨道表示式(电子排布图)为___________ 。
(2)“溶浸”中主要的化学方程式为__________ 。
(3)“滤渣 1”的主要成分是PbO、__________ 。
(4)“滤渣2”是Sb2O5,“氧化除杂” 的离子方程式为_________ 。
(5)“还原除杂” 中加过量锌粉的目的是__________ 。
(6)工业上一般利用闪锌矿(主要成分是ZnS)为原料制备锌,ZnS的晶胞结构如下图,已知晶胞参数为a cm,则该晶体的摩尔体积为_______ m3/mol (阿伏加德罗常数的值为NA)。___________ 。

回答下列问题:
(1)基态锌原子的价层电子轨道表示式(电子排布图)为
(2)“溶浸”中主要的化学方程式为
(3)“滤渣 1”的主要成分是PbO、
(4)“滤渣2”是Sb2O5,“氧化除杂” 的离子方程式为
(5)“还原除杂” 中加过量锌粉的目的是
(6)工业上一般利用闪锌矿(主要成分是ZnS)为原料制备锌,ZnS的晶胞结构如下图,已知晶胞参数为a cm,则该晶体的摩尔体积为

您最近一年使用:0次



