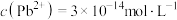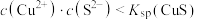在t℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。已知t℃时AgCl的Ksp=4×10-10,下列说法正确的是
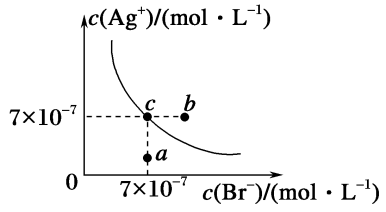
| A.图中a点对应的体系中将有AgBr沉淀生成 |
| B.加入NaBr固体,AgBr的溶解度减小,AgBr的Ksp也减小 |
| C.在AgBr饱和溶液中加入固体NaBr,可使溶液中c点变到b点 |
D.在t℃时,AgCl(s)+Br-(aq)  AgBr(s)+Cl-(aq)的平衡常数K≈816 AgBr(s)+Cl-(aq)的平衡常数K≈816 |
17-18高二下·云南保山·期末 查看更多[12]
陕西省安康市白河高中2021-2022学年高二上学期期末考试(实验班)化学试题陕西省安康市白河高中2021-2022学年高二上学期期末考试化学试题重庆市巫山县官渡中学2021-2022学年高二下学期期末考试化学试题陕西省汉中中学2021-2022学年高二上学期第三次月考化学试题甘肃省永昌县第一高级中学2021-2022学年高二上学期期末考试化学试题黑龙江省哈尔滨师范大学青冈实验中学校2018-2019学年高二下学期开学考试化学试题山西省怀仁市重点中学2019-2020学年高二上学期期末考试化学试题江西省丰城中学2018-2019学年高一上学期课改期末考试化学试题山西省长治市城区第二中学校2018-2019学年高二上学期期末考试化学试题【市级联考】四川省自贡市2019届高三上学期第一次诊断性考试理科综合化学试题(已下线)《2018-2019学年同步单元双基双测AB卷》第三单元 水溶液中的离子平衡单元测试A卷云南省腾冲市第八中学2017-2018学年高二下学期期末考试化学试题
更新时间:2019-01-02 21:51:34
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】判断下列正确的有几项:
①中和等体积、等pH的盐酸和醋酸,中和盐酸所需氢氧化钠的物质的量多于醋酸
②配置 溶液要加入铁粉,配置
溶液要加入铁粉,配置 溶液要加入盐酸,二者原理相同
溶液要加入盐酸,二者原理相同
③电解精炼铜,阳极为纯铜、阴极为粗铜,电解质溶液可以是硫酸铜或氯化铜溶液
④用 固体作为沉淀剂除去工业废水中的
固体作为沉淀剂除去工业废水中的 :
: ,反应达平衡后,继续加入
,反应达平衡后,继续加入 ,
, 的去除率增大
的去除率增大
⑤镀锌或镀锡的钢管在镀层破损后仍能对钢管起保护作用
⑥水电离出的 为
为 的溶液一定呈中性
的溶液一定呈中性
①中和等体积、等pH的盐酸和醋酸,中和盐酸所需氢氧化钠的物质的量多于醋酸
②配置
 溶液要加入铁粉,配置
溶液要加入铁粉,配置 溶液要加入盐酸,二者原理相同
溶液要加入盐酸,二者原理相同③电解精炼铜,阳极为纯铜、阴极为粗铜,电解质溶液可以是硫酸铜或氯化铜溶液
④用
 固体作为沉淀剂除去工业废水中的
固体作为沉淀剂除去工业废水中的 :
: ,反应达平衡后,继续加入
,反应达平衡后,继续加入 ,
, 的去除率增大
的去除率增大⑤镀锌或镀锡的钢管在镀层破损后仍能对钢管起保护作用
⑥水电离出的
 为
为 的溶液一定呈中性
的溶液一定呈中性| A.0项 | B.1项 | C.2项 | D.3项 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列根据实验操作和实验现象所得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 测定等浓度的NaClO溶液和Na2SO3溶液的pH | 前者的pH比后者的大 | 非金属性:S>Cl |
| B | 向KNO3和KOH混合溶液中加入铝粉并加热,然后在管口放一湿润的红色石蕊试纸 | 试纸变为蓝色 | NO3-被还原为NO |
| C | 将KI和FeCl3溶液混合后,加入CCl4振荡,静置 | 下层液体显紫红色 | 氧化性:Fe3+>I2 |
| D | 向10mL0.2mol/LNaOH 溶液中滴加2滴0.1mol/L MgCl2溶液,产生白色沉淀 后,再滴加2滴0.1mol/LFeCl3溶液 | 生成红褐色沉淀 | 相同的温度下的Ksp:Mg(OH)2<Fe(OH)3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。某研究小组利用软锰矿(主要成分为MnO2,另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下简化流程既脱除燃煤尾气中的SO2,又制得电池材料MnO2(反应条件已省略)。
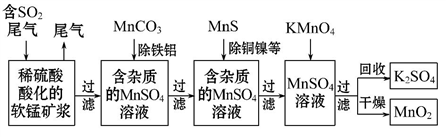
下列说法不正确 的是( )

下列说法
| A.上述流程脱硫实现了废弃物的综合利用和酸雨的减少 |
| B.用MnCO3能除去溶液中Al3+和Fe3+,其原因是碳酸铝和碳酸铁的溶解度比MnCO3更小。 |
C.MnO2是碱性锌锰电池的正极材料,碱性锌锰电池放电时,正极的电极反应式是MnO2+H2O+e- MnOOH+OH- MnOOH+OH- |
| D.假设脱除的SO2只与软锰矿浆中MnO2反应。按照图示流程,将am3(标准状况)含SO2的体积分数为b%的尾气通入矿浆,若SO2的脱除率为89.6%,最终得到MnO2的质量为C mol,则除去铁、铝、铜、镍等杂质时,所引入的锰元素相当于MnO2为(0.6C-0.4ab)mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法中,正确的是
A.两种难溶盐电解质,其中 小的溶解度一定小 小的溶解度一定小 |
B.溶液中存在两种可以与同一沉淀剂生成沉淀的离子,则 小的一定先沉淀 小的一定先沉淀 |
C. 只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关 只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关 |
D.凡是能自发进行的化学反应,一定是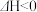 、 、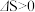 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】常温下,下列有关说法错误的是
A. 的醋酸溶液稀释至100mL,稀释后溶液的 的醋酸溶液稀释至100mL,稀释后溶液的 |
B.在稀释 溶液的过程中, 溶液的过程中, 的值不变 的值不变 |
C. 溶液中存在的离子浓度关系 溶液中存在的离子浓度关系 |
D.反应 的平衡常数 的平衡常数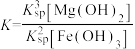 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】三种难溶金属硫化物的溶度积常数(25℃):
下列有关说法中正确的是
| 化学式 | FeS | CuS | MnS |
| 溶度积 | 1.59×10-19 | 1.3×10-36 | 4.65×10-14 |
| A.25℃时,CuS的溶解度大于MnS的溶解度 |
| B.25℃时,饱和CuS溶液中,Cu2+的浓度为1.3×10-18mol/L |
| C.因为H2SO4是强酸,所以反应CuSO4+H2S=CuS↓+H2SO4不能发生 |
| D.除去某溶液中的Cu2+,可以选用FeS作沉淀剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验及其结论都正确的是
| 实验 | 结论 | |
| A | 氯气的水溶液可以导电 | 氯气是电解质 |
| B | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝箔表面氧化铝熔点高于铝 |
| C | 将 Na2S 滴入 AgNO3 和 AgCl 的混合浊 液中产生黑色沉淀 | Ksp(AgCl)>Ksp(Ag2S) |
| D | 用分液漏斗分离苯和四氯化碳 | 四氯化碳密度比苯大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】已知25℃物质的溶度积常数为:FeS:Ksp=6.3×10-18;CuS:Ksp=1.3×10-36;ZnS: Ksp=1.6×10-24。下列说法错误的是
| A.相同温度下,CuS的溶解度小于ZnS的溶解度 |
| B.除去工业废水中的Cu2+,可以选用FeS做沉淀剂 |
| C.0.01molCuSO4完全溶解在1L 0.023mol/L的Na2S溶液中,Cu2+浓度为1.0×10-34mol/L |
| D.在ZnS的饱和溶液中,加入FeCl2溶液,一定不产生FeS沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
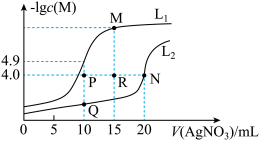
【推荐1】某温度下,分别向10.00 mL 0.1 mol·L-1 NaCl和Na2CrO4溶液中滴加0.1 mol·L-1 AgNO3溶液,滴加过程中-lgc(M)(M为Cl-或CrO )与AgNO3溶液体积(V)的变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
)与AgNO3溶液体积(V)的变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
 )与AgNO3溶液体积(V)的变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
)与AgNO3溶液体积(V)的变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
| A.该温度下,Ksp(Ag2CrO4) = 2×10-8 |
| B.该温度下,向浓度相同的 NaCl和Na2CrO4混合溶液滴加AgNO3溶液,先有粉红色沉淀生成 |
C.M点溶液中:c(Na+)>c(NO )>c(Ag+)>c(H+)>c(OH-) )>c(Ag+)>c(H+)>c(OH-) |
| D.相同实验条件下,若改为 0.05 mol/L NaCl和Na2CrO4溶液,则曲线L2中N点移到P点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某温度下,向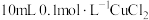 溶液中滴加
溶液中滴加 的
的 溶液,滴加过程中
溶液,滴加过程中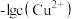 与
与 溶液体积的关系如图所示。下列有关说法正确的是
溶液体积的关系如图所示。下列有关说法正确的是
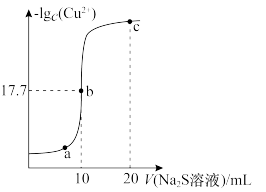
已知:
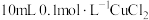 溶液中滴加
溶液中滴加 的
的 溶液,滴加过程中
溶液,滴加过程中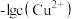 与
与 溶液体积的关系如图所示。下列有关说法正确的是
溶液体积的关系如图所示。下列有关说法正确的是
已知:

A. 溶液中: 溶液中: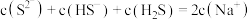 |
B.向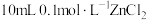 溶液中滴加 溶液中滴加 的 的 溶液,图中的b点向下平移 溶液,图中的b点向下平移 |
C.该温度下, |
| D.a、b、c三点对应的溶液中。水的电离程度最大的为b点 |
您最近一年使用:0次

 、
、 、
、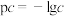 ,c为
,c为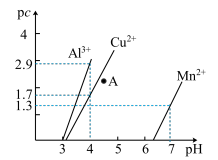
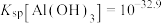
 时,
时, 的溶解度为
的溶解度为
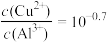
 溶液,并向深部渗透,遇到深层的闪锌矿(ZnS)和方铅矿(PbS),便慢慢转变为铜蓝(CuS),发生的反应有
溶液,并向深部渗透,遇到深层的闪锌矿(ZnS)和方铅矿(PbS),便慢慢转变为铜蓝(CuS),发生的反应有
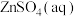 。下列说法不正确的是
。下列说法不正确的是 ,
, ,
,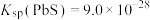

 、
、 均为
均为 的溶液中通入
的溶液中通入 气体,产生沉淀的顺序依次为CuS、PbS、ZnS
气体,产生沉淀的顺序依次为CuS、PbS、ZnS