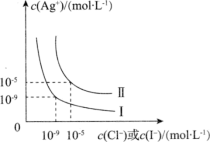
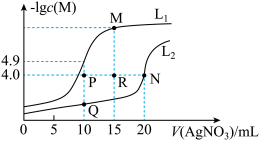
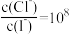某温度下,分别向10.00 mL 0.1 mol·L-1 NaCl和Na2CrO4溶液中滴加0.1 mol·L-1 AgNO3溶液,滴加过程中-lgc(M)(M为Cl-或CrO )与AgNO3溶液体积(V)的变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
)与AgNO3溶液体积(V)的变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
 )与AgNO3溶液体积(V)的变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
)与AgNO3溶液体积(V)的变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
| A.该温度下,Ksp(Ag2CrO4) = 2×10-8 |
| B.该温度下,向浓度相同的 NaCl和Na2CrO4混合溶液滴加AgNO3溶液,先有粉红色沉淀生成 |
C.M点溶液中:c(Na+)>c(NO )>c(Ag+)>c(H+)>c(OH-) )>c(Ag+)>c(H+)>c(OH-) |
| D.相同实验条件下,若改为 0.05 mol/L NaCl和Na2CrO4溶液,则曲线L2中N点移到P点 |
2023·湖南岳阳·三模 查看更多[2]
更新时间:2023-05-16 20:16:41
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是
A.用铁片和稀硫酸反应制取 时,改用铁片和浓硫酸可以加快产生 时,改用铁片和浓硫酸可以加快产生 的速率 的速率 |
B.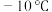 的液态水就会自动结冰成为固态,因为这是熵增的过程 的液态水就会自动结冰成为固态,因为这是熵增的过程 |
C.已知酸性: ,则等浓度等体积的 ,则等浓度等体积的 和 和 溶液中离子总数,前者大于后者 溶液中离子总数,前者大于后者 |
D.向 氨水中加入少量水,溶液中 氨水中加入少量水,溶液中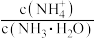 减小 减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】室温下,以酚酞为指示剂,用0.1000 mol·L-1 NaOH溶液滴定20.00mL 0.1000 mol·L-1一元酸HA的溶液。溶液中,pH、分布系数(δ,比如A-的分布系数:δ(A-)=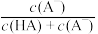 )随VNaOH的变化关系如图所示,下列叙述不正确的是
)随VNaOH的变化关系如图所示,下列叙述不正确的是

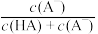 )随VNaOH的变化关系如图所示,下列叙述不正确的是
)随VNaOH的变化关系如图所示,下列叙述不正确的是
| A.曲线①代表δ(HA),曲线②代表δ(A-) |
| B.Ka(HA)的数量级为10-5 |
| C.从滴定开始到溶液呈中性过程中,水的电离度先增大后减小 |
| D.滴定终点时,c(Na+)>c(A-)>c(OH-)>c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】根据下列各图曲线表征的信息,得出的结论正确的是
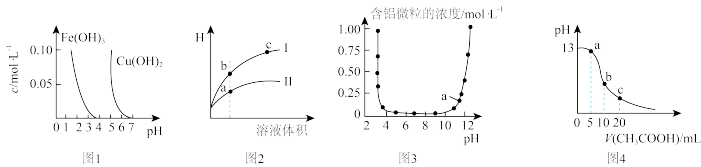
A.由图1得出若要除去 溶液中的 溶液中的 ,可采用向溶液中加入适量CuO,调节溶液的pH至4左右 ,可采用向溶液中加入适量CuO,调节溶液的pH至4左右 |
B.图2表示用水稀释pH相同的盐酸和 溶液时,溶液的pH变化曲线,其中I表示盐酸,II表示 溶液时,溶液的pH变化曲线,其中I表示盐酸,II表示 溶液,且溶液导电性:c>b>a 溶液,且溶液导电性:c>b>a |
C.图3表示 与 与 反应时含铝微粒浓度变化曲线,图中a点溶液中大量存在 反应时含铝微粒浓度变化曲线,图中a点溶液中大量存在 |
D.图4表示常温下向体积为 NaOH溶液中逐滴加入 NaOH溶液中逐滴加入 溶液后溶液的pH变化曲线,则b点处有: 溶液后溶液的pH变化曲线,则b点处有: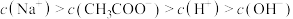 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某研究性学习小组为研究水垢的生成,查得CaCO3和Mg(OH)2溶解度曲线如图所示。已知:40°C时,Ksp(MgCO3)=7×10-6,下列有关分析错误的是( )
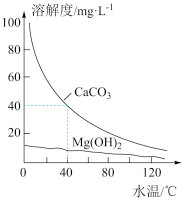

| A.CaCO3、Mg(OH)2溶解均放热 |
| B.MgCl2溶液中加入少量CaCO3粉末加热搅拌,有Mg(OH)2生成 |
| C.含有Ca(HCO3)2和Mg(HCO3)2的自来水长时间加热,水垢的主要成分为CaCO3和MgCO3 |
| D.40℃时,Ksp(CaCO3)=1.6×10-7 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验过程不能达到实验目的的是
| 选项 | 实验目的 | 实验过程 |
| A | 提高饱和氯水中的HClO浓度 | 向饱和氯水中加入碳酸钙粉末并通入适量Cl2,然后过滤 |
| B | 证明压强对平衡移动产生影响 | 向充有NO2和N2O4混合气体的恒容透明密闭容器中充入氦气增大压强,观察现象 |
| C | 探究浓度对化学平衡的影响 | 试管中盛有0.1 mol·L−1 K2Cr2O7溶液,向其中滴加10滴6 mol·L−1 NaOH溶液,观察到溶液黄色加深 |
| D | 比较CdS(黄色)与CuS(黑色)的溶解度[已知Ksp(CdS)>Ksp(CuS)] | 向H2S溶液中滴加0.01mol·L-1的CdSO4溶液至沉淀不再增加,然后滴入几滴0.01 mol·L-1CuSO4溶液,观察沉淀颜色变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】天然水体中的 与空气中的
与空气中的 保持平衡。某温度下,溶洞水体中
保持平衡。某温度下,溶洞水体中 (
( 为
为 、
、 、
、 或
或 )为与
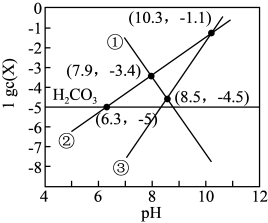
)为与 关系如图所示。下列说法错误的是
关系如图所示。下列说法错误的是
 与空气中的
与空气中的 保持平衡。某温度下,溶洞水体中
保持平衡。某温度下,溶洞水体中 (
( 为
为 、
、 、
、 或
或 )为与
)为与 关系如图所示。下列说法错误的是
关系如图所示。下列说法错误的是
A.斜线③表示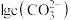 随pH变化关系 随pH变化关系 |
B.该温度下,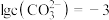 时溶液的pH=9.3 时溶液的pH=9.3 |
C.根据图象不能计算该温度下CaCO3的 |
D.该温度下,H2CO3的电离平衡常数Ka1数量级为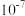 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】还原沉淀法是处理含铬(含Cr2O72-和CrO42-)工业废水的常用方法,过程如下: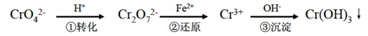
已知转化过程中的反应为2CrO42﹣(aq)+2H+(aq) Cr2O72﹣(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6 g/L,CrO42-有10/11转化为Cr2O72-,下列说法不正确的是
Cr2O72﹣(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6 g/L,CrO42-有10/11转化为Cr2O72-,下列说法不正确的是
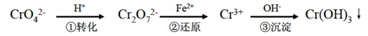
已知转化过程中的反应为2CrO42﹣(aq)+2H+(aq)
 Cr2O72﹣(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6 g/L,CrO42-有10/11转化为Cr2O72-,下列说法不正确的是
Cr2O72﹣(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6 g/L,CrO42-有10/11转化为Cr2O72-,下列说法不正确的是| A.溶液颜色保持不变,说明上述可逆反应达到平衡状态 |
| B.若用绿矾(FeSO4·7H2O)作还原剂,处理1L废水,至少需要917.4 g |
| C.常温下转化反应的平衡常数K=l×1014.则转化后所得溶液的pH=6 |
| D.常温下Ksp[Cr(OH)3]=1×10-32,要使处理后废水中的c(Cr3+)降至1×10-5mol/L,应调溶液的pH=5 |
您最近一年使用:0次

 减小
减小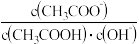 增大
增大