根据下列实验操作和现象所得出的结论错误的是
| 选项 | 操作 | 现象 | 结论 |
| A | 相同的铝片分别与同温同体积,且c(H+)=1mo l·L-1的盐酸、硫酸反应 | 铝与盐酸反应产生气泡较快 | 可能是Cl-对该反应起到促进作用 |
| B | 常温下,向等浓度、等体积的Na2CO3和NaHCO3溶液中滴加等量的酚酞试液 | Na2CO3溶液中红色更深 | 水解平衡常数Kh: > > |
| C | 向盛有H2O2溶液的试管中加入几滴酸化的硫酸亚铁溶液 | 溶液变成棕黄色,一段时间后,溶液中出现气泡,随后有红褐色沉淀生成 | Fe2+催化H2O2分解产生O2;H2O2分解反应放热,促进Fe2+的水解平衡正向移动 |
| D | 向浓度均为0.1mol/L的MgCl2和CuCl2的混合溶液中逐滴加入氨水 | 先出现蓝色沉淀 | Ksp[Mg(OH)2]>Ksp[Cu(OH)2] |
| A.A | B.B | C.C | D.D |
更新时间:2019-02-17 14:21:55
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】2023年电视剧《狂飙》火遍荧屏和网络,电视剧里面涉及许多化学知识,下列错误的是
| A.干嚼咖啡相比于水冲咖啡,干嚼咖啡会增加咖啡在身体里的浓度,提高化学反应速率 |
| B.冻鱼的方法保存鱼,是运用了降低温度减小化学反应速率的原理 |
| C.有压力要吃棒棒糖,棒棒糖主要成分是葡萄糖(C6H12O6),葡萄糖属于共价化合物 |
| D.“电鱼”属于原电池放电,放电时电流和电子都不能进入电解质溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】将同浓度、同体积的盐酸与醋酸分别与足量的镁条反应(忽略镁条表面积差异),测得恒容密闭容器中压强随时间的变化曲线如下图所示。下列说法正确的是
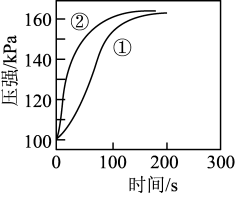

| A.曲线①表示盐酸与镁条的反应 | B.开始时,盐酸与醋酸c(H+)相等 |
| C.0~100s,醋酸的c(H+)下降更快 | D.较长时间后,容器内压强基本相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
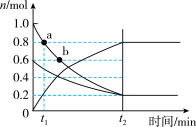
【推荐3】T1℃时,向容积为2L的恒容密闭容器中充入SO2和O2发生反应2SO2(g)+O2(g) 2SO3(g),容器中各组分的物质的量随时间变化如图所示。下列说法正确的是
2SO3(g),容器中各组分的物质的量随时间变化如图所示。下列说法正确的是
 2SO3(g),容器中各组分的物质的量随时间变化如图所示。下列说法正确的是
2SO3(g),容器中各组分的物质的量随时间变化如图所示。下列说法正确的是
| A.t2时刻,向容器中充入一定体积的气体氦,使容器中气体总的压强增大,则υ正、υ逆均增大 |
| B.气体密度不变时,反应达到平衡 |
C.0~t2时间段,反应速率υ(SO3)=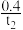 mol∙L−1∙min−1 mol∙L−1∙min−1 |
| D.若反应在T2℃进行(T2<T1),反应进行t1分钟后,n(SO2)<0.8mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】紫外光照射时,在不同催化剂作用下,可将CO2和H2O(g)转化为CH4和O2,CH4产量随光照时间的变化见图1。以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸,在不同温度下催化剂的催化效率与乙酸的生成速率的关系见图2。下列有关说法中正确的是( )


| A.由图1知,在0~15 h内,CH4的平均生成速率从大到小的顺序:Ⅲ>Ⅱ>Ⅰ |
| B.由图1知,在0~35 h内,CH4的平均生成速率从大到小的顺序:Ⅱ>Ⅲ>Ⅰ |
| C.由图2知,250 ℃时催化剂的活性最高 |
| D.由图2知,乙酸的生成最佳温度范围: 400 ℃以上 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
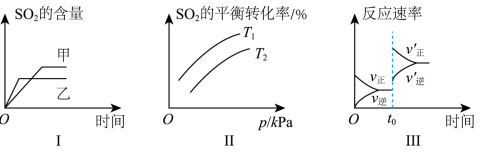
【推荐2】工业生产硫酸的一步重要反应是2SO2(g)+O2(g) 2SO3(g) ΔH<0,如果该反应在容积不变的密闭容器中进行,图中表示当其他条件不变时,改变某一条件对上述反应的影响,其中结论正确的是
2SO3(g) ΔH<0,如果该反应在容积不变的密闭容器中进行,图中表示当其他条件不变时,改变某一条件对上述反应的影响,其中结论正确的是
 2SO3(g) ΔH<0,如果该反应在容积不变的密闭容器中进行,图中表示当其他条件不变时,改变某一条件对上述反应的影响,其中结论正确的是
2SO3(g) ΔH<0,如果该反应在容积不变的密闭容器中进行,图中表示当其他条件不变时,改变某一条件对上述反应的影响,其中结论正确的是
| A.图Ⅰ表示催化剂对化学平衡的影响,且甲使用了催化剂 |
| B.图Ⅰ表示温度对化学平衡的影响,且甲温度高 |
| C.图Ⅱ表示SO2平衡转化率与温度及压强的关系,可以判断T1<T2 |
| D.图Ⅲ表示t0时刻升高温度或增大压强对反应速率的影响 |
您最近一年使用:0次
【推荐3】2SO2(g)+O2(g) 2SO3(g) ∆H=-198kJ•mol-1。在V2O5存在时该反应机理为:①V2O5+SO2→2VO2+SO3(快);②4VO2+O2→2V2O5(慢)。下列说法不正确的是
2SO3(g) ∆H=-198kJ•mol-1。在V2O5存在时该反应机理为:①V2O5+SO2→2VO2+SO3(快);②4VO2+O2→2V2O5(慢)。下列说法不正确的是
 2SO3(g) ∆H=-198kJ•mol-1。在V2O5存在时该反应机理为:①V2O5+SO2→2VO2+SO3(快);②4VO2+O2→2V2O5(慢)。下列说法不正确的是
2SO3(g) ∆H=-198kJ•mol-1。在V2O5存在时该反应机理为:①V2O5+SO2→2VO2+SO3(快);②4VO2+O2→2V2O5(慢)。下列说法不正确的是| A.该反应速率主要由第②步基元反应决定 |
| B.由反应机理可知,V2O5是该反应的催化剂 |
| C.V2O5的存在提高了该反应活化能,使单位时间内有效碰撞次数增加,反应速率加快 |
| D.逆反应的活化能比正反应的活化能大198kJ•mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验操作和现象正确,且所得到的结论也正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将 的NaHCO3溶液和等浓度的 CaCl2溶液混合 的NaHCO3溶液和等浓度的 CaCl2溶液混合 | 有沉淀生成 | 沉淀为碳酸氢钙 |
| B | 向5mL某无色溶液中滴加2滴酚酞溶液后呈橘红色溶液,再加5mL水混合均匀,加水后变为无色 | 加酚酞溶液后呈橘红色,加水后变为无色 | 原无色溶液可能为强酸性 |
| C | 将溴乙烷和 NaOH的乙醇溶液混合加热,产生气体通入酸性 KMnO4溶液 | 酸性KMnO4溶液褪色 | 产生了乙烯 |
| D | 向滴有酚酞的Na2CO3溶液中,逐滴加入BaCl2溶液 | 溶液红色逐渐褪去 | BaCl2溶液呈酸性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】25℃时,0.1 mol•L-1溶液的pH如下表,下列有关说法正确的是
| 序号 | ① | ② | ③ | ④ |
| 溶液 | NaCl | CH3COONH4 | NaF | NaHCO3 |
| pH | 7.0 | 7.0 | 8.1 | 8.4 |
| A.酸性强弱:HF<H2CO3 |
| B.①和②中溶质均未水解 |
| C.由水电离产生的c(H+):①>② |
| D.④溶液中:c(HCO3-)+c(CO32-)+c(H2CO3)= c(Na+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验操作、现象及结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将颗粒、大小相同的锌分别投入等体积、等pH的HA溶液和盐酸中 | HA溶液中产生气泡的速率比盐酸快 | 等浓度、等体积时溶液的酸性:HA>盐酸 |
| B | 常温下,将pH计置于 醋酸溶液中 醋酸溶液中 | pH计读数为2.9 | 醋酸是弱酸 |
| C | 将 溶液加入盛有2 mL浓度均为 溶液加入盛有2 mL浓度均为 的NaCl和NaI混合溶液的试管中 的NaCl和NaI混合溶液的试管中 | 混合溶液中出现黄色沉淀 | 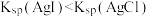 |
| D | 常温下,将滴有几滴酚酰试液的饱和碳酸钠溶液加热到50℃ | 溶液颜色加深,并产生大量气泡 |  的水解平衡正向移动 的水解平衡正向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在3 mL 0.1 mol·L-1NaCl溶液中加入2滴AgNO3溶液,出现白色沉淀,再加1滴KI溶液,沉淀变为黄色,再加入1滴Na2S溶液,沉淀又变为黑色。欲除去Ag2S中混有的AgCl杂质,应采用的方法是
| A.加入NaCl溶液振荡后过滤 | B.加入Na2S溶液振荡后过滤 |
| C.加入KI溶液振荡后过滤 | D.加入盐酸振荡后过滤 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】已知25℃时,Ksp(BaCO3)=8.1×10-9,Ksp(BaSO4)=1.0×10-10,下列说法正确的是( )
| A.因为Ksp(BaCO3)>Ksp(BaSO4),所以BaSO4不能转化成BaCO3 |
| B.25℃时,BaCO3要在Na2SO4溶液中开始转化成BaSO4,则Na2SO4的浓度必须不低于1.1×10-6mol·L-1 |
| C.在20mL0.002mol·L-1的Na2SO4溶液中加入20mL0.002mol·L-1的BaCl2溶液,无BaSO4沉淀生成 |
| D.向含有等浓度、等体积的BaCl2溶液的两支试管中同时滴加等浓度的Na2CO3和Na2SO4溶液,先生成BaCO3沉淀 |
您最近一年使用:0次

 的物质的量浓度相等的下列溶液:①(NH4)2SO4 ② (NH4)2Fe(SO4)2 ③(NH4)2CO3,溶质的物质的量浓度由大到小的顺序为
的物质的量浓度相等的下列溶液:①(NH4)2SO4 ② (NH4)2Fe(SO4)2 ③(NH4)2CO3,溶质的物质的量浓度由大到小的顺序为

