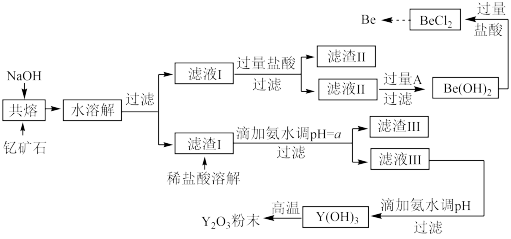
著名化学家徐光宪在稀土领域贡献突出,被誉为“稀土界的袁隆平”。钇是稀土元素之一,我国蕴藏着丰富的钇矿石(Y2FeBe2Si2O10),工业上通过如下工艺流程制取氧化钇,并获得副产物铍。
已知:ⅰ.钇(Y)的常见化合价为+3价;
ⅱ.铍和铝处于元素周期表的对角线位置,化学性质相似;
ⅲ.Fe3+、Y3+形成氢氧化物沉淀时的pH如下表:
(1)将钇矿石与NaOH共熔的反应方程式补充完整:
__ Y2FeBe2Si2O10+__ NaOH+____ 
__ Y(OH)3 +__ Fe2O3 + __ Na2SiO3 + __ Na2BeO2 + __ H2O
(2)滤渣Ⅱ的主要成分是____________ 。
(3)试剂A可以是___________ 。
A.NaOH溶液 B.氨水 C.CO2 D.CaO
(4)用氨水调节pH=a时,a的取值范围是_____________________ 。
(5)计算常温下Y3+ +3H2O Y(OH)3+3H+的平衡常数K=
Y(OH)3+3H+的平衡常数K=________ 。(常温下Ksp [Y(OH)3] = 8.0×10-23)
(6)滤液Ⅲ加入氨水产生沉淀的离子方程式为_______________ 。
(7)从BeCl2溶液中得到BeCl2固体的操作是________ 。
(8)常见的由BeCl2固体生产Be的工业方法有两种:①电解法:电解NaCl-BeCl2混合熔融盐制备Be;②热还原法:熔融条件下,钾还原BeCl2制备Be。以上两种方法你认为哪种更好并请说明理由_________ 。

已知:ⅰ.钇(Y)的常见化合价为+3价;
ⅱ.铍和铝处于元素周期表的对角线位置,化学性质相似;
ⅲ.Fe3+、Y3+形成氢氧化物沉淀时的pH如下表:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe3+ | 2.1 | 3.1 |
| Y3+ | 6.0 | 8.3 |

(2)滤渣Ⅱ的主要成分是
(3)试剂A可以是
A.NaOH溶液 B.氨水 C.CO2 D.CaO
(4)用氨水调节pH=a时,a的取值范围是
(5)计算常温下Y3+ +3H2O
 Y(OH)3+3H+的平衡常数K=
Y(OH)3+3H+的平衡常数K=(6)滤液Ⅲ加入氨水产生沉淀的离子方程式为
(7)从BeCl2溶液中得到BeCl2固体的操作是
(8)常见的由BeCl2固体生产Be的工业方法有两种:①电解法:电解NaCl-BeCl2混合熔融盐制备Be;②热还原法:熔融条件下,钾还原BeCl2制备Be。以上两种方法你认为哪种更好并请说明理由
更新时间:2019-05-26 13:35:52
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)。试回答:
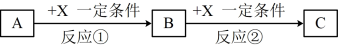
(1)若X是强氧化性单质,则A不可能是____ 。
a.S b.N2 c.Na d.Mg e.Al
(2)若A为强碱溶液,则X可能为____ 。
a.CO2 b.AlCl3 c.Al d.Mg e.Al2O3
(3)若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则B的化学式为____ ;C溶液在贮存时应加入少量X,理由是(离子方程式表示)___ ,检验此C溶液中金属元素价态的操作方法是____ 。
(4)若A、B、C为含有金属元素的化合物,X为强电解质,A溶液与C溶液反应生成B,则B的化学式为____ ,X的化学式可能为(写出不同类物质)____ 或____ ,反应②的离子方程式为___ 或___ 。

(1)若X是强氧化性单质,则A不可能是
a.S b.N2 c.Na d.Mg e.Al
(2)若A为强碱溶液,则X可能为
a.CO2 b.AlCl3 c.Al d.Mg e.Al2O3
(3)若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则B的化学式为
(4)若A、B、C为含有金属元素的化合物,X为强电解质,A溶液与C溶液反应生成B,则B的化学式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上从铝土矿(主要成分是Al2O3,还含有SiO2、Fe2O3等杂质)中提取铝可使用如下工艺流程:

已知:SiO2不溶于水且不与盐酸反应。请回答下列问题:
(1)图中涉及分离溶液与沉淀的实验方法是______ (填操作名称)。
(2)步骤(Ⅱ)中加入的烧碱溶液应该是______ (填“少量”或“过量”)。沉淀B的成分是______ (填化学式,下同);溶液D中含铝元素的溶质的是______ 。
(3)①物质M在生产生活中有重要用途,写出沉淀F转化为物质M的化学方程式:______ ;
溶液D中通入CO2生成沉淀F的离子方程式为:______ 。

已知:SiO2不溶于水且不与盐酸反应。请回答下列问题:
(1)图中涉及分离溶液与沉淀的实验方法是
(2)步骤(Ⅱ)中加入的烧碱溶液应该是
(3)①物质M在生产生活中有重要用途,写出沉淀F转化为物质M的化学方程式:
溶液D中通入CO2生成沉淀F的离子方程式为:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】A、J是日常生活中常见的两种金属,这两种金属和NaOH溶液组成原电池,A作负极;F常温下是气体,各物质有以下的转化关系(部分产物及条件已略去):
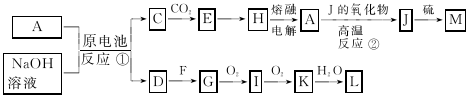
回答以下问题:
(1)A的原子结构示意图为_________________ ,M的化学式为________ 。
(2)A与NaOH溶液反应的离子方程式为_________________ 。
(3)反应②又称为________ 。
(4)含A元素的某盐X常作净水剂,X做焰色反应时,透过蓝色钴玻璃观察火焰呈紫色。X的水溶液与NaHCO3溶液混合,反应的离子方程式为_____________ 。

回答以下问题:
(1)A的原子结构示意图为
(2)A与NaOH溶液反应的离子方程式为
(3)反应②又称为
(4)含A元素的某盐X常作净水剂,X做焰色反应时,透过蓝色钴玻璃观察火焰呈紫色。X的水溶液与NaHCO3溶液混合,反应的离子方程式为
您最近一年使用:0次
【推荐1】回答下列问题:
(1)“84”消毒液是一种以NaClO为主要成分的高效消毒剂,NaClO溶液呈_______ 性(填“酸”“碱”或“中”),原因可用离子方程式表示为_______ 。
(2)25℃时,pH均为4的醋酸和硫酸铝两种溶液中,由水电离出的 之比为
之比为_______ 。
(3)已知热化学方程式:
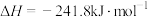 ,其正反应的活化能
,其正反应的活化能_______ 逆反应的活化能(填“>”“=”或“<”)。
(4)向浓度均为 的
的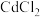 和
和 混合液中滳加碳酸铵溶液至生成两种沉淀,则溶液中
混合液中滳加碳酸铵溶液至生成两种沉淀,则溶液中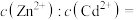
_______ 。[已知: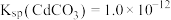 、
、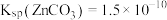 ]
]
(5)相同条件下, 下列溶液中,
下列溶液中, 由小到大的排列顺序是
由小到大的排列顺序是_______ (填序号)。
A. B.
B. C.
C. D.
D. E.
E.
(6)已知:
Ⅰ.
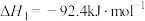
Ⅱ.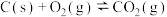
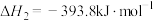
Ⅲ.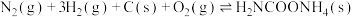
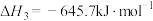
写出 分解生成
分解生成 与
与 气体的热化学方程式:
气体的热化学方程式:_______ 。
(1)“84”消毒液是一种以NaClO为主要成分的高效消毒剂,NaClO溶液呈
(2)25℃时,pH均为4的醋酸和硫酸铝两种溶液中,由水电离出的
 之比为
之比为(3)已知热化学方程式:

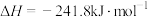 ,其正反应的活化能
,其正反应的活化能(4)向浓度均为
 的
的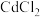 和
和 混合液中滳加碳酸铵溶液至生成两种沉淀,则溶液中
混合液中滳加碳酸铵溶液至生成两种沉淀,则溶液中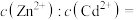
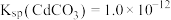 、
、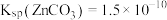 ]
](5)相同条件下,
 下列溶液中,
下列溶液中, 由小到大的排列顺序是
由小到大的排列顺序是A.
 B.
B. C.
C. D.
D. E.
E.
(6)已知:
Ⅰ.

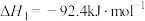
Ⅱ.
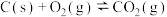
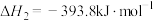
Ⅲ.
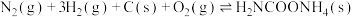
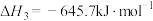
写出
 分解生成
分解生成 与
与 气体的热化学方程式:
气体的热化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】钒铬还原渣是钠化提钒过程的固体废弃物,其主要成分为VO2·xH2O、Cr(OH)3及少量的SiO2。一种初步分离钒铬还原渣中钒铬并获得Na2Cr2O7的工艺流程如下:
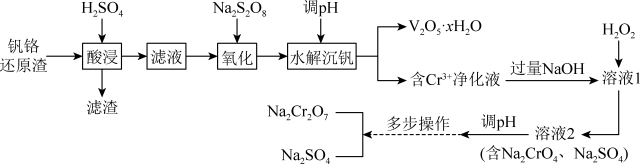
已知:①“酸浸”后VO2·xH2O转化为VO2+;
②Cr(OH)3的Ksp近似为1×10-30;
③有关物质的溶解度(g/100gH2O)如下表所示:
回答下列问题:
(1)“滤渣”的主要成分是___________ ,“氧化”生成VO ,发生反应的离子方程式为
,发生反应的离子方程式为___________ 。
(2)若“含Cr3+净化液”中c(Cr3+)=0.1mol/L,则“水解沉钒”调pH的范围是2.5~___________ 。
(3)“溶液1”中含CrO ,加入H2O2后发生反应的离子方程式为
,加入H2O2后发生反应的离子方程式为___________ ,该反应中氧化剂与还原剂的物质的量之比为___________ 。
(4)“多步操作”包括蒸发浓缩、___________ 、冷却结晶、过滤、洗涤等步骤。
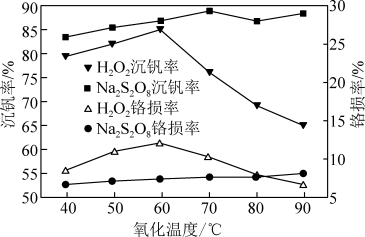
(5)研究温度对Na2S2O8与H2O2的氧化—水解沉钒率的影响,得到如图所示结果。钒铬还原渣酸浸液初始温度在90℃左右,降低温度能耗增加。由图可知,分别采用H2O2、Na2S2O8进行“氧化”时,应选择的适宜温度是___________ 、___________ ,与Na2S2O8相比,采用H2O2氧化的主要不足之处有___________ (写出两点)。

已知:①“酸浸”后VO2·xH2O转化为VO2+;
②Cr(OH)3的Ksp近似为1×10-30;
③有关物质的溶解度(g/100gH2O)如下表所示:
| 温度/℃ | 20 | 40 | 60 | 80 | 100 |
| Na2Cr2O7 | 183.6 | 215.1 | 269.2 | 376.4 | 415.0 |
| Na2SO4 | 19.5 | 48.8 | 45.3 | 43.7 | 42.5 |
(1)“滤渣”的主要成分是
 ,发生反应的离子方程式为
,发生反应的离子方程式为(2)若“含Cr3+净化液”中c(Cr3+)=0.1mol/L,则“水解沉钒”调pH的范围是2.5~
(3)“溶液1”中含CrO
 ,加入H2O2后发生反应的离子方程式为
,加入H2O2后发生反应的离子方程式为(4)“多步操作”包括蒸发浓缩、
(5)研究温度对Na2S2O8与H2O2的氧化—水解沉钒率的影响,得到如图所示结果。钒铬还原渣酸浸液初始温度在90℃左右,降低温度能耗增加。由图可知,分别采用H2O2、Na2S2O8进行“氧化”时,应选择的适宜温度是

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】工业上利用废镍催化剂(主要成分为Ni,还含有一定量的Zn、Fe、SiO2、CaO等)制备草酸镍晶体的流程如下:

(1)请写出一种能提高“酸浸”速率的措施:___________ ;滤渣I的成分是___________ (填化学式)。
(2)除铁时,控制不同的条件可以得到不同的滤渣II。已知滤渣II的成分与温度、pH关系如图所示:

①写出除铁步骤中次氯酸钠发生反应的离子方程式___________ 。
②若控制温度25℃、pH=4时除去铁,此时溶液中c(Fe3+)=___________ 。(已知25℃时,Fe(OH)3的Ksp[Fe(OH)3]=2.64×10-39)
(3)加入有机萃取剂除掉的金属阳离子主要是___________ 。
(4)某化学镀镍试剂的化学式为(NH4)xNi(SO4)y(Ni为+2价,,x、y均为正整数)。为测定该镀镍试剂的组成,进行如下实验:
I、称量28.7g镀镍试剂,配制100mL溶液A;
Ⅱ、准确量取10.00mL溶液A,用0.40mol·L-1的EDTA(Na2H2Y)标准溶液滴定其中的Ni2+(离子方程式为Ni2++H2Y2-=NiY2-+2H+),消耗EDTA标准溶液25.00mL;
Ⅲ、另取10.00mL溶液A,加入足量的BaCl2溶液,得到白色沉淀4.66g。
①配制100mL镀镍试剂时,需要的仪器除药匙、托盘天平、玻璃棒、烧杯、量筒、胶头滴管外,还需要___________ 。
②该镀镍试剂的化学式为___________ 。

(1)请写出一种能提高“酸浸”速率的措施:
(2)除铁时,控制不同的条件可以得到不同的滤渣II。已知滤渣II的成分与温度、pH关系如图所示:

①写出除铁步骤中次氯酸钠发生反应的离子方程式
②若控制温度25℃、pH=4时除去铁,此时溶液中c(Fe3+)=
(3)加入有机萃取剂除掉的金属阳离子主要是
(4)某化学镀镍试剂的化学式为(NH4)xNi(SO4)y(Ni为+2价,,x、y均为正整数)。为测定该镀镍试剂的组成,进行如下实验:
I、称量28.7g镀镍试剂,配制100mL溶液A;
Ⅱ、准确量取10.00mL溶液A,用0.40mol·L-1的EDTA(Na2H2Y)标准溶液滴定其中的Ni2+(离子方程式为Ni2++H2Y2-=NiY2-+2H+),消耗EDTA标准溶液25.00mL;
Ⅲ、另取10.00mL溶液A,加入足量的BaCl2溶液,得到白色沉淀4.66g。
①配制100mL镀镍试剂时,需要的仪器除药匙、托盘天平、玻璃棒、烧杯、量筒、胶头滴管外,还需要
②该镀镍试剂的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】如表为长式周期表的一部分,其中的编号代表对应的元素。
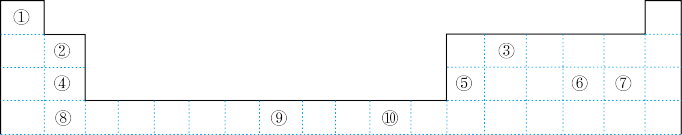
请回答下列问题:
(1)表中属于d区的元素是_______ (填编号)。
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为_______ 。
(3)④⑤⑥⑦四种元素的第一电离能由大到小的顺序是_______ (用元素符号表示)。
(4)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的未成对电子数为_______ ;该元素与元素①形成的分子X的立体构型为_______ ,与⑧在同一周期的元素中的未成对电子数目最多的元素的价电子排布式是_______ 。
(5)某些不同族元素的性质也有一定的相似性,如表中元素⑤与元素②的氢氧化物有相似的性质,请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:_______ 。

请回答下列问题:
(1)表中属于d区的元素是
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为
(3)④⑤⑥⑦四种元素的第一电离能由大到小的顺序是
(4)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的未成对电子数为
(5)某些不同族元素的性质也有一定的相似性,如表中元素⑤与元素②的氢氧化物有相似的性质,请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】如图是部分元素的第一电离能随原子序数变化的曲线(其中12~17号元素的有关数据缺失)。

(1)请写出 区铜原子基态电子排布式
区铜原子基态电子排布式_______
(2)同主族元素的第一电离能的变化规律是_______
(3)图中第一电离能最小的元素在周期表中的位置是_______
(4)根据对角线规则,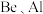 的最高价氧化物对应水化物的性质相似,它们都具有
的最高价氧化物对应水化物的性质相似,它们都具有_______ 性,能证明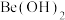 该性质的实验结论是
该性质的实验结论是_______
(5) 元素中,某元素M电离能如表所示:
元素中,某元素M电离能如表所示:
①由此判断该元素是_______ (填元素符号);
②分析图中同周期元素第一电离能的变化规律,推断: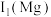
_______  。
。

(1)请写出
 区铜原子基态电子排布式
区铜原子基态电子排布式(2)同主族元素的第一电离能的变化规律是
(3)图中第一电离能最小的元素在周期表中的位置是
(4)根据对角线规则,
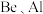 的最高价氧化物对应水化物的性质相似,它们都具有
的最高价氧化物对应水化物的性质相似,它们都具有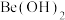 该性质的实验结论是
该性质的实验结论是(5)
 元素中,某元素M电离能如表所示:
元素中,某元素M电离能如表所示: | 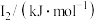 | 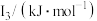 | 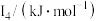 | 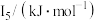 |
| 578 | 1817 | 2745 | 11575 | 14830 |
②分析图中同周期元素第一电离能的变化规律,推断:
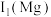
 。
。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】X、Y、Z、W是原子序数依次增大的短周期主族元素,且互不同族;其中X、Y为金属元素,Z、W为非金属元素;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9。Y的单质可与NaOH溶液反应。
(1)Z的原子结构示意图为_________ 。
(2)Y、Z、W的原子半径由小到大的顺序是__________ (用元素符号表示)。
(3)工业生产单质Y的原理是_________________ (用化学方程式表示)。
(4)X与Y的化学性质相似,则单质X与NaOH浓溶液反应的化学方程式是_____________ 。
(1)Z的原子结构示意图为
(2)Y、Z、W的原子半径由小到大的顺序是
(3)工业生产单质Y的原理是
(4)X与Y的化学性质相似,则单质X与NaOH浓溶液反应的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】最新研究发现新型催化剂M可稳定催化纯甲酸(HCOOH)脱氢生成H2和CO2,且M在室温下即可生效,95°C催化活性达最大值,有水存在的情况下催化活性略有降低。实验室利用该方法使纯甲酸分解并收集所得气体的装置如图所示,请回答下列问题:

(1)仪器a的名称是_______ ,其作用是_______ 。
(2)实验中为了使催化剂M的活性达到最大值,采用的措施有_______ 、_______ 、_______ 。
(3)若要将分解所得的气体中的CO2除去并收集氢气,可调节三通阀的位置将气体导出,并依次通过下列装置:装NaOH溶液的洗气瓶装浓硫酸的洗气瓶→氢气收集装置→装有碱石灰的干燥管→酒精灯点燃尾气。其中收集氢气应采用的方法是_______ ,可选择的装置是_______ (填标号)。
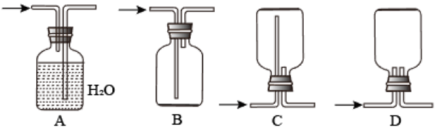

(1)仪器a的名称是
(2)实验中为了使催化剂M的活性达到最大值,采用的措施有
(3)若要将分解所得的气体中的CO2除去并收集氢气,可调节三通阀的位置将气体导出,并依次通过下列装置:装NaOH溶液的洗气瓶装浓硫酸的洗气瓶→氢气收集装置→装有碱石灰的干燥管→酒精灯点燃尾气。其中收集氢气应采用的方法是

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】硼镁泥是一种工业废料,主要成份是MgO(占40%),还有Al2O3、CaO、MnO、Fe2O3、FeO、SiO2等杂质,以此为原料提取硫酸镁晶体和氢氧化铝。
从硼镁泥中提取MgSO4·7H2O的流程如图:
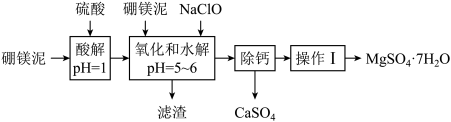
已知:NaClO与Mn2+反应产生MnO2沉淀。
请完成下列填空:
(1)实验中需用1.00mol/L的硫酸80.0mL,若用98%的浓硫酸(密度1.84g/cm3)来配制,除玻璃棒、胶头滴管、烧杯外,还需要的定量玻璃仪器有___ (注明规格)。
(2)加入的NaClO有三个作用,用离子方程式表示其中一个作用:___ 。
已知MgSO4、CaSO4的溶解度如下表:
(3)“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,操作步骤依次为蒸发浓缩、___ 。操作Ⅰ中的步骤之一是洗涤沉淀,具体的操作方法是___ 。
(4)如果测得提供的硼镁泥的质量为100.0g,得到的MgSO4·7H2O196.8g,则MgSO4·7H2O的产率为___ 。
(5)从硼镁泥提取硫酸镁晶体后的滤渣,主要还含有Al(OH)3、Fe(OH)3,MnO2、SiO2,先用稀盐酸除去MnO2和SiO2,请补全下面的流程图,完成从滤渣中获取Al(OH)3的方案(仿照上述流程图表示)。

___ 。
从硼镁泥中提取MgSO4·7H2O的流程如图:

已知:NaClO与Mn2+反应产生MnO2沉淀。
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 2.3 | 4.0 | 7.6 |
| 完全沉淀pH | 4.1 | 5.2 | 9.6 |
(1)实验中需用1.00mol/L的硫酸80.0mL,若用98%的浓硫酸(密度1.84g/cm3)来配制,除玻璃棒、胶头滴管、烧杯外,还需要的定量玻璃仪器有
(2)加入的NaClO有三个作用,用离子方程式表示其中一个作用:
已知MgSO4、CaSO4的溶解度如下表:
| 温度(℃) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
(4)如果测得提供的硼镁泥的质量为100.0g,得到的MgSO4·7H2O196.8g,则MgSO4·7H2O的产率为
(5)从硼镁泥提取硫酸镁晶体后的滤渣,主要还含有Al(OH)3、Fe(OH)3,MnO2、SiO2,先用稀盐酸除去MnO2和SiO2,请补全下面的流程图,完成从滤渣中获取Al(OH)3的方案(仿照上述流程图表示)。

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】物质的制备是化学学科的基本研究方向。
(1)氧化钠是一种碱性氧化物,主要用于制备钠的化合物,也可用作脱氢剂,还可用作化学反应的聚合或缩合剂。已知用金属钠制取氧化钠,可有多种方法:① ②
② ③
③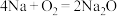 ,在上述三种方法中最好的是
,在上述三种方法中最好的是_______ (填序号)。
(2)某同学拟用50 mL NaOH溶液吸收 气体制备
气体制备 溶液,他设计了如下实验步骤:
溶液,他设计了如下实验步骤:
①用25 mL NaOH溶液吸收过量的 气体,至
气体,至 气体不再溶解;
气体不再溶解;
②小心加热溶液1~2min;
③在得到的溶液中加入另一半(25 mL)NaOH溶液,使溶液充分混合。
制备过程中涉及到的化学反应用离子方程式分别表示为_______ 、_______ 。
(3)过氧化钙( )是一种新型水产养殖增氧剂,常用于鲜活水产品的运输。实验室可用钙盐制取
)是一种新型水产养殖增氧剂,常用于鲜活水产品的运输。实验室可用钙盐制取 ,再经脱水制得
,再经脱水制得 ,
, 不溶于水,在0℃时稳定,加热至130℃时逐渐变为无水
不溶于水,在0℃时稳定,加热至130℃时逐渐变为无水 ,其制备过程如下:
,其制备过程如下:

Ⅰ.“沉淀”时反应温度不能过高的原因:①防止氨水挥发;②_______ ;
Ⅱ.“沉淀”时发生的反应用化学方程式表示为:_______ ;
(1)氧化钠是一种碱性氧化物,主要用于制备钠的化合物,也可用作脱氢剂,还可用作化学反应的聚合或缩合剂。已知用金属钠制取氧化钠,可有多种方法:①
 ②
② ③
③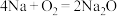 ,在上述三种方法中最好的是
,在上述三种方法中最好的是(2)某同学拟用50 mL NaOH溶液吸收
 气体制备
气体制备 溶液,他设计了如下实验步骤:
溶液,他设计了如下实验步骤:①用25 mL NaOH溶液吸收过量的
 气体,至
气体,至 气体不再溶解;
气体不再溶解;②小心加热溶液1~2min;
③在得到的溶液中加入另一半(25 mL)NaOH溶液,使溶液充分混合。
制备过程中涉及到的化学反应用离子方程式分别表示为
(3)过氧化钙(
 )是一种新型水产养殖增氧剂,常用于鲜活水产品的运输。实验室可用钙盐制取
)是一种新型水产养殖增氧剂,常用于鲜活水产品的运输。实验室可用钙盐制取 ,再经脱水制得
,再经脱水制得 ,
, 不溶于水,在0℃时稳定,加热至130℃时逐渐变为无水
不溶于水,在0℃时稳定,加热至130℃时逐渐变为无水 ,其制备过程如下:
,其制备过程如下:
Ⅰ.“沉淀”时反应温度不能过高的原因:①防止氨水挥发;②
Ⅱ.“沉淀”时发生的反应用化学方程式表示为:
您最近一年使用:0次



