在电解炼铝过程中加入冰晶石(用“A”代替),可起到降低Al2O3熔点的作用。冰晶石的生产原理为2Al(OH)3+12HF+3Na2CO3═2A+3CO2↑+9H2O。根据题意完成下列填空:
(1)冰晶石的化学式为________ ,含有的化学键类型为_________________ 。
(2)生成物中含有一个10个电子的分子,该分子的空间构型为________ ,中心原子的杂化方式为________ 。
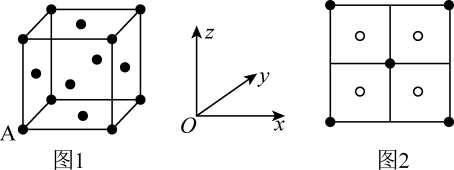
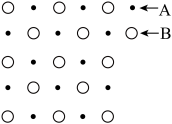
(3)冰晶石由两种微粒构成,冰晶石的晶胞结构如图甲所示,●位于大立方体的顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处所代表的微粒是________ (填微粒符号)。
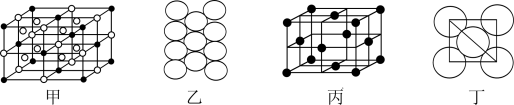
(4)Al单质的晶体中原子的堆积方式如图乙所示,其晶胞特征如图丙所示,原子之间相互位置关系的平面图如图丁所示。则一个晶胞中Al原子的数目为________ 个。
(1)冰晶石的化学式为
(2)生成物中含有一个10个电子的分子,该分子的空间构型为
(3)冰晶石由两种微粒构成,冰晶石的晶胞结构如图甲所示,●位于大立方体的顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处所代表的微粒是
(4)Al单质的晶体中原子的堆积方式如图乙所示,其晶胞特征如图丙所示,原子之间相互位置关系的平面图如图丁所示。则一个晶胞中Al原子的数目为

更新时间:2019-06-20 18:35:03
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】回答下列问题
(1)已知25℃时: Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-12。取一定量含有I-、Cl-的溶液向其中滴加AgNO3溶液,当AgCl 和AgI同时沉淀时,溶液中 为
为_______ 。
(2)下列粒子:①CS2;②PCl3;③H2S ;④CH2O;⑤H3O+;⑥ ;⑦BF3;⑧SO2。价层电子对的立体构型和粒子的立体构型一致的是
;⑦BF3;⑧SO2。价层电子对的立体构型和粒子的立体构型一致的是_______ ,②③⑥的键角从大到小的顺序是_______ 。
(3)已知拆开1mol H-H键、lmolN≡N 和lmol N-H键分别需要的能量是436kJ、948kJ、391 kJ。则N2、H2合成NH3的热化学方程式为_______ 。
(1)已知25℃时: Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-12。取一定量含有I-、Cl-的溶液向其中滴加AgNO3溶液,当AgCl 和AgI同时沉淀时,溶液中
 为
为(2)下列粒子:①CS2;②PCl3;③H2S ;④CH2O;⑤H3O+;⑥
 ;⑦BF3;⑧SO2。价层电子对的立体构型和粒子的立体构型一致的是
;⑦BF3;⑧SO2。价层电子对的立体构型和粒子的立体构型一致的是(3)已知拆开1mol H-H键、lmolN≡N 和lmol N-H键分别需要的能量是436kJ、948kJ、391 kJ。则N2、H2合成NH3的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氮、氟及其化合物在生产及生活中有着广泛的用途。请回答下列问题:
(1)氟磷灰石可用于制取磷肥,基态P原子有_______________ 个未成对电子, 的中心P原子的杂化方式为
的中心P原子的杂化方式为____________________ 。
(2)氟气可以用于制取惰性强于 的保护气
的保护气 ,也可以用于制取聚合反应的催化剂
,也可以用于制取聚合反应的催化剂 ,
, 可以作为工业制取硅单质的中间物质
可以作为工业制取硅单质的中间物质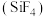 的原料。S、P、
的原料。S、P、 的第一电离能由大到小的顺序为
的第一电离能由大到小的顺序为_________________ 。
(3)键角比较:
___________  (填“>”或“<”)。
(填“>”或“<”)。
(1)氟磷灰石可用于制取磷肥,基态P原子有
 的中心P原子的杂化方式为
的中心P原子的杂化方式为(2)氟气可以用于制取惰性强于
 的保护气
的保护气 ,也可以用于制取聚合反应的催化剂
,也可以用于制取聚合反应的催化剂 ,
, 可以作为工业制取硅单质的中间物质
可以作为工业制取硅单质的中间物质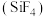 的原料。S、P、
的原料。S、P、 的第一电离能由大到小的顺序为
的第一电离能由大到小的顺序为(3)键角比较:

 (填“>”或“<”)。
(填“>”或“<”)。
您最近一年使用:0次
【推荐3】2019年的化学诺贝尔奖颁给了为锂电池研究作出贡献的三位科学家。有两种常见锂电池:一种是采用镍钴锰酸锂Li(NiCoMn)O2或镍钴铝酸锂为正极的“三元材料锂电池”;另一种是采用磷酸铁锂为正极的磷酸铁锂电池。请回答下列问题:
(1)基态钴原子的价电子排布式为____ ,Mn位于元素周期表的____ 区(填“s”或“p”或“d”或“ds”或“f”)。
(2)磷元素可以形成多种含氧酸H3PO4、H3PO2、H3PO3、HPO3,这四种酸中酸性最强的是___ 。PO43-的空间构型是 ___ ,中心原子的杂化方式是 ____ 。
(3)CoO、MnO两种氧化物的熔点由高到低的顺序是___ ,原因是 ___ 。
(4)PH3是____ 分子(填“极性”或“非极性”),其在水中的溶解性比NH3小,原因是 _____
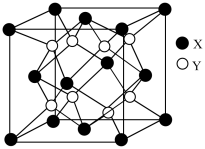
(5)硫化锂Li2S(摩尔质量Mg∙mol-1)的纳米晶体是开发先进锂电池的关键材料,硫化锂的晶体为反萤石结构,其晶胞结构如图。若硫化锂晶体的密度为ag.cm-3,则距离最近的两个S2-的距离是___ nm。(用含a、M、NA的计算式表示)
(1)基态钴原子的价电子排布式为
(2)磷元素可以形成多种含氧酸H3PO4、H3PO2、H3PO3、HPO3,这四种酸中酸性最强的是
(3)CoO、MnO两种氧化物的熔点由高到低的顺序是
(4)PH3是
(5)硫化锂Li2S(摩尔质量Mg∙mol-1)的纳米晶体是开发先进锂电池的关键材料,硫化锂的晶体为反萤石结构,其晶胞结构如图。若硫化锂晶体的密度为ag.cm-3,则距离最近的两个S2-的距离是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化 ,将
,将 转化为
转化为 ,反应过程如图所示:
,反应过程如图所示:___________ 。
(2) 的电子式是
的电子式是___________ 。
(3)与 互为等电子体的一种分子为
互为等电子体的一种分子为___________ (填化学式)。
 ,将
,将 转化为
转化为 ,反应过程如图所示:
,反应过程如图所示: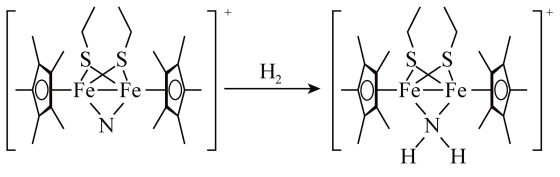
(2)
 的电子式是
的电子式是(3)与
 互为等电子体的一种分子为
互为等电子体的一种分子为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】N元素有多种化合物,它们之间可以发生转化,如:N2H4+HNO2=2H2O+HN3。请回答下列问题:
(1)N与C第一电离能较大的是________ 。
(2)NaN3的晶体类型是________ 。
(3)N的基态原子的电子排布中,有________ 个运动状态不同的未成对电子。
(4)纯叠氮酸HN3在常温下是一种液体,沸点较高,为308.8 K,主要原因是____________ 。
(5)HNO2中的N原子的杂化类型是________ 。
(6)NO2-离子是一种很好的配位体,能提供孤电子对的是________ 。
A.氧原子 B.氮原子 C.两者都可以
NO2-与钴盐通过配位键形成的[Co(NO2)6]3-能与K+离子结合生成黄色K3[Co(NO2)6]沉淀,此方法可用于检验溶液中的K+离子,写出该配合物中钴离子的电子排布式:______________ 。
(7)N2H4分子中________ (填“含”或“不含”)π键。
(1)N与C第一电离能较大的是
(2)NaN3的晶体类型是
(3)N的基态原子的电子排布中,有
(4)纯叠氮酸HN3在常温下是一种液体,沸点较高,为308.8 K,主要原因是
(5)HNO2中的N原子的杂化类型是
(6)NO2-离子是一种很好的配位体,能提供孤电子对的是
A.氧原子 B.氮原子 C.两者都可以
NO2-与钴盐通过配位键形成的[Co(NO2)6]3-能与K+离子结合生成黄色K3[Co(NO2)6]沉淀,此方法可用于检验溶液中的K+离子,写出该配合物中钴离子的电子排布式:
(7)N2H4分子中
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】根据下列信息,结合有关物质结构的知识回答:
(1)已知M是短周期金属元素,M的部分电离能如下表所示:

则M基态原子的电子排布式为___________ ,该金属晶体的堆积方式为六方最密堆积,配位数为___________ 。
(2)已知KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似,且三种离子晶体的晶格能数据如下表所示:

则KC1、CaO、TiN三种离子晶体熔点由高到低的顺序为___________ ,原因是___________ 。
(3)根据下图回答:
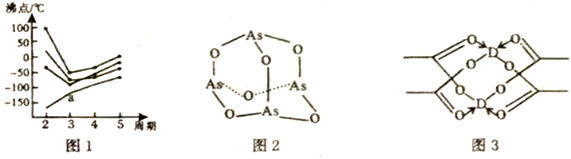
①如图1所示,每条折线表示周期表ⅣA~ⅦA中的某一主族元素的简单氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的物质是___________ (填化学式)。判断依据是___________ 。
②As4O6的分子结构如图2所示,则该化合物中As的杂化方式是___________ ,与AsO43-互为等电子体的微粒是___________ (写出一种即可)。
③D的醋酸盐晶体局部结构如图3所示,该晶体中含有的化学键类型有___________ (填字母标号)
A.极性键 B.非极性键 C.配位键 D.金属键
(4)Fe的一种晶体结构如图甲、乙所示,若按甲虚线方向切割乙,得到的截面图A~D中正确的是___________ (填字母标号)。

假设铁原子的半径是rcm,铁的相对原子质量为M,则该晶体的密度为___________ (设阿伏伽德罗常数的值为NA)
(1)已知M是短周期金属元素,M的部分电离能如下表所示:

则M基态原子的电子排布式为
(2)已知KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似,且三种离子晶体的晶格能数据如下表所示:

则KC1、CaO、TiN三种离子晶体熔点由高到低的顺序为
(3)根据下图回答:

①如图1所示,每条折线表示周期表ⅣA~ⅦA中的某一主族元素的简单氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的物质是
②As4O6的分子结构如图2所示,则该化合物中As的杂化方式是
③D的醋酸盐晶体局部结构如图3所示,该晶体中含有的化学键类型有
A.极性键 B.非极性键 C.配位键 D.金属键
(4)Fe的一种晶体结构如图甲、乙所示,若按甲虚线方向切割乙,得到的截面图A~D中正确的是

假设铁原子的半径是rcm,铁的相对原子质量为M,则该晶体的密度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)LiAlH4是有机合成中常用的还原剂。LiAlH4中,存在___________ (填标号)。
A.离子键 B.σ键 C.π键 D.氢键
(2)ZnF2具有较高的熔点(872℃),其化学键类型是___________ 。
(3)N2分子中σ键与π键的数目比n(σ)∶n(π)=___________ 。
(4)[Fe(H2O)6]2+与NO反应生成的[Fe(NO)(H2O)5]2+中,NO以N原子与Fe2+形成配位键。请在[Fe(NO)(H2O)5]2+结构示意图的相应位置补填缺少的配体___________ 。
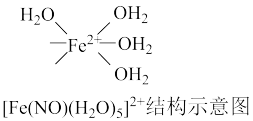
A.离子键 B.σ键 C.π键 D.氢键
(2)ZnF2具有较高的熔点(872℃),其化学键类型是
(3)N2分子中σ键与π键的数目比n(σ)∶n(π)=
(4)[Fe(H2O)6]2+与NO反应生成的[Fe(NO)(H2O)5]2+中,NO以N原子与Fe2+形成配位键。请在[Fe(NO)(H2O)5]2+结构示意图的相应位置补填缺少的配体
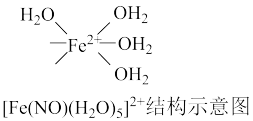
您最近一年使用:0次
【推荐2】H、C、N、O、F、S等是重要的非金属元素,回答下列问题:
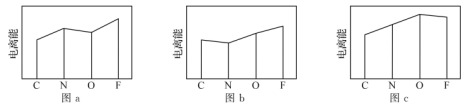
(1)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第二电离能的变化图是_______ (填标号),判断的根据是_______ 。
(2)已知C—H、C—F的键能分别为413.4 、485
、485 。在2022年冬奥会上“水立方”华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯(
。在2022年冬奥会上“水立方”华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯( )与四氟乙烯(
)与四氟乙烯( )的共聚物(ETFE)制成。
)的共聚物(ETFE)制成。 、
、 分子的稳定性关系:前者
分子的稳定性关系:前者_______ 后者(填“大于”或“小于”),原因是_______ 。
(3)相同条件下, 与
与 在水中的溶解度较大的是
在水中的溶解度较大的是_______ (写分子式),理由是_______ 。
(4)已知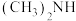 比
比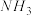 接收质子的能力强,可能的原因是
接收质子的能力强,可能的原因是_______ 。
(1)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第二电离能的变化图是

(2)已知C—H、C—F的键能分别为413.4
 、485
、485 。在2022年冬奥会上“水立方”华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯(
。在2022年冬奥会上“水立方”华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯( )与四氟乙烯(
)与四氟乙烯( )的共聚物(ETFE)制成。
)的共聚物(ETFE)制成。 、
、 分子的稳定性关系:前者
分子的稳定性关系:前者(3)相同条件下,
 与
与 在水中的溶解度较大的是
在水中的溶解度较大的是(4)已知
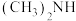 比
比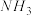 接收质子的能力强,可能的原因是
接收质子的能力强,可能的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】向硫酸铜水溶液中逐滴加入氨水,先形成蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色的透明溶液,再向溶液中加入乙醇有深蓝色晶体[化学式为[Cu(NH3)4]SO4·H2O]析出。
(1)写出上述实验前两步反应的离子方程式__________ ,____________ 。
(2)铜元素基态原子的电子排布式为_________________ ,铜单质晶体中的原则堆积模型属于_________ 堆积(填堆积模型名称)。
(3)在上述深蓝色晶体所含的非金属元素中,电负性最大的是_________ (填元素符号),第一电离能最大的是_________ (填元素符号)。该晶体中的阴离子的立体构型是_________ ,阴离子的中心原子的杂化方式为_________ 。
(4)氨的沸点_________ (填“高于”或“低于”)膦(PH3),原因是_____________ 。
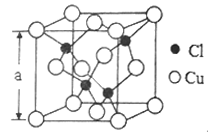
(5)Cu的一种氯化物晶胞结构如图所示,该氯化物的化学式是______________ 。若该晶体的密度为ρg·cm-3,以NA表示阿伏伽德罗常数,则该晶胞的边长为a=_____________ nm。
(1)写出上述实验前两步反应的离子方程式
(2)铜元素基态原子的电子排布式为
(3)在上述深蓝色晶体所含的非金属元素中,电负性最大的是
(4)氨的沸点

(5)Cu的一种氯化物晶胞结构如图所示,该氯化物的化学式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
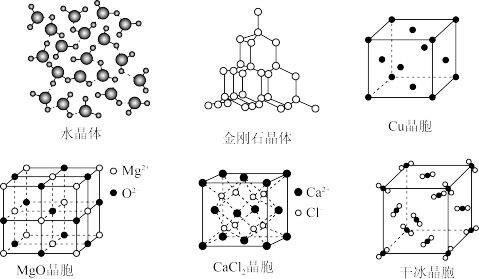
【推荐1】下列为几种晶体或晶胞的示意图:
请回答下列问题:
(1)上述晶体中,粒子之间以共价键结合形成晶体的是___________ 。
(2)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为___________ 。
(3)每个Cu晶胞中实际占有___________ 个 Cu原子;CaCl2晶体中Ca2+的配位数为___________ 。
(4)观察CO2分子晶体结构的一部分,每个CO2分子周围有___________ 个与之紧邻 且等距的CO2分子;

请回答下列问题:
(1)上述晶体中,粒子之间以共价键结合形成晶体的是
(2)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为
(3)每个Cu晶胞中实际占有
(4)观察CO2分子晶体结构的一部分,每个CO2分子周围有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)某物质的晶体内部一个截面上原子的排布情况如图所示,则该晶体的化学式可表示为________
(2)Si 元素以 Si-O-Si 链构成矿物界,由许多四面体(图 l)连接成无限长的单链或双链(图 2)结构。图 2 所示的多硅酸根离子的化学式通式为________ (以含正整数 n 的代数式表示)。


(2)Si 元素以 Si-O-Si 链构成矿物界,由许多四面体(图 l)连接成无限长的单链或双链(图 2)结构。图 2 所示的多硅酸根离子的化学式通式为

您最近一年使用:0次

 呈黑色或灰黑色,已知:晶胞中
呈黑色或灰黑色,已知:晶胞中 的位置如图1所示,
的位置如图1所示, 位于
位于