铁、钴、镍为第四周期第Ⅷ族元素,它们的性质非常相似,也称为铁系元素.
(1)铁、钴、镍都是很好的配位化合物形成体.
①[Co(H2O)6]2+在过量氨水中易转化为[Co(NH3)6]2+。写出Co2+的价层电子排布图__ .[Co(H2O)6]2+中Co2+的配位数为__ 。NH3分子的中心原子杂化方式为__ ,H2O分子的立体构型为__ 。
②铁、镍易与一氧化碳作用形成羰基配合物,如:Fe(CO)5,Ni(CO)4等.CO与N2属于等电子体,则CO分子中σ键和π键数目比为__ ,写出与CO互为等电子体的一种阴离子的离子符号__ 。
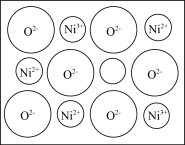
(2)+2价和+3价是Fe、Co、Ni等元素常见化合价.NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO__ FeO(选填“<”“>”“=”);某种天然NiO晶体存在如图所示缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代.其结果晶体仍呈电中性.某氧化镍样品组成为Ni0.97O.该晶体中Ni3+与Ni2+的离子数之比为__ 。
(1)铁、钴、镍都是很好的配位化合物形成体.
①[Co(H2O)6]2+在过量氨水中易转化为[Co(NH3)6]2+。写出Co2+的价层电子排布图
②铁、镍易与一氧化碳作用形成羰基配合物,如:Fe(CO)5,Ni(CO)4等.CO与N2属于等电子体,则CO分子中σ键和π键数目比为
(2)+2价和+3价是Fe、Co、Ni等元素常见化合价.NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO

更新时间:2019-07-11 13:17:36
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】I.铬、镍等过渡元素的单质、化合物在工业上有广泛的应用。
(1)基态镍原子核外共有_____ 种不同的能量的电子,3d能级上的未成对电子数为_____ 。
(2)Cu和Cr位于同一周期。
①向CuSO4溶液中逐滴加入氨水,可得深蓝色晶体[Cu(NH3)4]SO4•H2O,其中心离子是_____ (填元素符号),配体是_____ 。
②Cr元素所在周期中原子电负性最大的是_____ (不考虑零族元素)。
(3)过渡金属单质及其化合物是有机合成反应的重要催化剂。
例如: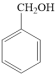 (苯甲醇)
(苯甲醇)
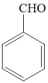 (苯甲醛)。
(苯甲醛)。
①苯甲醇分子中的碳原子的杂化类型是_____ 。
②苯甲醇、苯甲醛的沸点依次为206℃、179℃,造成二者沸点差异的主要原因是_____ 。
II.回答下列问题:
(4)向盛有硫酸铜溶液的试管中滴加氨水,先生成难溶物,继续滴加氨水,难溶物溶解,得到深蓝色透明溶液。下列对此现象的说法正确的是_____ 。
(5)向氯化铜溶液中加入过量浓氨水,然后加入适量乙醇,溶液中析出深蓝色的[Cu(NH3)4]Cl2晶体,深蓝色晶体中含有的化学键除普通的共价键外,还有_____ 。
(1)基态镍原子核外共有
(2)Cu和Cr位于同一周期。
①向CuSO4溶液中逐滴加入氨水,可得深蓝色晶体[Cu(NH3)4]SO4•H2O,其中心离子是
②Cr元素所在周期中原子电负性最大的是
(3)过渡金属单质及其化合物是有机合成反应的重要催化剂。
例如:
 (苯甲醇)
(苯甲醇)
 (苯甲醛)。
(苯甲醛)。①苯甲醇分子中的碳原子的杂化类型是
②苯甲醇、苯甲醛的沸点依次为206℃、179℃,造成二者沸点差异的主要原因是
II.回答下列问题:
(4)向盛有硫酸铜溶液的试管中滴加氨水,先生成难溶物,继续滴加氨水,难溶物溶解,得到深蓝色透明溶液。下列对此现象的说法正确的是
| A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 |
| B.沉淀溶解后,生成深蓝色的配离子[Cu(NH3)4]2+ |
| C.[Cu(NH3)4]2+的立体结构为正四面体形 |
| D.在[Cu(NH3)4]2+配离子中,Cu2+给出孤电子对,NH3提供空轨道 |
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】铜是人类最早发现并广泛使用的一种金属。黄铜矿是主要的炼铜原料,CuFeS2是其中铜的主要存在形式。回答下列问题:
(1)Cu的价电子排布式为___________ ,CuFeS2中三种元素的电负性从大到小的顺序为___________ (用元素符号表示)。
(2)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
①X分子的立体构型是___________ ,中心原子杂化类型为___________ 。
②X的沸点比水的沸点低,主要原因是___________ 。
(3)血红素是铁卟啉化合物,是血红蛋白的组成部分,其结构如图所示,该化合物中的化学键有___________ (填标号)
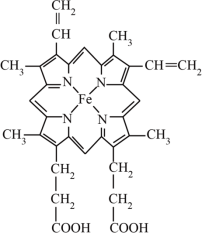
A.范德华力 B. 键 C.
键 C. 键 D.氢键 E.配位键
键 D.氢键 E.配位键
(4)某镍白铜合金的立方晶胞结构如图所示:
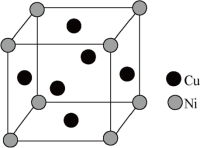
①晶胞中铜原子与镍原子的数目之比为___________ 。
②若该合金的晶胞边长为a nm,则该合金的密度为___________ g·cm-3(设NA为阿伏加德罗常数的值)
(1)Cu的价电子排布式为
(2)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
①X分子的立体构型是
②X的沸点比水的沸点低,主要原因是
(3)血红素是铁卟啉化合物,是血红蛋白的组成部分,其结构如图所示,该化合物中的化学键有

A.范德华力 B.
 键 C.
键 C. 键 D.氢键 E.配位键
键 D.氢键 E.配位键(4)某镍白铜合金的立方晶胞结构如图所示:

①晶胞中铜原子与镍原子的数目之比为
②若该合金的晶胞边长为a nm,则该合金的密度为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】微量元素硼对植物生长及人体健康有着十分重要的作用,也广泛应用于新型材料的制备。
(1)基态硼原子的价电子轨道表达式是________ 。与硼处于同周期且相邻的两种元素和硼的第一电离能由大到小的顺序为______ 。
(2)晶体硼单质的基本结构单元为正二十面体,其能自发地呈现多面体外形,这种性质称为晶体的____ 。
(3)B的简单氢化物BH3不能游离存在,常倾向于形成较稳定的B2H6或与其他分子结合。

①B2H6分子结构如图,则B原子的杂化方式为__________
②氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是__________ ,写出一种与氨硼烷互为等电子体的分子_________ (填化学式)。
(4)以硼酸(H3BO3)为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂。BH4-的立体构型为__________________ 。
(5)磷化硼(BP)是受高度关注的耐磨材料,可作为金属表面的保护层,其结构与金刚石类似,晶胞结构如图所示。

磷化硼晶胞沿z轴在平面的投影图中,B原子构成的几何形状是__________________ 。
(1)基态硼原子的价电子轨道表达式是
(2)晶体硼单质的基本结构单元为正二十面体,其能自发地呈现多面体外形,这种性质称为晶体的
(3)B的简单氢化物BH3不能游离存在,常倾向于形成较稳定的B2H6或与其他分子结合。

①B2H6分子结构如图,则B原子的杂化方式为
②氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是
(4)以硼酸(H3BO3)为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂。BH4-的立体构型为
(5)磷化硼(BP)是受高度关注的耐磨材料,可作为金属表面的保护层,其结构与金刚石类似,晶胞结构如图所示。

磷化硼晶胞沿z轴在平面的投影图中,B原子构成的几何形状是
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】氮及其化合物与人类生产、生活息息相关.回答下列问题:
(1)基态N原子中电子在2p轨道上的排布遵循的原则是__________ ,前4周期元素中,基态原子核外电子排布成单电子数最多的元素的价层电子排布式为__________ 。
(2)C、N、O三种元素第一电离能从大到小的顺序是__________ 。
(3)N2F2分子中N原子的杂化方式是__________ ,l mol N2F2含有__________ molσ键.
(4)NF3的键角__________ NH3的键角(填“<”“>”或“=”),原因是__________ .
(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一.l mol NH4BF4__________ mol配位键.
(6)安全气囊的设计原理为6NaN3+FeIO3 Na2O+2Fe+9N2↑
Na2O+2Fe+9N2↑
①等电子体的原理是:原子总数相同,价电子总数相同的分子或离子具有相似的化学键特征,具有许多相近的性质.写出两种与N3-互为等电子体的分子或离子__________ .
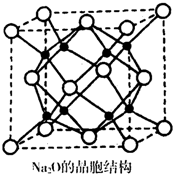
②Na2O的晶胞结构如图所示,晶胞边长为566pm,晶胞中氧原子的配位数为__________ ,Na2O晶体的密度为__________ g•cm-3(只要求列算式,不必计算出结果)。
(1)基态N原子中电子在2p轨道上的排布遵循的原则是
(2)C、N、O三种元素第一电离能从大到小的顺序是
(3)N2F2分子中N原子的杂化方式是
(4)NF3的键角
(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一.l mol NH4BF4
(6)安全气囊的设计原理为6NaN3+FeIO3
 Na2O+2Fe+9N2↑
Na2O+2Fe+9N2↑①等电子体的原理是:原子总数相同,价电子总数相同的分子或离子具有相似的化学键特征,具有许多相近的性质.写出两种与N3-互为等电子体的分子或离子
②Na2O的晶胞结构如图所示,晶胞边长为566pm,晶胞中氧原子的配位数为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】硼普遍存在于蔬果中,是维持骨的健康和钙、磷、镁正常代谢所需要的微量元素之一。回答下列问题:
(1)硼原子核外电子占据最高能层的符号是__________ ,占据最高能级的电子云轮廓图形状为___________ 。价层电子的轨道表达式(电子排布图)为____________ 。
(2)硼原子的第二电高能(I2) 和第三电离能(I3)的大小关系为:I2______ I3(填“>”或“<”),原因是____________ 。
(3)BF3可用于制造火箭的高能燃料。其分子构型为___________ ,已知BF3分子中F原子和B原子采用同种杂化方式为____________ ,BF3分子还中存在大π键,可用符号 表示(其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,如苯分子中的大π键可表示为
表示(其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,如苯分子中的大π键可表示为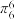 ),则分子中的大π键应表示为
),则分子中的大π键应表示为____________ 。
(4)硼酸(H3BO3)晶体为层状结构。其中一层的结构片段如图(a)所示,将这些H3BO3分子聚集在一起的作用为____________ 。
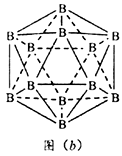
(5) 晶体拥有多种变体,但其基本结构单元都是由硼原子组成的正二十面体,如图(b),每个顶点为个硼原子,构成的三角形均为等边三角形,若该结构单元中有10个原子为10B (其余为11B),那么该结构单元有_________ 种不同类型。
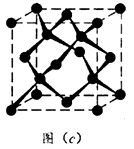
(6)立方氮化硼(BN) 晶体与金刚石晶体互为等电子体,图 (c) 为金刚石晶体的晶胞,立方氮化硼晶体可以取出多种晶胞。其中一种晶胞中N 全部位于晶胞体内,则B处于____________ 位置。

(1)硼原子核外电子占据最高能层的符号是
(2)硼原子的第二电高能(I2) 和第三电离能(I3)的大小关系为:I2
(3)BF3可用于制造火箭的高能燃料。其分子构型为
 表示(其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,如苯分子中的大π键可表示为
表示(其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,如苯分子中的大π键可表示为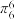 ),则分子中的大π键应表示为
),则分子中的大π键应表示为(4)硼酸(H3BO3)晶体为层状结构。其中一层的结构片段如图(a)所示,将这些H3BO3分子聚集在一起的作用为
(5) 晶体拥有多种变体,但其基本结构单元都是由硼原子组成的正二十面体,如图(b),每个顶点为个硼原子,构成的三角形均为等边三角形,若该结构单元中有10个原子为10B (其余为11B),那么该结构单元有
(6)立方氮化硼(BN) 晶体与金刚石晶体互为等电子体,图 (c) 为金刚石晶体的晶胞,立方氮化硼晶体可以取出多种晶胞。其中一种晶胞中N 全部位于晶胞体内,则B处于



您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】五种元素A、B、C、D、E,其中A元素形成的原子核内只有一个质子;B的基态原子s能级的总电子数比p能级的总电子数多1;C元素的原子最外层电子数是次外层的3倍;D在B的下一周期,在同周期元素中,D形成的简单离子半径最小;E是形成化合物种类最多的元素。
(1)A、E形成的化合物E2A4分子中σ键和π键数目之比为_______ ,B、C、E三种元素的第一电离能由大到小的顺序为_______ 。
(2)与PH3相比,BA3易液化的主要原因是_______ 。
(3)BC 离子的立体构型为
离子的立体构型为_______ ,BC 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为_______ 。
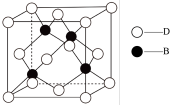
(4)化合物DB是人工合成的半导体材料,它的晶胞结构如图所示,其中最近两个D原子的核间距为a cm。该晶体的密度为_______ g·cm-3 (NA表示阿伏加德罗常数的值)。
(1)A、E形成的化合物E2A4分子中σ键和π键数目之比为
(2)与PH3相比,BA3易液化的主要原因是
(3)BC
 离子的立体构型为
离子的立体构型为 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为(4)化合物DB是人工合成的半导体材料,它的晶胞结构如图所示,其中最近两个D原子的核间距为a cm。该晶体的密度为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】I、吡啶(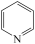 )是类似于苯的芳香化合物,工业上用作合成药品、消毒剂、染料等的原料。2-乙烯基吡啶(VPy)是合成治疗矽肺病药物的原料,可由如图路线合成。
)是类似于苯的芳香化合物,工业上用作合成药品、消毒剂、染料等的原料。2-乙烯基吡啶(VPy)是合成治疗矽肺病药物的原料,可由如图路线合成。
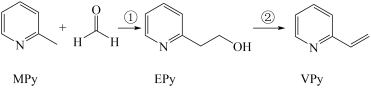
请回答下列问题:
(1)MPy分子中碳原子的杂化方式为_______
(2)EPy晶体中微粒间的作用力类型有_______ (填标号)。
a.离子键b.金属键c.极性键d.非极性键e.配位键f.氢键
(3)反应①中每生成1molEPy,断裂_______ 个π键,形成_______ 个σ键。
(4)吡啶、 与
与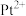 形成二氯二吡啶合铂配合物,有顺式和反式两种同分异构体。科学研究表明,顺式分子具有抗癌活性。
形成二氯二吡啶合铂配合物,有顺式和反式两种同分异构体。科学研究表明,顺式分子具有抗癌活性。
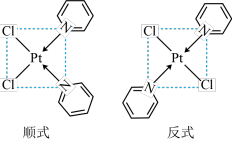
 的配位数为
的配位数为_______ 。顺式二氯二吡啶合铂分子能否溶于水_______ (填“能”或“否”),
Ⅱ、有下列实验:
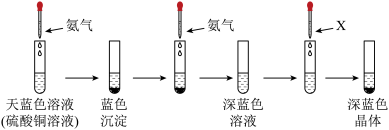
(5)该深蓝色晶体的化学式为_______ ,溶剂X可以是_______ (填名称),继续添加氨水,沉淀溶解,写出沉淀溶解的离子方程式为_______ 。
(6)该实验能说明 、
、 与
与 结合能力的强到弱的顺序是
结合能力的强到弱的顺序是_______ 。
(7)下列有关化学实验“操作→现象→解释”均正确的是_______ 。
 )是类似于苯的芳香化合物,工业上用作合成药品、消毒剂、染料等的原料。2-乙烯基吡啶(VPy)是合成治疗矽肺病药物的原料,可由如图路线合成。
)是类似于苯的芳香化合物,工业上用作合成药品、消毒剂、染料等的原料。2-乙烯基吡啶(VPy)是合成治疗矽肺病药物的原料,可由如图路线合成。
请回答下列问题:
(1)MPy分子中碳原子的杂化方式为
(2)EPy晶体中微粒间的作用力类型有
a.离子键b.金属键c.极性键d.非极性键e.配位键f.氢键
(3)反应①中每生成1molEPy,断裂
(4)吡啶、
 与
与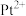 形成二氯二吡啶合铂配合物,有顺式和反式两种同分异构体。科学研究表明,顺式分子具有抗癌活性。
形成二氯二吡啶合铂配合物,有顺式和反式两种同分异构体。科学研究表明,顺式分子具有抗癌活性。
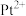 的配位数为
的配位数为Ⅱ、有下列实验:

(5)该深蓝色晶体的化学式为
(6)该实验能说明
 、
、 与
与 结合能力的强到弱的顺序是
结合能力的强到弱的顺序是(7)下列有关化学实验“操作→现象→解释”均正确的是
| 选项 | 操作 | 现象 | 解释 |
| A | 向某溶液中滴加KSCN溶液 | 产生红色沉淀 | 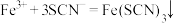 |
| B | 向由0.1molCrCl3·6H2O配成的溶液加入足量AgNO3溶液 | 产生0.2mol沉淀 | 已知 的配位数为6.则CrCl3·6H2O的化学式可表示为 的配位数为6.则CrCl3·6H2O的化学式可表示为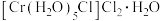 |
| C | 向K2Cr2O7溶液中先滴加3滴浓硫酸,再改加l0滴浓NaOH | 溶液先橙色加深,后变为黄色 | 溶液中存在: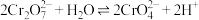 |
| D | 向AgCl悬浊液中滴加氨水 | 沉淀溶解 | AgCl不溶于水,但溶于氨水,重新电离成Ag+和Cl- |
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】氨基吡啶与铜等金属离子所形成的配合物具备良好的磁学性质和结构的多样性,特别是在存在桥基配体的铜配合物。同时给多个中心原子配位的配体称为桥基配体。
(1)基态氮原子的价层电子轨道表示式为___________ ,在元素周期表中铜属于___________ 区(填 “s”、“p”、“d” 或“ds”)。
(2)C、N、O的第一电离能由大到小的顺序为___________ 。
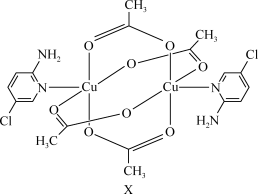
(3)某氨基吡啶衍生物铜配合物X的结构简式如图所示。X中Cu2+的配位数是___________ ,C原子的杂化轨道类型为___________ 。在高温下,Cu2O比CuO稳定,从离子的电子层结构角度分析,主要原因是___________ 。
(4)胆矾的简单平面结构式如图所示。
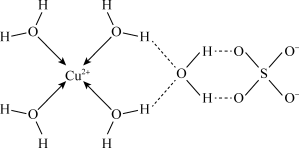
胆矾的化学式用配合物的形式可表示为___________ ;其阴离子的空间结构为___________ ;胆矾中存在的化学键有___________ (填字母)。
A.离子键 B.共价键 C.范德华力 D.氢键 E.配位键
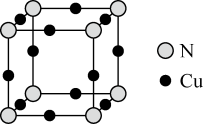
(5)某铜的氮化物广泛应用于光信息存储和高速集成电路领域,其晶胞结构如图所示, 晶胞参数为a pm。该晶体中,与Cu原子最近的Cu原子有___________ 个,若阿伏加德罗常数的值为NA,则该晶体的密度为___________ g·cm-3(列出计算式)。
(1)基态氮原子的价层电子轨道表示式为
(2)C、N、O的第一电离能由大到小的顺序为
(3)某氨基吡啶衍生物铜配合物X的结构简式如图所示。X中Cu2+的配位数是

(4)胆矾的简单平面结构式如图所示。

胆矾的化学式用配合物的形式可表示为
A.离子键 B.共价键 C.范德华力 D.氢键 E.配位键
(5)某铜的氮化物广泛应用于光信息存储和高速集成电路领域,其晶胞结构如图所示, 晶胞参数为a pm。该晶体中,与Cu原子最近的Cu原子有

您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】四种常见元素的性质或结构信息如下表。试根据信息回答有关问题。
(1)写出B原子的电子排布式__________
(2)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,可生成的配合物的化学式为__________ ,简要描述该配合物中化学键的成键情况:__________
(3)“。”表示氢原子,小黑点“·”表示没有形成共价键的最外层电子,短线表示共价键。
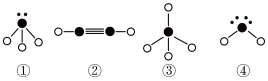
则在以上分子中,中心原子采用sp3杂化形成化学键的是__________ (填序号);在②的分子中有__________ 个σ键和__________ 个π键
(4)硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如下图所示:
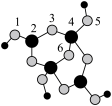
在Xm-中,硼原子轨道的杂化类型有__________ ;配位键存在于__________ 原子之间(填原子的数字标号);m=__________ (填数字)
(5)Co(NH3)5BrSO4可形成两种钴的配合物,已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物的溶液中加BaCl2溶液时,产生白色沉淀;在第二种配合物溶液中加入BaCl2溶液时,则无明显现象,则第一种配合物的化学式为__________ ,第二种配合物的化学式为_________ .
| 元素 | A | B | C | D |
| 性质结构信息 | 原子核外有两个电子层,最外层有3个未成对的电子 | 原子的M层有1对成对的p电子 | 原子核外电子排布为[Ar]3d104sx,有+1、+2两种常见化合价 | 有两种常见氧化物,其中有一种是冶金工业常用的还原剂 |
(2)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,可生成的配合物的化学式为
(3)“。”表示氢原子,小黑点“·”表示没有形成共价键的最外层电子,短线表示共价键。

则在以上分子中,中心原子采用sp3杂化形成化学键的是
(4)硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如下图所示:

在Xm-中,硼原子轨道的杂化类型有
(5)Co(NH3)5BrSO4可形成两种钴的配合物,已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物的溶液中加BaCl2溶液时,产生白色沉淀;在第二种配合物溶液中加入BaCl2溶液时,则无明显现象,则第一种配合物的化学式为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】亚铁氰化钾(K4[Fe(CN)6])双称黄血盐,是一种重要的化工原料。检验三价铁发生的反应为:K4[Fe(CN)6]+FeCl3=KFe[Fe(CN)6]↓(滕氏蓝) +3KCl,回答问题:
(1)写出基态Fe3+的核外电子排布式_________ 。
(2)K4[Fe(CN)6]中的作用力除共价键外,还有______ 和________ 。含有12mol σ键的K4[Fe(CN)6的物质的量为________ mol。
(3)黄血盐中N原子的杂化方式为______ ;C、N、O的第一电离能由大到小的排序为_____ ,电负性由大到小的排序为________ 。
(4)Fe、Na、K的晶体结构如图所示:
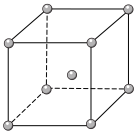
① 钠的熔点比钾更高,原因是__________________________ 。
② Fe原子半径是r cm,阿伏加 德罗常数为NA,铁的相对原子质量为a,则铁单质的密度是_______ g/cm3。
(1)写出基态Fe3+的核外电子排布式
(2)K4[Fe(CN)6]中的作用力除共价键外,还有
(3)黄血盐中N原子的杂化方式为
(4)Fe、Na、K的晶体结构如图所示:

① 钠的熔点比钾更高,原因是
② Fe原子半径是r cm,阿伏加 德罗常数为NA,铁的相对原子质量为a,则铁单质的密度是
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】MnO2、PbSO4、ZnO、少量锰铅氧化物Pb2Mn8O16和Ag是冶锌过程中产生的废渣,利用废渣回收金属元素锌、锰、铅和银的工艺如图所示。回答下列问题:

已知:在较高温度及酸性催化条件下,葡萄糖能发生如图所示的反应:

(1)滤液1的主要成分是_____ 。
(2)已知 Pb2Mn8O16中Pb为+2价,Mn为+4价和+2价,则氧化物中+4价和+2价Mn的个数比为________ 。
(3)“还原酸浸”过程中主要的化学方程式为_____ 。
(4)实际锰浸出最适宜的葡萄糖加入量远大于理论加入量,其原因是_____ ,为提高葡萄糖的有效利用率,可采取的措施为_____ (写两点)。
(5)加入Na2CO3溶液的主要目的是_____ (用离子方程式表示),Na2CO3溶液的最小浓度为_____ mol/L(保留两位小数)。[已知:20℃时Ksp(PbSO4)=1.6×10-8,Ksp(PbCO3)=7.4×10-14,1.262≈1.6]
(6)(CH3NH3)PbI3晶胞结构如图所示,其中A代表Pb2+。
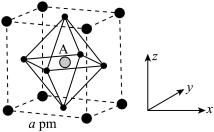
①已知(CH3NH3)PbI3的摩尔质量为Mg/mol,该晶胞的密度为bg•cm-3(设NA为阿伏加德罗常数的值),则晶胞参数a=_____ pm。
②该晶胞沿体对角线方向的投影图为_____ (填序号)。
A. B.
B. 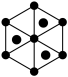 C.
C.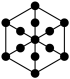 D.
D.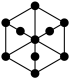

已知:在较高温度及酸性催化条件下,葡萄糖能发生如图所示的反应:

(1)滤液1的主要成分是
(2)已知 Pb2Mn8O16中Pb为+2价,Mn为+4价和+2价,则氧化物中+4价和+2价Mn的个数比为
(3)“还原酸浸”过程中主要的化学方程式为
(4)实际锰浸出最适宜的葡萄糖加入量远大于理论加入量,其原因是
(5)加入Na2CO3溶液的主要目的是
(6)(CH3NH3)PbI3晶胞结构如图所示,其中A代表Pb2+。

①已知(CH3NH3)PbI3的摩尔质量为Mg/mol,该晶胞的密度为bg•cm-3(设NA为阿伏加德罗常数的值),则晶胞参数a=
②该晶胞沿体对角线方向的投影图为
A.
 B.
B.  C.
C. D.
D.
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】铬是不锈钢的合金元素之一,目前被广泛应用于冶金、化工等领域。
(1)基态Cr原子价层电子的电子排布式为_______ 。
(2)金属铬的第二电离能(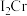 )和锰的第二电离能(
)和锰的第二电离能(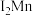 )分别为1590.6kJ/mol、1509.0kJ/mol,
)分别为1590.6kJ/mol、1509.0kJ/mol,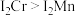 的原因是
的原因是_______ 。
(3) 的熔点(83℃)比
的熔点(83℃)比 的熔点(1100℃)低得多,这是因为
的熔点(1100℃)低得多,这是因为_______ 。
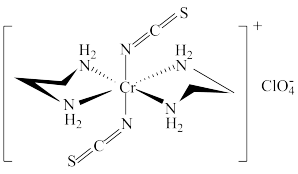
(4)Cr的一种配合物结构如图所示,该配合物阳离子中Cr的配位数为_______ ,阴离子 的空间构型为
的空间构型为_______ 。
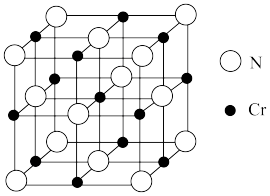
(5)氮化铬晶体的晶胞结构如图所示,若N与Cr核间距离为a pm( ),则氮化铬的密度为
),则氮化铬的密度为_______ g·cm-3。
(1)基态Cr原子价层电子的电子排布式为
(2)金属铬的第二电离能(
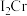 )和锰的第二电离能(
)和锰的第二电离能(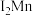 )分别为1590.6kJ/mol、1509.0kJ/mol,
)分别为1590.6kJ/mol、1509.0kJ/mol,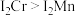 的原因是
的原因是(3)
 的熔点(83℃)比
的熔点(83℃)比 的熔点(1100℃)低得多,这是因为
的熔点(1100℃)低得多,这是因为(4)Cr的一种配合物结构如图所示,该配合物阳离子中Cr的配位数为
 的空间构型为
的空间构型为
(5)氮化铬晶体的晶胞结构如图所示,若N与Cr核间距离为a pm(
 ),则氮化铬的密度为
),则氮化铬的密度为
您最近半年使用:0次



