2018年6月27日,国务院发布《打赢蓝天保卫战三年行动计划》,该计划是中国政府部署的一项污染防治行动计划,旨在持续改善空气质量,为群众留住更多蓝天。对废气的进行必要的处理,让空气更加清洁是环境科学的重要课题。
(1)已知:N2(g)+O2(g)=2NO(g) △H1=+180.5kJ/mol
C (s)+O2(g)=CO2(g) △H2=-393.5kJ/mol
2C (s)+O2(g)=2CO(g) △H3=-221.0kJ/mol
若某反应的平衡常数表达式为 ,请写出此反应的热化学方程式
,请写出此反应的热化学方程式_________________ 。
(2)用如图所示的电解装置可将雾霾中的NO、SO2分别转化为NH 和SO
和SO
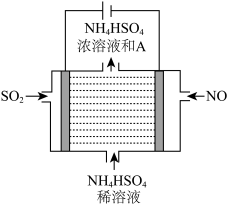
①写出物质A的化学式____________ 。
②NO在电极上发生的反应为_________________ 。
SO2在电极上发生的反应为__________________ 。
(3)工业上常用氨水吸收SO2,可生成NH4HSO3和(NH4)2SO3。
①某同学测得氨水吸收SO2所得溶液中NH4HSO3和(NH4)2SO3的物质的量之比恰好为2:1,写出该吸收过程的总反应方程式______________________________________ 。
②已知常温下H2S的电离常数Ka1=1.3×10-7,Ka2=7.1×10-15,将等物质的量浓度的NaHS与Na2S溶液等体积混合,所得溶液中离子浓度大小顺序为__________________ 。(用物质的量浓度符号由大到小排列)
(1)已知:N2(g)+O2(g)=2NO(g) △H1=+180.5kJ/mol
C (s)+O2(g)=CO2(g) △H2=-393.5kJ/mol
2C (s)+O2(g)=2CO(g) △H3=-221.0kJ/mol
若某反应的平衡常数表达式为
 ,请写出此反应的热化学方程式
,请写出此反应的热化学方程式(2)用如图所示的电解装置可将雾霾中的NO、SO2分别转化为NH
 和SO
和SO

①写出物质A的化学式
②NO在电极上发生的反应为
SO2在电极上发生的反应为
(3)工业上常用氨水吸收SO2,可生成NH4HSO3和(NH4)2SO3。
①某同学测得氨水吸收SO2所得溶液中NH4HSO3和(NH4)2SO3的物质的量之比恰好为2:1,写出该吸收过程的总反应方程式
②已知常温下H2S的电离常数Ka1=1.3×10-7,Ka2=7.1×10-15,将等物质的量浓度的NaHS与Na2S溶液等体积混合,所得溶液中离子浓度大小顺序为
更新时间:2019-07-03 15:59:09
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】废水中氨态氮以NH3·H2O、NH3和NH4+的形式存在,废水脱氮已成为主要污染物减排和水体富营养化防治的研究热点。
Ⅰ.沉淀法
向废水中投入MgCl2和Na2HPO4,生成MgNH4PO4·6H2O沉淀,可将氨态氮含量降至10mg·L−1以下。
(1)NH3的电子式:______ 。
(2)废水中的NH3·H2O转化为MgNH4PO4·6H2O的离子方程式是______ 。
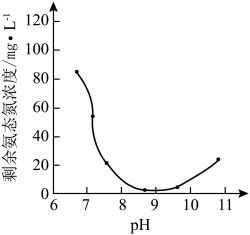
(3)16℃时,向废水中加入MgCl2和Na2HPO4,使镁、氮、磷物质的量之比为1︰1︰1,沉淀过程中的pH对剩余氨态氮浓度的影响如图。欲使剩余氨态氮浓度低于10mg·L−1,pH的适宜范围是______ ,pH偏大或者偏小均不利于MgNH4PO4·6H2O的生成,原因是______ 。
Ⅱ.微波−氧化法
(4)仅对废水进行微波加热,pH对氨态氮脱出的影响如下表。
表中数据表明:pH增大有利于废水中化学平衡______ (用化学用语表示)的移动。
(5)微波协同CuO和H2O2除去氨态氮
①其他条件相同,取相同体积的同一废水样品,微波10 min,剩余氨态氮浓度与一定浓度H2O2溶液添加量的关系如下图。据图推测CuO在氨态氮脱除中可能起催化作用,理由是______ 。
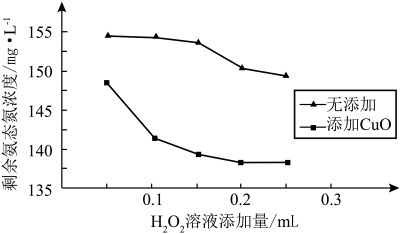
②微波协同CuO有利于H2O2除去氨态氮。该条件下,H2O2将NH3氧化为N2的化学方程式是______ 。
Ⅰ.沉淀法
向废水中投入MgCl2和Na2HPO4,生成MgNH4PO4·6H2O沉淀,可将氨态氮含量降至10mg·L−1以下。
(1)NH3的电子式:
(2)废水中的NH3·H2O转化为MgNH4PO4·6H2O的离子方程式是

(3)16℃时,向废水中加入MgCl2和Na2HPO4,使镁、氮、磷物质的量之比为1︰1︰1,沉淀过程中的pH对剩余氨态氮浓度的影响如图。欲使剩余氨态氮浓度低于10mg·L−1,pH的适宜范围是
Ⅱ.微波−氧化法
(4)仅对废水进行微波加热,pH对氨态氮脱出的影响如下表。
| 溶液pH | 6~7 | 8~9 | 10~11 | 11~12 |
| 剩余氨态氮浓度(mg·L−1) | 156 | 100 | 40 | 14 |
(5)微波协同CuO和H2O2除去氨态氮
①其他条件相同,取相同体积的同一废水样品,微波10 min,剩余氨态氮浓度与一定浓度H2O2溶液添加量的关系如下图。据图推测CuO在氨态氮脱除中可能起催化作用,理由是

②微波协同CuO有利于H2O2除去氨态氮。该条件下,H2O2将NH3氧化为N2的化学方程式是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】碱式硫酸铝溶液可用于烟气脱硫。室温下向一定浓度的硫酸铝溶液中加入一定量的碳酸钙粉末,反应后经过滤得到碱式硫酸铝溶液,反应方程式为(2−x)Al2(SO4)3+3xCaCO3+3xH2O=2[(1−x)Al2(SO4)3·xAl(OH)3]+3xCaSO4↓+3xCO2↑,生成物(1−x)Al2(SO4)3·xAl(OH)3中x值的大小影响碱式硫酸铝溶液的脱硫效率。
(1)制备碱式硫酸铝溶液时,维持反应温度和反应时间不变,提高x值的方法有___________________ 。
(2)碱式硫酸铝溶液吸收SO2过程中,溶液的pH___________ (填“增大”、“减小”、“不变”)。
(3)通过测定碱式硫酸铝溶液中相关离子的浓度确定x的值,测定方法如下:
①取碱式硫酸铝溶液25.00 mL,加入盐酸酸化的过量BaCl2溶液充分反应,静置后过滤、洗涤,干燥至恒重,得固体2.3300g。
②取碱式硫酸铝溶液2.50 mL,稀释至25 mL,加入0.1000 mol·L−1EDTA标准溶液25.00 mL,调节溶液pH约为4.2,煮沸,冷却后用0.08000 mol·L−1CuSO4标准溶液滴定过量的EDTA至终点,消耗CuSO4标准溶液20.00 mL(已知Al3+、Cu2+与EDTA反应的化学计量比均为1∶1)。
计算(1−x)Al2(SO4)3·xAl(OH)3中的x值____ (写出计算过程)。
(1)制备碱式硫酸铝溶液时,维持反应温度和反应时间不变,提高x值的方法有
(2)碱式硫酸铝溶液吸收SO2过程中,溶液的pH
(3)通过测定碱式硫酸铝溶液中相关离子的浓度确定x的值,测定方法如下:
①取碱式硫酸铝溶液25.00 mL,加入盐酸酸化的过量BaCl2溶液充分反应,静置后过滤、洗涤,干燥至恒重,得固体2.3300g。
②取碱式硫酸铝溶液2.50 mL,稀释至25 mL,加入0.1000 mol·L−1EDTA标准溶液25.00 mL,调节溶液pH约为4.2,煮沸,冷却后用0.08000 mol·L−1CuSO4标准溶液滴定过量的EDTA至终点,消耗CuSO4标准溶液20.00 mL(已知Al3+、Cu2+与EDTA反应的化学计量比均为1∶1)。
计算(1−x)Al2(SO4)3·xAl(OH)3中的x值
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】工业废水中常含有酚类、重金属、氰类、三氯甲烷及砷类等有害物质,必须处理后才可排放。
(1)处理废水时常需加入混凝剂,如明矾、PAN 等。
①写出明矾中Al3+水解的离子方程式___________ 。
②PAN化学式为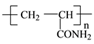 ,其单体的结构简式为
,其单体的结构简式为___________ 。
(2)处理高浓度的含酚废水的方法之一是萃取回收法,其流程如下:
①该流程中涉及分液操作___________ 次(填数字)。
②“操作Z”中发生反应的化学方程式为___________ 。
(3)用FeS除去废水中汞盐的反应为Hg2++FeS HgS + Fe2+,该反应的平衡常数为K=
HgS + Fe2+,该反应的平衡常数为K=____________ [填数值,已知:Ksp(FeS)=6.4×10-15,Ksp(HgS)=1.6×10-52]。
(4)处理含CN-废水有惰性电极电解法、NaClO氧化法等。
已知:HCN的Ka=6.3×10-10,沸点为25.7℃,有剧毒。
①电解前需将废水的pH调至10~11,其目的是___________ 。
②惰性电极电解时,CN-在阳极最终氧化为CO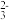 、CO2和N2。则1mol CN-在阳极被完全氧化,同时在阴极上产生H2的物质的量为
、CO2和N2。则1mol CN-在阳极被完全氧化,同时在阴极上产生H2的物质的量为___________ (不考虑副反应)。
③电解后期需在废水中加入食盐继续电解,加食盐除可提高电流效率外,还因为___________ 。
(5)纳米零价铁除去酸性废水中的三氯乙烯、五价砷的原理如下图所示:
纳米零价铁中Fe为负极, C2HCl3在其表面被还原的电极反应式为___________ ;在含高浓度SO 的酸性溶液中脱除砷的化学方程式为
的酸性溶液中脱除砷的化学方程式为___________ 。
(1)处理废水时常需加入混凝剂,如明矾、PAN 等。
①写出明矾中Al3+水解的离子方程式
②PAN化学式为
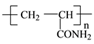 ,其单体的结构简式为
,其单体的结构简式为(2)处理高浓度的含酚废水的方法之一是萃取回收法,其流程如下:
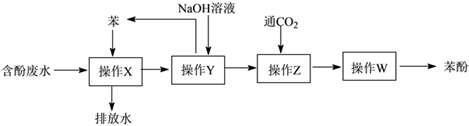
①该流程中涉及分液操作
②“操作Z”中发生反应的化学方程式为
(3)用FeS除去废水中汞盐的反应为Hg2++FeS
 HgS + Fe2+,该反应的平衡常数为K=
HgS + Fe2+,该反应的平衡常数为K=(4)处理含CN-废水有惰性电极电解法、NaClO氧化法等。
已知:HCN的Ka=6.3×10-10,沸点为25.7℃,有剧毒。
①电解前需将废水的pH调至10~11,其目的是
②惰性电极电解时,CN-在阳极最终氧化为CO
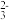 、CO2和N2。则1mol CN-在阳极被完全氧化,同时在阴极上产生H2的物质的量为
、CO2和N2。则1mol CN-在阳极被完全氧化,同时在阴极上产生H2的物质的量为③电解后期需在废水中加入食盐继续电解,加食盐除可提高电流效率外,还因为
(5)纳米零价铁除去酸性废水中的三氯乙烯、五价砷的原理如下图所示:
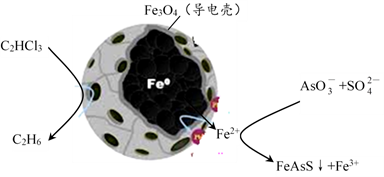
纳米零价铁中Fe为负极, C2HCl3在其表面被还原的电极反应式为
 的酸性溶液中脱除砷的化学方程式为
的酸性溶液中脱除砷的化学方程式为
您最近一年使用:0次
【推荐1】CO2的资源化应用已成为化学领域研究的重要课题,其包括CO2甲烷化、CO2碳酸二甲酯(DMC)化、CO2甲醇化等。回答下列问题:
(1) 甲烷化:其反应原理为
甲烷化:其反应原理为
 ,
,
其相关反应的热化学方程式如下:
i.
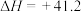 kJ·mol
kJ·mol ;
;
ii.
 kJ·mol
kJ·mol
① 甲烷化反应
甲烷化反应 的
的
___________ kJ·mol-1。
②实际生产中,为提高甲烷化时生产效率,反应适宜在___________ 温(填“低”“高”,下同)、___________ 压条件下进行。
③已知反应i的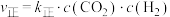 ,
, ,(
,( 、
、 为速率常数),若反应达平衡后升高温度或加入催化剂,则
为速率常数),若反应达平衡后升高温度或加入催化剂,则 值分别
值分别___________ 或___________ 。(填“增大”“不变”或“减小”)。
(2)CO2甲醇化:其原理为 ,一定条件下,在一密闭容器中充入4molCO2和12molH2发生该反应,在0.12MPa和5.0MPa下CO2的平衡转化率随温度的关系如图甲所示。
,一定条件下,在一密闭容器中充入4molCO2和12molH2发生该反应,在0.12MPa和5.0MPa下CO2的平衡转化率随温度的关系如图甲所示。
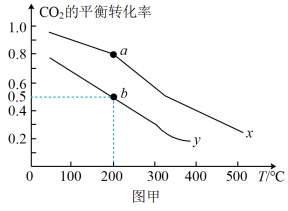
①表示压强为5.0MPa下CO2的平衡转化率随温度的变化曲线为___________ (填“x”或“y”),其理由是___________ 。
②b点对应的平衡常数
___________ MPa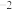 (
( 为以平衡分压代替平衡浓度表示的平衡常数,分压=总压×物质的量分数,保留三位有效数字)。
为以平衡分压代替平衡浓度表示的平衡常数,分压=总压×物质的量分数,保留三位有效数字)。
(3)CO2碳酸二甲酯(DMC)化:其反应历程如图乙所示。

合成DMC的总反应化学方程式为___________ (CH3OH不需标注同位素原子)。
(1)
 甲烷化:其反应原理为
甲烷化:其反应原理为
 ,
,其相关反应的热化学方程式如下:
i.

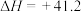 kJ·mol
kJ·mol ;
;ii.

 kJ·mol
kJ·mol
①
 甲烷化反应
甲烷化反应 的
的
②实际生产中,为提高甲烷化时生产效率,反应适宜在
③已知反应i的
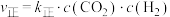 ,
, ,(
,( 、
、 为速率常数),若反应达平衡后升高温度或加入催化剂,则
为速率常数),若反应达平衡后升高温度或加入催化剂,则 值分别
值分别(2)CO2甲醇化:其原理为
 ,一定条件下,在一密闭容器中充入4molCO2和12molH2发生该反应,在0.12MPa和5.0MPa下CO2的平衡转化率随温度的关系如图甲所示。
,一定条件下,在一密闭容器中充入4molCO2和12molH2发生该反应,在0.12MPa和5.0MPa下CO2的平衡转化率随温度的关系如图甲所示。
①表示压强为5.0MPa下CO2的平衡转化率随温度的变化曲线为
②b点对应的平衡常数

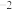 (
( 为以平衡分压代替平衡浓度表示的平衡常数,分压=总压×物质的量分数,保留三位有效数字)。
为以平衡分压代替平衡浓度表示的平衡常数,分压=总压×物质的量分数,保留三位有效数字)。(3)CO2碳酸二甲酯(DMC)化:其反应历程如图乙所示。

合成DMC的总反应化学方程式为
您最近一年使用:0次
【推荐2】碳的很多化合物在生产、生活中有广泛应用,对其进行综合利用是目前研究的热点之一、
已知:I.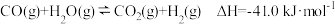 ;
;
II.
III.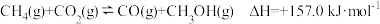 。
。
回答下列问题:
(1)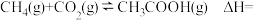
_______
(2)700℃时,将1 mol CO(g)、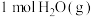 、
、 混合后,充入容积为20 L的刚性密闭容器中(容器容积不变),在适当催化剂条件下发生反应Ⅰ和反应Ⅲ.10 min末达到平衡时测得
混合后,充入容积为20 L的刚性密闭容器中(容器容积不变),在适当催化剂条件下发生反应Ⅰ和反应Ⅲ.10 min末达到平衡时测得 和
和 的体积分数分别为20%、10%。
的体积分数分别为20%、10%。
①0~10min内,反应Ⅰ的平均反应速率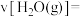
_______ 。
②反应Ⅲ的平衡常数K=_______ 。
③在750℃重复实验,容器内的平衡压强_______ (填“增大”“减小”或“不变”),理由为_______ 。
(3)中科院化学所研究了反应Ⅱ的反应历程,如图所示:
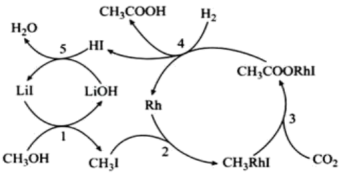
①反应历程中,能降低反应活化能的物质有_______ (填化学式);中间产物有_______ 种。
②第4步反应的化学方程式为_______ 。
已知:I.
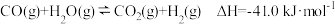 ;
;II.

III.
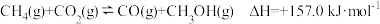 。
。回答下列问题:
(1)
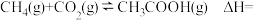
(2)700℃时,将1 mol CO(g)、
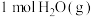 、
、 混合后,充入容积为20 L的刚性密闭容器中(容器容积不变),在适当催化剂条件下发生反应Ⅰ和反应Ⅲ.10 min末达到平衡时测得
混合后,充入容积为20 L的刚性密闭容器中(容器容积不变),在适当催化剂条件下发生反应Ⅰ和反应Ⅲ.10 min末达到平衡时测得 和
和 的体积分数分别为20%、10%。
的体积分数分别为20%、10%。①0~10min内,反应Ⅰ的平均反应速率
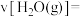
②反应Ⅲ的平衡常数K=
③在750℃重复实验,容器内的平衡压强
(3)中科院化学所研究了反应Ⅱ的反应历程,如图所示:

①反应历程中,能降低反应活化能的物质有
②第4步反应的化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】以 为原料加氢合成二甲醚、甲醇有利于促进实现“碳中和”。在二氧化碳加氢制取二甲醚的合成塔中发生以下3个反应:
为原料加氢合成二甲醚、甲醇有利于促进实现“碳中和”。在二氧化碳加氢制取二甲醚的合成塔中发生以下3个反应:
ⅰ.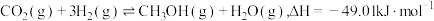
ⅱ.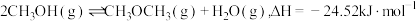
ⅲ.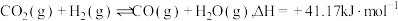
(1) 分子空间构型为
分子空间构型为_____ ,其属于_____ 分子(填“极性”或“非极性”), 分子中,
分子中, 原子杂化轨道类型为
原子杂化轨道类型为_____ ,在基态 原子中,核外存在
原子中,核外存在_____ 对自旋相反的电子。
(2) 的
的
_____  。
。
(3)在压强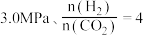 条件下,
条件下, 的平衡转化率、平衡时产物的选择性与温度的关系如图所示(选择性是指生成某物质消耗的
的平衡转化率、平衡时产物的选择性与温度的关系如图所示(选择性是指生成某物质消耗的 占
占 消耗总量的百分比)。
消耗总量的百分比)。
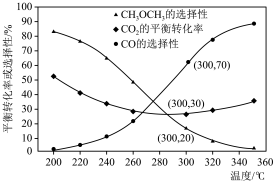
①当温度超过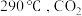 的平衡转化率随温度升高而增大的原因是
的平衡转化率随温度升高而增大的原因是_____ ;除改变温度外,能提高二甲醚选择性的措施有_____ (写一种即可)。
②根据图中的数据计算, 时
时 的平衡物质的量分数为
的平衡物质的量分数为_____ (保留三位有效数字),用气体分压计算反应ⅱ的化学平衡常数 为
为_____ (气体分压=总压×气体物质的量分数)
(4)在 时,只发生反应
时,只发生反应 ,设达到平衡状态时体系中甲醇物质的量分数为
,设达到平衡状态时体系中甲醇物质的量分数为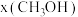 ,在温度
,在温度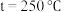 条件下的
条件下的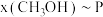 (压强)、在压强
(压强)、在压强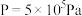 条件下的
条件下的 (温度)如图所示。当
(温度)如图所示。当 的平衡转化率为
的平衡转化率为 时,反应条件可能为
时,反应条件可能为_____ 。
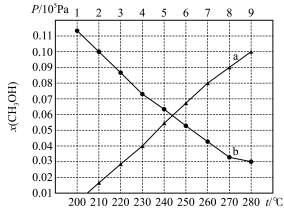
 为原料加氢合成二甲醚、甲醇有利于促进实现“碳中和”。在二氧化碳加氢制取二甲醚的合成塔中发生以下3个反应:
为原料加氢合成二甲醚、甲醇有利于促进实现“碳中和”。在二氧化碳加氢制取二甲醚的合成塔中发生以下3个反应:ⅰ.
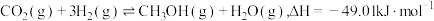
ⅱ.
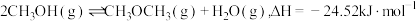
ⅲ.
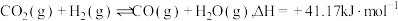
(1)
 分子空间构型为
分子空间构型为 分子中,
分子中, 原子杂化轨道类型为
原子杂化轨道类型为 原子中,核外存在
原子中,核外存在(2)
 的
的
 。
。(3)在压强
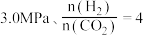 条件下,
条件下, 的平衡转化率、平衡时产物的选择性与温度的关系如图所示(选择性是指生成某物质消耗的
的平衡转化率、平衡时产物的选择性与温度的关系如图所示(选择性是指生成某物质消耗的 占
占 消耗总量的百分比)。
消耗总量的百分比)。
①当温度超过
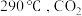 的平衡转化率随温度升高而增大的原因是
的平衡转化率随温度升高而增大的原因是②根据图中的数据计算,
 时
时 的平衡物质的量分数为
的平衡物质的量分数为 为
为(4)在
 时,只发生反应
时,只发生反应 ,设达到平衡状态时体系中甲醇物质的量分数为
,设达到平衡状态时体系中甲醇物质的量分数为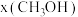 ,在温度
,在温度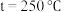 条件下的
条件下的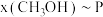 (压强)、在压强
(压强)、在压强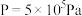 条件下的
条件下的 (温度)如图所示。当
(温度)如图所示。当 的平衡转化率为
的平衡转化率为 时,反应条件可能为
时,反应条件可能为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】甲醇是一种绿色能源,是机动车燃油的最佳替代品。请回答下列有关问题:
(1)用CO可以合成甲醇。已知:
ⅰ.CH3OH(g)+ O2(g)=CO2(g)+2H2O(l) △H=-764.5 kJ•mol-1;
O2(g)=CO2(g)+2H2O(l) △H=-764.5 kJ•mol-1;
ⅱ.CO(g)+ O2(g)=CO2(g) △H=-283.0 kJ•mol-1;
O2(g)=CO2(g) △H=-283.0 kJ•mol-1;
ⅲ.H2(g)+ O2(g)=H2O(g) △H=-285.8 kJ•mol-1;
O2(g)=H2O(g) △H=-285.8 kJ•mol-1;
则 CO(g)+2H2(g) CH3OH(g) △H=
CH3OH(g) △H=________ kJ·mol-1。
(2)利用CO2及H2为原料,在合适的催化剂(如Cu/ZnO催化剂)作用下,也可合成CH3OH,涉及的反应有:
ⅳ.CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-53.7 kJ•mol-1平衡常数 K1;
CH3OH(g)+H2O(g) △H=-53.7 kJ•mol-1平衡常数 K1;
ⅴ.CO2(g)+H2(g) CO(g)+H2O(g)△H=+41.2 kJ•mol-1平衡常数K2。
CO(g)+H2O(g)△H=+41.2 kJ•mol-1平衡常数K2。
下列四组实验,若控制CO2和H2初始投料比均为1∶2.2,经过相同反应时间测得如下实验数据:
①CO(g)+2H2(g) CH3OH(g)的平衡常数K=
CH3OH(g)的平衡常数K=___________ (用含K1、K2的表达式表示)。
②有利于提高CO2转化为CH3OH平衡转化率的措施有_________ 。
a.使用Cu/ZnO纳米棒衬料
b.使用Cu/ZnO纳米片材料
c.降低反应温度
d.保持投料比不变,增加反应物的浓度
e.增大CO2和H2的初始投料比
③由表格中的数据可知,相同温度下不同的催化剂对CO2的转化率不同,造成该结果的原因是_________________________________________ 。
(3)甲醇燃料电池是目前技术最成熟,应用最广泛的一种燃料电池,其工作原理如下图所示:
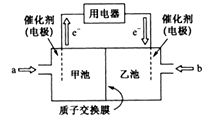
①a气体的名称是_________ 。
②甲池所在电极为原电池的______ 极,其电极反应式为__________________________ 。
③电解液中,H+的移动方向为_____________ 。
(1)用CO可以合成甲醇。已知:
ⅰ.CH3OH(g)+
 O2(g)=CO2(g)+2H2O(l) △H=-764.5 kJ•mol-1;
O2(g)=CO2(g)+2H2O(l) △H=-764.5 kJ•mol-1;ⅱ.CO(g)+
 O2(g)=CO2(g) △H=-283.0 kJ•mol-1;
O2(g)=CO2(g) △H=-283.0 kJ•mol-1;ⅲ.H2(g)+
 O2(g)=H2O(g) △H=-285.8 kJ•mol-1;
O2(g)=H2O(g) △H=-285.8 kJ•mol-1;则 CO(g)+2H2(g)
 CH3OH(g) △H=
CH3OH(g) △H=(2)利用CO2及H2为原料,在合适的催化剂(如Cu/ZnO催化剂)作用下,也可合成CH3OH,涉及的反应有:
ⅳ.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H=-53.7 kJ•mol-1平衡常数 K1;
CH3OH(g)+H2O(g) △H=-53.7 kJ•mol-1平衡常数 K1;ⅴ.CO2(g)+H2(g)
 CO(g)+H2O(g)△H=+41.2 kJ•mol-1平衡常数K2。
CO(g)+H2O(g)△H=+41.2 kJ•mol-1平衡常数K2。下列四组实验,若控制CO2和H2初始投料比均为1∶2.2,经过相同反应时间测得如下实验数据:
温度(K) | 催化剂 | CO2转化率(%) |
543 | Cu/ZnO纳米棒材料 | 12.3 |
543 | Cu/ZnO纳米片材料 | 10.9 |
553 | Cu/ZnO纳米棒材料 | 15.3 |
553 | Cu/ZnO纳米片材料 | 12.0 |
①CO(g)+2H2(g)
 CH3OH(g)的平衡常数K=
CH3OH(g)的平衡常数K=②有利于提高CO2转化为CH3OH平衡转化率的措施有
a.使用Cu/ZnO纳米棒衬料
b.使用Cu/ZnO纳米片材料
c.降低反应温度
d.保持投料比不变,增加反应物的浓度
e.增大CO2和H2的初始投料比
③由表格中的数据可知,相同温度下不同的催化剂对CO2的转化率不同,造成该结果的原因是
(3)甲醇燃料电池是目前技术最成熟,应用最广泛的一种燃料电池,其工作原理如下图所示:

①a气体的名称是
②甲池所在电极为原电池的
③电解液中,H+的移动方向为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】在80℃时,将0.4 mol的N2O4气体充入2 L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
(1)该反应的化学方程式为___________ ,表中b___________ c(填“>”、“<”或“=”)。
(2)20s时,N2O4的浓度为___________ mol/L,0~20 s内N2O4的平均反应速率为___________ 。
(3)该反应的平衡常数表达式为K=___________ ,在80℃时该反应的平衡常数K为___________ (结果精确到0.01)。
(4)在其他条件相同时,该反应的K值越大,表明建立平衡时___________ (填字母)。
A.N2O4的转化率越高 B.N2O4与NO2的浓度之比越大 C.正反应进行的程度越大
| c/(mol/L) | 时间/s | |||||
| 0 | 20 | 40 | 60 | 80 | 100 | |
| c(N2O4) | 0.20 | a | 0.10 | c | d | e |
| c(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
(2)20s时,N2O4的浓度为
(3)该反应的平衡常数表达式为K=
(4)在其他条件相同时,该反应的K值越大,表明建立平衡时
A.N2O4的转化率越高 B.N2O4与NO2的浓度之比越大 C.正反应进行的程度越大
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】随着低碳钢等洁净钢技术的发展,Al2O3-C耐火材料和钢水之间的相互作用已成为当前的一个研究重点。请回答下列问题:
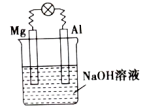
(1)将镁片、铝片平行插入一定浓度的NaOH溶液中,用导线连接成闭合回路,如图所示。写出铝电极的电极反应式:_____ 。
(2)在埋炭实验条件下,不同碳素材料的Al2O3-C耐火材料与铁液之间的可能反应如下:
①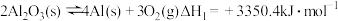
②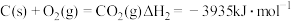
③
④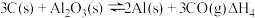 则
则

______  。
。
(3)直接碳热还原氧化铝法除需要高温外,系统中生成的碳化铝、碳氧化铝等会与生成的铝混合在一起,难以分离。实际生产中,至今仍未用直接碳热还原氧化铝法来炼铝。氧化铝碳热还原氯化法炼铝是生产铝的一种可行性新方法,其反应过程如下:
⑤
⑥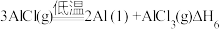
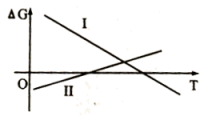
反应⑤、反应⑥中自由能( )与温度(T)的变化关系如图所示,由此判断反应⑤对应图中的曲线
)与温度(T)的变化关系如图所示,由此判断反应⑤对应图中的曲线____ (填“I”或“II”),试分析氧化铝碳热还原氯化法炼铝的可行性:______
(4)在埋炭情况下,碳过剩时,碳的氧化反应主要考虑: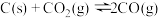 。在实验室研究该反应,一定温度下,向某体积可变的恒压密闭容器(总压强为p总)中加入足量的碳和2 molCO2(g),平衡时体系中气体体积分数与温度的关系如图所示。
。在实验室研究该反应,一定温度下,向某体积可变的恒压密闭容器(总压强为p总)中加入足量的碳和2 molCO2(g),平衡时体系中气体体积分数与温度的关系如图所示。
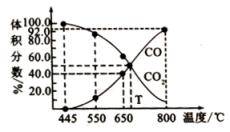
①650℃反应达到平衡时,容器体积为10L,则平衡时c(CO)=___________ 。
②T℃时,若向平衡体系中再充入一定量n(CO):n(CO2)=3:2的混合气体,则平衡___________ (填“向正反应方向”、“向逆反应方向”或“不”)移动。
③800℃时,如图CO的体积分数为92%,用平衡分压代替平衡浓度表示的化学平衡常数Kp=___________ [用含p总的代数式表示,气体分压(p分)=气体总压(p总) 体积分数]。
体积分数]。
(1)将镁片、铝片平行插入一定浓度的NaOH溶液中,用导线连接成闭合回路,如图所示。写出铝电极的电极反应式:

(2)在埋炭实验条件下,不同碳素材料的Al2O3-C耐火材料与铁液之间的可能反应如下:
①
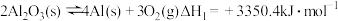
②
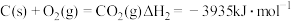
③

④
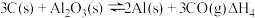 则
则
 。
。(3)直接碳热还原氧化铝法除需要高温外,系统中生成的碳化铝、碳氧化铝等会与生成的铝混合在一起,难以分离。实际生产中,至今仍未用直接碳热还原氧化铝法来炼铝。氧化铝碳热还原氯化法炼铝是生产铝的一种可行性新方法,其反应过程如下:
⑤

⑥
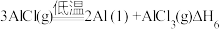
反应⑤、反应⑥中自由能(
 )与温度(T)的变化关系如图所示,由此判断反应⑤对应图中的曲线
)与温度(T)的变化关系如图所示,由此判断反应⑤对应图中的曲线
(4)在埋炭情况下,碳过剩时,碳的氧化反应主要考虑:
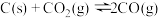 。在实验室研究该反应,一定温度下,向某体积可变的恒压密闭容器(总压强为p总)中加入足量的碳和2 molCO2(g),平衡时体系中气体体积分数与温度的关系如图所示。
。在实验室研究该反应,一定温度下,向某体积可变的恒压密闭容器(总压强为p总)中加入足量的碳和2 molCO2(g),平衡时体系中气体体积分数与温度的关系如图所示。
①650℃反应达到平衡时,容器体积为10L,则平衡时c(CO)=
②T℃时,若向平衡体系中再充入一定量n(CO):n(CO2)=3:2的混合气体,则平衡
③800℃时,如图CO的体积分数为92%,用平衡分压代替平衡浓度表示的化学平衡常数Kp=
 体积分数]。
体积分数]。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】杭州亚运会主火炬的燃料首次使用废碳再生的绿色甲醇,甲醇火炬被称为“零碳”火炬。目前,我国在相关设备及技术方面全球领先。请回答:
(1)二氧化碳催化加氢制甲醇的反应可表示为: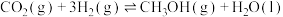 。
。
①已知: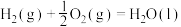
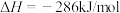


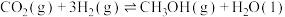
 =
=______ kJ/mol。该反应能自发进行的条件是______ 。
②在恒容条件下能加快二氧化碳催化加氢制甲醇的反应速率,并提高 转化率的措施是
转化率的措施是______ 。
③若二氧化碳催化加氢制甲醇的反应在恒温恒容的密闭容器中进行,能说明反应达到平衡状态的是______ ,(填字母)。
A.容器内压强不随时间变化 B.容器内各物质的浓度相等
C.单位时间消耗1mol ,同时生成3mol
,同时生成3mol D.混合气体的密度不再改变
D.混合气体的密度不再改变
(2)电催化法是制备甲醇的途径之一,原理如图所示。

①室温下, 溶液
溶液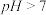 ,
, 水解的离子方程式为
水解的离子方程式为______ 。
② 电极的电极反应式为
电极的电极反应式为______ 。
③与其他有机合成相比,电有机合成的优点是______ 。
(1)二氧化碳催化加氢制甲醇的反应可表示为:
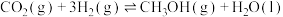 。
。①已知:
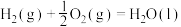
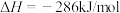


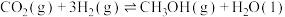
 =
=②在恒容条件下能加快二氧化碳催化加氢制甲醇的反应速率,并提高
 转化率的措施是
转化率的措施是③若二氧化碳催化加氢制甲醇的反应在恒温恒容的密闭容器中进行,能说明反应达到平衡状态的是
A.容器内压强不随时间变化 B.容器内各物质的浓度相等
C.单位时间消耗1mol
 ,同时生成3mol
,同时生成3mol D.混合气体的密度不再改变
D.混合气体的密度不再改变(2)电催化法是制备甲醇的途径之一,原理如图所示。

①室温下,
 溶液
溶液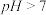 ,
, 水解的离子方程式为
水解的离子方程式为②
 电极的电极反应式为
电极的电极反应式为③与其他有机合成相比,电有机合成的优点是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】化学反应原理在科研和生产中有广泛应用。
(1)工业上制取Ti的步骤之一是:在高温时,将金红石(TiO2)、炭粉混合并通入Cl2先制得TiCl4和一种可燃性气体,已知:
①TiO2(s)+2Cl2(g)═TiCl4(1)+O2(g)△H=﹣410.0kJ•mol﹣1
②CO(g)═C(s)+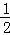 O2(g)△H=+110.5kJ•mol﹣1
O2(g)△H=+110.5kJ•mol﹣1
则上述反应的热化学方程式是______________________________ 。
(2)利用“化学蒸气转移法”制备二硫化钽(TaS2)晶体,发生如下反应:
TaS2(s)+2I2(g)⇌TaI4(g)+S2(g)△H1>0 (Ⅰ);若反应(Ⅰ)的平衡常数K=1,向某恒容且体积为15mL的密闭容器中加入1mol I2(g)和足量TaS2(s),I2(g)的平衡转化率为______________ 。

如图1所示,反应(Ⅰ)在石英真空管中进行,先在温度为T2的一端放入未提纯的TaS2粉末和少量I2(g),一段时间后,在温度为T1的一端得到了纯净TaS2晶体,则温度T1___________ T2(填“>”“<”或“=”);上述反应体系中循环使用的物质是___________ 。
(3)利用H2S废气制取氢气的方法有多种。
①高温热分解法:
已知:H2S(g)═H2(g)+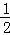 S2(g)△H2;在恒容密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为c mol•L﹣1测定H2S的转化率,结果如图2,图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率,△H2
S2(g)△H2;在恒容密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为c mol•L﹣1测定H2S的转化率,结果如图2,图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率,△H2_________ 0(填>,=或<);说明随温度的升高,曲线b向曲线a逼近的原因:___________________ 。
②电化学法:
该法制氢过程的示意图如3,反应后的溶液进入电解池,电解总反应的离子方程式为____________ 。
(1)工业上制取Ti的步骤之一是:在高温时,将金红石(TiO2)、炭粉混合并通入Cl2先制得TiCl4和一种可燃性气体,已知:
①TiO2(s)+2Cl2(g)═TiCl4(1)+O2(g)△H=﹣410.0kJ•mol﹣1
②CO(g)═C(s)+
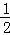 O2(g)△H=+110.5kJ•mol﹣1
O2(g)△H=+110.5kJ•mol﹣1则上述反应的热化学方程式是
(2)利用“化学蒸气转移法”制备二硫化钽(TaS2)晶体,发生如下反应:
TaS2(s)+2I2(g)⇌TaI4(g)+S2(g)△H1>0 (Ⅰ);若反应(Ⅰ)的平衡常数K=1,向某恒容且体积为15mL的密闭容器中加入1mol I2(g)和足量TaS2(s),I2(g)的平衡转化率为

如图1所示,反应(Ⅰ)在石英真空管中进行,先在温度为T2的一端放入未提纯的TaS2粉末和少量I2(g),一段时间后,在温度为T1的一端得到了纯净TaS2晶体,则温度T1
(3)利用H2S废气制取氢气的方法有多种。
①高温热分解法:
已知:H2S(g)═H2(g)+
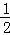 S2(g)△H2;在恒容密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为c mol•L﹣1测定H2S的转化率,结果如图2,图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率,△H2
S2(g)△H2;在恒容密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为c mol•L﹣1测定H2S的转化率,结果如图2,图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率,△H2②电化学法:
该法制氢过程的示意图如3,反应后的溶液进入电解池,电解总反应的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】高铁酸钾作为一种绿色水处理剂,兼具极强的氧化性和良好的絮凝效果,在水处理领域有着巨大的应用前景。制取高铁酸钾的方法主要有次氯酸盐氧化法、电解法、熔融法等。已知:K2FeO4可溶于水。
(1)次氯酸盐氧化法
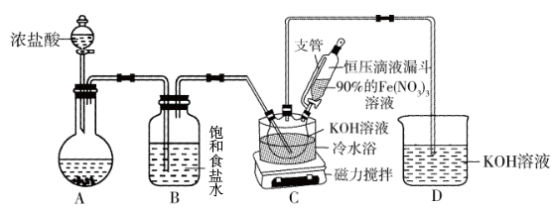
①圆底烧瓶中发生反应的化学方程式为___________ 。
②在0℃条件下,装置C中首先制备KClO,然后在剧烈搅拌下将90%的Fe(NO3)3,分别加入装置C中,充分反应可得K2FeO4溶液,写出该反应的离子方程式___________ 。
③反应后,将三颈烧瓶中溶液冷却结晶,过滤、得到的K2FeO4粗产品,进一步提纯所用方法是___________ 。
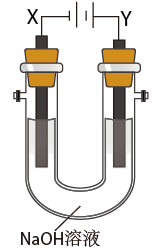
(2)电解法
①电解过程中,Y极放电的电极反应式是___________ 。
②研究电解液浓度、电解温度对高铁酸钾产量的影响(纵坐标为高铁酸钾产率)
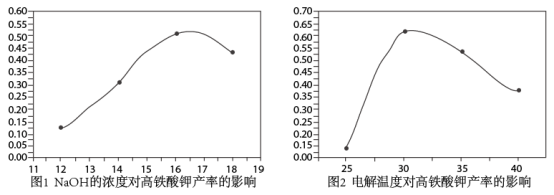
电解法制取高铁酸钾宜选择的NaOH的浓度和温度分别为___________ 。
A.14 mol/L,25℃ B.16 mol/L,30℃
C.14 mol/L,35℃ D.18 mol/L,40℃
③K2FeO4的纯度测定:
已知反应:


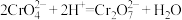
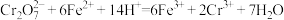
向3 mLCrCl3溶液中加入20 mL饱和KOH溶液,再加入5mL蒸馏水,冷却至室温,准确称取3.96 g样品,加入上述溶液中使其溶解(恰好反应),充分反应,过滤后加入稀硫酸酸化,并加入1 mL苯二胺磺酸钠作指示剂,用2.00 mol/L的标准硫酸亚铁铵(NH4)2Fe(SO4)2溶液滴定,至终点溶液变为绿色时,消耗(NH4)2Fe(SO4)2溶液的体积为14.40 mL,则K2FeO4的质量分数为___________ 。(过程中杂质不参与反应)。
(1)次氯酸盐氧化法

①圆底烧瓶中发生反应的化学方程式为
②在0℃条件下,装置C中首先制备KClO,然后在剧烈搅拌下将90%的Fe(NO3)3,分别加入装置C中,充分反应可得K2FeO4溶液,写出该反应的离子方程式
③反应后,将三颈烧瓶中溶液冷却结晶,过滤、得到的K2FeO4粗产品,进一步提纯所用方法是

(2)电解法
①电解过程中,Y极放电的电极反应式是
②研究电解液浓度、电解温度对高铁酸钾产量的影响(纵坐标为高铁酸钾产率)

电解法制取高铁酸钾宜选择的NaOH的浓度和温度分别为
A.14 mol/L,25℃ B.16 mol/L,30℃
C.14 mol/L,35℃ D.18 mol/L,40℃
③K2FeO4的纯度测定:
已知反应:


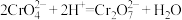
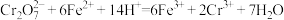
向3 mLCrCl3溶液中加入20 mL饱和KOH溶液,再加入5mL蒸馏水,冷却至室温,准确称取3.96 g样品,加入上述溶液中使其溶解(恰好反应),充分反应,过滤后加入稀硫酸酸化,并加入1 mL苯二胺磺酸钠作指示剂,用2.00 mol/L的标准硫酸亚铁铵(NH4)2Fe(SO4)2溶液滴定,至终点溶液变为绿色时,消耗(NH4)2Fe(SO4)2溶液的体积为14.40 mL,则K2FeO4的质量分数为
您最近一年使用:0次



