硫酸工业中2SO2(g)+O2(g) 2SO3(g) ΔH<0(放热反应)有关实验数据如下:
2SO3(g) ΔH<0(放热反应)有关实验数据如下:
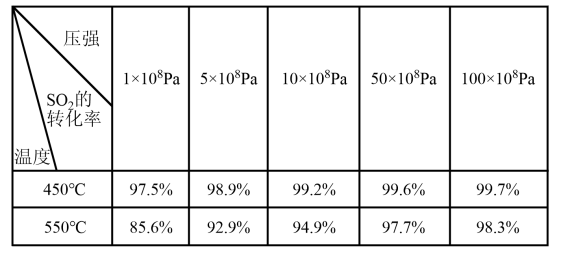
(1)在生产中常用过量的空气是为了________ 。
(2)高温对该反应有何影响?________ ,实际生产中采用400~500 ℃的温度除了考虑速率因素外,还考虑到________ 。
(3)增大压强对上述反应有何影响?__________ ,但工业上又常采用常压进行反应,其原因是______________ 。
(4)常用浓H2SO4而不用水吸收SO3是由于______ ,尾气中SO2必须回收,主要是为了________ 。
 2SO3(g) ΔH<0(放热反应)有关实验数据如下:
2SO3(g) ΔH<0(放热反应)有关实验数据如下:
(1)在生产中常用过量的空气是为了
(2)高温对该反应有何影响?
(3)增大压强对上述反应有何影响?
(4)常用浓H2SO4而不用水吸收SO3是由于
11-12高二上·重庆·期中 查看更多[1]
(已下线)2011-2012学年重庆市杨家坪中学高二上学期期中考试化学试卷
更新时间:2016-12-09 02:27:26
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】碳及其化合物与人类生产、 生活密切相关。请回答下列问题:
(1)羰基硫(O=C=S) 能引起催化剂中毒和大气污染等。羰基硫的氢解和水解反应是两种常用的脱硫方法,其反应原理为:
①氢解反应: COS(g)+H2(B) H2S(g)+CO(g) △H1
H2S(g)+CO(g) △H1
②水解反应: COS(g)+H2O(g) H2S(g)+CO2(g) △H2=-35 kJ·mol-1
H2S(g)+CO2(g) △H2=-35 kJ·mol-1
已知CO(g)+H2O(g) H2(g)+CO2(g) △H3=-42kJ·mol-1,则△H1=
H2(g)+CO2(g) △H3=-42kJ·mol-1,则△H1=______ ,羰基硫氢解反应_________ (填“能”或“示能”) 设计成原电池。若平衡常数K 与温度T之间存在1gK=a/T+b (a、b为常数) 的线性关系,图中直线符合该氢解反应平衡常数K与温度T关系的是_________ (填字母)。

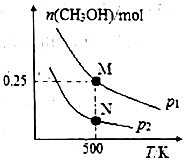
(2)CO 可以合成甲醇 CO(g)+2H2(g) CH3OH(g)。在体积可变的密闭容器中投入1molCO和2.5molH2,在不同条件下发生反应。实验测得平衡时CH3OH的物质的量随温度、压强变化如图所示。M点时,H2的转化率为
CH3OH(g)。在体积可变的密闭容器中投入1molCO和2.5molH2,在不同条件下发生反应。实验测得平衡时CH3OH的物质的量随温度、压强变化如图所示。M点时,H2的转化率为_________ ;反应速率N 点v 正(CO)_________ M 点v逆(CO) (填“>”“<”或“=”)。
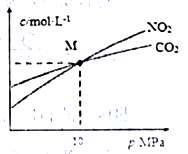
(3)焦炭还原NO2 发生反应2NO2(g)+2C(s) N2(g)+2CO2(g)。在恒温条件下,1molNO2 和足量焦炭发生该反应,测得平衡时NO2利CO2的物质的量浓度与平衡总压的关系如图所示,计算可得M点时该反应的平衡常数Kp(M)=
N2(g)+2CO2(g)。在恒温条件下,1molNO2 和足量焦炭发生该反应,测得平衡时NO2利CO2的物质的量浓度与平衡总压的关系如图所示,计算可得M点时该反应的平衡常数Kp(M)=_________ (Kp是用平衡分压代替平衡浓度表达反应的平衡常数,分压=总压×物质的量分数)。
(4)常温下,用氨水吸收CO2得到NH4HCO3溶液。在NH4HCO3 溶液中c(NH4+)________ c(HCO3-)(填“>”“<”或“=”)
。反应NH4++HCO3-+ H2O NH3· H2O +H2CO3 的平衡常数K=
NH3· H2O +H2CO3 的平衡常数K=_________ 。(已知常温下H2CO3的Ka1=4×10-7mol·L-1,Ka2=4×10-11 mol·L-1,NH3·H2O 的Kb=2×10-5mol·L-1)
(1)羰基硫(O=C=S) 能引起催化剂中毒和大气污染等。羰基硫的氢解和水解反应是两种常用的脱硫方法,其反应原理为:
①氢解反应: COS(g)+H2(B)
 H2S(g)+CO(g) △H1
H2S(g)+CO(g) △H1②水解反应: COS(g)+H2O(g)
 H2S(g)+CO2(g) △H2=-35 kJ·mol-1
H2S(g)+CO2(g) △H2=-35 kJ·mol-1已知CO(g)+H2O(g)
 H2(g)+CO2(g) △H3=-42kJ·mol-1,则△H1=
H2(g)+CO2(g) △H3=-42kJ·mol-1,则△H1=
(2)CO 可以合成甲醇 CO(g)+2H2(g)
 CH3OH(g)。在体积可变的密闭容器中投入1molCO和2.5molH2,在不同条件下发生反应。实验测得平衡时CH3OH的物质的量随温度、压强变化如图所示。M点时,H2的转化率为
CH3OH(g)。在体积可变的密闭容器中投入1molCO和2.5molH2,在不同条件下发生反应。实验测得平衡时CH3OH的物质的量随温度、压强变化如图所示。M点时,H2的转化率为
(3)焦炭还原NO2 发生反应2NO2(g)+2C(s)
 N2(g)+2CO2(g)。在恒温条件下,1molNO2 和足量焦炭发生该反应,测得平衡时NO2利CO2的物质的量浓度与平衡总压的关系如图所示,计算可得M点时该反应的平衡常数Kp(M)=
N2(g)+2CO2(g)。在恒温条件下,1molNO2 和足量焦炭发生该反应,测得平衡时NO2利CO2的物质的量浓度与平衡总压的关系如图所示,计算可得M点时该反应的平衡常数Kp(M)=
(4)常温下,用氨水吸收CO2得到NH4HCO3溶液。在NH4HCO3 溶液中c(NH4+)
。反应NH4++HCO3-+ H2O
 NH3· H2O +H2CO3 的平衡常数K=
NH3· H2O +H2CO3 的平衡常数K=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,同温度下涉及如下反应:
①2NO(g)+Cl2(g)⇌2ClNO(g) 平衡常数为K1;
②2NO2(g)+NaCl(s)⇌NaNO3(s)+ClNO(g) 平衡常数为K2。
(1)4NO2(g)+2NaCl(s)⇌2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=____ (用K1、K2表示)。
(2)若反应①在温度T下达到平衡时,平衡常数为K1,升高温度后K1增大,则正反应的焓变△H____ 0(填“>”、“<”或“=”)。若平衡后在其他条件不变的情况下,充入少量Cl2,Cl2的转化率___________ (填“变大”、“变小”或“不变”,下同),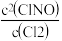 的值
的值___________ 。
Ⅱ.近年,科学家研究了乙醇催化合成乙酸乙酯的新方法:2C2H5OH(g) CH3COOC2H5(g)+2H2(g)在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图3所示。关于该方法,下列推测合理的是
CH3COOC2H5(g)+2H2(g)在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图3所示。关于该方法,下列推测合理的是________ 。
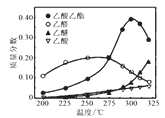
A.反应温度不宜超过300℃
B.增大体系压强,有利于提高乙醇平衡转化率
C.在催化剂作用下,乙醛是反应历程中的中间产物
D.提高催化剂的活性和选择性,减少乙醚、乙烯等副产物是工艺的关键
①2NO(g)+Cl2(g)⇌2ClNO(g) 平衡常数为K1;
②2NO2(g)+NaCl(s)⇌NaNO3(s)+ClNO(g) 平衡常数为K2。
(1)4NO2(g)+2NaCl(s)⇌2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=
(2)若反应①在温度T下达到平衡时,平衡常数为K1,升高温度后K1增大,则正反应的焓变△H
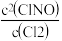 的值
的值Ⅱ.近年,科学家研究了乙醇催化合成乙酸乙酯的新方法:2C2H5OH(g)
 CH3COOC2H5(g)+2H2(g)在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图3所示。关于该方法,下列推测合理的是
CH3COOC2H5(g)+2H2(g)在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图3所示。关于该方法,下列推测合理的是
A.反应温度不宜超过300℃
B.增大体系压强,有利于提高乙醇平衡转化率
C.在催化剂作用下,乙醛是反应历程中的中间产物
D.提高催化剂的活性和选择性,减少乙醚、乙烯等副产物是工艺的关键
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)⇌2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
(1)反应的ΔH________ 0(填“大于”或“小于”);
(2)100 ℃时,体系中各物质浓度随时间变化如图所示。
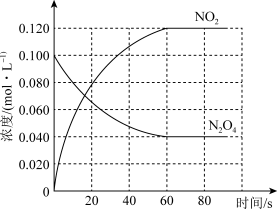
在0~60 s时段,反应速率v(N2O4)为___________________ mol·L-1·s-1;反应的平衡常数K的数值为_________________________ (保留两位小数)。
(3)100 ℃时,反应达平衡后,将反应容器的容积减少一半。平衡向________ (填“正反应”或“逆反应”)方向移动。
(4)100 ℃时达平衡后,改变反应温度为T,c(N2O4) 以0.0020mol·L-1·s-1的平均速率降低,经10s又达到平衡。T________ 100 ℃(填“大于”或“小于”)。
(1)反应的ΔH
(2)100 ℃时,体系中各物质浓度随时间变化如图所示。

在0~60 s时段,反应速率v(N2O4)为
(3)100 ℃时,反应达平衡后,将反应容器的容积减少一半。平衡向
(4)100 ℃时达平衡后,改变反应温度为T,c(N2O4) 以0.0020mol·L-1·s-1的平均速率降低,经10s又达到平衡。T
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】羰基硫(COS),用于合成除草剂、杀虫剂等,还能作为粮食熏蒸剂。CO、CO2分别与H2S反应均能制得COS,反应如下:
反应Ⅰ: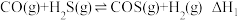
反应Ⅱ: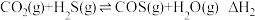
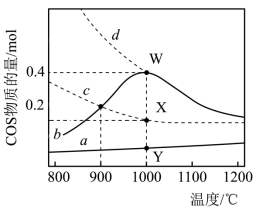
已知:在相同条件下,向两个容积相同且不变的密闭容器中按下表投料(N2不参与反应),分别发生上述反应。温度相同时,反应Ⅰ的平衡常数大于反应Ⅱ的平衡常数。实线a、b表示在相同的时间内两反应中n(COS)随温度的变化关系如下图所示;虚线c、d表示两反应的平衡曲线。
完成下列填空:
(1)COS的结构与二氧化碳类似,COS的结构式为:___________ ;
(2)下列可判断反应Ⅱ达到平衡的是___________ 。
A.v正(H2S)=v正(COS)
B.c(H2S):c(COS)不再变化
C.容器内压强不再变化
D.v正(H2S)=v逆(COS)
E.1 molH-S键断裂的同时1 molC=S键断裂
(3)实验测得反应Ⅱ的速率方程为: ,
, ,k为速率常数,则达到平衡后,仅升高温度k正增大的倍数
,k为速率常数,则达到平衡后,仅升高温度k正增大的倍数___________ (填“>”、“<”或“=”)k逆增大的倍数。
(4)上图中能表示反应Ⅰ的曲线是___________ ;相同条件下,延长足够的反应时间,反应体系中Y点COS的物质的量达到___________ 点(填“X”或“W”),该温度下反应Ⅰ的平衡常数为___________ 。
反应Ⅰ:
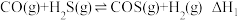
反应Ⅱ:
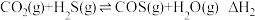
已知:在相同条件下,向两个容积相同且不变的密闭容器中按下表投料(N2不参与反应),分别发生上述反应。温度相同时,反应Ⅰ的平衡常数大于反应Ⅱ的平衡常数。实线a、b表示在相同的时间内两反应中n(COS)随温度的变化关系如下图所示;虚线c、d表示两反应的平衡曲线。
| 反应Ⅰ | 反应Ⅱ | |||||
| 起始投料 | CO | H2S | N2 | CO2 | H2S | N2 |
| 起始物质的量(mol) | 1 | 1 | 3 | 1 | 1 | 3 |

完成下列填空:
(1)COS的结构与二氧化碳类似,COS的结构式为:
(2)下列可判断反应Ⅱ达到平衡的是
A.v正(H2S)=v正(COS)
B.c(H2S):c(COS)不再变化
C.容器内压强不再变化
D.v正(H2S)=v逆(COS)
E.1 molH-S键断裂的同时1 molC=S键断裂
(3)实验测得反应Ⅱ的速率方程为:
 ,
, ,k为速率常数,则达到平衡后,仅升高温度k正增大的倍数
,k为速率常数,则达到平衡后,仅升高温度k正增大的倍数(4)上图中能表示反应Ⅰ的曲线是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】苯乙烯是生产塑料和合成橡胶的重要有机原料,国内外目前生产苯乙烯的方法主要是乙苯催化脱氢法,反应方程式为:

(1)实际生产过程中,通常向乙苯中掺混氮气(N2不参与反应),保持体系总压为100kPa下进行反应,不同投料比m下乙苯的平衡转化率随反应温度变化关系如图所示(其中投料比m为原料气中乙苯和N2的物质的量之比,取值分别为1:0、1:1、1:5、1:9)。
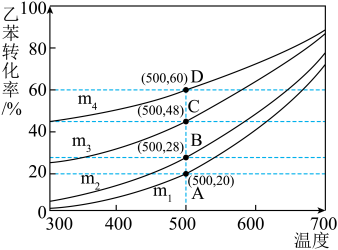
①乙苯催化脱氢反应的∆H______ 0(填“>”或“<”).
②投料比m为1:9的曲线是______ (填m1、m2、m3或m4).
(2)近年来,有研究者发现若将上述生产过程中通入N2改为通入CO2,在CO2气氛中乙苯催化脱氢制苯乙烯更容易进行,反应历程如图:
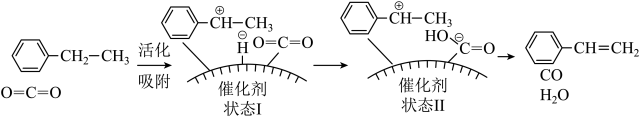
①该过程中发生的总反应化学方程式为______ .
②根据反应历程分析,催化剂表面酸碱性对乙苯脱氢反应性能影响较大,如果催化剂表面碱性太强,乙苯的转化率______ (填“升高”或“降低”)。
(3)苯乙烯与溴苯在一定条件下发生Heck反应:

根据上表数据,下列说法正确的是______。

(1)实际生产过程中,通常向乙苯中掺混氮气(N2不参与反应),保持体系总压为100kPa下进行反应,不同投料比m下乙苯的平衡转化率随反应温度变化关系如图所示(其中投料比m为原料气中乙苯和N2的物质的量之比,取值分别为1:0、1:1、1:5、1:9)。

①乙苯催化脱氢反应的∆H
②投料比m为1:9的曲线是
(2)近年来,有研究者发现若将上述生产过程中通入N2改为通入CO2,在CO2气氛中乙苯催化脱氢制苯乙烯更容易进行,反应历程如图:

①该过程中发生的总反应化学方程式为
②根据反应历程分析,催化剂表面酸碱性对乙苯脱氢反应性能影响较大,如果催化剂表面碱性太强,乙苯的转化率
(3)苯乙烯与溴苯在一定条件下发生Heck反应:

| 溴苯用量(mmol) | 100 | 100 | 100 | 100 | 100 | 100 | 100 |
| 催化剂用量(mmol) | 2 | 2 | 2 | 2 | 2 | 2 | 2 |
| 反应温度(℃) | 100 | 100 | 100 | 100 | 120 | 140 | 160 |
| 反应时间(h) | 10 | 12 | 14 | 16 | 14 | 14 | 14 |
| 4产率(%) | 81.2 | 84.4 | 86.6 | 86.2 | 93.5 | 96.6 | 89.0 |
| A.最佳反应温度为100℃ | B.最佳反应时间为16h |
| C.温度过高时催化剂活性可能降低 | D.反应产物是顺式结构 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)一定条件下,用Fe2O3、NiO或Cr2O3作催化剂对燃煤烟气进行回收。反应为2CO(g)+SO2(g) 2CO2(g)+S(l) ΔH=-270 kJ·mol-1
2CO2(g)+S(l) ΔH=-270 kJ·mol-1
①其他条件相同、催化剂不同,SO2的转化率随反应温度的变化如图1,Fe2O3和NiO作催化剂均能使SO2的转化率达到最高,不考虑催化剂价格因素,选择Fe2O3的主要优点是___________ 。
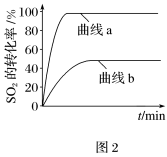
②某科研小组用Fe2O3作催化剂。在380℃时,分别研究了[n(CO)∶n(SO2)]为1∶1、3∶1时SO2转化率的变化情况(图2)。则图2中表示n(CO)∶n(SO2)=3∶1的变化曲线为___________ 。

(2)目前,科学家正在研究一种以乙烯作为还原剂的脱硝(NO)原理,其脱硝机理示意图如图3,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图4所示。


①写出该脱硝原理总反应的化学方程式:______________ 。
②为达到最佳脱硝效果,应采取的条件是___________ 。
(3)汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题。某研究小组在实验室以Ag-ZSM-5为催化剂,测得NO转化为N2的转化率随温度变化情况如图所示。
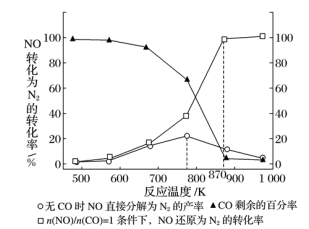
若不使用CO,温度超过775K,发现NO的分解率降低,其可能的原因是_______ ;在 的条件下,应控制的最佳温度在
的条件下,应控制的最佳温度在___________ 左右。
 2CO2(g)+S(l) ΔH=-270 kJ·mol-1
2CO2(g)+S(l) ΔH=-270 kJ·mol-1①其他条件相同、催化剂不同,SO2的转化率随反应温度的变化如图1,Fe2O3和NiO作催化剂均能使SO2的转化率达到最高,不考虑催化剂价格因素,选择Fe2O3的主要优点是
②某科研小组用Fe2O3作催化剂。在380℃时,分别研究了[n(CO)∶n(SO2)]为1∶1、3∶1时SO2转化率的变化情况(图2)。则图2中表示n(CO)∶n(SO2)=3∶1的变化曲线为


(2)目前,科学家正在研究一种以乙烯作为还原剂的脱硝(NO)原理,其脱硝机理示意图如图3,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图4所示。


①写出该脱硝原理总反应的化学方程式:
②为达到最佳脱硝效果,应采取的条件是
(3)汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题。某研究小组在实验室以Ag-ZSM-5为催化剂,测得NO转化为N2的转化率随温度变化情况如图所示。

若不使用CO,温度超过775K,发现NO的分解率降低,其可能的原因是
 的条件下,应控制的最佳温度在
的条件下,应控制的最佳温度在
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引用了各界的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g),该反应的能量变化如图所示:
CH3OH(g)+H2O(g),该反应的能量变化如图所示:

(1)上述反应平衡常数K的表达式为________________ ,温度降低,平衡常数K________ (填“增大”、“不变”或“减小”)。
(2)在体积为2 L的密闭容器中,充入1 mol CO2和3 mol H2,测得CO2的物质的量随时间变化如下表所示。从反应开始到5 min末,用氢气浓度变化表示的平均反应速率v(H2)=________ 。从反应到平衡时CO2转化率=________
(3)下列条件能使上述反应的反应速率增大,且平衡向正反应方向移动的是________ (填写序号字母)
a.及时分离出CH3OH气体
b.适当升高温度
c.保持容器的容积不变,再充入1 mol CO2和3 mol H2
d.选择高效催化剂
 CH3OH(g)+H2O(g),该反应的能量变化如图所示:
CH3OH(g)+H2O(g),该反应的能量变化如图所示:
(1)上述反应平衡常数K的表达式为
(2)在体积为2 L的密闭容器中,充入1 mol CO2和3 mol H2,测得CO2的物质的量随时间变化如下表所示。从反应开始到5 min末,用氢气浓度变化表示的平均反应速率v(H2)=
| t/min | 0 | 2 | 5 | 10 | 15 |
| n(CO2)/mol | 1 | 0.75 | 0.5 | 0.25 | 0.25 |
a.及时分离出CH3OH气体
b.适当升高温度
c.保持容器的容积不变,再充入1 mol CO2和3 mol H2
d.选择高效催化剂
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】环戊烯是生产精细化工产品的重要中间体,其制备涉及的反应如下:

回答下列问题:
(l)反应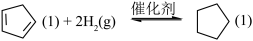 的△H=
的△H= _________ kJ/mol 。
(2)解聚反应在刚性容器中进行。
①其他条件不变,有利于提高双环戊二烯平衡转化率的条件是____ (填标号).
A.升高温度 B.降低温度 C.增大压强 D.减小压强
②实际生产中常通入水蒸气以降低双环戊二烯的沸点。某温度下,通入总压为l00kPa的双环戊二烯和水蒸气,达到平衡后总压为160kPa,双环戊二烯的转化率为8 0%,则 pH2O=___ kpa,平衡常数Kp=______ kPa (Kp为以分压表示的平衡常数)
(3) 一定条件下,将环戊二烯溶于有机溶剂中进行氢化反应,反应过程中保持氢气压力不变,测得环戊烯和环戊烷的产率(以环戊二烯为原料计)随时间变化如下图所示。
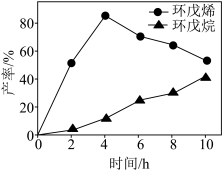
①将环戊二烯溶于有机溶剂中可减少二聚反应的发生,原因是____ ,
②最佳的反应时间为__ h。活化能较大的是__ (填“氢化反应”或“副反应”)。
(4)已知氢化反应平衡常数为1.6 × 1012,副反应的平衡常数为2.0×10l2。在恒温恒容下,环戊二烯与氢气按物质的量之比为1:1进行反应,则环戊二烯的含量随时间变化趋势是____ (不考虑环戊二烯的二聚反应)。

回答下列问题:
(l)反应
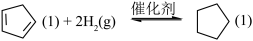 的△H=
的△H= (2)解聚反应在刚性容器中进行。
①其他条件不变,有利于提高双环戊二烯平衡转化率的条件是
A.升高温度 B.降低温度 C.增大压强 D.减小压强
②实际生产中常通入水蒸气以降低双环戊二烯的沸点。某温度下,通入总压为l00kPa的双环戊二烯和水蒸气,达到平衡后总压为160kPa,双环戊二烯的转化率为8 0%,则 pH2O=
(3) 一定条件下,将环戊二烯溶于有机溶剂中进行氢化反应,反应过程中保持氢气压力不变,测得环戊烯和环戊烷的产率(以环戊二烯为原料计)随时间变化如下图所示。

①将环戊二烯溶于有机溶剂中可减少二聚反应的发生,原因是
②最佳的反应时间为
(4)已知氢化反应平衡常数为1.6 × 1012,副反应的平衡常数为2.0×10l2。在恒温恒容下,环戊二烯与氢气按物质的量之比为1:1进行反应,则环戊二烯的含量随时间变化趋势是
您最近一年使用:0次

 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g) 

