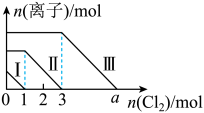
向仅含SO 、I-、Br-且物质的量分别为m、n、6 mol 的钠盐溶液中通入适量氯气,溶液中这三种离子的物质的量的变化如图所示。下列说法中正确的是( )
、I-、Br-且物质的量分别为m、n、6 mol 的钠盐溶液中通入适量氯气,溶液中这三种离子的物质的量的变化如图所示。下列说法中正确的是( )
 、I-、Br-且物质的量分别为m、n、6 mol 的钠盐溶液中通入适量氯气,溶液中这三种离子的物质的量的变化如图所示。下列说法中正确的是( )
、I-、Br-且物质的量分别为m、n、6 mol 的钠盐溶液中通入适量氯气,溶液中这三种离子的物质的量的变化如图所示。下列说法中正确的是( )
| A.曲线Ⅱ代表Br-的变化情况 |
B.曲线Ⅰ对应的反应:SO +Cl2+H2O===2H++SO +Cl2+H2O===2H++SO +2Cl- +2Cl- |
C.通入的氯气为5 mol时,溶液中的主要阴离子为Cl-、SO |
D.溶液中n(Na+)=n(SO )+n(I-)+n(Br-) )+n(I-)+n(Br-) |
更新时间:2019-09-30 16:54:00
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】下列过程中的化学反应,相应的离子方程式正确的是
A.FeCl3溶液腐蚀印刷电路板上的铜: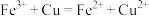 |
B.向 悬浊液中滴加NH4Cl溶液,沉淀逐渐解: 悬浊液中滴加NH4Cl溶液,沉淀逐渐解: |
C.将 溶液与Na2CO3溶液混合: 溶液与Na2CO3溶液混合: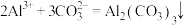 |
D.已知电离平衡常数:H2CO3>HClO> ,向NaClO溶液中通入少量二氧化碳:2ClO-+CO2+H2O=2 HClO+ ,向NaClO溶液中通入少量二氧化碳:2ClO-+CO2+H2O=2 HClO+  |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】对于Cu+2H2SO4(浓)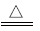 CuSO4+SO2↑+2H2O反应,下列说法正确的是( )
CuSO4+SO2↑+2H2O反应,下列说法正确的是( )
 CuSO4+SO2↑+2H2O反应,下列说法正确的是( )
CuSO4+SO2↑+2H2O反应,下列说法正确的是( )| A.Cu作还原剂,发生还原反应 |
| B.被还原的H2SO4与参加反应的H2SO4的物质的量比为1∶2 |
| C.当生成2.24 L(标准状况下)SO2时,转移的电子为2mol |
| D.当Cu足量时,H2SO4可完全反应 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】在25℃时,用一定浓度NaOH溶液滴定醋酸溶液,滴定终点附近溶液pH和导电能力的变化分别如下图所示(利用溶液导电能力的变化可判断滴定终点;溶液总体积变化忽略不计)。下列说法正确的是


| A.a→b过程中,水的电离程度不断增大 |
| B.d点对应的溶液中:c(CH3COO-)+c(CH3COOH)=c(Na+) |
| C.c→d过程中,溶液导电性增强的主要原因是c(OH-)和c(Na+)增大 |
| D.根据溶液pH和导电能力的变化可判断:V2>V3 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】25℃时,将amol/L、pH=m的一元酸HX溶液与bmol/L、pH=n的NaOH溶液等体积混合后pH>7。下列说法正确的是
| A.若a=b,则m+n<14 |
| B.若a=b,则HX一定是弱酸 |
| C.反应后溶液中一定存在c(Na+)>c(X-)>c(OH-)>c(H+) |
| D.若a=2b,则反应后溶液中一定存在2c(OH-)=c(HX)+2c(H+) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】常温下,用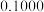
 盐酸滴定
盐酸滴定
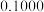

 溶液,其滴定曲线如图所示。下列说法正确的是
溶液,其滴定曲线如图所示。下列说法正确的是

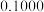
 盐酸滴定
盐酸滴定
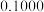

 溶液,其滴定曲线如图所示。下列说法正确的是
溶液,其滴定曲线如图所示。下列说法正确的是
A.a点溶液中 |
B.b液中 |
C. 的水解常数的数量级为 的水解常数的数量级为 |
D.d点溶液中存在 |
您最近一年使用:0次

 ,其中Cu、Fe均为+2价),其反应为:
,其中Cu、Fe均为+2价),其反应为: 。关于此反应,下列说法正确的是
。关于此反应,下列说法正确的是 仅是氧化产物
仅是氧化产物 ,有1mol硫被氧化
,有1mol硫被氧化

