下列过程中的化学反应,相应的离子方程式正确的是
A.FeCl3溶液腐蚀印刷电路板上的铜: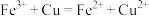 |
B.向 悬浊液中滴加NH4Cl溶液,沉淀逐渐解: 悬浊液中滴加NH4Cl溶液,沉淀逐渐解: |
C.将 溶液与Na2CO3溶液混合: 溶液与Na2CO3溶液混合: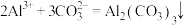 |
D.已知电离平衡常数:H2CO3>HClO> ,向NaClO溶液中通入少量二氧化碳:2ClO-+CO2+H2O=2 HClO+ ,向NaClO溶液中通入少量二氧化碳:2ClO-+CO2+H2O=2 HClO+  |
更新时间:2024-02-03 20:56:32
|
相似题推荐
【推荐1】已知常温下可用 制备
制备 ,反应前后存在六种微粒:
,反应前后存在六种微粒: 、
、 、
、 、
、 、
、 和
和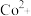 。下列叙述不正确的是
。下列叙述不正确的是
 制备
制备 ,反应前后存在六种微粒:
,反应前后存在六种微粒: 、
、 、
、 、
、 、
、 和
和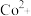 。下列叙述不正确的是
。下列叙述不正确的是A.氧化产物为 |
| B.氧化剂与还原剂的物质的量之比为1:2 |
C.若有 生成,则反应中有2 mol电子转移 生成,则反应中有2 mol电子转移 |
D.依题可知: 、 、 、 、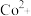 在水溶液中不能大量共存 在水溶液中不能大量共存 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】①2NaBrO3+Cl2====Br2+2NaClO3 ②HClO3+5HCl====3Cl2+3H2O
③2FeCl3+2KI====2FeCl2+I2+2KCl ④2FeCl2+Cl2====2FeCl3
根据上述氧化还原反应判断,氧化性由强到弱的顺序是
③2FeCl3+2KI====2FeCl2+I2+2KCl ④2FeCl2+Cl2====2FeCl3
根据上述氧化还原反应判断,氧化性由强到弱的顺序是
| A.NaBrO3>HClO3>Cl2>FeCl3>I2 |
| B.Cl2>FeCl3>I2>HClO3>NaBrO3 |
| C.I2>FeCl3>Cl2>HClO3>NaBrO3 |
| D.HClO3>NaBrO3>FeCl3>Cl2>I2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】NA为啊伏伽德罗常数,下列说法正确的是
A.1L1mol/LNa2CO3溶液中, 的数目为NA 的数目为NA |
| B.16gO2和O3的混合物中,含氧原子数目为NA |
| C.1molFe与足量硫粉反应,转移电子数目为3NA |
| D.46g乙醇含共价键的数目为7NA |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】在25℃时,下列说法正确的是
| A.pH相等的①醋酸钠溶液、②次氯酸钠溶液、③碳酸氢钠溶液,三者的物质的量浓度关系:①>③>② |
| B.等体积等pH的盐酸和醋酸,稀释相同倍数后与等量且足量的锌反应,两者反应速率相同,但醋酸产生氢气多 |
| C.向pH=a的盐酸中加入pH=b的氢氧化钠溶液,恰好完全反应时,测得盐酸与氢氧化钠溶液的体积比为10:1,则a+b=13 |
| D.pH=3的HA溶液与pH=11的BOH溶液等体积混合后溶液呈酸性,则HA为强酸、BOH为弱碱 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】下列实验操作、现象及其相应结论一定正确的是
| 选项 | 实验操作、现象 | 实验结论 |
| A | 将少量Cl2通入FeI2溶液,反应后溶液变黄 | C12将Fe2+氧化为Fe3+ |
| B | 将某无色气体通入溴水中,溴水褪色 | 该气体一定表现还原性 |
| C | 向盛有2ml0.1mol·L-1AgNO3的试管中滴加5滴0.1mol·L-1NaCl溶液,出现白色沉淀;再往试管中滴加5滴0.1mol·L-1KI溶液,出现黄色沉淀 | KSP(AgCl)>KSP(AgI) |
| D | 向Na2SiO3溶液中通入过量CO2,出现白色沉淀 | 非金属性:C>Si |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列实验操作、现象及解释(或结论)均正确的是
选项 | 实验操作 | 实验现象 | 解释(或结论) |
A | 向2 mL 1 mol/L MgCl2溶液中先加入5滴0.1 mol/L NaOH溶液,再加入5滴0.1 mol/L FeCl3溶液 | 先产生白色沉淀,随后转变为红褐色 | 可证明Ksp:Mg(OH)2>Fe(OH)3 |
B | 将CO2和SO2分别通入Ba(NO3)2溶液来鉴别CO2和SO2 | 均无明显现象 | SO2、CO2与水反应得到的酸均为弱酸,不能 与Ba(NO3)2溶液反应 |
C | 向2支盛有2 mL 5%H2O2溶液中分别滴加5滴0.1 mol/L的Fe2(SO4)3溶液和5滴0.1 mol/L的CuSO4溶液,观察实验现象 | 试管中均产生无色气体,前者较快 | Fe3+和Cu2+均能催化H2O2的分解,前者催化活性更高 |
D | 室温下,用pH试纸分别测定0.1 mol/L的Na2CO3溶液和0.1 mol/L的NaClO溶液的pH | 前者pH比后者大 | 非金属性:Cl>C |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐1】25℃时,用NaOH溶液分别滴定HX、 、
、 三种溶液,
三种溶液, [M表示
[M表示 、
、 、
、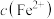 ]随pH变化关系如图所示,其中③的M代表
]随pH变化关系如图所示,其中③的M代表 。已知
。已知 ,下列有关分析不正确的是
,下列有关分析不正确的是
 、
、 三种溶液,
三种溶液, [M表示
[M表示 、
、 、
、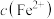 ]随pH变化关系如图所示,其中③的M代表
]随pH变化关系如图所示,其中③的M代表 。已知
。已知 ,下列有关分析不正确的是
,下列有关分析不正确的是
A.①代表滴定 溶液的变化关系 溶液的变化关系 |
B.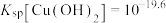 |
C.a点时,③中 与②中M的关系为 与②中M的关系为 |
D. 、 、 固体均易溶解于HX溶液 固体均易溶解于HX溶液 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】常温下,向某浓度的二元弱酸H2A溶液中逐滴加入NaOH溶液,pC与溶液pH的变化关系如图所示(pC=-lgx,x表示溶液中溶质微粒的物质的量浓度)。下列说法正确的是


| A.pH由2增大到3的过程中,水的电离程度先减小后增大 |
| B.溶液中存在点d满足3[c(H2A)+c(HA-)+c(A2-)] = 2c(Na+),该点位于b、c之间 |
| C.pH=3时,溶液中c(HA-)= c(A2-) > c(H2A) |
| D.常温下,溶液中c(H2A)·c(A2-)与c2(HA-)的比值为104.5 |
您最近一年使用:0次

 ,
, ,
,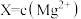 、
、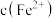 、
、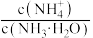 或
或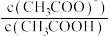 ]或与pH的关系如图所示。下列叙述正确的是
]或与pH的关系如图所示。下列叙述正确的是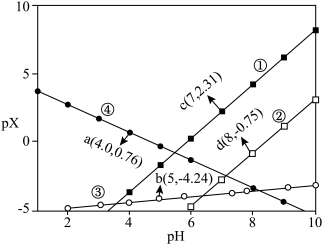
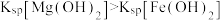 。
。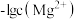 与pH的关系
与pH的关系
 中性溶液中
中性溶液中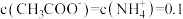 mol⋅L
mol⋅L
 的平衡常数K为
的平衡常数K为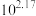
 溶液样品中加入硫酸酸化的
溶液样品中加入硫酸酸化的 溶液,紫色褪去,说明该样品中一定混有
溶液,紫色褪去,说明该样品中一定混有
 在一定条件下能自发进行,则该反应的
在一定条件下能自发进行,则该反应的
 ,向
,向 的
的 溶液中加水,
溶液中加水, 会增大
会增大 溶液处理
溶液处理 ,可将
,可将 ,因为该温度下
,因为该温度下
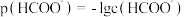 与
与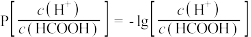 的变化关系如图所示。下列叙述错误的是
的变化关系如图所示。下列叙述错误的是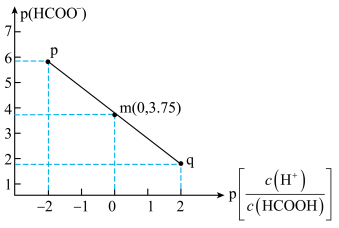
 始终不变
始终不变


