25℃时,在20mL0.1mol•L﹣1NaOH溶液中逐滴加入0.2mol•L﹣1的某一元弱酸HX溶液,曲线如图所示,有关粒子浓度关系的比较中,错误的是( )
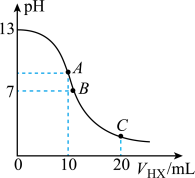

| A.在A点:c(Na+)>c(OH﹣)>c(X﹣)>c(H+) |
| B.在B点:c(OH﹣)=c(H+)=c(Na+)=c(X﹣) |
| C.在C点:c(X﹣)>c(Na+)>c(H+)>c(OH﹣) |
| D.在C点:c(X﹣)+c(HX)=2c(Na+) |
更新时间:2019-10-31 14:34:58
|
相似题推荐
多选题
|
适中
(0.65)
【推荐1】常温下,用0.1000 mol/L HCl溶液滴定20.00 mL 0.1000 mol/L NH3•H2O溶液,滴定曲线如下图。下列说法正确的是
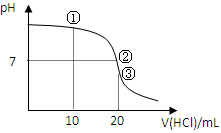

| A.①溶液:c(C1—)>c(NH4+)>c(OH—)>c(H+) |
| B.②溶液:c(NH4+)=c(C1—)>c(OH—)=c(H+) |
| C.③溶液:c(H+)>c(NH3·H2O) + c(OH—) |
| D.滴定过程中可能出现:c(NH3•H2O)>c(NH4+)>c(OH—)>c(Cl—)>c(H+) |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,Ka1(H2C2O4)=10-1.3, Ka2(H2C2O4)=10-4.2。用0.1000 mol·L-1 NaOH溶液滴定10.00 mL 0.1000 mol·L-1 H2C2O4溶液所得滴定曲线如右图。下列说法正确的是


A.点①所示溶液中:c(Na+)>c( )>c(H2C2O4)>c( )>c(H2C2O4)>c( ) ) |
B.点②所示溶液中:c( )=c( )=c( ) ) |
C.点③所示溶液中:c(Na+)=c( ) + c( ) + c( ) ) |
D.点④所示溶液中:c(Na+) + 2c(H2C2O4) + 2c(H+)=2c(OH-) + 2c( ) ) |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】已知:乙二酸(H2C2O4)是二元弱酸。向10 mL 0.1 mol·L-1Na2C2O4溶液中逐滴加入a mL 0.1 mol·L-1盐酸(混合前后溶液体积变化可忽略)。下列说法正确的是
| A.当a=5时,c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+2c(C2O42-) |
| B.当a=10时,c(Cl-)+c(OH-)=c(H+)+c(HC2O4-)+2c(H2C2O4) |
| C.当a=15时,c(H2C2O4)+c(HC2O4-)+c(C2O42-)="0.04" mol·L-1 |
| D.当a=20时,c(Na+)=c(H+)>c(HC2O4-)>c(C2O42-) |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】常温下将稀NaOH溶液与稀CH3COOH溶液混合,不可能出现的结果是
| A.pH>7,且c(OH-)>c(Na+)>c(CH3COO-)>c(H+) |
| B.pH>7,且c(Na+)+c(H+)=c(OH-)+c(CH3COO-) |
| C.pH<7,且c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
| D.pH=7,且c(CH3COO-)>c(Na+)>c(H+)=c(OH-) |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】向一定浓度的H3AsO4水溶液中滴加NaOH溶液,含砷的各物种分布系数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如图所示。下列说法正确的是


A.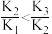 |
B.NaH2AsO4溶液中: c(HAsO )=c(H3AsO4) )=c(H3AsO4) |
C.P点: pH= |
D.Na2HAsO4溶液中: c(H2AsO ) +2c(H3AsO4)>c(AsO ) +2c(H3AsO4)>c(AsO ) ) |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】常温下,Ka(CH3COOH)=1.8×10-5,分别向20 mL 0.1 mol/L NaHCO3溶液和CH3COOH溶液中逐滴加入0.1 mol/L NaOH溶液,滴定曲线如图所示。下列叙述正确的是
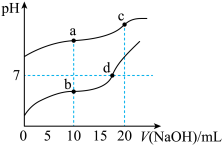

| A.b点溶液中粒子浓度大小关系:c(CH3COO-)>c(Na+)>c(H+)>c(CH3COOH)>c(OH-) |
| B.c点溶液中存在:c(H+)+c(HCO3-)+2c(H2CO3)=c(OH-) |
| C.溶液中由水电离出c(H+)大小关系:b<d<a=c |
D.d点溶液中: =180 =180 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】1,3-丙二胺[H2N(CH2)3NH2]类似氨的性质。25°C时,1,3-丙二胺溶液中各含氮微粒的分布系数δ(某含氮微粒的浓度占各含氮微粒浓度之和的分数)随溶液pH的变化曲线如图所示(已知:25°C时,Kb1=10-3.5,Kb2=10-5.5)。下列说法正确的是


| A.曲线I代表的微粒符号为H2N(CH2)3NH2 |
B.H2N(CH2)3NH2在水溶液中第一步电离的方程式:H2N(CH2)3NH2+H2O H2N(CH2)3NH H2N(CH2)3NH +OH- +OH- |
| C.曲线I与曲线II相交点对应pH=5.5 |
D.0.01mol·L-1H2N(CH2)3NH3Cl溶液中各离子浓度关系:c(Cl-)>c[H2N(CH2)3NH ]>c(OH-)>c(H+) ]>c(OH-)>c(H+) |
您最近一年使用:0次

 )
) )+2c(CO
)+2c(CO )+c(OH-)
)+c(OH-)

